INSTITUTO OSWALDO CRUZ
Pós-Graduação em Biologia Celular e Molecular
Regulação da resposta imune como alvo de
intervenção terapêutica na cardiomiopatia
chagásica crônica experimental
ISABELA RESENDE PEREIRA
RIO DE JANEIRO
2015
52
INSTITUTO OSWALDO CRUZ
Pós-Graduação em Biologia Celular e Molecular
ISABELA RESENDE PEREIRA
Regulação da resposta imune como alvo de intervenção terapêutica na
cardiomiopatia chagásica crônica experimental
Tese apresentada ao Instituto Oswaldo Cruz
como parte dos requisitos para obtenção do título de
Doutor em Biologia Celular e Molecular
Orientadora: Dra. Joseli Lannes-Vieira
RIO DE JANEIRO
2015
ii
iii
INSTITUTO OSWALDO CRUZ
Pós-Graduação em Biologia Celular e Molecular
ISABELA RESENDE PEREIRA
Regulação da resposta imune como alvo de intervenção terapêutica na
cardiomiopatia chagásica crônica experimental
ORIENTADORA: Dra. Joseli Lannes-Vieira
EXAMINADORES:
Prof. Dra. Tania Cremonini de Araujo-Jorge (Presidente)
Prof. Dr. Edecio Cunha-Neto (Membro)
Prof. Dra. Andrea Henriques Pons (Membro/Revisora)
Prof. Dra. Solange Lisboa de Castro (Suplente)
Prof. Dra. Regina Coeli dos Santos Goldenberg (Suplente)
Rio de Janeiro, 09 de julho de 2015
iv
“Posso, tudo posso Naquele que me fortalece
Nada e ninguém no mundo vai me fazer desistir
Quero, tudo quero, sem medo entregar meus projetos
Deixar-me guiar nos caminhos que Deus desejou pra mim e ali estar
Vou perseguir tudo aquilo que Deus já escolheu pra mim
Vou persistir, e mesmo nas marcas daquela dor
Do que ficou, vou me lembrar
E realizar o sonho mais lindo que Deus sonhou
Em meu lugar estar na espera de um novo que vai chegar
Vou persistir, continuar a esperar e crer
E mesmo quando a visão se turva e o coração só chora
Mas na alma, há certeza da vitória”.
Compositor: Celina Borges
v
Dedico este trabalho...
À minha família,
Meu pai Ormeu, minha mãe Silvia e meu irmão Eduardo, tesouros da minha vida.
Agradeço a vocês por tudo que fizeram e ainda têm feito por mim. Agradeço por
estarem sempre ao meu lado apoiando as minhas decisões. A vocês, minha eterna
gratidão.
vi
Agradecimentos
Nestes oito anos no Laboratório de Biologia das Interações muitas foram as pessoas
que, de inúmeras maneiras, contribuíram para o desenvolvimento deste trabalho,
transformando-o numa experiência prazerosa e intensa de formação científica e trabalho
intelectual. A experiência da pós-graduação não somente trouxe para mim
conhecimento científico-acadêmico, como também levo comigo exemplos de
determinação, eficiência, compromisso, paciência e confiança no futuro. Esta tese de
doutoramento reflete o trabalho de formação que começou na iniciação científica,
passou pelo mestrado e hoje, de forma madura, completa um ciclo de conhecimento e
abre caminhos e possibilidades para novas conquistas. Dessa forma gostaria de
agradecer a todos que me auxiliaram nesta caminhada.
"Se consegui ver mais longe
é porque estava aos ombros de gigantes"
Sir Isaac Newton
Primeiramente agradeço a Deus, que iluminou meus caminhos e me ajudou a vencer
mais uma etapa em minha vida.
À minha orientadora, Dra. Joseli Lannes-Vieira, pela dedicação, ensinamentos,
confiança, apoio e orientação ao longo de todos estes anos. Toda minha admiração e
respeito.
Aos pesquisadores do Laboratório de Biologia das Interações, Danielle, Daniel,
Verônica e Andrea, que sempre tiveram dispostos a ajudar e ensinar.
Aos colegas de laboratório Rafael Rodrigues, Rhaíssa, Leonardo, Ellen, Laura, Lucia
Helena, Dina, Isabela Forasteiro, Jéssica, Thaís e todos que por aqui passaram e
deixaram um pouco de si. Obrigada pelo companheirismo e agradáveis momentos de
convivência.
À veterinária e doutoranda Glaucia Vilar pelas análises eletrocardiográficas e todo o
suporte em experimentação animal.
Ao Dr. Otacilio Moreira e a todos do Laboratório de Biologia Molecular e Doenças
Endêmicas, que sempre me receberam muito bem, me auxiliaram e discutiram comigo
os resultados de PCR.
Às tecnologistas Cynthia Casabulho e Daniela Beghini pelo carinho e prontidão com
que sempre me ajudaram no citômetro de fluxo.
À fofíssima Isalira Peroba Ramos, pela colaboração nas análises ecocardiográficas.
vii
Aos profissionais do CECAL/Fiocruz, Biotérios de Experimentação do IOC/Fiocruz e
das plataformas, que permitiram o uso de animais e equipamentos indispensáveis à
realização deste trabalho.
À toda minha família por todo carinho, apoio e estímulo de sempre.
Ao meu noivo Bernardo por todo amor, cumplicidade, carinho, compreensão e
paciência.
Às companheiras de casa Magna, Milena, Juliana, Brenda e Letícia pelas palavras
amigas, choros, brigadeiros e risadas.
À Marina, que me adotou e apresentou o Rio de Janeiro. Você é muito especial.
À grande amiga carioca Alessandra, vou te levar por toda a vida.
À Lucilene, Joseane e todos os colegas do Pavilhão Cardoso Fontes por cada cafezinho,
favorzinho e mimo que me fizeram sentir querida.
Aos funcionários e colegas da Pós-Graduação em Biologia Celular e Molecular.
Agradeço aos membros da banca examinadora e suplentes, por aceitarem o convite e,
em especial, à Dra. Andrea Henriques Pons por rever meu trabalho, discutir e me
estimular cientificamente.
Ao IOC, FAPERJ e CNPq pelo apoio financeiro. Principalmente, agradeço ao prêmio
Doutorado-Bolsa Nota 10 que muito me estimulou.
A todos que, direta ou indiretamente, contribuíram para a realização deste trabalho.
Obrigada!
viii
Resumo
A doença de Chagas (DC) é uma infecção causada pelo protozoário flagelado Trypanosoma
cruzi que afeta milhões de pessoas principalmente na América latina. Na fase aguda, a resposta
imune associada à inflamação cardíaca pode levar ao controle do parasito. No entanto, em cerca
de 30% dos pacientes o processo inflamatório pode persistir resultando em cardiomiopatia
chagásica crônica (CCC). A CCC é caracterizada pela persistência do parasito, inflamação e
fibrose progressiva com alterações elétricas e funcionais. No tecido cardíaco afetado, a presença
de citocinas inflamatórias e quimiocinas pode dirigir a migração dos leucócitos que contribui
para a formação do infiltrado inflamatório. Neste trabalho desafiamos a hipótese de que a
regulação da resposta imune na fase crônica da DC é uma alternativa para estimular a
imunidade protetora, interromper a progressão e, até mesmo, reverter a CCC. Inicialmente,
descrevemos dois modelos experimentais, C3H/He e C57/BL6, infectados pela cepa
Colombiana do T. cruzi. Estes reproduziram aspectos da DC crônica, apresentando diferentes
níveis de lesão cardíaca em paralelo às alterações imunológicas, podendo ser classificados,
respectivamente, como portadores de CCC grave e moderada. Estes modelos experimentais
foram usados nos trabalhos seguintes. A gravidade da CCC foi associada com a intensidade do
parasitismo cardíaco, ao aumento dos níveis séricos do fator de necrose tumoral (TNF) e de
óxido nítrico (NO). Como prova de conceito, administramos o fármaco anti-TNF Infliximab na
fase crônica da infecção pelo T. cruzi e observamos que não há alteração na carga parasitária
tecidual, mas ocorre o reposicionamento da resposta imune com redução dos níveis séricos e
expressão de TNF e de seu receptor 1 (TNFR1) no tecido cardíaco, aumento da frequência de
células expressando IL-10 no baço, diminuição da atividade citotóxica de células T CD8+ e
melhora da função elétrica. A patologia da CCC é proposta estar associada à persistência do
parasito e ao desequilíbrio da resposta imune do hospedeiro, favorecendo a inflamação crônica
não benéfica que leva à lesão cardíaca. Assim, utilizando o imunorregulador pentoxifilina
(PTX) nos modelos de CCC moderada e grave, observamos melhora na função elétrica, com
redução da atividade da enzima CK-MB (biomarcador de lesão de cardiomiócitos) no soro,
menor distância entre as placas de conexina 43 (Cx43) e redução do depósito de fibronectina no
tecido cardíaco. A terapia com PTX reduziu a frequência de células T CD8+ que expressam
marcadores de ativação e migração no baço, a ativação das células endoteliais dos vasos
sanguíneos e a intensidade da miocardite. Embora a produção de interferon (IFN)γ tenha sido
preservada sistemicamente e no tecido cardíaco, a terapia com PTX reduziu o número de células
perforina (Pfn)+ neste tecido. PTX associada à droga tripanossomicida benznidazol, diminuiu a
carga parasitária, a miocardite, a expressão de TNF, TNFR1 e a enzima óxido nítrico sintase
induzível (iNOS) no tecido cardíaco e os níveis séricos de NO. De forma importante, a terapia
combinada sustentou a melhora na função elétrica 30 dias após o final da terapia. Por último,
usamos como estratégia de modulação da resposta imune na infecção cronica pelo T. cruzi a
vacina terapêutica em um protocolo homólogo de indução-reforço com adenovírus
recombinante transportando as sequências codificadoras da proteína-2 da superfície de
amastigota e a trans-sialidase (rAdVax). Os camundongos vacinados apresentaram menos lesão
cardíaca e anormalidades elétricas. A imunoterapia com rAdVax redirecionou a resposta imune
específica, aumentando a freqüência de células T CD8+ produtoras de IFNγ e diminuindo a
freqüência de células T CD8+ citotóxicas em camundongos cronicamente infectados pelo T.
cruzi. Além disso, rAdVax reduziu o número de células Pfn+, mas preservou o número de
células de IFNγ+ no tecido cardíaco. A imunoterapia com rAdVax reduziu os níveis séricos de
NO e a expressão de iNOS no tecido cardíaco. Nossos dados suportam que a fisiopatogenia da
DC é sustentada por persistência do parasito e por desregulação da resposta imune. Visto que
atualmente os tratamentos disponíveis apenas mitigam os sintomas da CCC, as intervenções
aqui propostas parecem ser alternativas viáveis para redirecionar a resposta imune para um
perfil protetor visando um melhor prognóstico para os pacientes.
ix
Abstract
Chagas disease (CD) is an infection caused by a flagellate protozoan Trypanosoma cruzi, which
affects millions of people especially in Latin America. In the acute phase, immune response
associated with heart inflammation can lead to parasite control. However, in about 30% of
patients, the inflammatory process may persist resulting in chronic chagasic cardiomyopathy
(CCC). This condition is characterized by parasite persistence, inflammation and progressive
fibrosis with electrical and functional changes. In the affected cardiac tissue, the presence of
inflammatory cytokines and chemokines can drive leukocyte migration that contributes to the
establishment of inflammatory infiltrates. In this work, we challenge the hypothesis that
regulation of the immune response in the chronic phase of CD is an alternative to stimulate
protective immunity, stop progression and even reverse CCC. Initially, we describe two
experimental models, C3H/He and C57BL/6, infected with the Colombian T. cruzi strain. These
models reproduced aspects of chronic CD, featuring different degrees of cardiac injury parallel
to immunological changes, being classified, respectively, as severe and moderate CCC. These
experimental models were used to challenge our hypothesis. CCC severity was associated with
the intensity of cardiac parasitism and increased levels of tumor necrosis factor (TNF) and nitric
oxide (NO) in the serum. As proof of concept, we administered the anti-TNF Infliximab in the
chronic phase of T. cruzi infection. There was no change in tissue parasite load, but we observed
repositioning in the immune response with reduced TNF levels in the serum and expression of
TNF and its receptor 1 (TNFR1) in the cardiac tissue, increase in the frequency of cells
expressing IL-10 in the spleen, reduction in the CD8 cytotoxic activity and improvement in
electrical function. The CCC pathology is proposed to be associated with parasite persistence
and immunological unbalance, favouring the non-beneficial chronic inflammation that leads to
heart damage. Thus, using the immunoregulatory agent pentoxifylline (PTX) in CCC models,
mild and severe, we noted an improvement in the cardiac function, reduced CK-MB
(cardiomyocyte injury biomarker) activity in the serum and decreased fibronectin deposition
and connexin 43 (Cx43) loss and disorganization in the cardiac tissue. PTX therapy decreased
the frequency of CD8+ T cells expressing activation and migration markers in the spleen, the
activation of the endothelial cells of blood vessels and the intensity of myocarditis. Although the
production of interferon (IFN)γ has been preserved systemically and in the cardiac tissue, PTX
therapy reduced the number of perforin (Pfn)+ cells in this tissue. Further, PTX associated with
the trypanocidal drug benznidazole, decreased parasite load, myocarditis, and the expression of
TNF, TNFR1 and the inducible nitric oxide synthase enzyme (iNOS) in the heart, as well as
NO levels in the serum. Importantly, the combined therapy sustained the improvement in
electrical function 30 days after the end of the therapy. Finally, we used as strategy of
modulation the immune response in chronic T. cruzi infection the therapeutic vaccine in a
homologous prime-boost protocol with recombinant adenovirus carrying the coding sequences
of the amastigote surface protein-2 and trans-sialidase (rAdVax). The vaccinated mice had less
heart damage and electrical abnormalities. Immunotherapy with rAdVax redirected specific
immune response, increasing the frequency of CD8+ T cells producing IFNγ and decreasing the
frequency of cytotoxic CD8+ T cells in mice chronically infected with T. cruzi. Further, rAdVax
reduced the number of Pfn+ cells, but preserved the number of IFNγ+ cells in the heart tissue.
Moreover, the rAdVax immunotherapy reduced the serum levels of NO and iNOS expression in
the cardiac tissue. Thus, our data support that the pathogenesis of CD is sustained by parasite
persistence and deregulation of the immune response. Presently, available treatments only
mitigate the symptoms of CCC. Therefore, the interventions proposed in our study appear to be
feasible to redirect the immune response to a protective profile aiming a better prognosis for CD
patients.
x
Lista de abreviaturas
AP-1
Proteína ativadora 1
APC
ASP2
Célula apresentadora de antígeno
Proteína da superfície das formas amastigotas do T. cruzi
BENEFIT
BENznidazole Evaluation For Interrupting Trypanosomiasis
AkT
Proteína quinase B
Btk
Proteína tirosina quinase de Bruton
Bz
Benznidazol
CAM
Molécula de adesão celular
CCC
Cardiomiopatia chagásica crônica
CCR
Receptor de quimiocina
CD62L
L- selectina
c-FLIP
Proteína inibidora de FLICE
c-IAP-1
Proteína inibidora da apoptose
CK-MB
Isoenzima MB da creatina quinase
CTL
Linfócito T citotóxico
CTLA-4
Antígeno 4 de linfócito T citotóxico
Cx43
Conexina 43
DC
Doença de Chagas
dpi
Dias pós-infecção
ERK
quinase reguladora de sinal extracelular
ETK
Proteína tirosina quinase epitelial/endotelial
FADD
Proteína com domínio de morte associado à Fas
FEVE
Fração de ejeção do ventrículo esquerdo
FLICE
Enzima conversora de IL-1β FADD-like
FN
Fibronectina
xi
GPI
Glicosil-fosfatidil-inositol
ICAM-1
Molécula de adesão intercelular do tipo 1 (CD54)
ICC
Insuficiência cardíaca congestiva
IFNγ
Interferon-γ
IgG
Imunoglobulina da classe G
IL
Interleucina
iNOS
Óxido nítrico sintase induzível
IRAK
Receptor de IL-1 associado à quinase 1
IκB
Inibidor do kappa B
JNK
Quinase c-Jun N-terminal
LFA-1
Antígeno funcional do tipo 1 presente em leucócitos
(CD11a/CD18)
LPS
Lipopolissacarídeo
MAPK
Proteína quinase ativada por mitógeno
Met-RANTES
Antagonista parcial de CCL5/RANTES, RANTES humano
recombinante com uma metionina na porção aminoterminal
MHC
Complexo principal de histocompatibilidade
MyD88
Gene de resposta primária à diferenciação mielóide (88)
NF-κB
Fator de transcrição nuclear kappa B
NK
Células natural killer
NO
Óxido nítrico
OMS
Organização mundial de saúde
OPAS
Organização Pan-Americana da Saúde
PAMPS
Padrão molecular associado a patógeno
Pfn
Proteína formadora de poro (perforina)
PLAD
Domínio de associação prévia ao ligante
PRRs
Receptores de reconhecimento de padrões
PTX
Pentoxifilina
xii
rAd
Adenovírus recombinante
rAdVax
Vacina de adenovírus recombinante transportando as
sequências codificadoras da proteína-2 da superfície de
amastigota e a trans-sialidase
RIP-1
Proteína de interação com o receptor quinase 1
RNS
Espécies reativas de nitrogênio
ROS
Espécies reativas de oxigênio
SIDA
Síndrome da imunodeficiência adquirida
SODD
Silenciadores do domínio de morte
TACE
Enzima conversora de TNF
TAP-1
Transportador associado a processamento de antígenos
TCR
Receptor de antígeno de célula T
TGF-β
Fator transformador de crescimento β
TLR
Receptor do tipo Toll
TNF
Fator de necrose tumoral
TNFR1/p55
Receptor 1 de TNF
TNFR2/p75
Receptor 2 de TNF
TRADD
Proteína do domínio de morte associada ao receptor de TNF
TRAF
Fator associado ao receptor de TNF
PI3K
Fosfatidilinositol 3 quinase
Treg
Célula T reguladora
TS
Trans-sialidase
VCAM-1
Molécula de adesão celular expressa pelo endotélio vascular
(CD106)
xiii
Índice
Resumo.........................................................................................................
IX
Abstract........................................................................................................
X
Lista De Abreviaturas..................................................................................
XI
Índice............................................................................................................
XIV
Introdução....................................................................................................
1
Revisão de Literatura...................................................................................
4
Justificativa..................................................................................................
40
Objetivo Geral..............................................................................................
41
Objetivos Específicos...................................................................................
41
Artigo I.........................................................................................................
42
Artigo II.......................................................................................................
53
Artigo III......................................................................................................
72
Artigo IV......................................................................................................
101
Artigo V.......................................................................................................
121
Discussão......................................................................................................
153
Conclusões....................................................................................................
174
Perspectivas..................................................................................................
175
Referências...................................................................................................
176
Anexos..........................................................................................................
203
xiv
1. Introdução
___________________________________________________________________________________
A doença de Chagas (DC) é uma doença tropical negligenciada, causada pelo
parasito Trypanosoma cruzi, capaz de levar o indivíduo a uma condição crônica
limitante (Rassi et al., 2010). Nas últimas décadas vimos a globalização da DC, devido
principalmente ao fluxo migratório de pessoas infectadas para áreas não endêmicas,
com alto número de portadores principalmente nos Estados Unidos e Europa (WHO,
2014).
Dados
recentes
da
Organização
Mundial
da
Saúde
mostram
que
aproximadamente 7-8 milhões de pessoas estão infectadas com o T. cruzi e cerca de 25
milhões estão expostas ao risco de contaminação (WHO, 2014). A cardiomiopatia
chagásica crônica (CCC), principal causa de morbidade e mortalidade entre os pacientes
da DC, é caracterizada por persistência do parasito, inflamação e fibrose progressiva
com remodelamento do miocárdio e da vascularização, que comumente causa
insuficiência cardíaca (IC) (Rassi et al., 2010). Devido a falta de tratamento específico e
eficaz contra a doença, a CCC é tratada de forma semelhante a outras síndromes de IC
(Rassi et al., 2010). Atualmente, um dos grandes desafios é encontrar terapia efetiva
para os pacientes de DC, em especial àqueles da forma cardíaca da fase crônica.
A patogenia da CCC é proposta estar relacionada a alterações miocárdicas
dependentes da persistência do parasito e da resposta imunológica (Marin-Neto et al.,
2007). Na fase aguda da infecção pelo T. cruzi,a resposta imune essencial ao controle do
parasito no tecido cardíaco está relacionada à geração de inflamação, que regride na
maioria dos pacientes. Contudo, em cerca de 30% dos pacientes a inflamação persiste,
levando à doença crônica. Acredita-se que as alterações na fase crônica sejam
consequências de mecanismos multifatoriais relacionados tanto ao parasito quanto ao
hospedeiro vertebrado. Entre os fatores relacionados ao parasito, o tamanho do inóculo,
a variabilidade das linhagens, o tropismo tecidual e a antigenicidade são aspectos
relevantes; quanto ao hospedeiro, é importante ressaltar, especialmente, as
características imunológicas e genéticas (Vago et al., 2000; Dutra et al., 2009). De fato,
é bem aceito que a ausência de manifestações clínicas na DC está associada à habilidade
do indivíduo em controlar a resposta imune desencadeada pela infecção e que resulta no
controle do parasitismo, mas que também pode contribuir para os danos inflamatórios,
característicos da doença (Brener & Gazzinelli, 1997).
52
1
A citocina fator de necrose tumoral (TNF) se encontra em níveis aumentados
no soro na infecção pelo T. cruzi (Perez-Fuentes et al., 2003; Ferreira et al., 2003;
Talvani et al., 2004). Esta citocina é proposta atuar no controle da replicação do parasito
na fase aguda, via indução da produção de óxido nítrico (NO), principalmente por
macrófagos ativados (Aliberti et al., 2001). Entretanto, níveis plasmáticos de TNF estão
correlacionados ao grau de disfunção cardíaca em portadores da CCC (Ferreira et al.,
2003; Talvani et al., 2004). Assim, especula-se que inicialmente TNF teria função
protetora na infecção pelo T. cruzi, porém seus elevados níveis nos soros dos pacientes
permitiriam a perpetuação do infiltrado inflamatório e o exacerbado processo oxidativo,
resultando na CCC (Perez-Fuentes et al., 2003). A participação de TNF na patogênese
da CCC não está elucidada (Lannes-Vieira et al., 2011). No presente trabalho, nos
perguntamos se TNF seria um fator chave na patogenia da DC, alimentando o
desequilíbrio imunológico e este contribuindo para as lesões cardíacas. Um dos entraves
para o entendimento da patogenia da DC é a não existência de modelo experimental que
reproduza aspectos parasitológicos, imunológicos e clínicos da CCC, de forma
simultânea e associada. Assim, antes de abordarmos nossa primeira proposta,
estabelecemos modelos experimentais que atendessem esta lacuna.
A importância das células T na DC está apoiada tanto nos achados que
demonstram a sua resposta in vitro como nos dados que evidenciam a presença dessas
células no infiltrado inflamatório no miocárdio de pacientes com CCC (Higuchi et al.,
1993). A alta frequência de células T CD4+ e CD8+ efetoras, secretoras de altos níveis
de citocinas inflamatórias, como TNF e interferon gama (IFNγ), e redução na frequência
de células com perfil regulador e baixa produção de interleucina (IL)-10 foram
encontradas em pacientes com CCC. Por outro lado, os pacientes com a forma
indeterminada da DC, além de apresentarem células ativadas produzindo citocinas
inflamatórias, possuem também aumento na frequência de células reguladoras e alta
produção de IL-10 (Gomes et al., 2003; 2005; Araujo et al., 2007; Cunha-Neto et al.,
2009). Independente de sua importância para a resistência do hospedeiro à infecção pelo
T. cruzi (Padilla et al., 2009), as células T CD8+ ganharam atenção especial por serem o
principal componente da miocardite aguda (Sun et al., 1993) e crônica (dos Santos et al.,
2001) na infecção experimental pelo T. cruzi e em pacientes com CCC (Higuchi et al.,
1993; 1997; Reis et al., 1993). Recentemente, mostramos que na fase crônica as células
T CD8+IFNγ+ exercem um papel benéfico, enquanto que as células T CD8+perforina
2
(Pfn)+ participam da lesão cardíaca induzida pelo T. cruzi (Silverio et al., 2012). Neste
trabalho, propusemos que uma terapêutica adequada poderia interferir com as
populações distintas de células T CD8+ melhorando a lesão cardíaca na fase crônica da
infecção pelo T. cruzi, o que abordaremos neste trabalho de tese.
É possível especular que o desenvolvimento de lesões cardíacas na DC seja
consequência da longa e complexa relação entre persistência do parasito e mecanismos
homeostáticos mal-adaptados do hospedeiro, levando a alterações patogênicas (PerezFuentes et al., 2003). Este trabalho de tese tem como hipótese que a interação entre o
parasito e o sistema imune seja responsável pelos danos teciduais nas células infectadas,
favorecendo a persistência da inflamação e a fibrose cardíaca, levando a alterações
elétricas e funcionais ao longo dos anos. Então, regular a resposta imune na fase crônica
da DC pode ser uma alternativa, ao reposicionar a resposta imune desbalanceada e
estimular a imunidade protetora, visando interromper a progressão e, até mesmo,
reverter a CCC. Assim, com este trabalho objetivamos: (i) estabelecer modelo
experimental que reproduza aspectos parasitológicos, imunológicos e clínicos da CCC,
de forma simultânea e associada; (ii) contribuir para o entendimento de mecanismos
celulares e moleculares envolvidos na patogenia e progressão da CCC experimental,
esclarecendo a participação de moléculas chave nestes processos; e (iii) propor
desenhos de estratégias de intervenção racional (usando fármacos imunorreguladores,
droga tripanossomicida e vacina) que preservem a resposta imune protetora e o controle
do parasitismo, que resolvam ou pelo menos mitiguem a inflamação crônica,
potencialmente envolvida na geração de fibrose e disfunção cardíaca. Assim, visamos
contribuir para alicerçar o caminho para a compreensão da patogênese da DC e o
desenvolvimento de estratégias terapêuticas racionais e potencialmente aplicáveis aos
portadores da DC.
3
2. Revisão de literatura
___________________________________________________________________________________
2.1 Panorama das doenças cardíacas
Doença cardíaca é um termo geral para designar diversas condições médicas
crônicas ou agudas que afetam um ou mais componentes do coração. No início do
século XX, as doenças cardíacas eram responsáveis por menos de 10% das mortes em
todo o mundo, enquanto no início do século XXI já são responsáveis por quase 50% das
mortes nos países desenvolvidos e 25% em países em desenvolvimento. Apesar do
grande avanço ocorrido na segunda metade do século em termos de fisiologia cardíaca,
dos meios para diagnóstico e para o tratamento das doenças cardíacas, sua incidência
alcançou proporções epidêmicas e permanece como a principal causa de morte no
mundo (Ministério da Saúde 2006). Um estudo de 2006 sobre projeções de mortalidade
em nível global mostrou que no período de 2002-2030 as doenças cardiovasculares
serão as maiores responsáveis por mortes no mundo (Mathers & Loncar 2006).
No Brasil, em 2002, as doenças que atingem o coração representaram 31% do
total de mortes, superando em mais de duas vezes a segunda causa, as neoplasias. As
doenças cardíacas ainda são responsáveis por alta frequência de internações,
ocasionando elevados custos médicos e socioeconômicos (Documento do Banco
Mundial 2005; DATASUS 2009). No ano de 2003, o maior custo nas internações pagas
pelo SUS correspondeu às doenças cardiovasculares (20% do total), dentre as quais a IC
é a principal causa de internação (Carvalho et al., 2008; Moura et al., 2011).
A IC é uma síndrome clínica complexa de caráter sistêmico e mau prognóstico.
É definida como disfunção cardíaca que ocasiona inadequado suprimento sanguíneo
para atender as necessidades metabólicas tissulares, na presença de retorno venoso
normal, ou fazê-lo somente com elevadas pressões de enchimento. No Brasil, a
principal etiologia da IC é a cardiopatia isquêmica crônica associada à hipertensão
arterial. Também podem levar à IC, alterações nas válvulas cardíacas, níveis não
controlados de pressão arterial, inflamações do músculo cardíaco, doença de Chagas e
outras causas (Bocchi et al., 2009).
4
2.2 Doença de Chagas
Em abril de 1909, Carlos Chagas comunicou ao mundo científico a descoberta
de uma nova doença humana, que denominou tripanossomíase americana (Chagas,
1909), posteriormente chamada DC. O agente etiológico da doença, o protozoário
flagelado Trypanosoma cruzi, e seu vetor, os triatomíneos, também haviam sido
identificados por ele, ao final de 1908. A descoberta de Chagas, considerada única na
história da medicina, constitui um marco decisivo na história da ciência e da saúde
brasileira. Por determinar uma condição inflamatória crônica, cuja patogenia é
amplamente questionada e que pode impossibilitar o indivíduo de exercer suas
atividades, esta doença tem grande importância no âmbito da saúde pública. Hoje,
mesmo após mais de cem anos de sua descoberta, a Organização Pan-Americana de
Saúde (OPAS) e a Organização Mundial da Saúde (OMS) estimam que 7-8 milhões de
pessoas estão cronicamente infectadas pelo T. cruzi e 10-14 mil mortes por ano são
causadas pela DC (Rassi Jr et al., 2012; Salvatella, 2013; WHO 2014). Há ainda a
questão importante que se refere à migração das populações latinas para outras partes do
mundo, levando à globalização da DC, que deixa de ser uma doença exclusivamente de
países pobres (Rassi et al., 2010; Bonney, 2014). A DC também é importante devido ao
fardo econômico que gera (Lee et al., 2013). A mortalidade precoce e substancial
invalidez causada por esta doença, que muitas vezes acomete a população em idade
mais produtiva, adultos jovens, resulta em uma perda econômica significativa (FrancoParedes et al., 2007). Nos países latino-americanos, a DC é uma das doenças mais
onerosas das chamadas "doenças tropicais negligenciadas" e à medida que a doença se
expande para além da América Latina, há uma preocupação crescente no que diz
respeito ao seu fardo econômico global (Lee et al., 2013).
2.3 Ciclo evolutivo do parasito e formas de transmissão da doença
O T. cruzi é um protozoário digenético, hemoflagelado da ordem Kinetoplastida
e família Trypanosomatidae, que apresenta diversas formas evolutivas em seu ciclo
biológico, sendo encontradas em organismos vertebrados ou no inseto vetor. No homem
e em outros vertebrados, o parasito apresenta-se sob a forma tripomastigota no sangue
periférico e a forma amastigota intracelular em todos os tecidos. O parasito se multiplica
5
apenas na forma intracelular por divisão binária. No inseto vetor, o desenvolvimento do
T. cruzi é extracelular e se processa no trato gastrointestinal, no qual são encontradas
formas epimastigotas, que se dividem, e tripomastigotas metacíclicas infecciosas. Estes
são depositados com as fezes e urina na pele do hospedeiro vertebrado na ocasião da
picada. A picada dos triatomíneos não é dolorosa, sendo facilitada por propriedades
anestésicas e anticoagulantes da saliva do inseto. No entanto, pode ser pruriginosa e
provocar fortes reações alérgicas. Em condições normais, os triatomíneos têm atividade
noturna e exercem sua hematofagia à noite, atraídos pela temperatura da pele e pelo teor
superficial de CO2 dos mamíferos. Desta forma, picam principalmente o rosto das
pessoas adormecidas (daí o nome de barbeiro). Quando um triatomíneo deposita as
fezes e urina na pele lesionada ou mucosa do hospedeiro vertebrado, as formas
tripomastigotas metacíclicas penetram ativamente em células do sistema fagocítico
mononuclear e se diferenciam em amastigotas; estas se multiplicam intensamente e
diferenciam para formas tripomastigotas. Em seguida, estas formas rompem a célula
hospedeira e caem na corrente sanguínea. As formas tripomastigotas penetram em
células vizinhas ou mais distantes (musculares ou nervosas, por exemplo), diferenciamse em amastigotas e repetem o ciclo. Quando o triatomíneo suga o sangue contaminado
do hospedeiro vertebrado ocorre diferenciação das formas tripomastigotas sanguíneas
em formas epimastigotas no estômago do barbeiro, estas se multiplicam intensamente
por divisão binária no intestino. Em seguida, há a diferenciação em formas
tripomastigotas metacíclicas na ampola retal, as quais são liberadas e são capazes de
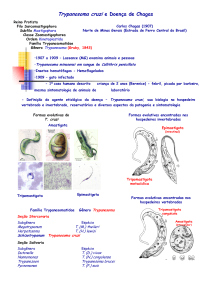
infectar os hospedeiros vertebrados (Figura 1) (Brenner & Andrade, 1979; de Souza et
al., 2008). Normalmente, um barbeiro se torna capaz de transmitir formas infectantes 20
dias após o repasto contaminante e pode permanecer assim durante um ano, que é
aproximadamente o tempo de vida do inseto.
No peri-domicílio o triatomíneo abriga-se nas imperfeições das casas de pau-apique e das construções e justifica a relação direta entre pobreza e o risco de infecção
(Miles, 2003). No Brasil, apesar do sucesso no controle do principal vetor (Triatoma
infestans), vetores autóctones começam a ter importância epidemiológica, como o
T. brasiliensis. Atualmente, o controle e eliminação de populações domésticas de
triatomíneos possui duas estratégias de efeito, que são o uso de inseticidas de ação
residual e a melhora das habitações. Apesar da redução da transmissão vetorial, no
Brasil, novas formas de infecção começam a se tornar epidemiologicamente
6
importantes, como a infecção oral por alimentos contaminados por insetos ou suas
excretas e/ou fragmentos contendo o parasito. Considerada esporádica e circunstancial
em humanos, tem se tornado frequente na região amazônica e está relacionada à
ocorrência de surtos recentes de fase aguda da doença em diversos estados brasileiros,
principalmente na Região Norte (Ianni & Mady, 2005). Essa é uma via natural de
disseminação do T. cruzi entre os animais no ciclo silvestre, que se alimentam de
insetos (Dias, 2006). Outro meio de transmissão relevante da DC é a transmissão
congênita (OPAS, 2007). Ocorre principalmente por via transplacentária, tanto na fase
aguda quanto na fase crônica da infecção, podendo ocorrer em qualquer período da
gestação. Também pode ocorrer no canal do parto, através do contato de mucosas do
feto com o sangue da mãe contaminado pelo T. cruzi (Gontijo et al, 2009). Além disso,
o transplante de órgãos e a transfusão de sangue também são formas de transmissão da
DC, que podem ocorrer quando não há triagem nos bancos de órgão e sangue (Silva,
2010; Moraes-Souza, 2011). Acidentalmente, a transmissão também pode ocorrer pelo
contato do parasito com alguma lesão na pele, mucosa oral ou auto-inoculação,
principalmente por indivíduos que trabalham em laboratório manipulando o parasito no
sangue de animais, fezes de triatomíneos, material de pacientes ou vetores infectados.
Diante destas situações, faz-se importante ressaltar a necessidade das medidas de
biossegurança (Neves et al., 2005; Cimermam, 2008; Dias, 2011).
Novos desafios surgem para as próximas décadas visando à manutenção do
controle da DC, tais como: (i) a vigilância epidemiológica (entomológica e sorológica) e
dos bancos de sangue, (ii) a busca de métodos de diagnóstico para a fase crônica e de
novas drogas tripanossomicidas, (iii) a atenção integral aos pacientes, particularmente às
crianças e mulheres em idade fértil, mas também aos pacientes cronicamente infectados
(Lannes-Vieira et al., 2010).
7
Figura 1: O ciclo biológico do T. cruzi. O T. cruzi é naturalmente transmitido pelo inseto hemíptero
(barbeiro) da família Reduviidae. Durante o repasto sanguíneo, o inseto deposita na pele do hospedeiro
vertebrado as fezes contendo a forma infectante do parasito (1). Em seguida, a forma tripomastigota
metacíclica alcança o tecido subjacente e a corrente sanguínea do hospedeiro através da picada do inseto,
pelo espalhamento até áreas lesionadas ou pelas mucosas. Nos hospedeiros mamíferos, formas
tripomastigotas penetram em células locais (2) e se diferenciam em amastigotas; que são formas
intracelulares e reprodutivas do parasita (3). Ocorre uma nova diferenciação para forma infectante
tripomastigota sanguínea (4) causando o rompimento da célula e liberação dos parasitos na circulação (5).
Estes podem invadir novas células, ficar no sangue (6) ou colonizar outros tecidos. Os hemípteros são
infectados quando ingerem formas tripomastigotas durante o seu repasto sanguíneo (7). No hospedeiro
invertebrado, as formas tripomastigotas ingeridas evoluem para as formas epimastigotas (8), as quais se
multiplicam intensamente ao longo do intestino médio do inseto (9) e ao atingirem a ampola retal
diferenciam-se em tripomastigotas metacíclicos (10), que são formas infectantes para o hospedeiro
mamífero (Criação Coletiva do LBI/IOC).
2.4 Patogenia da doença de Chagas
A DC caracteriza-se por apresentar duas fases clínicas: a fase aguda e a fase
crônica. A fase aguda ocorre logo após a infecção, sendo caracterizada pela presença de
parasitos circulantes no sangue periférico, resultado da replicação do parasito nos
tecidos alvo da infecção. Nos tecidos é possível detectar o parasito sob a forma de
ninhos de amastigotas. Nesta fase, nos tecidos alvos da infecção encontram-se intensos
infiltrados inflamatórios. Na fase aguda, em grande parte dos indivíduos a doença é
8
assintomática ou a sintomatologia pode passar despercebida. Porém, parte dos pacientes
pode apresentar inflamação no tecido cardíaco (miocardite) com alterações elétricas
transitórias, e/ou no sistema nervoso central (meningoencefalite), que é grave em
indivíduos imunocomprometidos ou crianças (Silva et al., 2010; Sanches et al., 2014). A
inflamação tecidual tende a diminuir após a fase aguda da infecção (Andrade, 2000;
Rassi Jr et al., 2010; Silva et al., 2010). Passada esta fase (com duração de 1-3 meses), a
doença entra na fase crônica, caracterizada por níveis sub-patentes de parasitos no
sangue e raros ninhos de formas amastigotas nos tecidos, sendo antígenos e material
genético do parasito detectados no tecido cardíaco e sangue por técnicas de
imunoistoquímica ou biologia molecular, respectivamente (Reis et al., 1993; Jones et
al.,1993; Moreira et al., 2013).
A fase crônica apresenta as seguintes formas: indeterminada, cardíaca, digestiva
e cardio/digestiva (ou mista) (Rassi et al., 2012). A forma indeterminada é a forma da
DC mais frequente em estudos populacionais em zonas endêmicas (Dias, 2007). Após
quatro a dez semanas de infecção, inicia-se a forma indeterminada da fase crônica,
caracterizada
pela
positividade
sorológica
e/ou
parasitológica,
ausência
de
manifestações clínicas, eletrocardiográficas ou radiológicas próprias da doença
(Consenso Brasileiro em Doença de Chagas, 2005). Enquanto alguns pacientes
permanecem nessa forma indefinidamente, outros, geralmente após intervalo de 20 a 30
anos, evoluem para alguma das formas crônicas determinadas da doença, com
surgimento de evidências de comprometimento cardíaco e/ou digestivo (Rassi et al.,
2012).
A forma cardíaca é caracterizada pela presença de infiltrados inflamatórios,
lesão nas fibras cardíacas e consequente remodelamento do tecido e fibrose, associados
à disfunção cardíaca crônica. Com o progresso da lesão tecidual ocorrem alterações
cardíacas, como a perda do tônus muscular, arritmias, dilatação do coração, aneurisma
apical, diminuição da fração de ejeção e IC (Laranja et al., 1953; Higuchi et al., 2003;
Rassi et al., 2012). Já a forma digestiva é caracterizada por alterações na secreção
gástrica, motilidade, absorção e, nos casos mais graves, pelo aumento do tubo digestório
em consequência de alterações nos plexos nervosos, principalmente no plexo
mioentérico, sendo o megaesôfago e o megacólon as formas mais comuns (Andrade et
al., 1983; Brener & Krettli, 1990; Meneghelli, 2004).
9
2.5 Cardiomiopatia chagásica crônica
A CCC é essencialmente uma miocardiopatia dilatada em que inflamação
crônica persistente provoca destruição tecidual progressiva e fibrose extensa no coração
(Marin-Neto et al., 2007). A destruição das fibras miocárdicas pelo processo
inflamatório e a sua substituição por tecido fibroso atinge um limite crítico, fazendo
com que os ventrículos se remodelem frente à perda gradativa dos elementos contráteis.
Inicialmente, no remodelamento ventricular ocorre hipertrofia das fibras íntegras e,
posteriormente, dilatação da cavidade ventricular. Essa hipertrofia extrínseca restaura
temporariamente o volume sistólico já comprometido, mas a dinâmica do processo leva
à dilatação cardíaca crescente, com perda progressiva da capacidade de ejeção
ventricular em virtude da evolução da miocardite e da sobrecarga mecânica. Nos
estágios mais avançados, além do componente sistólico, também se intensifica um
componente de restrição diastólica, devido à grande dilatação e enrijecimento cardíacos
pela fibrose (Acquatella et al., 2007). Contribuem ainda para o agravamento da
cardiopatia, as arritmias ventriculares complexas, o tromboembolismo pulmonar
repetido e a insuficiência das válvulas mitral e tricúspide (Dias & Coura, 1997; MarinNeto et al., 2007).
Com base em evidências de ordem experimental e clínica firmadas
recentemente, existe um consenso de que a essência da patogenia da CCC resida em
uma inflamação diretamente dependente da persistência parasitária e que esta, por sua
vez, desempenhe um papel no desenvolvimento e progressão da CCC (Higuchi et al.,
2003; Zacks, 2005; Biolo, 2010). As células T são o tipo predominante de células em
lesões inflamatórias na CCC (Reis et al., 1993). Além disso, citocinas reguladoras e próinflamatórias, como as IL-10, IL-4, IL-6, IFNγ, TNF e o fator de transformação do
crescimento beta (TGF-β), têm sido encontradas no sangue periférico de pacientes
crônicos com a forma indeterminada e com a forma cardíaca da DC (Vitelli-Avelar et
al., 2008; Perez et al., 2011). Outro ponto importante é que a progressão da gravidade da
CCC está associada ao aumento no dano oxidativo particularmente às proteínas, lipídios
cardíacos e às mitocôndrias (Wen, 2004; Oliveira, 2007). Vários estudos têm sugerido
que alterações na atividade da cadeia respiratória mitocondrial, principalmente
complexo I (NADH-ubiquitonaoxiredutase) e III (ubiquinol-citocromo c redutase),
estejam relacionadas com a geração de espécies reativas de oxigênio (ROS) e espécies
10
reativas de nitrogênio (RNS) no coração de portadores da DC, contribuindo para o dano
oxidativo (Wen, 2004; Oliveira, 2007). Desta forma, é de suma importância entender os
mecanismos moleculares que controlam a geração e progressão da CCC, para que assim
possamos desenhar estratégias de intervenção racional que levem ao controle do
parasitismo, de forma dissociada da inflamação potencialmente envolvida na geração de
fibrose e disfunção cardíaca (Lannes-Vieira 2003; Marino et al. 2004).
2.6 Resposta imunológica na infecção pelo T. cruzi
2.6.1 Aspectos gerais
Na infecção pelo T. cruzi há mobilização de diversos mecanismos efetores do
sistema imune, havendo a ativação de células e moléculas relacionados à imunidade
inata e à imunidade adquirida ao longo das fases da doença. Consequentemente, o
parasito passa a ser continuamente alvo do sistema imune e tem sua multiplicação
reduzida nos tecidos do hospedeiro. No entanto, a persistência deste parasito leva à
atividade prolongada do sistema imune, podendo culminar no aparecimento de lesões
teciduais e, eventualmente, em alterações funcionais musculares e nervosas
características da DC (Rassi et al., 2010; Marin-Neto et al., 2007). As células e
mecanismos efetores do sistema imune seriam então responsáveis, tanto pelo controle
da multiplicação do parasito nos tecidos como pelas lesões locais resultantes da
atividade anti-parasitária.
2.6.2 Imunidade inata e adaptativa
Diversos mecanismos efetores humorais e celulares estão envolvidos na resposta
imune do hospedeiro frente à infecção pelo T. cruzi (Junqueira et al., 2010). O
reconhecimento imune inato depende de um número ilimitado de receptores. Esses
receptores de reconhecimento de padrões (PRRs) estão envolvidos na identificação de
padrões moleculares associados aos patógenos (PAMPs) (Abbas & Lichtman, 2002).
Dentre os diversos PRRs, proteínas transmembrana denominadas de receptores do tipo
Toll (TLR) são os mais bem estudados. Membros dessa família reconhecem
componentes essenciais dos mais variados microorganismos (Tarleton, 2007).
Diferentes grupos identificaram moléculas no T. cruzi que atuam como agonistas dos
11
receptores TLR, induzindo a produção de NO e a secreção de citocinas e quimiocinas
em células de linhagem monocítica (revisado em Rodrigues et al., 2012). Dentre essas
moléculas destacam-se as âncoras de glicosil-fosfatidil-inositol (GPI), as GPI ligadas
covalentemente às glicoproteínas semelhantes a mucinas, as GPI-mucinas, e a enzima
trans-sialidase (TS) (Gazzinelli & Denkers, 2006; Tarleton, 2007). A ativação dos TLR
utiliza principalmente a via de transdução de sinal que consiste no recrutamento de
várias proteínas intracelulares (MyD88, IRAK e TRAF-6) que vão desencadear as vias
Jun-N-terminal quinase (JNK), e quinases que regulam sinal extracelular (ERK) da
cascata MAP quinase (MAPK), envolvidas na ativação dos fatores de transcrição AP-1
(proteína ativadora 1) e NF-κB (fator nuclear κB), favorecendo a expressão de genes
envolvidos na resposta inflamatória (Abbas & Lichtman, 2002; Kawai & Akira, 2011).
O NF-κB é um fator de transcrição, ativado em resposta a sinais incluindo o CD3
associado ao receptor de antígenos de células T (TCR), essencial na síntese de citocinas
(Abbas & Lichtman, 2002; Kawai & Akira, 2011). O fator de transcrição NF-κB é
importante na transcrição de muitos genes em vários tipos de células, particularmente
nas células do sistema imune (Abbas & Lichtman, 2002; Kawai & Akira, 2011). A
ativação de células apresentadoras de antígenos (APCs) via os TLRs 2, 4 e 6 leva à
indução de genes de citocinas pró-inflamatórias tais como o TNF, o IFNγ e a IL-12
(Campos & Gazzinelli, 2004).
A imunidade inata apresenta componentes clássicos, como as células dendríticas,
macrófagos e células natural killer (NK), que têm um papel crucial na imunidade
parasitária e principalmente anti-T. cruzi (Junqueira et al., 2010). As células NK são de
grande importância na imunidade inata contra o T. cruzi, limitando o crescimento
parasitário e promovendo o desenvolvimento da imunidade adquirida (Scott &
Trinchieri, 1995). Além disso, a invasão de macrófagos leva à secreção de IL-12, que
ativa as células NK a produzirem IFNγ (Aliberti et al., 1996), que atua reciprocamente
sobre macrófagos ativando-os para a atividade microbicida (Gazzineli et al., 1992). A
citocina pró-inflamatória TNF, produzida por macrófagos durante a infecção pelo
T. cruzi, participa dessa interação de forma sinérgica tanto com IL-12 como com IFNγ
(Muñoz-Fernandez et al., 1992).
Os macrófagos ativados produzem altos níveis de citocinas pró-inflamatórias e
produtos microbicidas, como: peróxido de hidrogênio (H2O2), peroxinitrito (ONOO-) e
NO. Contudo, apesar de extensas investigações experimentais, o mecanismo usado pelo
12
macrófago ativado para eliminar o T. cruzi ainda não é totalmente entendido (Fabrino et
al., 2011). A produção de grandes quantidades de NO, através da NO sintase induzível
(iNOS) pelos macrófagos, é proposta como uma das principais vias para a morte do
parasito (Silva et al., 2003; Fabrino et al., 2010). Entretanto, tem sido demonstrado que
nem a produção de NO nem iNOS (Cummings & Tarleton, 2004; Marinho et al., 2007)
são essenciais para o controle in vivo do T. cruzi em camundongos.
Ao analisar os infiltrados inflamatórios do tecido cardíaco de pacientes da DC, é
possível observar grande quantidade de células T CD4+ e T CD8+, com predomínio das
células CD8+ (relação aproximada de 2:1 - CD8+:CD4+) (Higuchi et al., 1993). Nas
diferentes formas da fase crônica, indeterminada, cardíaca e digestiva foi observado que
o maior percentual de células T CD8+ estava associado às formas mais graves da DC
(Vitelli-Avelar et al., 2005). O predomínio destas células no tecido cardíaco é proposto
estar relacionado à expressão de moléculas de adesão celular (CAMs) (Dos Santos et
al., 2001, Lannes-Vieira 2003). Estas são glicoproteínas expressas na superfície celular,
importantes no processo de migração, sendo responsáveis pela adesão firme de
linfócitos circulantes no sangue periférico com células do endotélio. No endotélio
vascular adjacente ao tecido em situação de infecção ou injúria, alguns mediadores
induzem a expressão de CAMs, assim o tecido torna-se permissivo à interação com
células
inflamatórias
(Sigmoundsdottir
&
Butcher,
2008).
Michailowsky
e
colaboradores (2004) demonstraram a importância da molécula de adesão intercelular
do tipo 1 (ICAM-1) na formação da miocardite chagásica. Camundongos geneticamente
deficientes em ICAM-1 (icam1-/-) foram altamente susceptíveis à infecção pelo T. cruzi.
Neste modelo, o elevado parasitismo estava associado à diminuição do número de
células T inflamatórias (CD4+ e CD8+) no tecido cardíaco, suportando que ICAM-1
desempenha um papel crucial no recrutamento de linfócitos T para o tecido cardíaco,
estando pelo menos parte das células que migram na dependência de ICAM-1
envolvidas no controle do parasito e na susceptibilidade do hospedeiro durante a
infecção pelo T. cruzi.
Em relação aos receptores de quimiocinas, as células T (CD4+ e CD8+) e
monócitos do sangue periférico de pacientes de DC apresentam frequência aumentada
de CCR5 (Gomes et al., 2005). De modo interessante, as células inflamatórias presentes
no tecido cardíaco, bem como nas células T CD8+ do sangue periférico de camundongos
infectados pelo T. cruzi, expressam maior frequência de CCR5 (Marino et al., 2004;
13
Machado et al., 2005; Medeiros et al., 2009). O tratamento com Met-RANTES
("regulated on activation normal T cell expressed and secreted"), antagonista parcial
que se liga aos receptores CCR1 e CCR5 em camundongos (Proudfoot et al.,1999),
controla a formação da miocardite, diminuindo o recrutamento de células T CD4+ e
CD8+, sem alterar o parasitismo cardíaco, resultando no aumento da sobrevida dos
animais. Assim, o tratamento com Met-RANTES demonstrou que o influxo massivo de
células inflamatórias, em especial as CCR5+, para o tecido cardíaco não é crucial para a
resposta anti-T. cruzi (Marino et al., 2004; Medeiros et al., 2009).
Vários trabalhos têm mostrado o papel não somente das células T CD8+, que
serão melhor exploradas a diante, mas também das células T CD4+ e das células B, no
aumento da sobrevida, assim como no controle do parasitismo durante a infecção
chagásica (Tarleton, 1990; Kumar & Tarleton, 1998; Padilla et al., 2009). Alguns
trabalhos sugerem que linfócitos T-CD4+ constituam as principais populações celulares
envolvidas no perfil regulador em pacientes com forma indeterminada da DC. Além
disso, verificou-se que monócitos e linfócitos T CD4+ também determinam o perfil
inflamatório em indivíduos com cardiomiopatia, uma vez que apresentaram maior
frequência de TNF (Vitelli-Avelar et al., 2008). Uma subpopulação de células T
(CD4+CD25+FoxP3+) com capacidade reguladora (Treg) tem sido descrita como uma
classe de células que regula a resposta imune, tendo a capacidade de controlar resposta
imune excessiva a patógenos ou a antígenos próprios (Sakaguchi et al., 2010). Dados da
literatura já mostraram que pacientes com a forma indeterminada da DC apresentam
maior percentual de células CD4+CD25highFoxP3+ produtoras de IL-10, enquanto que
pacientes cardiopatas apresentaram maior percentual de células CD4+CD25highFoxP3+
expressando CTLA-4 (antígeno 4 de linfócito T citotóxico). Estes dados sugerem que as
células Treg podem ter um papel na resposta imune contra a infecção pelo T. cruzi,
embora com efeitos distintos em pacientes com as diferentes formas da doença (Araújo
et al., 2007). Um estudo na fase aguda da infecção experimental pelo T. cruzi mostrou
que a inativação das células CD4+ CD25+ leva a um pequeno aumento da resistência à
infecção pela cepa Colombiana do T. cruzi e que a maior resistência foi associada a uma
maior ativação das células CD4+ e à produção de IFNγ (Sales-Junior et al., 2008). Por
outro lado, os autores não observaram nenhum papel significativo para estas células na
patogenia da CCC experimental. De fato, os caminhos que levam à regulação da
resposta imune na infecção pelo T. cruzi não estão totalmente elucidados. Especula-se
14
que a expansão de células Treg possa ser benéfica durante a fase crônica da doença por
limitar o dano tecidual, suprimindo a atividade das células T efetoras, mantendo o
indivíduo na forma indeterminada da DC, entretanto os mecanismos pelos quais isso
acontece necessitam ser esclarecidos (Martins et al., 2004).
O CTLA-4 é um receptor co-estimulátório negativo que se liga ao CD80 e CD86
(Salomon & Bluestone, 2001). O bloqueio de CTLA-4 com anticorpos aumentou a
produção de IFNγ e NO por esplenócitos e aumentou a resistência à infecção pelo
T. cruzi (Martins et al., 2004). Por outro lado, a co-estimulação com CTLA-4 reduz a
resposta imune do hospedeiro a infecções, uma vez que CTLA-4 pode reduzir a ativação
de células T (Salomon & Bluestone, 2001). Nas populações de linfócitos T clássicos
(CD4+ e CD8+) provenientes de pacientes com cardiomiopatia dilatada observou-se uma
expressão elevada de CTLA-4 intracelular, enquanto que a expressão de superfície
dessa molécula foi baixa (Souza et al., 2007). Esses autores sugeriram que pacientes
com CCC apresentam uma deficiência na expressão membranar dessa molécula. Nesse
mesmo trabalho foi observado um aumento da expressão de CTLA-4 nos pacientes com
a forma indeterminada, especialmente nos linfócitos T CD8+. Anticorpos anti-CTLA-4
já foram propostos para o tratamento de cânceres (Kwek et al., 2012). Recentemente, foi
mostrado que o bloqueio de CTLA-4 durante a vacinação terapêutica com uma cepa
atenuada do T. cruzi (CL) expressando NY-ESO-1 (antígeno expresso em uma
variedade de tumores como melanomas, câncer de pulmão e próstata - neste caso o
T. cruzi serviria como um vetor vacinal) em um modelo experimental de melanoma
(células B16-NY-ESO-1 injetadas via subcutânea) aumentou a frequência de células T
CD8+ específicas produtoras de IFNγ e promoveu a migração de linfócitos efetores para
o tumor controlando o seu crescimento, propondo esta estratégia para estimular a
resposta imune específica (dos Santos et al., 2014).
Em suma, a resposta imune tem sido alvo de diversos estudos na infecção pelo
T. cruzi. É proposto que a resistência à infecção esteja relacionada a uma resposta aguda
pró-inflamatória que contém os parasitos. Entretanto, com a persistência do parasito, há
manutenção dessa robusta atividade pró-inflamatória, que está associada à evolução
para a forma crônica grave da DC (Dutra et al., 2009; Perez et al., 2011). Neste sentido,
faz-se necessário o entendimento da relação controle do parasito/inflamação a fim de
identificar alvos terapêuticos para a interferência neste sistema e possível melhora no
quadro clínico.
15
2.6.3 Células T CD8
Visto que o T. cruzi é um parasito intracelular, a resposta mediada por células,
principalmente relacionada à ativação dos linfócitos T CD8+ é um evento fundamental
no combate à infecção. Os primeiros dados que apontaram para a participação dos
linfócitos T CD8+ na imunoproteção contra o T. cruzi foram observados em
camundongos desprovidos de linfócitos T (por timectomia neonatal, por inativação por
anticorpos anti-CD4 ou anti-CD8 ou geneticamente modificados). Estes dados mostram
que ambas as populações, CD4+ e CD8+, são essenciais para o controle da parasitemia e
sobrevivência do hospedeiro nas fases aguda e crônica da infecção (Rottenberg et al.,
1993; Tarleton et al., 1994; Cotta-de-Almeida et al., 1997). Ainda, a ausência de células
T CD8+ em camundongos mutantes para o gene da β2-microglobulina resultou no
aumento da susceptibilidade à infecção (Tarleton et al., 1992), sugerindo que estas
células possuem papel central no controle da resposta imune da DC.
Devido à habilidade dos linfócitos T CD8+ secretar diversas citocinas e atuar
diretamente em células-alvo infectadas (Harty & Badovinac, 2002), estas células têm
sido relacionadas tanto à resistência ao parasito quanto com a patogenicidade da DC
(Lannes-Viera, 2003). A demonstração de que células CD8+ predominam em sítios
inflamatórios no coração de portadores da DC (Higuchi et al., 1993; Reis et al., 1993)
sugere a participação dessas células na lesão cardíaca da fase crônica. Em termos
efetores, os linfócitos T CD8+ podem conter a infecção por inúmeros mecanismos,
incluindo a secreção de citocinas, o que induz a produção de atividades microbicidas na
célula hospedeira, e também por atividades citotóxicas por meio da secreção de Pfn e
granzimas, assim como a ativação da via Fas/FasL (CD95/CD95L) (Martin & Tarleton,
2004). Embora os mecanismos de indução de morte pela liberação de grânulos
citotóxicos sejam bastante estudados, ainda não existe um modelo definido de como a
combinação Pfn/granzima age nas células. A maior parte dos trabalhos mostra que é a
Pfn que “entrega” as granzimas para célula alvo, mas como isto ocorre é ainda um
grande debate na literatura. Trapani & Smyth (2002) revisaram diferentes modelos
propostos no mecanismo de morte por células com atividade citotóxica. A hipótese
inicial é de que a Pfn polimeriza formando um poro na membrana plasmática da célula
alvo por onde passam as granzimas. No entanto, os autores ressaltam o fato de que os
poros formados (15nm) podem ser pequenos demais para a passagem de moléculas
16
grandes como as granzimas. O paradigma foi questionado quando foram publicados
trabalhos mostrando que a Granzima B pode ser endocitada mesmo na ausência de
perforina (Froelich et al., 1996; Shi et al., 1997). A partir destes dados, Froelich e
colaboradores (1996) sugeriram que a Pfn age na membrana do endossoma e contribui
para a liberação da granzima dentro da célula. Pipkin e Lieberman (2007), por outro
lado, propuseram um modelo híbrido, no qual a Pfn forma poros na membrana que leva
ao influxo de Ca+. Este efeito, por sua vez, induz reparo na membrana celular que
termina por englobar as granzimas, que são reconhecidas pelo receptor manose-6fosfato da célula-alvo. Os autores sugerem também que a liberação da granzima deste
endossoma é mediada por Pfn, mas como isto acontece ainda não está elucidado. Juntas,
Pfn e granzimas, terminam por induzir morte celular dependente de caspase na célulaalvo, mas também foram mostradas levar à morte na ausência de caspases ativas (revisto
em Trapani & Smyth, 2002).
Sugere-se que a maior contribuição das células T CD8+ para o combate à
infecção seja a produção de IFNγ, surpreendentemente mais relevante do que a sua
atividade citotóxica (Martin & Tarleton, 2004). Como descrito anteriormente, o efeito
protetor do IFNγ na infecção pelo T. cruzi está relacionado principalmente à sua
capacidade de induzir a produção de IL-12, TNF e, em especial, NO pelos macrófagos.
Vários estudos mostram que o IFNγ também é capaz de induzir a produção de NO em
células musculares, alvo da infecção pelo T. cruzi (Muñoz-Fernandez et al., 1992;
Grazzinelli et al., 1992; Machado et al., 2000; Fichera el al., 2004). A importância do
IFNγ no controle da infecção foi estabelecida por experimentos nos quais a
neutralização por meio do tratamento in vivo com anticorpos monoclonais (Cardillo et
al., 1996) ou a deleção gênica (Martins et al., 1999) do IFNγ aumentou a parasitemia e o
parasitismo.
Em resumo, populações distintas de células T CD8+ podem coexistir durante o
curso da infecção e desempenhar diferentes funções. Dados recentes do nosso grupo
mostram que enquanto as células T CD8+ específicas (que reconhecem o peptídeo H2Kb/VNHRFTLV+ ASP2 do T. cruzi) do baço e sangue periférico de camundongos
infectados pelo T. cruzi são predominantemente Pfn-IFNγ+, no tecido cardíaco existe
um predomínio de células T CD8+Pfn+IFNγ-. Estas células apresentam um
comportamento migratório diferencial, favorecendo o acúmulo das células Pfn+ no
tecido cardíaco, reforçando sua participação na lesão cardíaca (Silverio et al., 2012). A
17
participação das células T CD8+ na infecção pelo T. cruzi não está totalmente elucidada,
sendo necessários maiores estudos tendo como alvo esta população celular tanto em
modelos murinos como em pacientes, acreditando que, assim, novas estratégias
terapêuticas sejam propostas com o objetivo de melhorar a qualidade da resposta de
linfócitos T CD8+ antígeno específicas e com isso prevenir as alterações cardíacas.
2.6.4 Citocinas
A ativação do sistema imune é importante no controle da carga parasitária, por
outro lado, pode levar ao dano tecidual e contribuir para o aparecimento das
manifestações crônicas graves observadas em alguns portadores da DC (Bahia-Oliveira
et al., 1998; Gomes et al., 2003). Dentre os vários fatores imunológicos que têm sido
demonstrados como importantes para o desenvolvimento da forma grave da DC,
destacamos a ativação dos leucócitos e consequente produção e secreção de citocinas.
As citocinas são moléculas solúveis, produzidas e secretadas como produtos celulares
em resposta a patógenos e outros estímulos. Elas medeiam e regulam a resposta imune
por meio de ligações a receptores específicos e podem atuar de forma autócrina,
parácrina ou sistêmica (Abbas & Lichtman, 2002). Estas moléculas estão envolvidas,
tanto na resistência quanto nos mecanismos relacionados à patologia da DC (Silva et al.,
1992; Abrahamsohn & Coffman, 1995; Samudio et al., 1998) e também à gravidade de
outras cardiopatias (Oikonomou et al., 2011).
Dentre as diversas citocinas estudadas na infecção pelo T. cruzi, o IFNγ tem sido
associado tanto em modelos experimentais (Silva et al., 1992; Samudio et al., 1998)
quanto em humanos com a resistência do hospedeiro à infecção (Bahia-Oliveira et al.,
1998, 2000). O IFNγ pode desempenhar papel protetor no desenvolvimento da patologia
chagásica e, em conjunto com uma quimioterapia específica, o IFNγ pode levar à
eliminação do parasito em pacientes na fase aguda da infecção (Bahia-Oliveira et al.,
1998). De forma interessante, a frequência de células T CD8+ produtoras de IFNγ
específicas para T. cruzi foi inversamente correlacionada com a gravidade da DC
(Albareda et al., 2006). Por outro lado, Gomes e colaboradores (2003) demonstraram
que pacientes com a forma grave da CCC apresentam intensa resposta imune contra o
parasito, com altas frequências de células CD4+ expressando IFNγ e baixas frequências
de células CD4+ expressando IL-10, quando comparados com portadores da forma
indeterminada da doença. Estes dados sugerem que altos níveis de IFNγ podem estar
18
associados à patologia da forma cardíaca grave (Gomes et al., 2003). Mais tarde,
Guedes e colaboradores (2009), utilizando modelo canino de infecção pelo T. cruzi,
mostraram que a alta produção de IFNγ e TNF e a baixa produção de IL-10 na fase
aguda estão associadas à CCC. Anos mais tarde, camundongos com diferentes
susceptibilidades à infecção pela cepa Colombiana do T. cruzi, C3H/HeSnJ (100% de
mortalidade, parasitismo descontrolado) e C57BL/6J (<10% de mortalidade,
parasitismo controlado), foram sistematicamente comparados e exibiram diferentes
frequências de células T CD4+ e CD8+ produtoras de IL-10+ e IFNγ+IL-10+ no tecido
cardíaco. Estes dados sugeriram que a IL-10 proveniente de linfócitos T duplo
produtores (IFNγ/IL-10) ou simples produtores (IL-10) poderia impedir a intensa
resposta inflamatória e parasitemia observada nos camundongos C3H/HeSnJ infectados
pelo T. cruzi (Roffê et al., 2012).
O TNF foi mostrado apresentar papel protetor no controle dos parasitos e na
sobrevivência dos camundongos na fase aguda da infecção pelo T. cruzi (Lima et al.,
1997), por outro lado apresentou efeitos deletérios na resposta do hospedeiro na fase
crônica (Perez-Fuentes et al., 2003). Sua participação na patogenia da CCC ainda não
está completamente elucidada (Lannes-Vieira et al., 2011). Em associação com o IFNγ,
TNF induz atividade microbicida em macrófagos (Gazzineli et al., 1992). Contudo,
níveis plasmáticos de TNF estão correlacionados ao grau de disfunção cardíaca em
portadores da CCC (Ferreira et al., 2003; Talvani et al., 2004). Assim, especula-se que
inicialmente TNF teria função protetora na infecção pelo T. cruzi, porém seus elevados
níveis nos soros dos pacientes permitiriam a perpetuação do infiltrado inflamatório e o
exacerbado processo oxidativo, contribuindo para a CCC (Perez-Fuentes et al., 2003;
Lannes-Vieira et al., 2011).
Citocinas como IL-4, IL-10 e TGF-β exibem importante papel regulador na
infecção pelo T. cruzi, inibindo in vitro a produção de NO e a atividade
tripanossomicida de macrófagos infectados e ativados por TNF e IFNγ (Gazzineli et al.,
1992; Roffê et al., 2012). A presença de células IL-4+ no tecido cardíaco foi relacionada
à presença de pseudocistos do T. cruzi em pacientes com CCC grave (Higuchi et
al.,1997, Reis et al.,1997), sugerindo que a IL-4 participe da disseminação do parasito.
Em suporte a esta ideia, animais deficientes em IL-4 exibiram redução de parasitismo e
mortalidade na fase aguda da infecção (Michailowisky et al., 2001). Sendo IL-4 um
importante fator fibrinogênico (Huaux et al., 2003) e estando a fibrose associada à
19
disfunção cardíaca na infecção pelo T. cruzi (Higuchi et al., 2003, Marino et al., 2003),
poderíamos pensar que IL-4 contribui para a fibrose na infecção chagásica. Contudo, a
ausência de IL-4 foi associada à pronunciada inflamação e fibrose na infecção crônica
(Soares et al., 2001), sugerindo que outros fatores contribuam para a fibrose na infecção
chagásica, podendo ser TGF-β um destes fatores (Waghabi et al., 2002). TGF-β é a
principal citocina associada a fibrose. Tanto o TGF-β quanto a citocina anti-inflamatória
ou reguladora IL-10 modulam de forma seletiva a expressão de quimiocinas induzidas
pela infecção pelo T. cruzi (Aliberti et al., 2001), levando ao questionamento se IL-10 e
TGF- β participariam também do controle do influxo de células para o tecido cardíaco.
De fato, o uso de um inibidor da via de sinalização do TGF-β (SB431542) mostrou que
camundongos infectados com a cepa Y do T. cruzi quando tratados na fase aguda da
infecção apresentaram maior sobrevivência, menor parasitemia e menos lesão cardíaca
(analisada sob a forma de ECG e biomarcadores enzimáticos) (Waghabi et al., 2009).
Anos mais tarde, estes dados foram reforçados como uso de um outro inibidor da via de
sinalização
do
TGF-β
(GW788388)
que,
no
mesmo
modelo
experimental
(camundongos Swiss infectados com a cepa Y do T. cruzi), mostrou ser eficiente em
aumentar a sobrevivência dos camundongos infectados, reduzir a parasitemia, e, no
tecido cardíaco, diminuir a fibrose e aumentar a expressão das placas de conexina-43
(Cx43) (Oliveira et al., 2012). Estes dados sugerem que a modulação de citocinas do
perfil regulador também pode ser alvo terapêutico da DC.
A IL-17 é conhecida como uma citocina pró-inflamatória produzida
principalmente por células T CD4+ (Weaver et al., 2006), tem papel chave na resposta
inflamatória em infecções bacterianas e fúngicas, sendo importante na proteção do
hospedeiro contra a infecção pelo T. cruzi na fase aguda (Miyazaki et al., 2010). Células
mononucleares isoladas do sangue periférico de pacientes com diferentes graus de CCC
revelaram que pacientes sem CCC/com CCC leve apresentam alta frequência de células
CD3+CD4+IL-17+, quando comparados com os pacientes com CCC moderada e grave
(Guedes et al., 2012). Recentemente, a alta expressão de IL-17 foi associada a melhor
função cardíaca (dado pelo aumento na fração de ejeção do ventrículo esquerdo FEVE) em portadores da CCC (Magalhães et al., 2013), sugerindo que IL- 17 pode ser
um fator de proteção para lesão no miocárdio. Em outro estudo, a IL-17 se mostrou
aumentada em pacientes com a forma cardíaca da DC (Pérez et al., 2011), revelando
que os dados da literatura são controversos e que a IL-17 precisa ser melhor estudada na
20
infecção pelo T. cruzi. Outro aspecto importante na imunopatogenia da CCC diz
respeito à participação da IL-1β. Postula-se, a partir de estudos em modelos
experimentais, que essa citocina seja um mediador primário da hipertrofia de
cardiomiócitos induzida na infecção pelo T. cruzi (Petersen et al., 2005), tendo papel
primordial na CCC.
Com base nos aspectos imunológicos, a fase crônica da infecção pelo T. cruzi
pode ser caracterizada pelo (des)balanço entre o acúmulo de eficiente resposta imune
(inata e adaptativa) e a presença de poucos parasitos no tecido do hospedeiro (Dos Reis
et al., 1993; Higuchi et al., 1993; Jones et al., 1993), que mantém o sistema
constantemente ativado, favorecendo o aparecimento das manifestações clínicas graves
da doença na fase crônica (Figura 2) (Dutra et al., 2009). Portanto, interferir
racionalmente nesse circuito pode ser a chave para um bom prognóstico da doença.
2.7 TNF e sua sinalização
O TNF é sintetizado por diversos tipos celulares, tais como macrófagos, células
dendríticas, linfócitos T e cardiomiócitos, como uma proteína homotrimérica
transmembranar de 26 kDa (Tracey et al., 2008), sendo um importante regulador da
imunidade e inflamação, bem como da diferenciação e da morte celular (Clark, 2007).
TNF é sintetizado em resposta à inflamação, infecção ou injúria e subsequentemente
clivado por uma metaloproteinase, a TNF- convertase (TACE) que libera o peptídeo
solúvel de 17 kDa. A citocina TNF é um potente mediador inflamatório e tem sua
atividade biológica reconhecida pelas células através dos receptores p55/TNFR1
(CD120a) e p75/TNFR2 (CD120b), ambos estão presentes na maioria dos tipos de
células e tecidos e participam de processos biológicos agindo de forma conjunta ou
distinta (Brockhaus et al., 1990; Hohmann et al., 1990; Lewis et al., 1991; Tartaglia &
Goeddel, 1992; Curtin & Cotter, 2002). Estes receptores apresentam homologia em suas
regiões extracelulares, contendo em suas estruturas sequências ricas em cisteína que
formam os domínios de ligação do TNF, mas diferem em seus domínios intracelulares
(Bradley et al., 1995). A afinidade de ambos os receptores para o TNF solúvel é
semelhante, porém o TNF de membrana pode interagir preferencialmente com TNFR2
(Waters et al., 2013). Existem ainda os receptores solúveis de TNF (sTNFR), que
21
possuem a mesma estrutura que o receptor de membrana e apresentam função biológica
de captar TNF solúvel e posteriormente liberá-lo, e, assim, controlar a sua
biodisponibilidade. Os receptores TNFR1 e TNFR2 não são apenas receptores de TNF,
mas também de outros membros da superfamília TNF, como a linfotoxina (LTA)
(MacEwan, 2002; Ruddle et al., 2014).
A
B
Figura 2: Citocinas e populações celulares envolvidas na geração de proteção e patogenicidade na fase
crônica da doença de Chagas. Pouco tempo após a infecção pelo Trypanosoma cruzi a parasitemia é
controlada e os pacientes entram na fase crônica da doença. Nesta fase, as respostas imunes diferenciadas
podem ser a chave que permite definir o estabelecimento de um quadro mais regulado que controla o
parasito (A- forma indeterminada) vs uma resposta desregulada que continua a controlar o parasito mas
leva a patologia (B- formas cardíaca e digestiva). A interação inicial entre o parasito e o hospedeiro é
fundamental no estabelecimento do controle efetivo da parasitemia e ao mesmo tempo é crítico na
formação de citocinas, que vão orquestrar a ativação e diferenciação de populações de células T
reguladoras e efetoras. Dependendo do equilíbrio entre as subpopulações de células T biologicamente
ativas a resposta global será bem sucedida em manter a forma clínica indeterminada ou progredir para as
formas mais graves (cardíacas ou digestivas). As células T estão presentes em todas as formas clínicas
produzindo citocinas inflamatórias e reguladoras, no entanto estudos recentes demonstraram diferenças
entre as formas clínicas em termos de produção relativa de citocinas inflamatórias (TNF e IFNγ) e
expressão de moléculas reguladoras (IL-10 e CTLA-4). Além disso, vários outros fatores influenciam na
progressão diferencial dos indivíduos nas formas clínicas da doença de Chagas, incluindo a cepa do
parasito, a carga inoculada, fatores ambientais tais como experiências imunológicas anteriores, nutrição e
genética do hospedeiro. Modificado de Dutra et al., 2009.
22
O TNF induz proliferação, diferenciação celular e inflamação através da
ativação de proteínas quinases e fosfatases, tendo como vias sinalizadoras conhecidas a
JNK/AP1, P38MAPK e NF-κB, sendo a última preferencialmente envolvida com
ativação de respostas inflamatórias (MacEwan et al., 2002). Na ausência do ligante, o
domínio citoplasmático de TNFR1 está associado com uma proteína silenciadora do
domínio de morte (SODD) (Figura 3). A ligação do TNF ao receptor promove
mudanças conformacionais neste, que induzem a dissociação da SODD e, por
conseguinte, a exposição dos domínios de morte, que podem recrutar as moléculas
TRADD (proteína do domínio de morte associada ao receptor de TNF), sua principal
via de sinalização (Ihnatko et al., 2007). A TRADD inicia a sinalização associando-se a
RIP-1 (proteína de interação com receptor quinase 1) e a TRAF-2 (fator associado ao
receptor de TNF-2), formando o complexo I que se destaca do TNFR1 após a
internalização do receptor (Bradley, 2008). Antes de separar-se do receptor, esta
estrutura mobiliza a via de NF-κB, através da ativação de IKK (IκB quinase), um
complexo formado por duas subunidades, uma catalítica (IKK-α) e uma reguladora
(IKK-β), que leva à fosforilação de IκB-α, que pode servir de sinal para a posterior
ubiquitinação e degradação desta proteína. Este evento libera o NF-κB, anteriormente
retido no citoplasma pela associação com IκB-α, o que permite sua translocação para o
núcleo, onde poderá regular a transcrição de diversos genes (Figura 3). Em paralelo com
a sua atuação em NF-kB, o TNFR1 pode ativar outras proteínas como MAP3Ks,
iniciando cascatas de sinalização que conduzem à ativação de JNK e p38 MAP quinase
que, por sua vez, influenciam decisões de morte ou sobrevivência celular (Figura 3)
(Kassardjian & Kreydiyyeh, 2008).
O TNFR2 não possui domínio de morte em sua porção citoplasmática e por isso,
assim que é ativado, recruta TRAF-2, que se associa à TRAF-1, formando um complexo
heterodimérico capaz de ativar a via de NF-κB (Figura 3) (Bradley, 2008). As
moléculas c-IAP-1 e c-IAP-2 (proteínas inibidoras da apoptose) juntam-se a esse
complexo após a indução de sua transcrição por NF-κB e atuam bloqueando a atividade
da caspase-8 e inibindo a apoptose celular (Ihnatko & Kubes, 2007). O TNFR2 pode
sinalizar independentemente de TRAF, ativando uma proteína tirosina quinase
citosólica pertencente à família tirosina quinase de Bruton (Btk) (Pan et al., 2002),
conhecida em seres humanos como tirosina quinase epitelial/endotelial (ETK). Etk é um
novo regulador de junções celulares epiteliais e medeia a indução da via
23
fosfatidilinositol 3 quinase (PI3K) - proteína quinase B (Akt) por TNFR2 (Figura 3). A
sinalização mediada por TNFR2 também ativa vias pró-apoptóticas através da
cooperação com TNFR1 pelo fenômeno de “passagem de ligante”, no qual a ativação
inicial de TNFR2 leva à depleção de TRAF-2 do citoplasma, indisponibilizando esta
molécula para a montagem do complexo I do TNFR1 e, assim, comprometendo a
posterior indução das vias de NF-κB e JNK por esse receptor (Wicovsky et al., 2009).
Esta interação entre os receptores de TNF parece afetar não apenas TNFR1 e TNFR2
uma vez que a ativação da apoptose por FasL em macrófagos foi inibida pela deleção
dos receptores de TNF (Takada et al., 2007). Quando TNFR1 e TNFR2 são ativados
simultaneamente, TNFR2 induz a degradação de TRAF2, evitando assim a ligação de
cIAP1 e cIAP2 para TNFR1, portanto, aumentando a capacidade pró-apoptótica deste
receptor. Este fenômeno pode ser encarado como uma situação em que o equilíbrio
quantitativo entre os sinais pró- e anti-apoptóticos desencadeados pelo TNF irão
determinar se o resultado final será morte ou sobrevivência celular. Neste sentido,
fazem-se necessários novos estudos relacionados à degradação de TRAF2, o seu papel
na ativação do NF-kB e no desencadeamento de vias de morte celular (Cabal-Hierro &
Lazo 2012).
A sinalização via TNF atua de diversas formas na regulação da liberação de
citocinas e quimiocinas que são responsáveis por mediar grande parte dos fenômenos
imunológicos (MacEwan et al., 2002). Desta forma, o TNF apresenta sinalização
complexa, com ampla variedade de funções celulares dentro do organismo.
2.7.1 TNF nas cardiopatias
Inicialmente, pensava-se que a produção de TNF era exclusivamente realizada
por monócitos e macrófagos quando adequadamente estimulados (Beyaer et al., 1999).
Entretanto, os cardiomiócitos expressam tanto o TNF quanto seus receptores (TorreAmione et al., 1995) e a expressão gênica e proteica de TNF já foi mostrada na fibra
muscular esquelética humana (Saghizadeh et al.,1996). Estes dados indicam que a
mesma pode produzir TNF e esta citocina pode atuar de maneira autócrina e parácrina,
em quantidade suficiente para mediar uma série de alterações morfológicas e funcionais
no tecido (Larsen et al., 2002; Spate et al., 2004).
24
A
B
Figura 3: Vias de sinalização de TNF. TNF sinaliza através dos receptores TNFR1 e TNFR2 para ativar
vias de sinalização distintas e que se sobrepõem mediando os diversos efeitos celulares desta citocina. (A)
Após TNF se ligar a seu receptor TNFR1 ocorre a formação do complexo I contendo importantes
proteínas adaptadoras TRADD, TRAF2, RIP e FADD. Estas proteínas recrutarão enzimas (por exemplo,
caspase-8, MAP3K e IKK), que estimulam a apoptose e a ativação de AP-1 e NF -κB. (B) TNFR2 não
possui domínio de morte intracelular, a ligação do TNF provoca trimerização do TNFR2, permitindo a
sua interação direta com a TRAF2. TRAF2 interage com TRAF1, TRAF3, cIAP-1 e cIAP -2, resultando
na ativação de fatores de transcrição NF-κB ou AP-1, através da ativação do complexo IKK e degradação
de IκB, respectivamente, ou a ativação de JNK e MAP3K. TNFR2 pode ativar a enzima tirosina quinase
endotelial/epitelial (ETK), independentemente de TRAF2. ETK ativa medeia interação com o receptor 2
do fator de crescimento endotelial vascular (VEGFR2) através da fosforilação recíproca, resultando na
ativação da via angiogénica de fosfatidilinositol-3-quinase (PI3K)-Akt. Modificado de Waters et al.,
2013.
Os níveis circulantes de TNF estão elevados em pacientes com insuficiência
cardíaca congestiva (ICC) grave (Levine et al., 1990) e o coração humano não infartado
não expressa TNF, enquanto que o coração humano em estágio final de IC expressa
grandes quantidades desta proteína (Mann et al., 1996). No entanto, se o TNF tem
efeitos deletérios sobre a função do cardiomiócito, esta é uma questão controversa. A
administração intravenosa de TNF foi associada com o desenvolvimento de
cardiomiopatia dilatada (Hegewisch et al., 1990). Valores aumentados de TNF e de seus
receptores solúveis estão associados ao maior índice de mortalidade em pacientes com
25
ICC (Mann, 2001). Por outro lado, camundongos deficientes em receptores de TNF
apresentaram maiores níveis de apoptose quando submetidos ao infarto isquêmico
(Kurrelmeyer et al., 2000). Este trabalho concluiu que a sinalização por TNF resulta em
sinais citoprotetores, que impedem a apoptose de cardiomiócitos após o infarto
isquêmico. De fato, aparentemente o TNF e sua sinalização via ativação de seus
receptores tem um papel ambivalente na isquemia miocárdica e proteção contra a
mesma. O excesso de expressão de TNF e subsequente ativação do TNFR1 nos
cardiomiócitos gera um estímulo que induz disfunção contrátil, hipertrofia, fibrose e
morte celular, enquanto que uma menor concentração de TNF e subsequente ativação
do TNFR2 nos cardiomiócitos gera um estímulo protetor (Kleinbongard et al., 2011).
Tendo em vista este papel aparentemente controverso da sinalização por TNF nas
cardiopatias, numerosos ensaios clínicos têm sido realizados para estudar os efeitos da
inibição do TNF na ICC (Deswal et al 1999; Bozkurt et al. 2000; Coletta et al. 2002;
Anker & Coats, 2002; Chung et al., 2003).
Os receptores solúveis sTNFR1 e sTNFR2 também têm uma importante
participação nas cardiopatias e já foram mostrados estarem aumentados na cardiopatia
isquêmica, havendo uma correlação inversa com a FEVE (Rivera et al., 2006). O
sTNFR1 é apresentado, por alguns autores, como marcador de mortalidade superior a
FEVE em pacientes com ICC (Herrmann et al., 2012). Além disso, tem sido encontrada
relação entre o aumento plasmático e urinário desses receptores solúveis com a classe
funcional de ICC de acordo com a classificação da New York Heart Association
(NYHA) (Brockhaus et al., 1997; MacEwan et al., 2002; Rivera et al., 2004).
Apesar de nos últimos anos a maioria dos estudos sobre IC ter se concentrado
nas citocinas pró-inflamatórias, atualmente as citocinas anti-inflamatórias, em especial a
IL-10, têm se destacado e podem ter um papel importante na fisiopatologia das
cardiopatias (Stumpf et al., 2003; Amir et al., 2010). Em pacientes com IC e,
principalmente, nos casos de disfunção ventricular esquerda, uma diminuição na
concentração plasmática de IL-10 tem sido relatada e correlacionada positivamente com
uma piora na FEVE (Kaur et al., 2006). Além disso, a utilização da relação da produção
de IL-10 e TNF (diminuição da razão IL-10/TNF) tem sido relacionada com o grau de
disfunção ventricular (Kaur et al., 2006).
26
2.7.2 TNF na infecção pelo T. cruzi
A produção de TNF é diretamente induzida pelo T. cruzi e seus antígenos,
envolvendo mecanismos dependentes do fator de transcrição NF-κB (Ropert et al.,
2002). Neste cenário, outras moléculas do parasito, incluindo as tGPI mucinas e DNA,
estimulam a produção de citocinas pró-inflamatórias e quimiocinas, envolvendo a via
mediada por TLR2 e dependente de MyD88 (Almeida & Gazzinelli, 2001; Shoda et al.,
2001). O TNF atuando via TNFR1 desempenha papel crítico na resistência à infecção
aguda, controlando a captura do parasito e a produção de NO e quimiocinas (Aliberti et
al., 2001). Altos níveis séricos de TNF estão correlacionados à disfunção cardíaca em
pacientes crônicos da DC (Ferreira et al., 2003; Pérez-Fuentes et al., 2003; Talvani et
al., 2004). Contudo, estudos de polimorfismo gênico de TNF em pacientes não foram
conclusivos, suportando (Rodriguez-Perez et al.,2005) ou não (Beraun et al.,1998) a
associação do genótipo TNF-308G/A (alta produção de TNF). Recentemente, Pissetti e
colaboradores (2011) estudaram os SNPs -308G/A e -238G/A da região promotora do
gene TNF em uma população brasileira do estado de Minas Gerais e não observaram
qualquer associação significativa entre esses SNPs e as formas clínicas crônicas da DC.
Resultados semelhantes foram encontrados por Drigo e colaboradores (2007) ao
avaliarem o papel do SNP -308G/A do gene de TNF entre indivíduos assintomáticos e
portadores de CCC (agrupados de acordo com o grau de disfunção do ventrículo
esquerdo). Neste caso, os autores não observaram associação entre o polimorfismo e o
desenvolvimento de doença cardíaca ou progressão para formas graves da CCC. Por
outro lado, Criado e colaboradores (2012) ao analisarem o SNP -308G/A do gene TNF
em uma coorte colombiana encontraram uma frequência elevada do alelo A nos
portadores de CCC. Este dado foi estatisticamente significativo quando comparado com
a frequência do mesmo alelo nos indivíduos assintomáticos. Nesta mesma linha, um
estudo brasileiro envolvendo 42 pacientes portadores da DC com fração de ejeção
ventricular ≤ 40%, mostrou que os pacientes que expressam o alelo -308G/A têm uma
menor sobrevivência quando comparados aos pacientes com outros alelos (Drigo et al.,
2006). Este aparente paradoxo reforça a necessidade de maiores estudos envolvendo a
participação dos polimorfismos do gene de TNF na patogenia da DC.
As concentrações de TNF estão aumentadas no soro de camundongos infectados
pelo T. cruzi (Starobinas et al., 1991) e é implicado na perda de peso observada na
27
infecção aguda (Truyens et al.,1995). A administração de TNF a animais infectados
pelo T. cruzi aumentou a taxa de mortalidade dos mesmos (Black et al., 1989). De modo
interessante, o TNF atua como segundo sinal para a indução da atividade microbicida
por macrófagos ativados por IFNγ (Silva et al., 1995; Aliberti et al., 2001). TNF
também está envolvido na indução da expressão de iNOS em cardiomiócitos infectados,
que desencadeia a produção de NO, proposto desempenhar papel essencial na resposta
imune contra o T. cruzi (Machado et al., 2000). Contudo, há questionamentos quanto a
participação de NO na infecção pelo T. cruzi, havendo evidências de que a produção
excessiva de NO causa alterações patológicas no tecido cardíaco, uma vez que este
tecido tem um sistema muito eficiente de controle dos níveis de ROS (Huang et al.,
1999; Chandra et al., 2002; Silva et al., 2003).
Na fase aguda da infecção pelo T. cruzi, o TNF e a via TNFR1 são importantes
para o controle do parasito, mas a sinalização TNF/TNFR1 também está envolvida na
lesão miocárdica, controlando a deposição de fibronectina (FN) e a expressão de Cx43,
relevantes para a integridade cardíaca (Kroll-Palhares et al., 2008). Além disso, já foi
mostrado que a infecção de animais tnfr1-/- pelo T. cruzi leva ao aumento da parasitemia
e redução da sobrevivência dos animais, enquanto animais tnfr2-/- apresentam resposta
imune semelhante aos animais imunocompetentes infectados (Aliberti, et al., 2001). O
TNFR1 está envolvido no desenvolvimento da esplenomegalia induzida pelo T. cruzi
(Kroll-Palhares et al., 2008), que tem sido associada à ativação policlonal de células B e
T (Minoprio, 2001), especialmente células T CD8+ (dos Santos et al., 2001; Tzelepis et
al., 2007), principais componentes da miocardite chagásica (Higuchi et al., 1993; Reis et
al., 1993; dos Santos et al., 2001). Curiosamente, camundongos tnfr1-/- quando
infectados pelo T. cruzi apresentaram redução da miocardite, marcada principalmente
pela redução do número de células T CD8+, quando comparados aos camundongos
imunocompetentes infectados. Esta redução de células CD8+ foi correlacionada com
diminuição da frequência de células CD8+CD44+CD62Llow/- com perfil de
ativação/memória no sangue e retenção desse subconjunto de células no baço (KrollPalhares et al., 2008). Estes dados indicam que a sinalização via TNF/TNFR1 não é
essencial para a plena diferenciação desse subconjunto de células T, como indicado pela
expressão de marcadores de ativação/memória CD44 e CD62L, mas de alguma forma
controla a compartimentalização das células T CD8+ na infecção pelo T. cruzi.
28
Assim, estes resultados sugerem que a desregulação na produção de TNF bem
como sua sinalização via TNFR1 participem da evolução da CCC. Com isso, torna-se
importante entender os mecanismos pelos quais esta citocina participa da patogenia da
miocardite chagásica crônica, modulando os processos que envolvem a migração de
células para o tecido cardíaco, o balanço pró/anti-inflamatório sistêmico, bem como a
ativação das subpopulações de células T CD8+ e o reflexo na funcionalidade cardíaca.
2.7.3 Estratégias de bloqueio de TNF
Uma vez conhecida a associação entre a ativação inflamatória e a ICC, seria
coerente procurar potenciais alvos terapêuticos que modulem essa inflamação. Nos
últimos anos tivemos a expansão das opções terapêuticas principalmente para as
doenças autoimunes (que também apresentam um importante componente inflamatório)
com o desenvolvimento de terapias direcionadas especificamente para mediadores
inflamatórios (Tracey et al., 2008; Tanaka et al., 2014).
Tendo em vista o papel do TNF na gênese e perpetuação da inflamação, o seu
antagonismo poderia reduzir o processo de remodelamento, melhorar a função
ventricular e reduzir a mortalidade. Os estudos que buscaram antagonizar o TNF
apresentaram, todavia, resultados não muito animadores. O estudo "Anti-TNF Therapy
Against Congestive Heart Failure" (ATTACH) randomizou pacientes para receber
placebo ou infliximab (Remicade, Schering-Plough - Figura 4), um anticorpo
monoclonal quimérico (humano-murino) que se liga com alta afinidade a formas
solúveis e transmembranares do TNF, mas não à LTA. Os pacientes que receberam
infliximab não apresentaram diferença significativa na incidência do desfecho primário
(um escore composto que visava avaliar a mudança no perfil clínico em 14 semanas).
Além disso, apesar de haver uma redução nos níveis de proteína C reativa (PCR) e IL-6,
a incidência de morte ou hospitalização foi significativamente maior no grupo que
recebeu a terapia anti-TNF na dose de 10 mg/kg (Chung et al., 2003). O ensaio clínico
"Randomized Etanercept Worldwide Evaluation" (RENEWAL) avaliou o uso do
etanercept em dois sub-estudos: o "Research into Etanercept Cytokine Antagonism in
Ventricular Dysfunction" (RECOVER) e o "Randomized Etanercept North American
Strategy to Study Antagonism of Cytokines" (RENAISSANCE). O etanercept (Enbrel,
Wyeth - Figura 4) é um dímero de uma proteína quimérica obtida por engenharia
29
genética pela fusão do domínio de ligação extracelular do TNFR2/p75 com o domínio
Fc da IgG1 humana. Este componente Fc contém as regiões CH2 e CH3, mas não
possui a região CH1 da IgG. O etanercept inibe a ligação do TNF e da LTA aos
receptores de TNF na superfície celular, tornando o TNF biológico indisponível e
impedindo as respostas celulares mediadas por esta citocina (Kapadia et al., 1995;
Kubota et al., 2000). Assim como no ATTACH, a terapia anti-TNF mostrou-se ineficaz,
pois não houve diferença significativa na incidência de morte ou hospitalização entre os
grupos eternacept e placebo (Mann et al., 2004). Dentre as possíveis razões para a falha
da terapia anti-TNF, foram apontados: o possível efeito tóxico direto dos antagonistas;
uma possível potencialização do efeito do TNF; uma dose não adequada; o fato de que
os antagonistas não conseguem bloquear completamente o processo inflamatório ou que
o aumento de citocinas poderia ser um mecanismo apenas adaptativo (Chung et al.,
2003; Mann et al., 2004). Alguns estudos sugeriram que níveis fisiológicos (baixos
níveis) de TNF podem conferir efeito citoprotetor ao tecido cardíaco durante a lesão
isquêmica aguda (Nakano et al., 1998; Kurrelmeyer et al., 2000). Além disso, o TNF
pode desempenhar um papel adaptativo, reforçando a produção de NO vascular e,
portanto, influenciando no fluxo de sangue periférico em pacientes com ICC (Katz et
al., 1994, Sugamori et al., 2002). Desta forma, níveis fisiológicos de TNF poderiam
desempenhar um papel importante na regeneração e reparação tecidual (Mann, 2002).
Assim, é possível que terapias anti-TNF possam diminuir TNF abaixo dos níveis
fisiológicos necessários para o reparo do miocárdio. Também devemos lembrar que a
resposta inflamatória à ICC está associada com outras citocinas como a IL-6 e IL-1, que
têm propriedades de sinalização similares ao TNF e são produzidas por cardiomiócitos
durante a ICC (Gullestad & Aukrust, 2005).
Apesar do insucesso dos grandes ensaios clínicos (ATTACH, RENEWAL
eRENAISSANCE) que avaliaram a ação de antagonistas específicos do TNF, novos
fármacos invadem o mercado com a proposta de bloquear TNF e tratar principalmente
as doenças autoimunes (Tracey et al., 2008). O adalimumab (Humira, AbbVie - Figura
4) é um anticorpo monoclonal recombinante 100% humanizado com eficácia similar ao
infliximab para o tratamento de doenças como artrite reumatoide, psoríase e doença de
Crohn (Tracey et al., 2008). Entretanto ainda não existem ensaios clínicos envolvendo o
uso deste fármaco em pacientes cardiopatas.
30
C
B
A
Figura 4. Agentes anti-TNF. Moléculas anti- fator de necrose tumoral (TNF) ligam-se ao TNF para
neutralizar sua atividade. Infliximab e adalimumab são anticorpos monoclonais. (A) Infliximab é uma
quimera camundongo/humano, que une as regiões variáveis de um anticorpo de camundongo com a
região constante de IgG1 humana; e (C) adalimumab é um anticorpo IgG1 humano. (B) Etanercept é uma
proteína de fusão dimérica que junta o receptor p75 de TNF humano com o domínio Fc de IgG1 humano.
Modificado de Russo & Polosa 2005.
Alguns estudos que utilizaram agentes anti-inflamatórios e imunomoduladores
inespecíficos mostraram-se promissores. Um estudo que avaliou em pacientes com IC
os efeitos da talidomida, conhecida por propriedades anti-inflamatórias e antioncogenéticas, a talidomida promoveu aumento significativo da FEVE e redução
significativa dos níveis de TNF plasmático após seis semanas de tratamento (Gullestad
et al., 2002). Um outro ensaio clínico randomizado avaliou em pacientes com IC
isquêmica a ação da pentoxifilina (PTX), uma metilxantina que tem como principal
ação
o
bloqueio
das
enzimas
fosfodiesterases.
A
PTX
tem
metabolismo
predominantemente hepático, sendo inicialmente utilizada em pacientes com
claudicação intermitente e doença vascular periférica (Frampton & Brogden , 1995). O
uso do medicamento para este fim se justificava pela ação de relaxamento da
musculatura vascular (Kamphuis et al., 1994) e alterações da deformidade eritrocitária
mostrada no início dos trabalhos com o fármaco (Angelkort et al., 1979). Entretanto,
após sua utilização com este intuito, foi observado também que o medicamento possuía
propriedades anti-inflamatórias e imunomoduladoras importantes, com os primeiros
estudos nesta linha demonstrando seus efeitos sobre a redução da migração de
neutrófilos e hiperreatividade leucocitária (Mandell et al., 1988, De Prost et al., 1990).
Estes estudos também demonstraram que seu principal efeito anti-inflamatório se dava
sobre a resposta do tipo Th1, sendo o fármaco considerado um agente supressor da
31
produção do TNF (Coimbra et al., 2004). Em cardiopatias, o principal uso da medicação
foi no tratamento da ICC. Desde o primeiro trabalho em 1998, vários autores
demonstraram que o uso da PTX melhorou a função sistólica de pacientes com ICC
avançada, com melhora dos sintomas clínicos e redução da inflamação sistêmica medida
pela redução dos níveis plasmáticos de TNF, proteína C reativa e pró-BNP (Sliwa et al.,
1998; Skudicky et al., 2001; Sliwa et al., 2002; Sliwa et al., 2004). Concomitante aos
estudos avaliando a disfunção ventricular, a PTX também demonstrou um bom perfil
anti-inflamatório em pacientes submetidos à cirurgia cardíaca, nos quais o uso de
circulação extracorpórea promove uma ativação importante da resposta inflamatória
(Boldt et al., 2001). Coletivamente, esses ensaios mostraram que a terapia com PTX em
cardiopatias não infecciosas parece resultar em uma melhora dos sintomas clínicos, não
necessariamente em associação com a redução da concentração de TNF circulante, mas
com efeitos significativos na funcionalidade cardíaca (Skudicky et al., 2001).
Na infecção pelo T. cruzi, o bloqueio de TNF na CCC experimental se mostrou
aparentemente contraditório. O tratamento com infliximab reduziu a inflamação por
células CD8+ e o dano cardíaco na infecção aguda (Kroll-Palhares et al., 2008) e a
inflamação por células CD8+ na fase crônica (Pérez et al., 2009). Por outro lado, o uso
de etanercept foi prejudicial à função cardíaca na fase crônica da infecção, sem interferir
na alta expressão de mRNA codificando TNF no tecido cardíaco (Bilate et al., 2007).
Este aparente paradoxo realça a necessidade de compreensão dos modos de ação e os
fatores limitantes das ferramentas terapêuticas que visam modular a ação de TNF
(Wong et al. 2008). Dados do nosso laboratório sugerem que os efeitos prejudiciais de
TNF na infecção pelo T. cruzi podem ser determinados pela quantidade e duração da
produção de TNF. Assim, a redução (mas não a completa abolição) da produção de TNF
ou da sua ação biológica pode ter um efeito benéfico por manter sob controle a
disseminação do parasito. Em paralelo, interfere reduzindo o desenvolvimento da
miocardite e lesões durante a infecção pelo T. cruzi (Lannes-Vieira et al., 2011).
2.8 Tratamento da infecção pelo T. cruzi
O tratamento etiológico da DC continua o mesmo desde a década de 70, sendo
parcialmente ineficaz, devido à resistência parcial de algumas cepas ou a fatores
intrínsecos ao hospedeiro. Uma das dificuldades para o controle da eficácia de uma
droga tripanossomicida é o critério de cura, ou seja, ter métodos que permitam medir
32
com segurança a eficácia do fármaco. Outro problema é a diversidade genética do
parasito. Entre inúmeras drogas testadas, duas têm sido usadas com cautela e
acompanhamento criterioso, obtendo bons resultados na fase aguda da infecção, o
benznidazol (Bz - inicialmente produzido pela Roche como Rochagan ou Radanil e
atualmente produzido pela LAFAPE, PE, Brasil e pelo laboratório argentino ELEA com
o nome de Abarax®) e o nifurtimox (produzido pela Bayer Health Care, com o nome
comercial de Lampit).
O Bz (Figura 5) é uma droga nitroheterocíclica (N-benzil-2-nitroimidazole-1acetamida) introduzido na terapêutica da DC em 1967. É considerado mais efetivo que o
nifurtimox, porém, apresenta moderada toxicidade. O Bz possui uma consistente
capacidade anti-protozoário, conseguindo eliminar os parasitas nas formas sanguíneas e
teciduais, se administrado na dose certa e durante o período de dois meses na fase aguda
da DC (Oliveira et al, 2008; Bezzera, 2012). O modo de ação do Bz pode envolver
ligação covalente ou outras interações de intermediários nitroredutores com
componentes do parasito ou ainda ligações ao DNA, lipídios e proteínas (Coura &
Castro 2002).
O nifurtimox (Figura 5), 3-metil-4 (5’-nitrofurfurilidenamino)- tetraidro (1,4)tiazina-1-1-dióxido, tem como efeito a inibição do desenvolvimento intracelular do
parasito. Atua bem contra as formas sanguíneas e parcialmente contra as formas
teciduais. É administrado oralmente por três meses sob a forma de comprimido, sendo
mais bem tolerado por pacientes jovens (Cimerman, 2008; Neves et al, 2005; Rey,
2008).
Tais medicamentos mostram sua eficácia se administrados imediatamente após a
infecção, ou seja, na fase aguda. O tratamento também é indicado para pessoas onde a
infecção foi reativada, por exemplo, por imunossupressão, para crianças com infecção
congênita e para pacientes durante o início da fase crônica (WHO, 2010). Estas
estratégias terapêuticas têm como desvantagens o fato de serem eficazes quando
adotadas na fase aguda ou crônica recente da doença e serem tóxicas para uma parcela
dos pacientes, com efeitos colaterais que torna necessária, muitas vezes, a interrupção
do tratamento (Rassi Jr et al., 2010). Em 2004 iniciou-se o estudo BENEFIT, que visa
analisar se o tratamento com Bz, nas doses habituais (5-10 mg/Kg/dia) modifica ou não
a evolução da CCC. Esse estudo envolve Brasil, Argentina e Colômbia, tendo previsão
de acompanhamento de 3 mil pacientes portadores da fase crônica da DC com
33
cardiopatia instalada (grau funcional de I a III da New York Heart Association). Ao final
do estudo espera-se ser possível definir o real papel do tratamento com Bz na fase
crônica da DC (Marin-Neto et al., 2009).
Apesar dos vários efeitos colaterais que o uso do Bz acarreta aos pacientes que
estão sendo tratados pela DC, esta é a droga ainda indicada pelos médicos como o
fármaco de linha de frente (Mejia et al., 2012). A terapêutica da DC prossegue
parcialmente ineficaz, apesar do real progresso alcançado nas últimas décadas. Diversas
drogas vêm sendo estudadas (Menezes et al., 2011), porém, nenhuma consegue eliminar
a infecção pelo T. cruzi, ou seja, promover a cura estéril em definitivo.
Figura 5: Estrutúra química das drogas usadas no tratamento etiológico da doença de Chagas: nifurtimox
e benznidazol. Modificado de Patterson et al., 2014.
O tratamento sintomático da forma cardíaca é feito como em outras cardiopatias,
usando cardiotônicos, diuréticos, vasodilatadores, betabloqueadores, implante de
marcapasso ou transplante cardíaco (nos casos graves de IC). Nas formas digestivas são
indicadas dietas, laxativos, enemas ou cirurgia. Outras possibilidades de tratamento das
sintomatologias de fase crônica estão em teste, como a terapia celular, que se mostrou
benéfica melhorando a fibrose e inflamação cardíaca em modelos experimentais (Soares
et al., 2004) e o uso de células-tronco (administração intracoronariana) em pacientes
com IC chagásica, que se mostrou eficaz melhorando a qualidade de vida e capacidade
funcional dos pacientes nos 2 meses após o tratamento (Vilas-Boas et al., 2006),
entretanto esses resultados não se reproduziram na coorte de Goiás (de Souza et al.,
2014). Também, a injeção intracoronariana de células mononucleares derivadas da
medula óssea não melhorou a FEVE ou a qualidade de vida dos pacientes com CCC
(Ribeiro dos Santos et al., 2012), o que sugere a necessidade de mais estudos na área.
Além disso, existe a proposta do uso de imunomoduladores sozinhos ou em associação
34
com drogas tripanossomicidas, objetivando regular mecanismos patogênicos de forma
associada ou não ao controle do parasito na CCC (Lannes-Vieira, 2003; Lannes-Vieira
et al., 2010). No futuro, possivelmente, em analogia à hanseníase, SIDA e tuberculose
(Simon et al., 2006; Nahid et al., 2006), teremos uma terapia combinada mais efetiva e
mais racional para a infecção pelo T. cruzi.
Por se tratar de uma doença debilitante e incurável, a DC constitui ainda hoje,
em um Brasil com baixa transmissão vetorial, um grave problema de saúde pública,
especialmente pelo tratamento dos pacientes já infectados no passado. A pesquisa de
novos fármacos com maior eficácia na fase crônica da infecção, e menor toxicidade ao
paciente, não representa o interesse dos laboratórios de medicamentos. Das mais de mil
novas entidades químicas que entraram no mercado farmacêutico entre 1975 e 1999,
apenas 16 eram indicadas para o tratamento de doenças tropicais e tuberculose
(Trouiller et al., 2002). Entretanto, há várias classes de drogas aprovadas para uso em
outras enfermidades e com atividade comprovada contra o T. cruzi, que poderiam ser
desenvolvidas para o tratamento da DC (Rodriguez-Morales, 2005). Por isso, mesmo
após mais de cem anos da descoberta de Carlos Chagas, a DC ainda representa um
desafio à saúde pública no Brasil e em outras áreas endêmicas, pois conta com uma
patogenia complexa, medidas profiláticas e terapias parcialmente efetivas e ainda com
entraves político-econômicos que a tornam negligenciada frente às outras enfermidades
que assolam o planeta (Lannes-Vieira et al., 2010).
2.9 Vacina
Recentemente foi demonstrado que, do ponto de vista econômico, é interessante
o desenvolvimento de uma vacina contra a DC na América Latina, mesmo em regiões
de baixo risco de infecção e baixa eficiência vacinal (Lee et al., 2010). Várias formas de
imunização têm sido testadas, seja com cepas atenuadas, frações ou formas inativadas
do T. cruzi, usando parasitos semelhantes, proteína recombinante e vacina de DNA ou
vírus recombinantes expressando epítopos do T. cruzi (Paiva et al., 1999; De Alencar et
al., 2009; Boscardin et al., 2003; Vasconcelos et al., 2004; Machado et al., 2006;
Aparicio-Burgos et al., 2015).
Inicialmente, a infecção residual decorrente da imunização com parasitos vivos
(Basombrio et al., 1982; Paiva et al., 1999) impulsionou a elaboração de vacinas
35
compostas por parasitos mortos ou vivos atenuados. A avirulência do parasito era
produzida pelo tratamento prévio com agentes atenuantes químicos, radiação, ou
passagens seriadas em cultura, mas objetivando preservar sua imunogenicidade (Bhatia
et al., 2004). A proteção oferecida pelas vacinas com parasitos atenuados ou mortos foi
semelhante à oferecida pela imunização com formas vivas do T. cruzi, observada por
maior sobrevida e menor parasitemia nos camundongos vacinados (Basombrio et al.,
1987). Então, novos modelos de imunização começaram a ser aplicados, visando expor
antígenos intracelulares do T. cruzi a partir da lise celular, o que contribuiu para os
estudos de imunogenicidade e compreensão da resposta imune do hospedeiro. Além
disso, com a evolução das técnicas laboratoriais, tornou-se possível selecionar proteínas
de frações do parasito, bem como epítopos imunogênicos contidos em uma determinada
proteína e testar a capacidade destas em gerar proteção. Atualmente, os candidatos que
mais se destacam são: as proteínas cruzipaína, TS proteínas de superfície de formas
amastigotas, proteína Rod paraflagelar, entre outros (Cazorla et al., 2009). A proteína de
superfície de amastigota (ASP)-2, que é importante na manutenção da infecção crônica
(Boscardin et al., 2003; Vasconcelos et al., 2004), e a TS, uma enzima das formas
tripomastigotas que catalisa a transferência do ácido siálico de glicoproteínas do
hospedeiro para moléculas receptoras na membrana do parasito (Schenkman et al 1994),
pertencem à mesma família de genes e foram descritas como proteínas altamente
imunodominantes (Low et al., 1998; Myahira et al., 2005; Araujo et al., 2005).
Inúmeros grupos vêm testando em diferentes protocolos e linhagens de camundongos o
uso de proteína recombinante, vacina de DNA ou vírus recombinantes expressando
epítopos ou genes da família TS com o intuito de obter uma resposta imune protetora
contra a infecção pelo T. cruzi (Garg e Tarleton, 2002; De Alencar et al., 2009;
Boscardin et al., 2003; Vasconcelos et al., 2004; Machado et al., 2006). A administração
profilática de preparações vacinais contendo ASP2 e TS suscitou resposta imune
humoral e celular, além de impactar na melhora da parasitemia e sobrevivência dos
camundongos vacinados (Machado et al., 2006; Haolla et al., 2009, de Alencar et al.,
2009; Barbosa et al., 2013). Por exemplo, a vacinação de camundongos C57BL/6 (H-2b)
usando o adenovírus recombinante tipo 5 (rAd5) carreando sequências de ASP
(rAdASP2), TS (rAdTS), ou ambas (rAdASP+rAdTS) mostrou que somente a última foi
capaz de gerar proteção frente ao desafio com a cepa Y do T. cruzi (Machado et al.,
36
2006). Estes dados foram corroborados em camundongos A/Sn (H-2a) (Haolla et al.,
2009).
Outra alternativa seria a vacina de DNA, que se baseia na inclusão de genes que
codificam proteínas antigênicas aos plasmídeos. Estes são inoculados no organismo do
hospedeiro e fagocitados por células apresentadoras de antígenos e células dendríticas.
Dessa forma, o plasmídeo se interioriza na célula e utiliza o aparato celular do
hospedeiro para transcrever e traduzir a proteína imunogênica que estimulará respostas
imunes específicas. Em experimentos com plasmídeos de DNA contendo genes que
codificam as proteínas cruzipaína (Schnapp et al., 2002) e o antígeno de superfície de
tripomastigotas-1 (a ASP-240) (Wizel et al., 1998) produziram imunidade parcial, sem
produzir imunidade estéril. Outra estratégia usada foi o protocolo heterólogo usando
DNA plasmidial no prime (indução) e o rAd5 carreando sequências de ASP2 no boost
(reforço). Esta proposta vacinal estimulou resposta imune protetora, com o aumento na
frequência de células T CD8+ de memória específicas para T. cruzi (Rigato et al., 2011).
A imunização com proteínas recombinantes de protozoários semelhantes ao T. cruzi,
por exemplo, o Trypanosoma rangeli, que não é patogênico para o homem, também é
um candidato vacinal para a DC. Camundongos imunizados com o T. rangeli fixado
com glutaraldeído apresentaram ativação de células B e T que foram capazes de
reconhecer antígenos de T. cruzi e ainda controlaram a parasitemia, reduziram a
mortalidade e as lesões histopatológicas após desafio com o T. cruzi (Basso et al., 2004;
Basso et al., 2008). Recentemente, foi testada a eficácia de uma vacina de DNA (prime)
e T. rangeli inativado (boost) em modelo canino da DC, mostrando redução na
parasitemia, no infiltrado inflamatório do tecido cardíaco e preservação da função
cardíaca após desafio com a cepa SylvioX10/4 (Aparicio-Burgos et al., 2015).
Paralelamente aos esforços na identificação de candidatos à vacina, muitos
adjuvantes foram testados na modulação de imunidade protetora. Além do objetivo de
melhorar diretamente a eficácia das vacinas, propôs-se a administração conjunta dos
adjuvantes para estimular uma resposta imune eficaz no controle do parasito (Tarleton
2005). Atualmente, os esforços na busca por uma vacina efetiva contra a infecção
continuam expressivos (Dumonteil et al., 2012). Entretanto, e infelizmente, não se
dispõe ainda de nenhuma vacina, seja de uso veterinário ou de uso humano, que
assegure proteção. Esforços futuros são necessários na identificação de sistemas de
vacinação eficientes, adjuvantes e regimes de vacinação para aumentar as respostas
37
protetoras a já conhecidos e novos candidatos vacinais. Dada a complexidade do
genoma do parasito, os vários estágios do ciclo evolutivo nos hospedeiros e as variações
das cepas, é essencial que se empreguem esforços na escolha de candidatos apropriados
à vacina.
2.10 Controle e prevenção
O controle da transmissão constitui-se na estratégia básica de superação da DC,
priorizam-se o controle do inseto vetor, sobretudo os presentes no domicilio e
peridomicílio, e a prevenção da transmissão transfusional e vertical. A forma de
prevenção da DC mais eficiente na América Latina é sem dúvida o controle do vetor.
No final do ano de 2006 o Brasil foi declarado área livre de transmissão pelo principal
vetor da DC, o Triatoma infestans, uma vez que dos doze estados onde ainda havia
registros de transmissão vetorial até a década de 90, em dez deles a transmissão já havia
sido interrompida e nos dois estados restantes o trabalho de controle químico do vetor
encontrava-se bastante avançado (WHO 2010). Os programas de controle da DC
mostraram ser efetivos em reduzir a incidência da infecção e resultaram num custo
econômico muito menor para prevenção, quando comparado ao despendido no
tratamento da doença crônica. Além do controle químico, outras medidas contra o vetor
são pertinentes. A melhoria das habitações é primordial, uma vez que casas de alvenaria
sem frestas, limpas e arejadas, por si mesmas já oferecem grande resistência à
colonização triatomínica, (Dias, 1991). A triagem do sangue também é necessária para
evitar a transmissão da doença por transfusão sanguínea e transplante de órgãos (WHO,
2010). Medidas como a seleção apropriada de doadores de sangue, o uso de testes
sensíveis de triagem e a aplicação de um sistema de garantia de qualidade mantêm a
segurança dos bancos de sangue. O uso de testes de diagnóstico moleculares avançados,
mais precisos e sensíveis tem reduzido grandemente o risco da aquisição da DC
transmitida por sangue infectado (Teixeira et al., 2006).
Outro fator importante é a migração de pessoas infectadas pelo T. cruzi, já que
indivíduos de áreas endêmicas têm migrado para alguns lugares, tais como Estados
Unidos da América, Canadá, Austrália, Japão e países europeus, isso tem representado
uma ameaça para os países onde a transmissão da DC pelos triatomíneos não ocorre,
tornando a DC um problema de ordem mundial (Rassi et al., 2010; Bonney 2014).
38
Segundo a OMS (2010) as metas de controle principais são a eliminação da transmissão
e o acesso à assistência médica para a população infectada e doente.
Uma maneira de prevenir a DC é sem dúvida a educação para a saúde, a ser
realizada de modo permanente nas áreas endêmicas: melhoria das habitações,
reconhecer a doença e suas formas de transmissão, manejar de forma adequada o
peridomicílio, reconhecer, capturar e notificar triatomíneos são objetivos importantes a
serem perseguidos nas práticas políticas, escolares e comunitárias (Lannes-Vieira et al.,
2010).
39
3. Justificativa
___________________________________________________________________________________
Diante da importância da DC, com cerca de 7-8 milhões de pessoas
cronicamente infectadas, das elevadas taxas de morbidade e mortalidade, sobretudo na
CCC, e a ausência de terapia efetiva, justificam-se estudos que visem aprofundar o
entendimento dos fatores que estão envolvidos na patogenia da doença, na busca de
alvos terapêuticos e possíveis biomarcadores relacionados à progressão para as formas
sintomáticas e evolução das mesmas. Assumimos que componentes celulares (como as
células T CD8+) e moleculares (como as citocinas e quimiocinas) do hospedeiro estão
envolvidos na resistência à infecção pelo T. cruzi, bem como em processos patogênicos.
Considerando que a complexa resposta imunológica do hospedeiro constitui fator chave
nas diferentes manifestações clínicas da DC crônica, a modulação desta resposta, bem
como a busca de estratégias terapêuticas racionais e a caracterização de modelos
experimentais adequados ao estudo são abordagens de extrema relevância no âmbito da
saúde pública em DC. Diante do exposto, o presente trabalho traz a validação de
modelos experimentais para o estudo da CCC, a participação da citocina TNF e seu
receptor TNFR1 na resposta imune frente à infecção crônica, propostas de tratamento e
o desenvolvimento de uma vacina terapêutica.
40
4. Objetivo geral
___________________________________________________________________________________
Caracterizar a participação de células e moléculas chave da resposta
imunológica na patogênese da cardiomiopatia chagásica crônica experimental, visando
desenvolver uma terapia para esta patologia.
Objetivos específicos:
1. Propor modelos experimentais que reproduzam aspectos da cardiomiopatia
chagásica humana.
2. Investigar a participação da sinalização TNF/TNFR1 sobre os diferentes
perfis de células T CD8+ (inflamatório – IFNγ+; citotóxico – perforina+) e na
geração da lesão cardíaca na infecção crônica experimental pelo T. cruzi.
3. Analisar os efeitos de diferentes terapias imunorreguladoras sobre a lesão e a
funcionalidade cardíaca, procurando identificar componentes-chave da
imunopatogenia da cardiomiopatia chagásica crônica.
4. Propor novas estratégias terapêuticas, usando imunorreguladores, droga
tripanossomicida e vacina, visando melhor prognóstico da CCC.
41
ARTIGO I
O uso de modelos animais para o entendimento da patogenia da infecção pelo
Trypanosoma cruzi vem desde o artigo original de Carlos Chagas. Ao longo desses mais
de cem anos de estudos, hamsters, ratos, cães, coelhos, macacos, camundongos e outros,
foram utilizados para o estudo da infecção experimental e alguns aspectos das fases
aguda e crônica da infecção humana foram reproduzidos nestes. No entanto, um dos
maiores problemas para o entendimento e sistematização dos dados existentes na
literatura sobre a imunobiologia da infecção e imunopatogenia da doença de Chagas
(DC) é o fato de não haver um modelo comum, eleito pela maioria dos grupos que
trabalham na área e cujos resultados encontrados sejam transponíveis para humanos.
Aqui, descrevemos a infecção crônica experimental com a cepa Colombiana do T. cruzi
(Tipo 1) em duas linhagens isogênicas de camundongos (C3H/He e C57BL/6). Ambas
reproduzem aspectos da fase crônica da DC humana, tais como: parasitemia subpatente,
infiltrado inflamatório, fibrose e redução e desorganização da expressão de conexina 43
no tecido cardíaco. Aumento da atividade da isoenzima MB da creatina quinase (CKMB) no soro, bem como elevados níveis séricos do fator de necrose tumoral (TNF) e
óxido nítrico (NO). Em paralelo a estes achados, observamos alterações elétricas tais
como arritmias e bloqueios atrioventriculares. Por fim, confrontando a infecção nas
duas linhagens, segundo os parâmetros analisados, os animais C3H/He desenvolvem
patologia mais grave, quando comparados ao modelo C57BL/6. Logo, neste artigo
caracterizamos a infecção crônica experimental sob vários parâmetros em duas
linhagens distintas, nos permitindo adotá-los no estudo da fisiopatogenia da doença, na
busca de biomarcadores de progressão e também no desenvolvimento de estratégias
terapêuticas para a cardiomiopatia chagásica crônica.
42
43
44
45
46
47
48
49
50
51
52
ARTIGO II
Dados da literatura sustentam que a fase crônica da doença de Chagas (DC) possui
uma complexa patogenia. Fatores chave que levem às diferentes formas da doença,
bem como à progressão desta, ainda não estão completamente elucidados.
A
cardiomiopatia chagásica crônica (CCC) é caracterizada por miocardite difusa, com
destruição das fibras cardíacas e substituição por fibrose cicatricial, associada ao
infiltrado inflamatório composto por linfócitos T e macrófagos. Estas células
inflamatórias têm sido implicadas no processo de destruição do tecido cardíaco.
Alguns trabalhos também propõem o envolvimento das citocinas inflamatórias na
patogênese da CCC. A infecção pelo T. cruzi e seus antígenos induzem a produção
do fator de necrose tumoral (TNF), envolvendo mecanismos dependentes do fator de
transcrição nuclear-κB. O TNF é uma citocina multifuncional, medeia atividade
microbicida de macrófagos e, ao nível tecidual, inflamação aguda e crônica. TNF foi
identificado por imunoistoquímica no tecido cardíaco de cardiopatas na DC e altos
níveis séricos desta citocina estão correlacionados à disfunção cardíaca. Dados da
literatura suportam que TNF participe da evolução da CCC, tornando-se importante
entender os mecanismos pelos quais esta citocina atua na patogênese desta. Usamos
como estratégia o bloqueio da citocina TNF (com o anticorpo monoclonal quimérico
infliximab) em camundongos C57BL/6 cronicamente infectados pelo T. cruzi
(Artigo I). O uso do infliximab não reativou a parasitemia, mas reposicionou a
resposta imune reduzindo a frequência de células com o perfil inflamatório e
aumentando a proporção de células com perfil regulador. Além disso, a terapia antiTNF diminuiu a atividade citotóxica, mas conservou a produção de IFNγ por células
T CD8+ específicas (VNHRFTLV) no baço e reduziu o número de células perforina+
no tecido cardíaco. A terapia com o infliximab também melhorou a função elétrica
nos camundongos infectados e ainda reduziu a fibrose no tecido cardíaco. Logo,
concluímos que o TNF é componente chave na patogênese da DC sustentando o
desequilíbrio imunológico que contribui para as alterações cardíacas. Esses dados
nos levam a propor que TNF pode ser alvo de terapias para a forma cardíaca da
doença, visando melhor prognóstico.
53
54
55
56
57
58
59
60
61
62
63
64
65
66
67
68
69
70
71
ARTIGO III
A cardiomiopatia chagásica crônica (CCC) está associada à miocardite com componente
inflamatório enriquecido em células CD8+, fibrose e alterações cardíacas estruturais e
elétricas. Na infecção pelo T. cruzi as alterações nos perfis de memória e ativação das
células T CD8+ foram anteriormente descritas. Recentemente, descrevemos a
participação antagônica de diferentes perfis de células T CD8+ na patogênese da CCC
(IFNγ+, protetor; Pfn+, deletério). No presente trabalho, visamos elaborar uma proposta
terapêutica que interfira nas anormalidades destas células vislumbrando um melhor
prognóstico para a CCC. A pentoxifilina (PTX), um derivado da metilxantina, apresenta
efeito imunorregulador, anti-tumoral e cardioprotetor. No presente estudo, utilizamos
um modelo experimental de CCC moderada (Artigo I) para averiguar os efeitos
reguladores da terapia com PTX sobre as células T CD8+ e na progressão ou reversão da
forma cardíaca da doença de Chagas (DC). Verificamos que a PTX não tem ação sobre
o T. cruzi, não alterando a carga parasitária, que se mantém em baixos níveis mesmo
após o tratamento. Entretanto, a terapia com PTX reduziu: (i) a frequência de células T
CD8+ no baço que expressam receptores de TNF, marcadores de ativação e de migração
celular; (ii) a ativação das células endoteliais dos vasos sanguíneos; e (iii) a intensidade
da inflamação no tecido cardíaco. Embora a produção de IFNγ tenha sido conservada
sistemicamente e no tecido cardíaco, a terapia com PTX reduziu o número de células
Pfn+ presentes neste tecido. De maneira importante, a terapia com PTX diminuiu
significativamente a lesão cardíaca e melhorou a função elétrica, tanto na CCC
moderada quanto na grave (modelos descritos no Artigo I). Ainda, os camundongos
tratados com PTX apresentaram diminuição da dilatação dos ventrículos e aumento da
fração de ejeção do ventrículo esquerdo, quando comparados aos animais injetados com
salina. Estes resultados demonstram que o tratamento com a PTX na fase crônica da
infecção pelo T. cruzi reposiciona a resposta de células T CD8+ e impede o
desenvolvimento da CCC grave, fazendo deste fármaco um potencial adjuvante no
tratamento da forma cardíaca da DC, sugerindo que ele possa ser usado sozinho e
levando a proposta de seu uso em associação ao tratamento etiológico.
72
73
74
75
76
77
78
79
80
81
82
83
84
85
86
87
88
89
90
91
92
93
94
95
96
97
98
99
100
ARTIGO IV
A hipótese consensual propõe que a patogênese da cardiomiopatia chagásica crônica
(CCC) é dependente da persistência do T. cruzi e que este, ou seus antígenos, induzem
resposta inflamatória desregulada. Acredita-se que pelo menos parte das manifestações
clínicas da doença de Chagas (DC) sejam consequências da resposta imune dirigida ao
parasita, que contribuiriam para lesões teciduais. Então, seria racional propor uma
terapia efetiva que iniba a fibrose e a disfunção cardíaca em associação ao controle do
agente etiológico, o T. cruzi, possibilitando assim um melhor prognóstico aos pacientes.
Neste sentido, a terapia combinada surge como uma alternativa para o tratamento da
DC. O benznidazol (Bz) é a principal droga disponível para tratar a DC e, embora não
haja nenhuma evidência científica sólida sobre o seu uso na fase crônica da infecção,
em modelos experimentais o tratamento com Bz na fase aguda impediu o
desenvolvimento de CCC grave. Como anteriormente mostrado, a pentoxifilina (PTX)
exibiu efeitos cardioprotetores em ensaios clínicos envolvendo pacientes com
insuficiência cardíaca crônica e melhorou aspectos críticos da CCC experimental
reposicionando a resposta de células T CD8+ (Artigo III), principal componente da
inflamação cardíaca. Isto nos levou a propor que a combinação de Bz a esta terapia que
modula a inflamação crônica não benéfica possa ser uma estratégia terapêutica para o
tratamento da CCC. Então, neste trabalho mostramos que a terapia combinada PTX-Bz
reduziu a expressão de TNF, do receptor 1 de TNF (TNFR1/p55) e da enzima óxido
nítrico sintase induzível (iNOS) no coração, assim como as concentrações de TNFR1
solúvel e óxido nítrico (NO) no soro. Além disso, a terapia PTX-Bz diminuiu
inflamação, fibrose e carga parasitária no tecido cardíaco e reverteu as alterações
elétricas, mantendo este efeito mesmo após 30 dias do final da terapia. Portanto, Bz
combinado a PTX controla o parasito, regenera a lesão cardíaca e melhora a função
elétrica, tornando esta uma estratégia viável para o tratamento da forma cardíaca da DC.
101
102
103
104
105
106
107
108
109
110
111
112
113
114
115
116
117
118
119
120
ARTIGO V
A infecção pelo T. cruzi induz resposta imune humoral e celular que desempenham
papel vital no controle do crescimento do parasito. Contudo, em cerca de 30% dos
pacientes a inflamação se torna progressiva, resultando em doença crônica caracterizada
por miocardite associada à fibrose e à disfunção cardíaca. Todavia, a persistência do
parasito associada a mecanismos homeostáticos mal-adaptados, como os processos
oxidantes/antioxidantes e o balanço entre as citocinas pró-inflamatórias/antiinflamatórias/quimioatraentes são propostos estar criticamente envolvidos na progressão
da cardiomiopatia chagásica crônica (CCC). Assim, além de métodos imunoprofiláticos, novas drogas tripanossomicidas e métodos que contribuam para o resgate
da função cardíaca (Artigo III), é plausível propor o desenvolvimento de uma vacina
que estimule a imunidade protetora e previna a progressão da CCC. Neste sentido,
utilizamos a estratégia do protocolo homólogo prime-boost com o adenovírus
recombinante (rAd) carreando sequências codificadoras da proteína de superfície de
amastigota-2 (ASP2) e trans-sialidase (TS) do T. cruzi. A vacinação profilática com
rAdASP2 + rAdTS (rAdVax ) induziu a produção de anticorpos, reduziu o parasitismo
cardíaco na fase aguda e as alterações elétricas na fase crônica da infecção. A
imunoterapia com rAdVax reduziu a resposta ao estímulo policlonal, mas preservou a
imunidade específica mediada por IFNγ e diminuiu a frequência de células T CD8+
potencialmente citotóxicas. Além disso, rAdVax reverteu as alterações elétricas, reduziu
as alterações histopatológicas e aumentou a sobrevida dos animais. Assim, a
imunoterapia com adenovírus recombinante surge como uma um candidato vacinal
capaz de reprogramar a resposta imunológica, sendo uma alternativa racional para
interromper a progressão e reverter a lesão cardíaca na DC crônica.
121
122
123
124
125
126
127
128
129
130
131
132
133
134
135
136
137
138
139
140
141
142
143
144
145
146
147
148
149
150
151
152
5. Discussão
___________________________________________________________________________________
Embora os mecanismos exatos associados com o desenvolvimento da patologia
na DC não estejam totalmente esclarecidos, a participação do sistema imunológico do
hospedeiro parece estar evidente. Postula-se que a interação entre o parasito e
mediadores do sistema imune seja o principal fator responsável pelos danos teciduais
nas células infectadas, favorecendo a persistência da inflamação cardíaca e da fibrose
reparativa subsequente, levando à perda funcional do órgão ao longo dos anos. É
proposto que as formas crônicas da DC resultam de mecanismos imunológicos
multifatoriais e a resposta imune desregulada associada à imparidade na rede de
citocinas tem sido apontada como um dos fatores determinantes na gravidade da
doença. No presente estudo, desafiamos a hipótese de que a modulação e reprogramação
da resposta imune na fase crônica da DC, na presença ou não de terapia
tripanossomicida coadjuvante, seja uma alternativa para estimular a imunidade
protetora, interromper a progressão e, até mesmo, reverter a CCC, tornando esta uma
estratégia terapeutica a ser explorada.
O estabelecimento de modelos experimentais que reflitam a doença humana e
estudos para o tratamento específico das diferentes formas da DC fazem-se necessários.
Aqui, nossos dados mostraram que tanto a linhagem de camundongos C3H/He quanto a
C57BL/6 quando infectadas com baixo inóculo da cepa Colombiana de “Discrete
Typing Units” (DTU) Tipo I do T. cruzi (Zingales et al., 2012) sobreviveram à infecção
aguda e desenvolveram uma fase crônica com miocardite e parasitismo persistente,
corroborando dados anteriores (Talvani et al., 2000; dos Santos et al., 2001; Medeiros et
al., 2009; Silverio et al., 2010; Silverio et al., 2012). Todos os camundongos
sobreviventes apresentaram níveis elevados de TNF no soro, confirmando a observação
prévia de aumento da expressão de TNF mRNA e proteína no tecido cardíaco dos
camundongos (Talvani et al., 2000; Santos et al., 2001; Medeiros et al., 2009),
reproduzindo os resultados em pacientes (Ferreira et al., 2003; Perez-Fuentes et al.,
2003; Talvani et al., 2004). Durante a infecção aguda, sozinho ou em associação com
outras citocinas, TNF é proposto participar do controle da replicação do parasito através
da produção de NO por macrófagos (Aliberti et al., 1999) e cardiomiócitos (Machado et
al., 2000). Em nosso estudo, o NO também se encontra aumentado no soro dos
camundongos C3H/He e C57BL/6 infectados em paralelo à gravidade das alterações
153
elétricas e lesões cardíacas. Anteriormente, foi mostrado que altos níveis de NO estão
associados com a gravidade da lesão cardíaca e anormalidades elétricas em macacos
rhesus cronicamente infectados pela cepa Colombiana do T. cruzi (Carvalho et al.,
2012). Além disso, trazemos evidências de que ambos os modelos de CCC apresentam
miocardite, aumento de deposição de FN, perda de expressão de Cx43, aumento da
atividade sérica de CK-MB e alterações eletrocardiográficas, características da forma
cardíaca crônica da infecção pelo T. cruzi (Marin-Neto et al., 2007; Andrade et al.,
1989; Garcia et al., 2005; Medeiros et al., 2009; Waghabi et al., 2009; Silverio et al.,
2010). Curiosamente, os camundongos infectados da linhagem C3H/He exibem uma
miocardite mais intensa, confirmado em nosso trabalho posterior (Daliry et al., 2014),
maior parasitismo, maiores níveis de TNF e NO e significativamente maior perda de
Cx43, bem como anormalidades de ECG mais graves, quando em comparação com
camundongos infectados da linhagem C57BL/6. Estes modelos cobrem parte da gama
de anormalidades descritas para portadores da forma cardíaca da DC crônica (Rocha et
al., 2007; Marin -Neto et al., 2009; Waghabi et al., 2009; Anis Rassi Jr et al., 2010).
Assim, eles podem ser explorados em estudos de patogênese da CCC, busca de
biomarcadores e testes de novas drogas tripanossomicidas e estratégias terapêuticas para
a DC. No presente trabalho exploramos estes modelos para o teste de nossas hipóteses.
Uma provável combinação da composição genética do hospedeiro e do parasito,
além do sistema imune do hospedeiro e o ambiente, podem contribuir para a
determinação da forma clínica da DC (Dutra et al., 2005). Variações ou polimorfismos
em um único nucleotídeo na sequência do DNA (single nucleotide polymorphism- SNP)
podem regular a maneira como indivíduos desenvolvem doenças e respondem a
patógenos, drogas, vacinas e outros agentes. O papel da variabilidade genética do
hospedeiro desperta interesses no estudo da suscetibilidade à infecção, em relação à sua
gravidade, sua progressão e as taxas de infecção em nível populacional (Segal et al.,
2003). Vários trabalhos estudando diferentes genes candidatos têm sido realizados.
Polimorfismos em citocinas é um deles, com o objetivo de obter uma associação com o
desenvolvimento da infecção e/ou com a progressão para a CCC. Entre os pacientes
portadores de CCC grave, o alelo -308G/A que confere alta produção de TNF mostrou
associação com a redução na sobrevida (Drigo et al., 2006). Em contra partida, em um
trabalho posterior, o mesmo grupo não observou associação entre o polimorfismo (SNP
-308G/A do gene de TNF) e o desenvolvimento de doença cardíaca (Drigo et al., 2007).
154
Estudos conduzidos com outras doenças cardiológicas não infecciosas, como a doença
arterial coronariana e a síndrome coronariana aguda, não conseguiram demonstrar
associação entre o SNP -308G/A do gene TNF e a suscetibilidade a essas doenças do
coração, apesar de ambas também serem doenças crônicas inflamatórias, onde o TNF já
foi previamente relacionado com seu acometimento (Babu et al., 2012; Bezerra, 2013;
Chu et al., 2012). Já o polimorfismo na posição -238 do gene do TNF mostrou ter
influencia na susceptibilidade para a infecção juntamente com o aumento da produção
sérica de TNF, mas não mostrou associação com as formas clínicas da DC (Pissetti et
al., 2011). O gene da IL-10 na posição -1082 é altamente polimórfico e o alelo A leva a
produção reduzida de IL-10, tendo sido associando com a forma cardíaca da DC (Costa
et al., 2009). Outro estudo avaliando o polimorfismo da IL-10, não somente o -1082
G/A, mas também o -819 C/T e -592 C/A, não encontrou significância estatística, mas
sugere que fator genético na produção da IL-10 pode influenciar a susceptibilidade e a
forma clínica na doença (Flórez et al., 2011). Existem controvérsias na relação entre
certos polimorfismos de gene de citocinas, que merecem ser melhor explorados.
Em relação ao parasito, o T. cruzi possui genótipos e fenótipos diversificados
(Miles et al. 2009; Guhl & Ramírez 2011; Zingales et al., 2012), caracterizados e
compreendidos consensualmente em seis distintas DTUs TcI - TcVI (Zingales et al.,
2009). Vago e colaboradores (2000) demonstraram a variabilidade genética do parasita
como sendo um dos fatores determinantes da forma digestiva ou cardíaca da DC. A
correlação das DTUs com a forma clínica da DC crônica é circunstancial, mas não
comprovada, em muitos casos pela ocorrência de infecções mistas e a complexa
interação do parasito com a resposta imune do hospedeiro (Urbina 2010; Zingales et al.,
2012). Aqui, utilizamos a cepa Colombiana (TcI), que é um importante agente de
infecção humana na Amazônia, Região Andina, América Central e México.
Apresentações clínicas incluem miocardiopatia chagásica e casos graves de
meningoencefalite em hospedeiros imunocomprometidos (Zingales et al., 2014).
Anteriormente, Federici (1964) utilizando uma cepa de T. cruzi (Colombiana) isolada de
um paciente na Colômbia e injetada em camundongos C3H/He, mostrou que os mesmos
apresentaram pico de parasitemia após o dia 30 de infecção, inflamação e fibrose
cardíaca, características semelhantes a DC humana (Higuchi et al., 2003) e reproduzidas
experimentalmente por nosso grupo (Artigo I). Sendo a infecção pelo T. cruzi uma
desordem multifatorial, diferentes modelos genéticos experimentais são potentes
155
ferramentas para identificar moléculas chave na patogenia da doença e direcionar novas
estratégias de intervenção na doença.
O progressivo processo de lesão tecidual e disfunção cardíaca característica da
DC crônica resulta de um conjunto de mecanismos celulares e moleculares ainda não
esclarecidos. Evidências, como a presença de TNF no tecido cardíaco e em órgãos
linfóides de animais aguda e cronicamente infectados (Talvani et al., 2000; dos Santos
et al., 2001) e no tecido cardíaco de pacientes portadores da CCC (Reis et al., 1993;
Reis et al., 1997), indicaram que esta citocina pudesse contribuir para alterações
fisiopatológicas durante a infecção pelo T. cruzi. Um possível envolvimento do TNF na
fisiopatogenia da CCC foi trazido pelos trabalhos demonstrando correlação positiva
entre níveis de TNF e disfunção cardíaca, indicada pela diminuição da fração de ejeção
do ventrículo esquerdo (FEVE) (Ferreira et al., 2003; Pérez-Fuentes et al., 2003;
Talvain et al., 2004). O nível elevado de TNF em pacientes com doenças cardíacas
despertou interesse dos pesquisadores em investigar o efeito das terapias anti-TNF nas
doenças cardíacas e também na CCC. Alguns estudos mostram que a utilização de
terapia anti-TNF (anticorpo monoclonal infliximab) nas fases aguda (Kroll-Palhares et
al., 2008) e crônica (Perez et al., 2009) da infecção pelo T. cruzi foi benéfico na redução
dos danos ao coração, reduzindo em especial a miocardite por célula CD8+. O estudo de
Perez e colaboradores (2009) mostra que o efeito benéfico de anti-TNF na miocardite
foi associado a redução da expressão de mRNA de TNF no tecido cardíaco. Por outro
lado, um único estudo utilizando o etarnecept (TNFR2 solúvel), como proposta para
bloqueio da ação de TNF, em hamsters infectados pelo T. cruzi sugeriu piora na CCC
experimental com alterações ecocardiográficas e redução de sobrevivência (Bilate et al.,
2007). Contudo, não houve redução do mRNA de TNF no ventrículo esquerdo. Este
aparente paradoxo enfatiza a necessidade de se compreender os mecanismos de ação
dos fármacos bem como o papel do TNF e os fatores limitantes das novas ferramentas
terapêuticas que o tem como alvo (Wong et al. 2008). Neste sentido, nós mostramos que
o uso da terapia anti-TNF usando infliximab na fase crônica da infecção pelo T. cruzi
não reativa a parasitemia nem exacerba o parasitismo já controlado. Além disso, a
terapia imunorreguladora melhora as alterações eletrocardiográficas e reduz os danos ao
tecido cardíaco. Em paralelo à redução da expressão de mRNA de TNF no tecido
cardíaco e dos baixos níveis séricos de TNF, a terapia com infliximab reposicionou a
resposta imune favorecendo a expressão de IL-10, reduzindo a atividade citotóxica de
156
células T CD8+ parasito específicas, enquanto a produção de IFNγ manteve-se
preservada. A frequência de células CD4+ e CD8+ esplênicas expressando o receptor 1
de TNF (TNFR1) foi reduzida. Além disso, nos camundongos tratados com infliximab
houve redução no número de células CD8+ infiltrando o tecido cardíaco, bem como o
número de células Pfn+, entretanto o número de células IFNγ+ não foi alterado.
Anteriormente, a terapia com anti-TNF (infliximab) foi associada à redução do número
de células T de memória efetora (CD8+CCR7-CD45RA+) que expressam perforina e
granulisina na infecção por Mycobacterium tuberculosis (Miller & Ernst, 2009). Na
infecção pelo T. cruzi, a presença de células Pfn+ na inflamação cardíaca,
provavelmente sustentada por TNF (uma vez que tratando com anti-TNF as mesmas
diminuem), é peça-chave na patogênese da CCC (Silverio et al., 2012). Após a infecção,
o próprio TNF pode desencadear e/ou manter o circuito inflamatório sistêmico e
cardíaco não benéficos, o que pode contribuir para a patogênese da CCC, trazendo a
citocina TNF como um ponto central no desequilíbrio imunológico relacionado à forma
cardíaca da DC.
Na CCC, o infiltrado inflamatório cardíaco é composto principalmente de
células mononucleares, em especial os linfócitos T CD8+ (Higuchi et al., 1997),
reproduzido experimentalmente em camundongos infectados com a cepa Colombiana
do T. cruzi (dos Santos et al., 2001; Silverio et al., 2010; Silverio et al., 2012).
Anteriormente propusemos que uma ferramenta terapêutica adequada poderia interferir
com as subpopulações distintas de células T CD8+ melhorando a lesão cardíaca
(Silverio et al., 2012) e, como vimos anteriormente, essa modulação pode ser
dependente da (ou apenas ter uma alça na) regulação de TNF/TNFR1. Então, lançamos
mão da PTX, um agente imunorregulador não esteróide com efeitos hemorreológicos
que tem sido usado em uma gama de doenças infecciosas, vasculares e condições
inflamatórias inibindo a síntese de citocinas pró-inflamatórias, como o TNF,
(Windmeier & Gressner 1997; Rauchhaus, 2000; Martín et al., 2003). Em doenças
parasitárias PTX já foi sugerida como adjuvante para o tratamento de leishmaniose
cutânea e malária (Lessa et al., 2001; Báfica et al., 2003; Muniz-Junqueira, 2007). É
importante salientar que este é o primeiro estudo usando a PTX para o tratamento da
fase crônica da infecção pelo T. cruzi. Anteriormente, PTX foi utilizada na fase aguda
da DC e mostrou uma redução na extensão das áreas de necrose e do número de células
TNF+ no baço (Andrade et al., 2008), porém nenhum outro efeito benéfico foi relatado
157
em relação à sobrevivência (todos os animais de todos os grupos estavam mortos de 1213 dpi), sobretudo não foi avaliado o efeito da PTX em relação à função cardíaca,
principal alvo de interesse nesta infecção (Lannes-Vieira et al., 2009, Rassi Jr. et al.,
2010). Em ambos os modelos experimentais de CCC, moderada (C57BL/6) e grave
(C3H/He), a administração de PTX teve um efeito benéfico não só em diminuir a
progressão da CCC, mas também revertendo as alterações já instaladas, restaurando a
condução elétrica do coração. PTX foi previamente mostrada ter efeitos benéficos na
falha cardíaca isquêmica aumentando a FEVE em pacientes (Sliwa et al., 2004). No
nosso estudo vimos que a infecção de camundongos C57BL/6 com a cepa Colombiana
do T. cruzi leva a dilatação das câmaras do coração, com aumento de massa e perda de
FEVE. Assim, o tratamento destes animais com PTX reduziu as áreas ventriculares e
aumentou a FEVE mostrando o efeito benéfico de PTX em uma condição diferente das
outras já estudadas (no caso, uma cardiopatia de natureza inflamatória e parasitária).
No presente trabalho, a terapia com PTX apresentou excelentes resultados,
reduzindo a distância entre as Cx43, diminuindo fibrose e os níveis de atividade de CKMB no soro em animais de ambos os modelos de CCC. Mais importante, nem a
administração de anti-TNF (infliximab), nem de a de PTX influenciaram no parasitismo
cardíaco, mas melhoraram a função cardíaca e a condução elétrica nos camundongos
revertendo significativamente o dano cardíaco já instalado, suportando que a inflamação
persistente associada à lesão cardíaca (Freitas et al., 2005) é dissociada da resposta
imunológica eficaz que contribui para o controle dos parasitos (Marino et al., 2004;
Medeiros et al., 2009). Na CCC existe a busca por terapias efetivas, como o uso do
antagonista parcial de CCR1/CCR5 - o MetRANTES - em modelos experimentais, já
mostrou ser capaz de reduzir a deposição de FN no tecido cardíaco nas fases aguda e
crônica da infecção pelo T. cruzi (Marino et al., 2004, Medeiros et al., 2009), algo
também mostrado no tratamento com a droga tripanossomicida Bz (Andrade et al.,
1991). O uso de MetRANTES na fase crônica também levou à redução dos níveis da
atividade de CK-MB no soro e à preservação das fibras cardíacas, com distribuição
regular das Cx43 (Medeiros et al., 2009) no tecido cardíaco dos camundongos
infectados pelo T. cruzi. No modelo de infecção in vitro de células musculares cardíacas
cultivadas em monocamada, o uso de Amiodarona, um fármaco antiarrítmico indicado
para pacientes com sintomatologia cardíaca da DC e que apresenta propriedades antiT. cruzi (Benaim et al., 2006), também restaurou a expressão de Cx43 nos
158
cardiomiócitos e ainda restabeleceu a contratilidade espontânea destas células (Adesse
et al., 2011). Camundongos A/J infectados com a cepa Brazil do T. cruzi e tratados na
fase aguda com o inibidor da enzima conversora de angiotensina, captopril,
apresentaram redução da fibrose e inflamação cardíaca, sem alteração do parasitismo
(Leon et al., 2003). Outro fármaco já no mercado, a sinvastatina, que além dos efeitos
nos níveis de colesterol apresenta propriedades anti-inflamatórias, também já foi testada
em modelos murinos (Silva et al., 2012) e caninos (Melo et al., 2011) de infecção pelo
T. cruzi mostrando ser capaz de diminuir o infiltrado inflamatório no tecido cardíaco.
Recentemente, ao estudar pacientes com a forma cardíaca da DC em uma coorte do
estado de Pernambuco mostramos que pacientes tratados com cardioprotetores
(inibidores de ECA e outros) apresentam redução dos níveis séricos de TNF, quando
comparados aos que não fazem uso deste tipo de fármaco (Marinho et al., em
preparação). Juntos, estes trabalhos buscam uma alternativa viável para o tratamento da
CCC, visando uma melhora dos sintomas clínicos e principalmente uma maior
qualidade de vida para o paciente cardiopata.
A esplenomegalia é caracterizada pela persistente ativação policlonal de células
T e B no baço (Minoprio et al., 1986). Esta está presente na infecção pelo T. cruzi,
tanto na fase aguda (Kierszenbaum & Hayes, 1980) quanto na fase crônica (Pereira et
al., 1999) da infecção e tem como resultado o aumento da quantidade de células
ativadas do baço. A terapia com PTX reduziu significativamente o peso relativo do
baço, indicando que os animais tratados não apresentaram a esplenomegalia intensa
como os animais não tratados (NT) ou que receberam o veículo do tratamento (salina).
Esses dados corroboram dados anteriores (Kroll-Palhares et al., 2008), que mostram que
a esplenomegalia na infecção pelo T. cruzi está associada à sinalização TNF/TNFR1,
uma vez que PTX reduziu a expressão de TNFR1 (mas não alterou a expressão de TNF)
no tecido cardíaco e a frequência de células T CD8+ expressando este receptor.
Anteriormente, a administração de PTX foi mostrada reduzir a expressão de TNFR1 em
hepatócitos (Mahmoud et al., 2012), indicando que este efeito não se restringe
particularmente a um tipo celular. Em pacientes com DC, as células T CD8+ mostram
fenótipos anormais de ativação marcados por baixa expressão de CD8 e TCR (Albareda
et al., 2006). Embora em camundongos cronicamente infectados com a cepa
Colombiana não foram detectadas alterações na frequência de células T CD8+
esplênicas e na densidade de moléculas de CD8 na superfície das células, a baixa
159
modulação na expressão do TCRαβ em células T CD8+ foi notada, corroborando dados
anteriores (Grisotto et al., 2001). Em camundongos tratados com PTX a frequência de
células expressando TCR e a densidade de TCRαβ na membrana celular foram
restauradas para intensidades semelhantes aos camundongos controles não infectados.
Nas células T naïve, o complexo TCR é constitutivamente internalizado e rapidamente
volta para a superfície celular. No entanto, por um processo molecular ainda não
completamente compreendido, a estimulação antigênica aumenta a retenção/degradação
do TCR baixando a densidade do mesmo na superfície celular em associação com a
função efetora reduzida (Jang et al., 2003; James et al., 2010). Portanto, na infecção
crônica pelo T. cruzi a terapia com PTX pode interferir com o processamento do TCR e
restaurar a capacidade de células T CD8+ para responder aos sinais de ativação, mas isto
deve ser melhor explorado. As células T CD8+ tem um importante papel na resistência à
infecção pelo T. cruzi (Rodrigues et al., 2003). Portadores de DC apresentam aumento
significativo na frequência de células T CD8+ com perfil de memória/efetora (CD45RACCR7-), suportando um estímulo contínuo por antígenos dos parasitos (Albareda et al.,
2006). De forma semelhante, o aumento da frequência de células T CD8+ com perfil de
memória/efetora (CD45RA-CCR7-) foi detectado
em
camundongos
C57BL/6
cronicamente infectados pelo T. cruzi. A terapia com PTX não interferiu com a
frequência destas células, suportando que os animais tratados são potencialmente
propensos a controlar patógenos invasores (Sallusto et al., 1999). Por outro lado, a
terapia
com
PTX
restaurou
o
compartimento
de
células
T
CD8+
naive
(CD45RA+CCR7+), restaurando potencialmente a homeostase e permitindo a resposta
imune a novos estímulos. Durante a infecção crônica pelo T. cruzi há um aumento
significativo na frequência de células CD8+ com o fenótipo de ativação, ou seja, células
expressando CD44+CD62L-, corroborando dados anteriores mostrando este efeito
durante a infecção aguda (Paiva et al., 1999). A terapia com PTX diminuiu a frequência
de células CD8+ expressando CD44+CD62L- e aumentou a frequência de células CD8+
CD44-CD62L+. Portanto, PTX interferiu com o perfil de memória/ativação das células
esplênicas.
Na CCC, os infiltrados inflamatórios no tecido cardíaco são compostos
principalmente por células mononucleares, em especial linfócitos T CD8+ (Higuchi et
al., 1997), e não estão diretamente relacionados à intensidade do parasitismo, diante da
escassez de parasitas, mas aparentemente com a persistência destes, como reproduzido
160
nos camundongos infectados com a cepa Colombiana do T. cruzi (dos Santos et al.,
2001, Medeiros et al., 2009, Silverio et al., 2012). Neste trabalho, mostramos que a
terapia com PTX alterou significativamente o número e a composição de células
inflamatórias no tecido cardíaco. Considerando o possível papel dos distintos perfis de
células T produtoras de IFN e Pfn, respectivamente, no controle do T. cruzi e nos
danos ao tecido cardíaco (Michailowsky et al., 2001; Silverio et al., 2010; Silverio et al.,
2012) e as ferramentas imunológicas disponíveis (peptídeos imunodominantes H2-Kb
restrito ao antígeno ASP2 do T. cruzi e camundongos imunodeficientes com
background B6), adotamos o modelo de CCC moderada (C57BL/6) para explorar o
efeito das diferentes estratégias terapêuticas sobre essas células. Analisamos a
influência de PTX na resposta imune sistêmica específica do parasito e a composição
diferencial de células inflamatórias infiltrantes no tecido cardíaco. Os nossos resultados
mostraram que os camundongos cronicamente infectados tratados com PTX
mantiveram o status de IFNγ produzido por células CD8+ que reconhecem o peptideo
imunodominante H-2Kb ASP2 VNHRFTLV. Um número reduzido de células Pfn+ foi
detectado no coração dos camundongos tratados, enquanto que o número de células de
IFNγ+ manteve-se inalterado quando comparado aos camundongos infectados controles,
dados semelhantes à terapia com infliximab. Considerando o papel funcional das células
inflamatórias que infiltram o tecido cardíaco, há uma boa correlação entre o número de
células IFNy+ e células T CD8+ de portadores de DC que apresentam controle dos
parasitos (Reis et al., 1997). Por outro lado, as células infiltrantes Pfn+, provavelmente a
maioria delas células T CD8+ que atuam como CTL, estão relacionadas aos danos no
tecido cardíaco durante a CCC experimental (Silverio et al., 2010; Silverio et al., 2012).
De maneira interessante, os estudos em pacientes com CCC grave mostraram que a
presença de células expressando granzima A, um outro componente da maquinaria lítica
de células de CD8+ com atividade citotóxica, nas lesões do tecido cardíaco (Reis et al.,
1993). Além disso, camundongos deficientes em Pfn apresentaram menor atividade de
CK-MB no soro e redução na perda de expressão de Cx43, paralelo à diminuição das
anormalidades elétricas (Silverio et al., 2010). As células CD8+Pfn+ já foram mostradas
ter maior capacidade de migrar para o tecido cardíaco, uma vez que co-expressam alta
frequência de CCR5+LFA-1+ como consequência, lesioná-lo (Silverio et al., 2012). Na
infecção pelo T. cruzi há aumento na frequência de células T CD8+CCR5+LFA-1+ no
baço (Medeiros et al., 2009), o tratamento com PTX reduz a freqüência destas células,
161
potencialmente capazes de migrar para o tecido cardíaco, além de tornar esse tecido
menos permissivo à entrada destas células, uma vez que reduz a expressão de ICAM-1,
ligante de LFA-1, no endodélio. Um trabalho anterior demonstrou, em modelo de
injúria pulmonar, o efeito benéfico de PTX reduzindo a expressão de ICAM-1 no tecido
alvo da injúria, o pulmão (Zhang et al., 2010). Assim, estes dados podem explicar o
menor número de células inflamatórias no tecido cardíaco e também a redução do
número de células Pfn+ neste sítio e, consequentemente, menos lesão.
Consensualmente, a persistência do parasito e a desregulação da resposta imune
contribuem para a patogenia da CCC (Lannes-Vieira et al., 2009, Dutra et al., 2009). A
terapia com Bz (100 mg/kg/dia), iniciada na infecção aguda impediu as anormalidades
elétricas na fase crônica (Garcia et al., 2005). Como a terapia com PTX mostrou-se
benéfica na CCC, mas o parasitismo persistiu, elaboramos uma terapia combinada
usando PTX com dose sub-ótima (25 mg/kg/dia) de Bz, para minimizar possíveis
efeitos colaterais (Guedes et al., 2011). A terapia combinada pode ser uma valiosa
alternativa para melhoria da eficácia terapêutica, uma vez que: (i) permite o uso de pelo
menos dois compostos que podem atuar sobre diferentes elementos celulares e vias
metabólicas; (ii) pode reduzir as concentrações das drogas e o número de doses,
contribuindo assim para a diminuição dos efeitos tóxicos; (iii) pode minimizar o risco
de resistência às drogas (Vivas et al., 2008). Durante a infecção crônica, Bz deverá
desempenhar seu papel tripanossomicida bem como dar suporte ao controle do
desbalanço imunológico, uma vez que já foi descrito ter atividades imunomoduladoras
(Ronco et al., 2011). Embora as terapias com PTX, Bz e Bz+PTX tenham melhorado e
até mesmo revertido os aspectos da CCC, a única terapia que sustentou a reversão nas
alterações eletrocardiográficas após a interrupção do tratamento foi a associação das
drogas PTX+Bz, enfatizando a complexidade dos fatores que contribuem para a CCC.
Em contraste com a PTX, que não teve nenhum efeito, Bz reduziu a carga parasitária no
tecido cardíaco e a parasitemia. Entretanto, na terapia associada (PTX+Bz), vimos que
PTX não interferiu com a eficácia de Bz em controlar os parasitos. Ainda, os
camundongos tratados com Bz e PTX+Bz apresentaram redução na expressão de
mRNA de TNF no coração e diminuição dos níveis de NOx e sTNFR1 no soro. Então
especulamos que Bz complementa os efeitos da PTX quer por controlar diretamente o
T. cruzi ou agindo de forma indireta, pois além do seu papel adjuvante na resposta
imunológica efetora em matar o parasita, Bz pode atuar como um imunomodulador, por
162
exemplo, através da diminuição da expressão do fator de transcrição NF-kB, que é
fundamental para a produção de TNF (Ronco et al., 2011). De forma importante, TNF
favorece a infecção pelo T. cruzi (Pinto et al., 2011). Assim, a redução da expressão de
TNF por Bz também pode interferir neste circuito em que TNF alimenta o parasitismo.
A gravidade da DC foi associada com níveis elevados de NO (Pérez-Fuentes et
al., 2007) e NO tem sido implicado na lesão cardíaca em macacos e camundongos
(Carvalho et al., 2012) infectados pelo T. cruzi. Embora, NO seja um agente
tripanossomicida na infecção aguda (Silva et al., 2003), sua redução durante a infecção
crônica, particularmente após a terapia PTX+Bz, não altera o controle dos parasitos. Em
2012, Paiva e colaboradores mostraram que o estresse oxidativo contribui para a
persistência do parasito nas células do hospedeiro e mais recentemente mostrou-se que
TNF e NO favorecem a infecção de astrócitos pelo T. cruzi (Silva et al., 2015). Neste
caso, o uso de anti-oxidantes pode ser benéfico. Os mecanismos subjacentes a melhoria
da condição do coração após a terapia PTX+Bz permanecem incertos. É possível que os
efeitos positivos desta terapia combinada sejam devido a intervenção em um circuito
não benéfico desencadeada por um aumento de TNF na infecção pelo T. cruzi, o qual
pode promover a expressão de TNFR1 e o TNF sinalizando via TNFR1 são
combustíveis para a produção de NO. Assim, a terapia combinada seria uma proposta
para interferir racionalmente neste circuito, com o objetivo de melhorar o prognóstico
da CCC.
Terapias combinadas não são novidade, infecções crônicas como a tuberculose
(Nahid et al., 2006), a síndrome da imunodeficiência adquirida (SIDA) (Simon et al.,
2006), a malária (Ngasala et al., 2011) e tripanossomíase africana (Priotto et al., 2009)
já adotam esta estratégia em seus tratamentos. Na infecção pelo T. cruzi o uso
concomitante de uma ou mais drogas vem sendo proposto, quer seja usando drogas com
alvo no parasito (Ribeiro et al., 2009), quer seja usando drogas com diferentes alvos,
como parasito e sistema imunológico (Lannes-Vieira et al., 2010), para minimizar os
efeitos colaterais e otimizar o tratamento. A combinação de cetoconazol e Bz foi testada
para tratar camundongos infectados com diferentes cepas do T. cruzi (cepa CL, Y e
Colombiana) mostrando ser somente efetivo (teste parasitológico e sorológico) para as
cepas CL e Y (Araújo et al., 2000). Clomipramina e alopurinol foram utilizados para o
tratamento da infecção aguda experimental pelo T. cruzi impedindo a evolução da
cardiopatia crônica (Rivarola et al., 2001). Recentemente, clomipramina foi associada a
163
Bz para o tratamento de fase aguda em camundongos Swiss infectados com a cepa
Tulahuen do T. cruzi reduzindo a mortalidade, a parasitemia e o infiltrado inflamatório
no tecido cardíaco (Strauss et al., 2013). Além disso, Bz e posaconazol foram
administrados individualmente ou em combinação em modelo murino de infecção
aguda, mostrando que o curto tratamento (7 dias) a combinação de drogas tem mais
eficácia em reduzir a parasitemia que as drogas usadas isoladamente (Diniz et al., 2013),
ressaltando a importância de se estudar terapias combinadas.
A fibrose é um marco da CCC (Andrade et al., 1989; Andrade et al., 1991;
Marino et al., 2003). Um efeito marcante observado nas terapias com PTX, Bz e
PTX+Bz foi a redução da deposição de FN. Essa possível reversão da fibrose no tecido
cardíaco já fora descrita na terapia com Bz e MK-436 (3-(1-methyl-5-nitroimidazol-2yl)-3a,4,5,6,7,7a-hexahydro1,2-benzisoxazole) na fase crônica da infecção pelas cepas
21SF e Colombiana do T. cruzi (Andrade et al., 1991), o que revelou ser a fibrose
cardíaca induzida pela infecção pelo T. cruzi um processo reversível. A PTX é um dos
vários agentes que tem sido estudado como terapia potencial antifibrogênica. Estudos in
vitro realizados em fibroblastos dérmicos sugerem que a PTX pode exercer um efeito
antifibrogênico, reduzindo a proliferação celular, diminuindo a síntese de componentes
da
matriz
extracelular
(incluindo
colágeno
tipo
I,
colágeno
tipo
III,
e
glicosaminoglicanos), e aumentando a atividade da colagenase (Berman & Duncan,
1989; Duncan et al., 1995). O que nos leva a especular que PTX (sozinha ou combinada
a Bz) pode estar, de fato, revertendo a fibrose em nossos modelos de CCC, visto que
este fármaco já mostrou possuir propriedades antifibrogênicas em outros modelos, como
de fibrose hepática in vitro (Windmeier & Gressner, 1996) e in vivo (Peterson, 1993).
Tanto Bz quanto PTX, sozinhos ou combinados, reduziram a expressão de
TNFR1 no tecido cardíaco. Embora TNFR1 participe do controle do T. cruzi durante a
infecção aguda (Aliberti et al., 2001), a ausência de TNFR1 na fase crônica não
interferiu com o controle do parasito. TNF, atuando em TNFR1, mas não em TNFR2,
agrava a insuficiência cardíaca induzida por ligação coronariana em modelos
experimentais (Hamid et al., 2009). Na cardiopatia experimental induzida por
angiotensina II, TNFR1 contribuiu para a fibrose cardíaca, aumentando a expressão de
mRNA para colágeno tipo I e III no tecido cardíaco (Duerrschmid et al., 2013). Diante
de nossos dados e da literatura, TNF atuando via TNFR1 parece estar relacionado à
perda da expressão de Cx43 e ao depósito de matriz extracelular (fibrose). Receptores
164
solúveis do TNF podem ser poderosos preditores de mortaliadade em pacientes com IC
(Rauchhaus et al., 2000; Deswal et al., 2001). Além disso, esses receptores já foram
mostrados refletir a manifestação sistêmica da gravidade da IC congestiva em pacientes
(Nozaki et al., 1997), o que demonstra a importância da identificação e possivelmente
modulação destes receptores em doenças cardíacas em geral. Considerando que a
doença isquêmica cardíaca é a principal causa de mortalidade no Brasil e no mundo, e
que a sua prevalência está aumentando, é importante aprofundar o estudo acerca dos
biomarcadores laboratoriais úteis na avaliação diagnóstica e na estratificação de risco,
por exemplo para o infarto agudo do miocárdio. Neste sentido, vários marcadores têm
apresentado eficácia na detecção da necrose, isquemia, inflamação e disfunção cardíaca,
dentre eles a troponina, mioglobina, CK-MB, proteína C reativa, peptídeo natriurético
tipo B, moléculas de adesão e até mesmo as citocinas, como IL-6 e TNF (revisado em
Silva & Moresco, 2011). Biomarcadores também são potencialmente úteis para avaliar a
eficácia do tratamento e progressão da DC. Recentemente, vários marcadores de
prognóstico e progressão para T. cruzi foram descobertos e descritos, incluindo
moléculas do parasito, como as tGPI-mucinas, e moléculas do sistema imune do
hospedeiro, como IFNγ e IL-10, mas apenas alguns deles foram avaliadas após
tratamento específico (revisado em Pinazo et al., 2015).
O ECO permite quantificar a lesão miocárdica com grande potencial para
avaliação da morbidade e do prognóstico dos pacientes com DC. Esse método
complementar permite melhor estratificação de risco, com impacto no manejo clínico da
CCC (Nunes et al., 2010). Estudos prévios registraram anormalidade precoce do
relaxamento ventricular esquerdo em portadores da DC (Barros et al., 2001; Caeiro et
al., 1985). O acúmulo de fibras colágenas intersticial na CCC pode, inicialmente,
determinar alterações no relaxamento ventricular e, progressivamente, reduzir a
complacência miocárdica causando aumento da pressão atrial esquerda. A disfunção
diastólica causa estiramento dos cardiomiócitos, levando ao remodelamento ventricular
e intensa ativação neuro-hormonal (Barbosa et al., 2007). Esses fatores contribuem para
a evolução desfavorável da CCC. Assim, a disfunção diastólica é um importante
marcador de gravidade da DC (Nunes et al., 2009; 2010). No conhecimento da história
natural da DC, alterações no ECG precedem o aparecimento de sintomas (Garzon et al.,
1994). Estudando anormalidades no ECG e sua relação com função ventricular sistólica
(volumes ventriculares e FE pela angiografia) na DC, observa-se uma relação entre a
165
diminuição da função sistólica ventricular esquerda com a progressão e associação de
anormalidades no ECG, como arritmias ventriculares (Casado et al., 1990). Sendo o
ECO e o ECG técnicas não invasivas, estas se mostram potentes ferramentas para o
diagnóstico e acompanhamento dos pacientes com DC.
Em relação a DC há necessidade de se encontrar drogas eficientes e menos
tóxicas para agir especificamente contra o patógeno (Coura & Castro, 2002). Vários
estudos observacionais têm mostrado que os pacientes crônicos submetidos ao
tratamento antiparasitário com Bz, embora não obtenham a cura parasitológica, tiveram
uma redução significativa na ocorrência de alterações eletrocardiográficas e menor
frequência de piora na sua condição clínica (Viotti & Vigliano 2007). Entretanto, Bz
possui algumas limitações como efeitos colaterais indesejáveis, longo protocolo de
tratamento e eficácia limitada (Dias & Dessoy 2009; Becerra et al., 2012). A busca por
novos compostos para o tratamento da DC é estimulada. Fármacos para seu tratamento
não são do interesse das indústrias farmacêuticas, estando na raiz do problema o elevado
custo dos investimentos e a falta de um mercado potencial. Nos últimos 25 anos, apenas
1% de todos os medicamentos desenvolvidos foi para tratar alguma doença
negligenciada (Chirac & Torreele, 2006). Aparentemente, os inibidores da biossíntese
de ergosterol são os candidatos mais promissores para novos tratamentos da DC
(Urbina, 2009). O D0870 (Zeneca Pharmaceuticals, Macclesfield, UK) e o SCH56592
(posaconazol, Schering-Plough Research Institute, New Jersey, USA), com atividade
inibitória seletiva na biossíntese de novos esteróides no parasito mostraram-se ativos
contra cepas do T. cruzi resistentes a Bz e nifurtimox e mantiveram sua atividade
mesmo em hospedeiros imunossuprimidos (Urbina, 2002). Entre camundongos tratados
com D0870, verificou-se cura parasitológica em 70% a 90%, além de uma menor
incidência de morte (Urbina et al, 1996; Molina et al., 2000). O DO870 foi capaz de
curar 70% a 100% de camundongos infectados na fase aguda com várias cepas do
T. cruzi, incluindo a Colombiana, ao passo que, na fase crônica, a taxa de cura
parasitológica foi de 30% a 45%. O Posaconazol, um análogo do itraconazol, pode
eliminar seletivamente amastigotas intracelulares do T. cruzi em cultura de
cardiomiócitos e permite a completa reorganização do citoesqueleto da célula
hospedeira e do aparelho contrátil (Silva et al., 2006). Recentemente, posaconazol se
mostrou eficiente no tratamento de paciente com a forma crônica da DC (Pinazo et al.,
2010). Está previsto um estudo clínico de fase II com o Pozaconazol na Espanha,
166
financiado pela Merck & Co (Buckner e Navabi., 2010). O ravuconazol é outro triazol
com potente atividade antifúngica in vitro e in vivo, sendo comparável ou superior a
outros triazóis, como o posaconazol. A atividade do ravuconazol na dose de 15mg/Kg
na infecção experimental aguda causada por diferentes cepas do T. cruzi resistentes a
nitrofurano e nitroimidazol, foi capaz de induzir cura parasitológica em todos os
animais infectados com a cepa CL e em 58% dos animais infectados com cepa Y; em
animais infectados com a cepa Colombiana, não houve cura. Outro triazol, o
cetoconazol, suprimiu a parasitemia entre animais infectados com cepas CL e Y, porém,
em camundongos infectados com a cepa Colombiana, a parasitemia reincidiu em 35
dias (Urbina et al , 2003). Uma série de estudos clínicos randomizados (BENEFIT,
TRAENA, CHAGAZOL, STOP CHAGAS, E1224, revisados em Urbina et al., 2014)
foram lançados na última década para avaliar a segurança e eficácia do Bz e dois
inibidores da biossíntese do ergosterol, posaconazol e ravuconazol. Os primeiros
resultados indicam que Bz é eficaz na indução de uma redução acentuada e prolongada
no nível dos parasitos circulantes na maioria dos pacientes, mas os efeitos adversos
podem levar ao abandono do tratamento em 10-20% dos casos. Inibidores da biossíntese
do ergosterol são melhor tolerados, mas sua eficácia na duração da dose de tratamento
utilizado nos estudos iniciais foi significativamente menor. As terapias combinadas
emergem como perspectiva promissora, mas a falta de biomarcadores validados de
resposta ao tratamento etiológico e eventuais curas parasitológicas em pacientes
crônicos continuam a ser um desafio (Urbina et al., 2014). Apesar da potente atividade
contra o T. cruzi dos inibidores da biossíntese do ergosterol e da ausência de resistência
cruzada com as drogas utilizadas correntemente, a resposta ao tratamento é
extremamente variável entre diferentes cepas do parasito (Guedes et al., 2004, Toledo et
al., 2003, Molina et al., 2000, Diniz et al., 2010). Além disso, mesmo alguns compostos
como o Posaconazol e o E1224, uma pró-droga do Ravuconazol já estarem em estudos
clínicos o alto custo e a complexidade de produção são fatores limitantes na utilização
desses compostos no tratamento humano (Urbina, 2009). Aqui, mostramos que mesmo
usando 1/4 da dose recomendada de Bz, a carga parasitária (T. cruzi, cepa Colombiana)
foi reduzida e as alterações elétricas, como arritmias e bloqueios átrio ventriculares,
melhoradas, atestando a eficiência do uso de Bz na fase crônica da infecção
experimental.
167
O desenvolvimento de novas terapias ou até mesmo o melhoramento das
existentes e ainda uma vacina eficaz é um importante passo para a saúde pública em
DC. Uma série de grupos está avançando no desenvolvimento de vacinas baseadas no
uso do parasito atenuado, proteína purificada, proteína recombinante, DNA e, mais
recentemente, bactérias deficientes na replicação e vetores virais recombinantes para
reduzir parasitismo, inflamação aguda do coração e miocardite crônica (Paiva et al.,
1999; Garg & Tarleton 2002; Dumonteil et al., 2004; Cazorla et al., 2009; Nogueira et
al., 2011; Dumonteil et al., 2012; Gupta et al., 2013). Dois antígenos promissores de
T. cruzi utilizados como candidatos vacinais são a proteína 2 de superfície de
amastigota (ASP2) (Garg et al., 2002) e a trans-sialidase (TS) (Schenkman et al., 1994).
A proteína ASP2, epítopo VNHRFTLV, é um membro da conservada família de
proteínas trans-sialidases (Low et al., 1998). Mostrou-se imunodominante após a
infecção de camundongos C57BL/6 com parasitos de diferentes cepas (Tzelepis et al.,
2008) e foi descrita ter potente atividade indutora de CTL (Low et al., 1998). A ASP2
foi utilizada em preparações de vacina de DNA ou de proteína recombinante (Boscardin
et al., 2003; Vasconcelos et al., 2004) e incorporada em adenovírus (Machado et al.,
2006) mostrando serem capazes de induzir resposta específica de células T citotóxicas,
reduzir parasitemia e aumentar sobrevivência. Recentemente, o nosso grupo demonstrou
por ensaio ELISPOT que o número de células específicas para o peptídeo ASP2
VNHRFTLV produtoras de IFNγ e com atividade CTL foi mantido elevado, mesmo
com a redução da parasitemia na infecção crônica pela cepa Colombiana do T. cruzi
(Silverio et al., 2012). Já as TS compõem uma família de proteínas codificadas por mais
de 1.400 genes e estão ligadas, em sua maioria, à membrana do parasita através de
âncoras de GPI (El-Sayed et al., 2005; Freitas et al., 2011). Freire-de-Lima et al. (2010)
demonstraram que o T. cruzi utiliza a TS para manipular a sialilação de células T CD8+
permitindo o escape do parasita do sistema imune e o estabelecimento da infecção no
hospedeiro. Essas enzimas atuam especificamente removendo resíduos de ácido siálico
ligados na posição α-2,3 de glicoproteínas, glicolipídeos e oligossacarídeos do
hospedeiro, transferindo-os para moléculas aceptoras localizadas na superfície do
parasita (Freire-de-Lima et al., 2010). Como uma mudança fisiológica, após a ativação,
os linfócitos T CD8+ são desializados, aumentando a sua atividade efetora por modular
a acessibilidade de seus receptores às moléculas de MHC de classe I (Moody et al.,
2001; Daniels et al., 2001; Moody et al., 2003). No entanto, durante a infecção, o
168
T. cruzi utiliza a TS para resializar a superfície das células T CD8+, o que dificulta a
interação antígeno-célula efetora, enfraquecendo a resposta imune celular (Freire-DeLima et al., 2010). Experimentos vacinais (vacina de DNA) em camundongo mostraram
que TS induz resposta celular (mediadas por células T tanto CD4+ quanto CD8+) e
humoral (Rodrigues et al., 1999). Aqui usamos o adenovírus recombinante humano tipo
5 (rAdHu5) transportando sequências dos antígenos de T. cruzi ASP2 e TS. A vacinação
usando vetores virais recombinantes tem se tornado uma estratégia promissora para a
indução de imunidade mediada por células T contra agentes infecciosos intracelulares
(Miyahira, 2005). Estes vetores vacinais caracterizam-se pela alta capacidade de
infecção, imunogenicidade e servem como veículos para endereçamento vacinal,
tornando os antígenos disponíveis para a maquinaria intracelular de processamento
antigênico e subsequente apresentação e consequentemente ativação de diferentes tipos
celulares (Rocha et al., 2004). Recentemente, um ensaio clínico de fase 1 realizado na
China testou os efeitos de uma vacina composta por diferentes concentrações (baixa e
alta) de rAdHu5 expressando glicoproteínas do vírus Ebola Zaire 2014 em pacientes
saudáveis. Uma única dose (alta concentração) da vacina foi capaz de induzir produção
de anticorpos anti-glicoproteína e resposta específica de células T produtoras de IFNγ
contra o vírus Ebola em 14 dias pós-imunização, mostrando que esta preparação foi
segura (uma vez que nenhum efeito adverso significativo foi observado) e imunogênica
(Zhu et al., 2015).
A administração de rAdVax (rAdASP2 + rAdTS) em um protocolo de
imunização profilática induziu imunogenicidade, resposta de células T CD8 específicas
com atividade citotóxica e produtoras de IFNγ, além de reduzir o parasitismo cardíaco
na fase aguda e as anormalidades elétricas na fase crônica. Diferentes estratégias já
foram testadas para melhorar a resposta imune e sobrevivência na DC. Em estudo de
Alencar e colaboradores (2009), camundongos A/Sn foram imunizados (com uma ou
duas doses) com o rAdHu5 expressando ASP2 e duas semanas após a última dose de
imunização os camundongos foram desafiados com 150 tripomastigotas sanguíneos da
cepa Y do T. cruzi. O pico da parasitemia foi maior nos camundongos imunizados com
uma dose da vacina, quando comparado àqueles que receberam duas doses. A
sobrevivência também diferiu significativamente entre os grupos de camundongos
imunizados com duas doses de AdASP2 em comparação com os animais injetados
apenas uma vez (P < 0,001), indicando que a imunidade protetora nos camundongos que
169
receberam a dose de reforço foi elevada. Machado e colaboradores (2006)
demonstraram que duas imunizações sequenciais com o rAdHu5 expressando ASP2 e
TS foram capazes de reduzir significativamente a parasitemia e melhorar a
sobrevivência dos camundongos vacinados, quando eles foram desafiados com a cepa Y
do T. cruzi. Estes dados nos encorajaram a testar o protocolo homólogo de indução e
reforço (prime-boost) como estratégia profilática e terapêutica para retardar a
progressão da doença.
Este trabalho foi o primeiro a propor uma vacina terapêutica para a CCC. Na
vacinação terapêutica observamos o aumento da sobrevida e redução das anormalidades
elétricas após o prime (análise de 160 dpi) e boost (análise em 180 e 230 dpi). Na pósterapia os camundongos apresentaram menos lesão cardíaca, refletido pela redução na
deposição de FN, menor distancia entre as Cx43 e atividade sérica de CK-MB; e ainda
apresentaram menores anormalidades elétricas em comparação com os camundongos
analisados na pré-terapia. Em relação a resposta imune, a vacinação terapêutica com
rAdVax (i) preservou a imunidade específica mediada por IFNγ, mas reduziu a resposta
a estímulos policlonais (anti-CD3 mais anti-CD28) e (ii) diminuiu a frequência de
células T CD8+CD107a+. Além disso, a terapia com rAdVax reposicionou a resposta
imune no tecido cardíaco, reduzido o número de células Pfn+, preservando o número de
células IFNγ+, que tiveram a expressão de seu mRNA aumentado. O efeito benéfico da
imunoterapia com rAdVax pode residir na relação favorável entre IFNγ/Pfn. Ainda no
tecido cardíaco, a vacinação com rAdVax reduziu a expressão de mRNA de iNOS e
baixou os níveis de NO no soro. iNOS/NO têm sido implicados na lesão cardíaca em
macacos e camundongos infectados com T. cruzi (Carvalho et al., 2012) e associado
com a gravidade da DC (Pérez-Fuentes et al., 2007).
Imunizações sequenciais são questionadas quanto ao risco de que os anticorpos
anti-vetor gerados após a primeira dose podem neutralizar o vetor quando ele é usado na
dose reforço e, consequentemente, a resposta imune seria dificultada. Contudo,
recentemente, uma vacina para tuberculose utilizando o rAdHu5 expressando um
antígeno dominante do M. tuberculosis (Ag85A - AdHu5Ag85A) demonstrou ser
segura e fortemente imunogênica. Não houve correlação entre anticorpos IgG antirAdHu5 preexistentes e anticorpos neutralizantes ou entre a magnitude da ativação de
células T induzidas pela vacina e os títulos de anticorpos neutralizantes rAdHu5 préexistentes (Smaill et al., 2013). Além disso, os anticorpos neutralizantes pré-existentes
170
não afetaram a imunogenicidade de uma vacina contra a malária baseada no uso de
rAdHu5 (Tamminga et al., 2011). No presente trabalho, a dose de reforço foi importante
para reduzir significativamente os níveis de NOx no soro, paralelamente, os
camundongos que receberam duas doses de rAdVax apresentaram redução do dano
cardíaco, anormalidades elétricas de menor gravidade e maior sobrevivência. Isto nos
sugere que o protocolo homólogo prime-boost usando rAdVax pode ser uma alternativa
racional para reprogramar a resposta imune e recuperar a lesão tecidual e funcionalidade
cardíaca na DC crônica.
Parcerias à nível mundial tem unido esforços para a elaboração de uma vacina
efetiva para da DC (Dumonteil et al., 2013). Recentemente, uma vacina de DNA
codificando os antígenos TSA-1 e TC24 do T. cruzi foi testada num modelo canino de
infecção aguda. Os cães foram imunizados com duas doses de 500 g de vacina de DNA,
com duas semanas de intervalo entre as mesmas, em seguida foram infectados por
T. cruzi (cepa SylvioX10) duas semanas após a segunda dose da vacina. Um outro
grupo de cães foi infectado e tratado com a vacina nos dias 15 e 30 pós infecção. Ambos
os protocolos de vacinação preventiva e terapêutica na fase aguda reduziram
significativamente a parasitemia, inflamação cardíaca e carga parasitária no tecido
cardíaco e ainda mantiveram os níveis de IG anti-T. cruzi. Na vacina terapêutica foi
observado um aumento dos níveis séricos de IFNγ, entretanto outras alterações
imunológicas não foram abordadas e ainda as alterações eletrocardiográficas não foram
estatisticamente significativas, provavelmente devido ao pequeno número de animais.
Porém os dados prévios levaram os autores a sugerir que esta vacina de DNA
codificando os antígenos TSA-1 e Tc24 pode ser um candidato à vacina veterinária
(Quijano-Hernández et al., 2013). Uma outra estratégia de vacina profilática foi testada
em camundongos C57BL/6 imunizados com vacina de DNA contendo TcG2/TcG4
(proteínas altamente conservadas entre as cepas do T. cruzi) em um protocolo DNA prime/proteína-boost. Os camundongos foram desafiados com a cepa Sylvio X10/4 do
T. cruzi em 120 ou 180 dias pós-vacinação. A vacina reduziu em 2-3 vezes a carga
parasitária e forneceu imunidade anti-T. cruzi a longo prazo, uma vez que induziu uma
potente atividade nas células T citotóxicas e estimulou predominantemente o fenótipo
de células T CD8+ de memória efetora (CD44+CD62L-), capaz de responder ao desafio
com o T. cruzi 4-6 meses após o boost com rápida expansão de um fenótipo de células
poli-funcionais (CD107a+IFNγ+Pfn+), que levou a redução da carga parasitária no tecido
171
(Gupta & Garg et al., 2015), porém a integridade e a função cardíaca não foram
exploradas neste trabalho.
Tantas intervenções variáveis podem gerar certo grau de ceticismo para o
eventual desenvolvimento e produção de uma vacina contra a DC. Entretanto, alguns
desses problemas podem ser mais acadêmicos que práticos e não necessariamente
precisam ser resolvidos antes que uma vacina efetiva seja alcançada (Brener & Camargo
et al., 1982). Ironicamente, há menos conhecimento acerca do genoma e proteoma do
Schistosoma mansoni, causador da esquistossomose, e do Ancylostoma duodenale,
causador da ancilostomose, em que há estudos clínicos da vacina em humanos em
andamento, do que para a maioria das outras infecções em que nenhum estudo humano
está em andamento, como a DC, demonstrando que o conhecimento técnico não é o
fator limitante (Hotez & Ferris, 2006). Outro problema enfrentado pelas vacinas são os
movimentos de resistência à vacinação. Com pouca ou nenhuma informação baseada
em evidências científicas, ativistas anti-vacinas têm tentado influenciar toda uma
geração de pais com medos e dúvidas sobre vacinas. As vacinas já foram associadas a
todo tipo de problema, o autismo é um exemplo bem conhecido, uma vez que suas
causas diretas não estão claras. A despeito da histeria e da cobertura da mídia, não há
provas ligando as vacinas em uso a patologias. Na verdade, evidências epidemiológicas
mostram que as vacinas evitam uma grande quantidade de doenças e mortes no mundo
(Shelby & Ernst, 2013). Os benefícios de uma vacina potencial para T. cruzi em
comparação com a utilização de agentes quimioterapêuticos padrão incluem toxicidade
reduzida, permitindo a utilização expandida em pacientes crônicos e os doentes com comorbidades, uso potencial durante a gravidez para prevenir a transmissão congênita,
uma maior proteção contra complicações cardíacas, e remoção de barreiras de
tratamento associados com o esforço e custo de administrar tratamentos repetidos de
drogas.
A DC faz parte do grupo de doenças infecciosas consideradas “extremamente
negligenciadas”, afetando milhões de pessoas em toda a América Latina. Embora
recentes avanços tenham sido alcançados no controle da transmissão vetorial e
transfusional, ainda existem problemas críticos, incluindo um tratamento efetivo para os
casos crônicos da doença. Após quase um século do descobrimento da DC e, apesar do
grande volume de trabalhos científicos envolvendo a biologia, imunologia e genética do
T. cruzi, ainda não foi possível desenvolver novas e eficazes ferramentas terapêuticas
172
para as pessoas afetadas em diferentes pontos do globo. Aqui, voltamos nosso olhar
para os casos crônicos da doença, em especial para o acometimento cardíaco.
Desenvolvemos modelos experimentais que reproduziram aspectos críticos da CCC e
que serviram de ferramenta para nossas perguntas. Em todos os trabalhos utilizamos o
modelo de CCC moderada, que nos permite estudar a regeneração e também a evolução
para a CCC grave. Nosso alvo é propor um tratamento para aqueles pacientes portadores
da forma cardíaca cujo estadiamento do comprometimento miocárdico na CCC
encontra-se nos grupos A-C (segundo a classificação do Consenso Brasileiro em doença
de Chagas, 2005), para que não progridam clinicamente e até mesmo obtenham reversão
das alterações instaladas. Assim como o Consenso, vislumbramos a melhora da
qualidade de vida e da sobrevida dos pacientes. Neste trabalho trouxemos várias
alternativas para o tratamento da DC crônica, que vão de agentes imunorreguladores,
passado pela quimioterapia, terapia combinada e chegando até a vacina, mostrando que
é possível interferir racionalmente com os fatores não benéficos da DC e que a resposta
imune é chave neste contexto.
Como comparado por Hotez e colaboradores em 2012, a SIDA e a DC são duas
condições crônicas causadas por patógenos sanguíneos que requerem tratamento caro e
de longo prazo, para a qual não há cura ou vacina preventiva eficaz. Ambas as doenças
afetam grande número de pessoas e produzem um fardo social e econômico substancial.
Atualmente, o número de pessoas infectadas com o T. cruzi na América do Sul é
estimado em mais de cinco vezes o número de pessoas infectadas com o HIV na mesma
região; no entanto, o número global de infecções por HIV é maior do que o número de
indivíduos infectados com T. cruzi (Rassi et al., 2010; Mahy et al., 2014). Ambas as
doenças apresentam riscos de infecção para os destinatários de transfusão de sangue e
doação de órgãos e aos filhos de mães infectadas não tratadas. Além disso, ambas as
doenças são altamente estigmatizadas e afetam desproporcionalmente as pessoas que
vivem na pobreza e não têm condições de buscar apoio médico e social necessário para
manter a melhor qualidade de vida possível nestas condições. Estas comparações fazemse necessárias para aumentar a conscientização sobre a gravidade da DC e a necessidade
de buscar alternativas para o controle da mesma. O futuro sucesso na luta contra a DC é
dependente de uma gestão eficaz de focos infecciosos emergentes, manutenção de
elevados níveis de consciência pública, interesse governamental no controle da doença,
ferramentas terapêuticas, diagnóstico e vigilância. Lições aprendidas a partir dos
173
últimos 100 anos de luta contra a infecção pelo T. cruzi devem ser continuamente
aplicadas e melhoradas para se obter um progresso contínuo e até mesmo chegar a
eliminar a DC.
6. Conclusões
___________________________________________________________________________________
Neste estudo descrevemos dois modelos experimentais de CCC, um moderado
(C57BL/6) e outro grave (C3H/He), que reproduzem aspectos relevantes da doença de
Chagas.
Mostramos que o desequilíbrio imunológico é ponto chave na manutenção da
lesão cardíaca na infecção crônica pelo T. cruzi e que interferir neste ponto é benéfico
no tratamento da CCC.
Trazemos evidências de que TNF/TNFR1 não é crucial para o controle do
parasito na fase crônica da infecção pelo T. cruzi, mas participa do mecanismo
patogênico da lesão cardíaca.
Na infecção crônica pelo T. cruzi os diferentes perfis de células T CD8+ (IFNγ –
inflamatório / Pfn – citotóxico) são passíveis de modulação via tratamento
farmacológico.
Os nossos dados demonstram que interferir na inflamação e no agente etiológico
da doença (terapia combinada) é uma estratégia terapêutica eficaz visando a não
progressão ou, mesmo, a reversão da forma cardíaca crônica da DC.
Propomos uma vacina terapêutica, como uma alternativa para reposicionar o
status imunológico e, consequentemente, melhorar e/ou reverter aspectos patológicos
que contribuem para a CCC.
Juntos, os trabalhos mostram que é possível interferir na inflamação crônica não
benéfica e manter o controle dos parasitos, seja usando fármacos imunorreguladores,
seja usando vacina, associado ou não à droga tripanossomicida. Isto abre caminhos e
possibilidades para o tratamento de fase crônica de pacientes com DC.
174
7. Perspectivas
___________________________________________________________________________________
Este trabalho trouxe as seguintes perspectivas:
Caracterizar a participação da via de sinalização de TNF (TNFR1 e TNFR2) na
patogenia da CCC experimental, estudando os mecanismos moleculares (vias: NFκB,
PI3K/AKT, AMPK e mTOR) pelos quais TNF e seus receptores levariam à formação
de lesão das células cardíacas e à cardiomiopatia chagásica crônica.
Estudar os efeitos da inibição/ativação das vias NFκB, PI3K/AKT, AMPK e
mTOR na expressão de TNF, seus receptores e as consequências biológicas para as
células
T
CD8+
(proliferação,
expressão
de
marcadores
de
memória/ativação/senescência, expressão de IFNγ e Pfn e padrão de migração celular),
associando às alterações histológicas e funcionais cardíacas.
Dar continuidade ao estudo da imunoterapia com rAdVax testando o protocolo
experimental em outros modelos de infecção pelo T. cruzi (ex.: modelo canino), com o
objetivo de termos uma vacina veterinária para a DC visando impactar o ciclo
peridoméstico de transmissão da DC.
Contribuir para a identificação dos alvos moleculares associados à patogenia da
CCC, de modo a propor novas estratégias terapêuticas, incluindo a multiterapia com
dois ou mais alvos terapêuticos, abordando o tripé sustentador da CCC (o parasito, a
desregulação imunológica e as alterações cardíacas), com a finalidade de melhorar o
prognóstico dos portadores da forma cardíaca crônica da DC.
175
8. Referências
___________________________________________________________________________________
Abbas AK, Lichtman AH, Pober JS. Imunologia Celular e Molecular. 4ª ed. Rio de Janeiro:
Revinter, 2002.
Abrahamsohn IA, Coffman RL. Cytokine and nitric oxide regulation of the immunosuppression
in Trypanosoma cruzi infection. J Immunol. 155: 3955–3963, 1995.
Acquatella H. Echocardiography in Chagas heart disease. Circulation. 115: 1124–1131, 2007.
Adesse D, Azzam EM, Meirelles Mde N, Urbina JA, Garzoni LR. Amiodarone inhibits
Trypanosoma cruzi infection and promotes cardiac cell recovery with gap junction and
cytoskeleton reassembly in vitro. Antimicrob Agents Chemother. 55: 203–210, 2011.
Albareda MC, Laucella SA, Alvarez MG, Armenti AH, Bertochi G, Tarleton RL, Postan M.
Trypanosoma cruzi modulates the profile of memory CD8+T-cells in chronic Chagas' disease
patients. Int Immunol. 18: 465–471, 2006.
Aliberti JC, Machado FS, Souto JT, Campanelli AP, Teixeira MM, Gazzinelli RT, Silva JS.
Betachemokines enhance parasite uptake and promote nitric oxide-dependent microbiostatic
activity in murine inflammatory macrophages infected with Trypanosoma cruzi. Infect Immun
67: 4819–4826, 1999.
Aliberti JCS, Cardoso MAG, Martins GA, Gazinelli RT, Vieira LQ and Silva JS. Interleukin-12
mediates resistance to Trypanosoma cruzi in mice and is produced by murine macrophages in
response to live trypomastigotes. Infect. Immun. 64: 1961–1967, 1996.
Aliberti JCS, Souto JT, Marino APMP, Lannes-Vieira J, Teixeira MM, Farber J, Gazzinelli RT,
e Silva JS. Modulation of chemokine production and inflammatory responses in IFN-γ and
TNFR1 deficient mice during Trypanosoma cruzi infection. Am. J. Pathol. 158: 1433–1440,
2001.
Almeida IC, Gazzinelli RT. Proinflammatory activity of glycosylphosphatidylinositol anchors
derived from Trypanosoma cruzi: structural and functional analyses. J Leukoc Biol. 70: 467–
477, 2001.
Amir O, Rogowski O, David M, Lahat N, Wolff R, Lewis BS. Circulating interleukin 10:
association with higher mortality in systolic heart failure patients with elevated tumor necrosis
factor - alpha. Isr Med Assoc J. 12:158–62, 2010.
Andrade SG, Freitas LA, Peyrol S, Pimentel AR, Sadigursky M. Experimental chemotherapy of
Trypanosoma cruzi infection: persistence of parasite antigens and positive serology in
parasitologically cured mice. Bull World Health Organ. 69: 191–197, 1991.
Andrade SG, Magalhães JB, Pontes AL. Therapy of the chronic phase of the experimental
infection by Trypanosoma cruzi with benzonidazole and nifurtimox. Rev Soc Bras Med Trop.
22:113–118, 1989.
Andrade SG, Magalhães LA, Pessina DH, Importance of TNF-a in the course of acute infection
with Trypanosoma cruzi: influence of its inhibition by pentoxifylline treatment, Mem Inst
Oswaldo Cruz. 103: 21–26, 2008.
176
Andrade SG, Stocker-Guerret S, Pimentel AS, Grimaud JA. Reversibility of cardiac fibrosis in
mice chronically infected with Trypanosoma cruzi, under specific chemotherapy. Mem Inst
Oswaldo Cruz. 86: 187–200, 1991.
Andrade ZA. Fisiopatogenia da doença de Chagas. Revista de Patologia Tropical. 29: 131–140,
2000.
Andrade ZA. Mechanisms of myocardial damage in Trypanosoma cruzi infection. Ciba Found
Symp. 99: 214–233, 1983.
Angelkort B, Maurin N, Boateng K. Influence of pentoxifylline on erythrocyte deformability in
peripheral occlusive arterial disease. Curr Med Res Opin. 6 :255–258, 1979.
Anker SD, Coats AJ. How to RECOVER from RENAISSANCE? The significance of the results
of RECOVER, RENAISSANCE, RENEWAL and ATTACH. Int J Cardiol. 86: 123–130, 2002.
Aparicio-Burgos JE, Zepeda-Escobar JA, de Oca-Jimenez RM, Estrada-Franco JG, BarbabosaPliego A, Ochoa-García L, Alejandre-Aguilar R, Rivas N, Peñuelas-Rivas G, Val-Arreola M,
Gupta S, Salazar-García F, Garg NJ, Vázquez-Chagoyán JC. Immune protection against
Trypanosoma cruzi induced by TcVac4 in a canine model. PLoS Negl Trop Dis. 9: e0003625,
2015.
Araujo AF, de Alencar BC, Vasconcelos JR, Hiyane MI, Marinho CR, Penido ML, Boscardin
SB, Hoft DF, Gazzinelli RT, Rodrigues MM. CD8+-T-cell-dependent control of Trypanosoma
cruzi infection in a highly susceptible mouse strain after immunization with recombinant
proteins based on amastigote surface protein 2. Infect Immun. 2005 Sep;73(9):6017-25.
Araujo FF, Gomes JA, Rocha MO, Williams-Blangero S, Pinheiro VM, Morato MJ, Correa
Oliveira R. Potential role of CD4+CD25HIGH regulatory T cells in morbidity in Chagas
disease. Front Biosci. 12: 2797–2806, 2007.
Araujo M.S., Martins-Filho O.A., Pereira M.E. & Brener Z. A combination of benznidazole and
ketoconazole enhances efficacy of chemotherapy of experimental Chagas' disease. J
Antimicrob Chemother. 45: 819–824, 2000.
Babu BMVS, Reddy BP, Priya VH, Munshi A, Rani HS, Latha GS, Rao VD, Jyothy A.
Cytokine gene polymorphisms in the susceptibility to acute coronary syndrome. Genetic Testing
and Molecular Biomarkers. New York. 16: 359–365, 2012.
Báfica A, Oliveira F, Freitas LA, Nascimento EG, Barral A. American cutaneous leishmaniasis
unresponsive to antimonial drugs: successful treatment using combination of Nmethilglucamine antimoniate plus pentoxifylline. Int J Dermatol. 42: 203–207, 2003.
Bahia-Oliveira LM, Gomes JA, Cançado JR, Ferrari TC, Lemos EM, Luz ZM, Moreira MC,
Gazzinelli G, Correa-Oliveira R. Immunological and clinical evaluation of chagasic patients
subjected to chemotherapy during the acute phase of Trypanosoma cruzi infection 14-30 years
ago. J Infect Dis. 182: 634–638, 2000.
Bahia-Oliveira LM, Gomes JA, Rocha MO, Moreira MC, Lemos EM, Luz ZM, Pereira ME,
Coffman RL, Dias JC, Cançado JR, Gazzinelli G, Corrêa-Oliveira R. IFN-gamma in human
Chagas' disease: protection or pathology? Braz J Med Biol Res. 31: 127–31, 1998.
Barbosa MM, Nunes Mdo C, Ribeiro AL, Barral MM, Rocha MO. N-terminal pro BNP levels
in patients with Chagas disease: A marker of systolic and diastolic dysfunction of the left
ventricle. Eur J Echocardiogr. 8: 204–212, 2007.
177
Barbosa RP, Filho BG, Dos Santos LI, Junior PA, Marques PE, Pereira RV, Cara DC, BruñaRomero O, Rodrigues MM, Gazzinelli RT, Machado AV. Vaccination using recombinants
influenza and adenoviruses encoding amastigote surface protein-2 are highly effective on
protection against Trypanosoma cruzi infection. PLoSOne 8:e61795, 2013.
Barros MVL, Rocha OdCM, Ribeiro LPA, Machado SF. Tissue doppler Imaging in the
evaluation of the regional diastolic function in Chagas’ disease. Eur J Echocardiography. 2: 94–
99, 2001.
Basombrio MA, Arredes H. Long-term immunological response induced by attenuated
Trypanosoma cruzi in mice. Journal of Parasitology. 73: 236–238, 1987.
Basombrio MA, Besuschio S, Cossio PM. Side effects of immunization with live attenuated
Trypanosoma cruzi in mice and rabbits. Infection and Immunity 36: 342–350, 1982.
Basombrio MA, Besuschio S. Trypanosoma cruzi culture used as a vaccine to prevent chronic
Chagas’ disease in mice. Infection and Immunity. 36: 351–356, 1982.
Basso B, Cervetta L, Moretti E, Carlier Y, Truyens C. Acute Trypanosoma cruzi infection: IL12, IL-18, TNF, sTNFR and NO in T. rangeli-vaccinated mice. Vaccine. 22: 1868–1872, 2004.
Basso B, Moretti E, Fretes R.Vaccination with epimastigotes of diferente strains of
Trypanosoma rangeli protects mice against Trypanosoma cruzi infection. Mem Inst Oswaldo
Cruz. 103: 370–374, 2008.
Becerra MC, Guiñazú N, Hergert LY, Pellegrini A, Mazzieri MR, Gea S, Albesa I. In vitro
activity of N-benzenesulfonylbenzotriazole on Trypanosoma cruzi epimastigote and
trypomastigote forms. Exp Parasitol. 131 :57–62, 2012.
Benaim G, Sanders JM, Garcia-Marchán Y, Colina C, Lira R, Caldera AR, Payares G, Sanoja
C, Burgos JM, Leon-Rossell A, Concepcion JL, Schijman AG, Levin M, Oldfield E, Urbina JA.
Amiodarone has intrinsic anti-Trypanosoma cruzi activity and acts synergistically with
posaconazole. J Med Chem. 49: 892–899, 2006.
Beraún Y, Nieto A, Collado MD, González A, Martín J. Polymorphisms at tumor necrosis
factor (TNF) loci are not associated with Chagas' disease. Tissue Antigens. 52: 81–83, 1998.
Berman B, Duncan MR. Pentoxifylline inhibits normal human dermal fibroblast in vitro
proliferation, collagen, glycosaminoglycan, and fibronectin production, and increases
collagenase activity. J Invest Dermatol. 92: 605–610, 1989.
Beyaert R, Fiers W. Tumor necrosis factor and lymphotoxin. In: Mire-Sluis A, Thorpe R (eds).
Cytokines. 2nd ed. California: Academic Press, 335–45, 1999.
Bezerra, M. J. R. Avaliação da associação de polimorfismos nos genes do TNF-α e do receptor
de leptina com a Síndrome Coronariana Aguda em pacientes do Real Hospital Português – PE.
2013. Dissertação (Mestrado Acadêmico em Saúde Pública) – Centro de Pesquisas Aggeu
Magalhães, Recife, 2013.
Bezzera WS, Meneguetti DUO, Camargo LMA. A busca de fármacos para tratamento da
Tripanossomíase Americana: 103 anos de negligência. Revista Saúde (Sant Maria). 38: 09–20,
2012.
Bhatia V, Sinha M, Luxon B, Garg N. Utility of the Trypanosoma cruzi sequence database for
identification of potential vaccine candidates by in silico and in vitro screening. Infect Immun.
72: 6245–6254, 2004.
178
Bilate AM, Salemi VM, Ramires FJ, de Brito T, Russo M, Fonseca SG, Faé KC, Martins DG,
Silva AM, Mady C, Kalil J, Cunha-Neto E. TNF blockade aggravates experimental chronic
Chagas disease cardiomyopathy. Microbes Infect. 9: 1104–1113, 2007.
Biolo A, Ribeiro AL, Clausell N. Chagas cardiomyopathy – where do we stand after a hundred
years? Prog Cardiovasc Dis. 2010.
Black CM, Israelski DM, Suzuki Y, Remington JS. Effect of recombinant tumour necrosis
factor on acute infection in mice with Toxoplasma gondii or Trypanosoma cruzi. Immunology.
68: 570–574, 1989.
Bocchi EA, Marcondes-Braga FG, Ayub-Ferreira SM, Rohde LE, Oliveira WA, Almeida DR, e
cols. Sociedade Brasileira de Cardiologia. III Diretriz Brasileira de Insuficiência Cardíaca
Crônica. Arq Bras Cardiol. 93: 1–71, 2009.
Boldt J. Cardiovascular system. Curr Opin Crit Care. 7: 313, 2001.
Bonney KM: Chagas disease in the 21st Century: a public health success or an emerging threat?
Parasite. 21: 11, 2014.
Boscardin SB, Kinoshita SS, Fujimura AE, Rodrigues MM. Immunization with Cdna expressed
by amastigotes of Trypanosoma cruzi elicits protective immune response against experimental
infection. Infect Immun. 71: 2744–2757, 2003.
Bozkurt B, Torre-Amione G, Warren MS, Whitmore J, Soran OZ, Feldman AM, Mann DL.
Results of targeted anti-tumor necrosis factor therapy with etanercept (ENBREL) in patients
with advanced heart failure. Circulation.103: 1044–1047, 2001.
Bradley JR, Thiru S, Pober JS. Disparate localization of 55-kd and 75-kd tumor necrosis factor
receptors in human endothelial cells. Am J Pathol. 146: 27–32, 1995.
Bradley JR. TNF-mediated inflammatory disease. J Pathol. 214: 149−160, 2008.
Brener Z, Krettli AU. Immunology of Chagas' disease. In Wyler, D. J. Modern Parasite
Biology. Cellular, immunological and molecular aspects. USA: 247–261, 1990.
Brener Z, Andrade Z. (Org.) - Trypanosoma cruzi e Doença de Chagas. Rio de
Janeiro:Guanabara Koogan, 1979.
Brener Z, Camargo EP. Perspectives of vaccination in Chagas´ disease. Scripta Varia
Academiae Vaticanum. 1982.
Brener Z, Gazzinelli RT. Immunological control of Trypanosoma cruzi infection and
pathogenesis of Chagas' disease. Int Arch Allergy Immunol. 114: 103–110, 1997.
Brockhaus M, Schoenfeld HJ, Schlaeger EJ, Hunziker W, Lesslauer W, Loetscher H.
Identification of two types of tumor necrosis factor receptors on human cell lines by monoclonal
antibodies. Proc Natl Acad Sci USA. 87: 3127–3131, 1990.
Buckner FS, Navabi N. Advances in Chagas disease drug development: 2009-2010.
Curr.Opin.Infect.Dis. 23: 609–616, 2010.
Cabal-Hierro L, Lazo PS. Signal transduction by tumor necrosis factor receptors. Cell Signal.
24: 1297–305, 2012.
179
Caeiro T, Amuchastegui LM, Moreyra E, Gibson DG. Abnormal left ventricular diastolic
function in chronic Chagas' disease: an echocardiographic study. Int J Cardiol. 9: 417–424,
1985.
Campos MA, Gazzinelli RT. Trypanosoma cruzi and its components as exogenous mediators of
inflammation recognized through Toll-Like receptors. Mediators Inflamm. 13: 139–143, 2004.
Cardillo F, Voltarelli JC, Reed SG, Silva JS. Regulation of Trypanossoma cruzi infection in
mice by gamma interferon and interleukin 10: Role of NK cells. Infect Immun. 64: 128–134,
1996.
Carvalho BG, de Souza RKT, Soares DA, Yagi MCN. Doenças Cardiovasculares antes e após o
Programa Saúde da Família, Londrina. Arq Bras Cardiol. 93: 645–650, 2009.
Carvalho CM, Silverio JC, da Silva AA, Pereira IR, Coelho JM, Britto CC, Moreira OC,
Marchevsky RS, Xavier SS, Gazzinelli RT, Bonecini-Almeida MG, Lannes-Vieira J. Inducible
nitric oxide synthase in heart tissue and nitric oxide in serum of Trypanosoma cruzi-infected
rhesus monkeys: association with heart injury. PLoS Negl Trop Dis 6: e1644, 2012.
Casado J, Davila DF, Donis JH, Torres A, Payares A, Colmenares R, Gottberg CF.
Electrocardiographic abnormalities and left ventricular systolic function in Chagas’ heart
disease. Int J Cardiol. 27: 55–62, 1990.
Cazorla SI, Frank FM, Malchiodi EL. Vaccination approaches against Trypanosoma cruzi
infection. Expert Rev Vaccines. 8: 921–935, 2009.
Cazorla SI, Frank FM, Malchiodi EL. Vaccination approaches against Trypanosoma cruzi
infection. Expert Rev Vaccines. 8: 921–935, 2009.
Chagas C. Nova tripanosomiaze humana. Mem. Inst. Oswaldo Cruz. 1:159–218, 1909.
Chandra M, Tanowitz HB, Petkova SB, Huang H, Weiss LM, Wittner M, Factor SM, Shtutin V,
Jelicks LA, Chan J, Shirani J. Significance of inducible nitric oxide synthase in acute
myocarditis caused by Trypanosoma cruzi (Tulahuen strain). Int J Parasitol. 32: 897–905, 2002.
Chirac P. & Torreele E. Global framework on essential health R&D. Lancet. 367: 1560–1561,
2006.
Chu, H, Yang J, Mi S, Bhuyan SS, Li J, Zhong L, Liu S, Tao Z, Li J, Chen H. Tumor necrosis
factor-alpha G-308A polymorphism and risk of coronary heart disease and myocardial
infarction: A case-control study and meta-analysis. Journal of Cardiovascular Disease Research.
3: 84–90, 2012.
Chung ES, Packer M, Hung K, Lo KH, Fasanmade AA, Willerson JT. Randomized,
doubleblind, placebo-controlled, pilot trial of infliximab, a chimeric monoclonal antibody to
tumor necrosis factor-α, in patients with moderate-tosevere heart failure. Circulation. 107:
3133−3140, 2003.
Cimerman, B.; Cemerman, S. Parasitologia Humana e seus Fundamentos Gerais. 2 ed. São
Paulo: editora Atheneu, 81–112, 2008.
Clark IA. How TNF was recognized as a key mechanism of disease. Cytokine Growth Factor
Rev. 18: 335–343, 2007.
Coimbra R, Melbostad H, Hoyt DB. Effects of phosphodiesterase inhibition on the
inflammatory response after shock: role of pentoxifylline. J Trauma. 56: 442–449, 2004.
180
Coletta AP, Clark AL, Banarjee P, Cleland JG. Clinical trials update: RENEWAL
(RENAISSANCE and RECOVER) and ATTACH. Eur J Heart Fail. 4: 559–561, 2002.
Consenso Brasileiro em Doença de Chagas, Secretaria de Vigilância em Saúde do Ministério da
Saúde. Revista da Sociedade Brasileira de Medicina Tropical. 38 (Suplemento III), 2005.
Costa GC, da Costa Rocha MO, Moreira PR, Menezes CA, Silva MR, Gollob KJ, Dutra WO.
Functional IL-10 gene polymorphism is associated with Chagas disease cardiomyopathy.
Journal of Infectious Diseases. 199: 451–454, 2009.
Cotta-de-Almeida V, Bertho AL, Villa-Verde DM, Savino W. Phenotypic and functional
alterations of thymic nurse cells following acute Trypanosoma cruzi infection. Clin Immunol
Immunopathol. 82: 125–32, 1997.
Coura JR, Castro SL de. A critical review on Chagas disease chemotherapy. Mem Inst Oswaldo
Cruz. 97: 3–24, 2002.
Criado L, Flórez O, Martín J, González CI. Genetic polymorphisms in TNFA/TNFR2 genes and
Chagas disease in a Colombian endemic population. Cytokine. 57: 398–401, 2012.
Cummings KL, Tarleton RL. iNOS is not essential for control of Trypanosoma cruzi infection
in mice. Infection and Immunity. 72: 4081–4089, 2004.
Cunha-Neto E, Nogueira LG, Teixeira PC, Ramasawmy R, Drigo SA, Goldberg AC, Fonseca
SG, Bilate AM, Kalil J. Immunological and non-immunological effects of cytokines and
chemokines in the pathogenesis of chronic Chagas disease cardiomyopathy. Mem Inst Oswaldo
Cruz. 104: 252–258, 2009.
Curtin JF, Cotter TG. Anisomycin activates JNK and sensitises DU145 prostate carcinoma cells
to Fas mediated apoptosis. Br J Cancer. 87: 1188-1194, 2002.
Daliry A, Pereira IR, Pereira-Junior PP, Ramos IP, Vilar-Pereira G, Silvares RR, Lannes-Vieira
J, Campos De Carvalho AC. Levels of circulating anti-muscarinic and anti-adrenergic
antibodies and their effect on cardiac arrhythmias and dysautonomia in murine models of
Chagas disease. Parasitology. 141: 1769–1778, 2014.
Daniels MA, Devine L, Miller JD, Moser JM, Lukacher AE, Altman JD, Kavathas P, Hogquist
KA, Jameson SC. CD8 binding to MHC class I molecules is influenced by T cell maturation
and glycosylation. Immunity. 15: 1051–1061, 2001.
De Alencar BC, Persechini PM, Haolla FA, de Oliveira G, Silverio JC, etal. Perforina and
gamma interferon expression. Are required for CD4+ and CD8+T-cell-dependent protective
immunity against a human parasite,Trypanosoma cruzi, elicited by heterologous plasmid DNA
prime-recombinant adenovirus 5 boost vaccination. Infect Immun 77: 4383–4395, 2009.
de Oliveira FL, Araujo-Jorge TC, de Souza EM, de Oliveira GM, Degrave WM, Feige JJ, Bailly
S, Waghabi MC. Oral Administration of GW788388, an Inhibitor of Transforming Growth
Factor Beta Signaling, Prevents Heart Fibrosis in Chagas Disease. PLoS Negl Trop Dis. 6:
e1696, 2012.
De Prost D, Ollivier V, Hakim J. Pentoxifylline inhibition of procoagulant activity generated by
activated mononuclear phagocytes. Mol Pharmacol. 38: 562–566, 1990.
de Souza ASB, Souza WKSB, Costa SA, de Moreira Freitas EM, Carvalho G, Batista Sá LM,
Rassi S. Incidence of Ventricular Arrhythmias after Stem Cell Therapy in Patients with Chagas
Cardiomyopathy. Arq Bras Cardiol. 102: 489–494, 2014.
181
de Souza W. Electron microscopy of trypanosomes - A historical view. Mem Inst Oswaldo
Cruz. 103: 313–325, 2008.
Deswal A, Bozkurt B, Seta Y, Parilti-Eiswirth S, Hayes FA, Blosch C, Mann DL. Safety and
efficacy of a soluble P75 tumor necrosis factor receptor (Enbrel, etanercept) in patients with
advanced heart failure. Circulation. 99: 3224–3226, 1999.
Deswal A, Petersen NJ, Feldman AM, Young JB, White BG, Mann DL. Cytokines and
Cytokine Receptors in Advanced Heart Failure An Analysis of the Cytokine Database from the
Vesnarinone Trial (VEST). Circulation. 103: 2055–2059, 2001.
Dias JCP, Amato Neto V, Luna EJA. Mecanismos alternativos de transmissão do Trypanosoma
cruzi no Brasil e sugestões para sua prevenção. Revista da Sociedade Brasileira de Medicina
Tropical, 44: 375–379, 2011.
Dias JC. Chagas disease control in Brazil: which strategy after the attack phase? Ann Soc Belg
Med Trop. 1:75–86, 1991.
Dias JCP, Coura JR, org. Clínica e terapêutica da doença de Chagas: uma abordagem prática
para o clínico geral [online]. Rio de Janeiro: Editora FIOCRUZ, ISBN 85-85676- 31-0, 1997.
Dias JCP. Doença de Chagas: sucessos e desafios. Cad Saude Publica. 22: 2020, 2006.
Dias JCP. Notas sobre o Trypanosoma cruzi e suas características bio-ecológicas, como agente
de enfermidades transmitidas por alimentos. Revista da Sociedade Brasileira de Medicina
Tropical. 39: 370–375, 2006.
Dias LC, Dessoy MA. Chemoterapy of Chagas' Disease: State of the art and perspectives for the
development of new drugs. Quim.Nova. 32: 2444–2457, 2009.
Dias, J. C. Globalization, inequity and Chagas disease. Cad Saude Publica. 23: 13-22, 2007.
Diniz LdF, Urbina JA, de Andrade IM, Mazzeti AL, Martins TAF, Caldas IS, Talvani A,
Ribeiro I, Bahia MT. Benznidazole and Posaconazole in Experimental Chagas Disease: Positive
Interaction in Concomitant and Sequential Treatments. PLoS Negl Trop Dis 7: e2367, 2013.
Diniz LF, Caldas IS, Guedes PM, Crepalde G, De LM, Carneiro CM, Talvani A, Urbina JA,
Bahia MT. Effects of ravuconazole treatment on parasite load and immune response in dogs
experimentally infected with Trypanosoma cruzi. Antimicrob Agents Chemother. 54: 2979–
2986, 2010.
Documento do Banco Mundial. Enfrentando o desafio das doenças nãotransmissíveis no Brasil.
Relatório No 32576-BR. 15 de novembro de 2005.
Dos Santos LI, Galvão-Filho B, de Faria PC, Junqueira C, Dutra MS, Teixeira SM, Rodrigues
MM, Ritter G, Bannard O, Fearon DT, Antonelli LR, Gazzinelli RT. Blockade of CTLA-4
promotes the development of effector CD8+ T lymphocytes and the therapeutic effect of
vaccination with an attenuated protozoan expressing NY-ESO-1. Cancer Immunol Immunother.
64 :311–23, 2015.
dos Santos PVA, Roffê E, Santiago HC, Torres RA, Marino APMP, Paiva CN, Silva AA,
Gazzinelli RT & Lannes-Vieira J. Prevalence of CD8+alpha beta T cells in Trypanosoma cruzi
elicited myocarditis is associated with acquisition of CD62LLowLFA-1HighVLA-4High
activation phenotype and expression of IFN-γ-inducible adhesion and chemoattractant
molecules. Microbes and Infection. 3: 971–984, 2001.
182
Drigo SA, Cunha-Neto E, Ianni B, Cardoso MR, Braga PE, Faé KC, Nunes VL, Buck P, Mady
C, Kalil J, Goldberg AC. TNF gene polymorphisms are associated with reduced survival in
severe Chagas' disease cardiomyopathy patients. Microbes Infect. 8: 598–603, 2006.
Drigo SA, Cunha-Neto E, Ianni B, Mady C, Faé KC, Buck P, Kalil J, Goldberg AC. Lack of
association of tumor necrosis factor alpha polymorphisms with Chagas disease in Brazilian
patients. Immunol Lett. 108: 109–111, 2007.
Duerrschmid C, Crawford JR, Reineke E, Taffet GE, Trial J, Entman ML, Haudek SB. TNF
receptor 1 signaling is critically involved in mediating angiotensin-II-induced cardiac fibrosis. J.
Mol Cell Cardiol. 57: 59–67, 2013.
Dumonteil E, Bottazzi ME, Zhan B, Heffernan MJ, Jones K, Valenzuela JG, Kamhawi S,
Ortega J, Rosales SP, Lee BY, Bacon KM, Fleischer B, Slingsby BT,Cravioto MB, TapiaConyer R, Hotez PJ. Accelerating the development of a therapeutic vaccine for human Chagas
disease: rationale and prospects. Expert Rev Vaccines. 11: 1043–1055, 2012.
Dumonteil E, Escobedo-Ortegon J, Reyes-Rodriguez N, Arjona-Torres A, Ramirez-Sierra MJ
Immunotherapy of Trypanosoma cruzi infection with DNA vaccines in mice. Infect Immun. 72:
46–53, 2004.
Duncan MR, Hasan A, Berman B. Pentoxifylline, pentifylline, and interferons decrease type I
and III procollagen mRNA levels in dermal fibroblasts: evidence for mediation by nuclear
factor 1 down-regulation. J Invest Dermatol. 104: 282–286, 1995.
Dutra WO, Menezes CAS, Villani FNA, da Costa GC, da Silveira ABM, d’Ávila Reis D,
Gollob KJ. Cellular and genetic mechanisms involved in the generation of protective and
pathogenic immune responses in human Chagas disease Mem Inst Oswaldo Cruz. 104: 208–
218, 2009.
Dutra WO, Rocha MO, Teixeira MM. The clinical immunology of human Chagas
Trends Parasitol. 21: 581–587, 2005.
disease.
El-Sayed NM, Myler PJ, Blandin G, Berriman M, Crabtree J, Aggarwal G, Caler E, Renauld H,
Worthey EA, Hertz-Fowler C, Ghedin E, Peacock C, Bartholomeu DC, Haas BJ, Tran AN,
Wortman JR, Alsmark UC, Angiuoli S, Anupama A, Badger J, Bringaud F, Cadag E, Carlton
JM, Cerqueira GC, Creasy T, Delcher AL, Djikeng A, Embley TM, Hauser C, Ivens AC,
Kummerfeld SK, Pereira-Leal JB, Nilsson D, Peterson J, Salzberg SL, Shallom J, Silva JC,
Sundaram J, Westenberger S, White O, Melville SE, Donelson JE, Andersson B, Stuart KD,
Hall N. Comparative genomics of trypanosomatid parasitic protozoa. Sci, 309: 404–409, 2005.
Fabrino DL, Leon LL, Genestra M, Parreira GG, Melo RC. Rat models to investigate host
macrophage defense against Trypanosoma cruzi. Journal of Innate Immunity. 3: 71–82, 2011.
Federici EE, Abelmann WH, and Neva FA. Chronic and progressive myocarditis in C3H mice
infected with Trypanosoma cruzi. Am. J. Trop. Med. Hyg. 13: 272–280, 1964.
Ferreira RC, Ianni BM, Abel LC, Buck P, Mady C, Kalil J, Cunha-Neto E. Increased plasma
levels of tumor necrosis factor-alpha in asymptomatic/“indeterminate” and Chagas disease
cardiomyopathy patients. Mem Inst Oswaldo Cruz . 98: 407–411, 2003.
Fichera LE, Albareda MC, Laucella SA, Postan M. Intracellular growth of Trypanosoma cruzi
in cardiac myocytes is inhibited by cytokine-induced nitric oxide release. Infect Immun. 72:
359–363, 2004.
183
Flórez O, Martín J, González CI. Interleukin 4, interleukin 4 receptor- and interleukin 10 gene
polymorphisms in Chagas disease. Parasite Immunology. 33: 506–511, 2011.
Frampton JE, Brogden RN. Pentoxifylline (oxpentifylline). A review of its therapeutic efficacy
in the management of peripheral vascular and cerebrovascular disorders. Drugs Aging. 7:480–
503, 1995.
Franco-Paredes C, Von A, Hidron A, Rodríguez-Morales AJ, Tellez I, Barragán M, Jones D,
Náquira CG, Mendez J. Chagas disease: an impediment in achieving the Millennium
Development Goals in Latin America. BMC Int Health Hum Rights 7:7, 2007.
Freire-De-Lima L, Alisson-Silva F, Carvalho ST, Takiya CM, Rodrigues MM, DosReis GA,
Mendonça-Previato L, Previato JO, Todeschini AR. Trypanosoma cruzi subverts host cell
sialylation and may compromise antigen-specific CD8+ T cell responses. J. Biol. Chem. 285:
13388–13396, 2010.
Freitas HFG, Chizzola PR, Paes AT, Lima ACP, Mansur AJ. Risk stratification in a Brazilian
hospital-based cohort of 1220 outpatients with heart failure: role of Chagas’ heart disease.
International Journal of Cardiology. 102: 239–247, 2005.
Freitas LM, dos Santos SL, Rodrigues-Luiz GF, Mendes TA, Rodrigues TS, Gazzinelli RT,
Teixeira SM, Fujiwara RT, Bartholomeu DC. Genomic analyses, gene expression and antigenic
profile of the trans-sialidase superfamily of Trypanosoma cruzi reveal an undetected level of
complexity. PLoS ONE 6: 25914, 2011.
Froelich CJ, Orth K, Turbov J, Seth P, Gottlieb R, Babior B, Shah GM, Bleackley RC, Dixit
VM, Hanna W. New paradigm for lymphocyte granule-mediated cytotoxicity. Target cells bind
and internalize granzyme B, but an endosomolytic agent is necessary for cytosolic delivery and
subsequent apoptosis. J Biol Chem. 271: 29073–29079, 1996.
Garcia S, Ramos CO, Senra JF, Vilas-Boas F, Rodrigues MM, Campos-de-Carvalho AC,
Ribeiro-Dos-Santos R, Soares MB. Treatment with benznidazole during the chronic phase of
experimental Chagas' disease decreases cardiac alterations. Antimicrob Agents Chemother. 49:
1521–1528, 2005.
Garg N, Tarleton RL. Genetic immunization elicits antigen-specific protective immune
responses and decreases disease severity in Trypanosoma cruzi infection. Infect Immun. 70:
5547–5555, 2002.
Garzon SAC, Lorga AM, Nicolau JC. Eletrocardiografia na cardiopatia chagásica. Rev Soc
Cardiol Est São Paulo. 4: 33–43, 1994.
Gazzinelli RT, Denkers EY. Protozoan encounters with Toll-like receptor signalling pathways:
implications for host parasitism. Nat Rev Immunol. 6: 895–906, 2006.
Gazzinelli RT, Oswald IP, Hieny S, James SL, Sher A. The microbicidal activity of interferongamma-treated macrophages against Trypanosoma cruzi involves an L arginine-dependent,
nitrogen oxide-mediated mechanism inhibitable by interleukin-10 and transforming growth
factor-beta. Eur J Immunol. 22: 2501-2056, 1992.
Gomes JA, Bahia-Oliveira LM, Rocha MO, Busek SC, Teixeira MM, Silva JS, Correa-Oliveira
R. Type 1 chemokine receptor expression in Chagas' disease correlates with morbidity in
cardiac patients. Infect Immun.73: 7960–7966, 2005.
184
Gomes JA, Bahia-Oliveira LM, Rocha MO, Martins-Filho OA, Gazzinelli G, Correa-Oliveira R.
Evidence that development of severe cardiomyopathy in human Chagas' disease is due to a
Th1specific immune response. Infect Immun.71: 1185–1193, 2003.
Gontijo ED, Andrade GMQ, Santos SE, Galvão LMC, Moreira EF, Pinto FS, Dias JCP,
Januário JN. Triagem neonatal da infecção pelo Tripanosoma cruzi em Minas Gerais, Brasil:
transmissão congênita e mapeamento das áreas endêmicas. Revista Epidemiol. Serv. Sáude. 18:
243–245, 2009.
Grisotto MG, D'Império Lima MR, Marinho CRF, Tadokoro CE, Abrahamsohn IA, Alvarez
JM. Most parasite-specific CD8+ cells in Trypanosoma cruzi-infected chronic mice are downregulated for T-cell receptor-αβ and CD8 molecules. Immunology. 102: 209–217, 2001.
Guedes PM, Silva GK, Gutierrez FR, Silva JS. Current status of Chagas disease chemotherapy.
Expert Rev Anti Infect Ther. 9: 609–620, 2011.
Guedes PM, Urbina JA, De LM, Afonso LC, Veloso VM, Tafuri WL, Hado-Coelho GL, Chiari
E, Bahia MT. Activity of the new triazole derivative albaconazole against Trypanosoma
(Schizotrypanum) cruzi in dog hosts. Antimicrob Agents Chemother. 48: 4286–4292, 2004.
Guedes PM, Veloso VM, Afonso LC, Caliari MV, Carneiro CM, Diniz LF, Marques-da-Silva
EA, Caldas IS, Do Valle Matta MA, Souza SM, Lana M, Chiari E, Galvão LM, Bahia MT.
Development of chronic cardiomyopathy in canine Chagas disease correlates with high IFNgamma, TNF-alpha, and low IL-10 production during the acute infection phase. Vet Immunol
Immunopathol. 130: 43–52, 2009.
Guedes PMM, Gutierrez FR, Silva GK, Dellalibera-Joviliano R, Rodrigues GJ, Bendhack LM,
Rassi A Jr, Rassi A, Schmidt A, Maciel BC, Marin Neto JA, Silva JS. Deficient Regulatory T
Cell Activity and Low Frequency of IL-17-Producing T Cells Correlate with the Extent of
Cardiomyopathy in Human Chagas’ Disease. PLoS Negl Trop Dis. 6: e1630, 2012.
Guedes PMM, Veloso VM, Talvani A, Diniz LF, Caldas IS, Do-Valle-Matta MA, Santiago
Silva J, Chiari E, Galvão LMC, Silva JS, Bahia MT. Increased type 1 chemokine expression
in experimental Chagas disease correlates with cardiac pathology in Beagle dogs. Veterinary
Immunology and Immunopathology. 138:106–113, 2010.
Guhl F, Ramírez JD. Trypanosoma cruzi I diversity: towards the need of genetic subdivision?
Acta Trop. 119: 1–4, 2011.
Gullestad L, Aukrust P. Review of trials in chronic heart failure showing broad-spectrum
antiinflammatory approaches. Am J Cardiol. 95: 17C–40C, 2005.
Gullestad L, Semb AG, Holt E, Skardal R, Ueland T, Yndestad A, Frøland SS, Aukrust P.
Effect of thalidomide in patients with chronic heart failure. Am Heart J. 144: 847–850, 2002.
Gupta S, Garg NJ. A Two-Component DNA-Prime/Protein-Boost Vaccination Strategy for
Eliciting Long-Term Protective T Cell Immunity against Trypanosoma cruzi. PLoS Pathog. 11:
e1004828, 2015.
Gupta S, Garg NJ. Tc Vac 3 induced control of Trypanosoma cruzi infection and chronic
myocarditis in mice. PLoS One. 8: 59434, 2013.
Guyton, A. C.; Hall, J. E. Tratado de fisiologia médica. 12aed. Rio de Janeiro, Elsevier Ed.,
2011.
185
Hamid T, Gu Y, Ortines RV, Bhattacharya C, Wang G, Xuan YT, Prabhu SD. Divergent tumor
necrosis factor receptor-related remodeling responses in heart failure: role of nuclear factorkappaB and inflammatory activation. Circulation. 119: 1386–1397, 2009.
Haolla FA, Claser C, de Alencar BC, Tzelepis F, de Vasconcelos JR, de Oliveira G, Silvério JC,
Machado AV, Lannes-Vieira J, Bruna-Romero O, Gazzinelli RT, dos Santos RR, Soares MB,
Rodrigues MM. Strain-specific protective immunity following vaccination against experimental
Trypanosoma cruzi infection. Vaccine. 27: 5644–5653, 2009.
Harty JT, Badovinac VP. Influence of effector molecules on the CD8(+) T cell response to
infection. Curr Opin Immunol. 14: 360–365, 2002.
Hegewisch S, Weh HJ, Hossfeld DK. TNF-induced cardiomyopathy. Lancet. 335: 294–295,
1990.
Herrmann R, Sandek A, von Haehling S, Doehner W, Schmidt HB, Anker SD, Rauchhaus M.
Risk stratification in patients with chronic heart failure based on metabolic-immunological,
functional and haemodynamic parameters. Int J Cardiol. 156: 62–68, 2012.
Higuchi ML, Benvenuti LA, Martins Reis M, Metzger M. Pathophysiology of the heart in
Chagas' disease: current status and new developments. Cardiovasc Res. 60: 96–107, 2003.
Higuchi ML, Gutierrez PS, Aiello VD, Palomino S, Bocchi E, Kalil J, Bellotti G, Pileggi F.
Immunohistochemical characterization of infiltrating cells in human chronic chagasic
myocarditis: comparison with myocardial rejection process. Virchows Arch A Pathol Anat
Histopathol. 3: 157–160, 1993.
Higuchi, ML, Reis MM, Aiello VD, Benvenuti LA, Gutierrez PS, Bellotti G and Pileggi F.
Association of an increase in CD8+ T cells with the presence of Trypanosoma cruzi antigens in
chronic, human chagasic myocarditis. Am. J. Trop. Med. Hyg. 56: 485–489, 1997.
Hohmann HP, Brockhaus M, Baeuerle PA, Remy R, Kolbeck R, van Loon AP. Expression of
the types A and B tumor necrosis factor (TNF) receptors is independently regulated, and both
receptors mediate activation of the transcription factor NF-kappa B. TNF alpha is not needed for
induction of a biological effect via TNF receptors. J Biol Chem. 265: 22409–22417, 1990.
Hotez PJ, Dumonteil E, Woc-Colburn L, Serpa JA, Bezek S, Edwards MS, Hallmark CJ,
Musselwhite LW, Flink BJ, Bottazzi ME. Chagas disease: "the new HIV/AIDS of the
Americas". PLoS Negl Trop Dis. 6: e1498, 2012.
Hotez PJ, Ferris MT. The antipoverty vaccines. Vaccine. 24: 578–799, 2006.
http:// w3.datasus.gov.br/datasus/index.php?area=0203.
Huang H, Chan J, Wittner M, Jelicks LA, Morris SA, Factor SM, Weiss LM, Braunstein VL,
Bacchi CJ, Yarlett N, Chandra M, Shirani J, Tanowitz HB. Expression of cardiac cytokines and
inducible form of nitric oxide synthase (NOS2) in Trypanosoma cruzi-infected mice. J Mol Cell
Cardiol. 31: 75–88, 1999.
Huaux F, Liu T, McGarry B, Ullenbruch M, Phan SH. Dual roles of IL-4 in lung injury and
fibrosis. J Immunol. 170: 2083–2092, 2003.
Ianni BM, Mady C. The sugarcane juice was delicious, but.... Arq. Bras. Cardiol. 85: 379–381,
2005.
Ihnatko R, Kubes M. TNF signaling: early events and phosphorylation. Gen Physiol Biophys.
26: 159–167, 2007.
186
James SE, Greenberg PD, Jensen MC, Lin Y, Wang J, Budde LE, etal. Mathematical Modeling
of Chimeric TCR Triggering Predicts the Magnitude of Target Lysis and Its Impairment by
TCR Downmodulation. J Immunol. 184: 4284–4294, 2010.
Jang IK, Gu H. Negative regulation of TCR signalling and T-cell activation by selective protein
degradation. Curr Opin Immunol. 15: 315–320, 2003.
Jones EM, Colley DG, Tostes LER. Venencab-Jones MC, Curley TL. Amplification of
Trypanosoma cruzi DNA sequence from inflammatory lesions in human chagasic
cardiomyopathy. American Journal of Tropical Medicine and Hygiene. 48: 348–357, 1993.
Junqueira C, Caetano B, Bartholomeu DC, Melo MB, Ropert C, Rodrigues MM, Gazzinelli RT.
The endless race between Trypanosoma cruzi and host immunity: lessons for and beyond
Chagas disease. Expert Rev Mol Med. 12: e29, 2010.
Kamphuis J, Smits P, Thien T. Vascular effects of pentoxifylline in humans. J Cardiovasc
Pharmacol. 24: 648–654, 1994.
Kapadia S, Torre-Amione G, Yokoyama T, Mann DL. Soluble tumor necrosis factor binding
proteins modulate the negative inotropic effects of TNF-α in vitro. Am J Physiol. 37: H517–
H525, 1995.
Kassardjian A, Kreydiyyeh SI. JNK modulates the effect of caspases and NF-kappaB in the
TNF-alpha-induced down-regulation of Na+/K+ATPase in HepG2 cells. J Cell Physiol. 216:
615-620, 2008.
Katz SD, Rao R, Berman JW, Schwarz M, Demopoulos L, Bijou R, LeJemtel TH.
Pathophysiological correlates of increased serum tumor necrosis factor in patients with
congestive heart failure. Relation to nitric oxide-dependent vasodilation in the forearm
circulation. Circulation. 90: 12–16, 1994.
Kaur K, Sharma AK, Dhingra S, Singal PK. Interplay of TNF-alpha and IL-10 in regulating
oxidative stress in isolated adult cardiac myocytes. J Mol Cell Cardiol. 41: 1023–30, 2006.
Kawai T, Akira S. Toll-like Receptors and Their Crosstalk with Other Innate Receptors in
Infection and Immunity. Immunity. 34: 637–650, 2011.
Kevin M. Bonney. Chagas disease in the 21st Century: a public health success or an emerging
threat? Parasite. 21: 11, 2014.
Kierszenbaum F, Hayes MM. Mechanisms of resistance against experimental Trypanosoma
cruzi infection. Requirements for cellular destruction of circulating forms of T. cruzi in human
and murine in vitro systems. Immunology. 40: 61–66, 1980.
Kleinbongard P, Schulz R, Heusch G. TNFα in myocardial ischemia/reperfusion, remodeling
and heart failure. Heart Fail Rev. 16: 49–69, 2011.
Kroll-Palhares K, Silverio J.C, Silva A.A., Michailowsky V., Marino A.P., Silva N.M.,
Carvalho C.M., Pinto L.M.O, Gazzinelli R.T., Lannes-Vieira J., TNF/TNFR1 signaling upregulates CCR5 expression by CD8þ T lymphocytes and promotes heart tissue damage during
Trypanosoma cruzi infection: beneficial effects of TNF-alpha blockade, Mem. Inst. Oswaldo
Cruz. 103: 375–385, 2008.
Kubota T, Bounoutas GS, Miyagishima M, Kadokami T, Sanders VJ, Bruton C, Robbins PD,
McTiernan CF, Feldman AM. Soluble tumor necrosis factor receptor abrogates myocardial
inflammation but not hypertrophy in cytokine-induced cardiomyopathy. Circulation. 101: 2518–
2525, 2000.
187
Kumar S, Tarleton RL. The relative contribution of antibody production and CD8+ T cell
function to immune control of Trypanosoma cruzi. Parasite Immunol. 5: 207–216, 1998.
Kurrelmeyer KM, Michael LH, Baumgarten G, Taffet GE, Peschon JJ, Sivasubramanian N,
Entman ML, Mann DL. Endogenous tumor necrosis factor protects the adult cardiac myocyte
against ischemic-induced apoptosis in a murine model of acute myocardial infarction. Proc Natl
Acad Sci USA. 97: 5456–5461, 2000.
Kwek SS, Dao V, Roy R, Hou Y, Alajajian D, Simko JP, Small EJ, Fong L. Diversity of
antigen-specific responses induced in vivo with CTLA-4 blockade in prostate cancer patients. J
Immunol. 189: 3759–3766, 2012.
Lannes-Vieira J, de Araújo-Jorge TC, Soeiro Mde N, Gadelha P, Corrêa-Oliveira R. The
centennial of the discovery of Chagas disease: facing the current challenges PLoS Negl Trop
Dis. 4: e645, 2010.
Lannes-Vieira J, Pereira IR, Vinagre NF, Arnez LE. TNF-α and TNFR in Chagas disease: from
protective immunity to pathogenesis of chronic cardiomyopathy. Adv Exp Med Biol. 691: 221–
230, 2011.
Lannes-Vieira J, Silverio JC, Pereira IR, Vinagre NF, Carvalho CM, Paiva CN, Silva AA.
Chronic Trypanosoma cruzi-elicited cardiomyopathy: from the discovery to the proposal of
rational therapeutic interventions targeting cell adhesion molecules and chemokine receptorshow to make a dream come true. Mem Inst Oswaldo Cruz.104: 226–235, 2009.
Lannes-Vieira J. Trypanosoma cruzi-elicited CD8+T Cell-Mediated Myocarditis: Chemokine
Receptors and Adhesion Molecules as Potential Therapeutic Targets to Control Chronic
Inflammation? Mem I Oswaldo Cruz. 98: 299–304, 2003.
Laranja FS. Clinical aspects of Chagas' disease. Rev Bras Med.10: 482–91, 1953.
Larsen AI, Lindal S, Aukrust P, Toft I, Aarsland T, Dickstein K. Effect of exercise training on
skeletal muscle fibre characteristics in men with chronic heart failure: correlation between
skeletal muscle alterations, cytokines and exercise capacity. Int J Cardiol. 83: 25–32, 2002.
Lee BY, Bacon KM, Bottazzi ME, Hotez PJ. Global economic burden of Chagas disease: a
computational simulation model. Lancet Infect Dis. 13: 342–348, 2013.
Lee BY, Bacon KM, Wateska AR, Bottazzi ME, Dumonteil E, Hotez PJ. Modeling the
economic value of a Chagas’ disease therapeutic vaccine. Hum Vaccin Immunother 8: 1293–
1301, 2012.
Lee BY, Bacon KM, Connor DL, Willig AM, Bailey RR. The potential economic value of a
Trypanosoma cruzi (Chagas disease) vaccine in Latin America. PLoS Negl Trop Dis. 4: e916,
2010.
Leon JS, Wang K, Engman DM. Captopril Ameliorates Myocarditis in Acute Experimental
Chagas Disease Circulation. 107: 2264–2269, 2003.
Lessa HA, Machado P, Lima F, Cruz AA, Bacellar O, Guerreiro J, Carvalho EM. Successful
treatment of refractory mucosal leishmaniasis with pentoxifylline plus antimony. Am J Trop
Med Hyg. 65: 87-89, 2001.
Levine B, Kalman J, Mayer L, Fillit HM, Packer M. Elevated circulating levels of tumor
necrosis factor in severe chronic heart failure. N Engl J Med. 223: 236–241, 1990.
188
Lima EC, Garcia I, Vicentelli MH, Vassalli P, Minoprio P. Evidence for a protective role of
tumor necrosis factor in the acute phase of Trypanosoma cruzi infection in mice. Infect Immun.
65: 457–465, 1997.
Low HP, Santos MA, Wizel B, Tarleton RL. Amastigote surface proteins of Trypanosoma cruzi
are targets for CD8+ CTL. J Immunol. 160: 1817–1823, 1998.
MacEwan DJ. TNF ligands and receptors--a matter of life and death. Br J Pharmacol 135: 855–
875, 2002.
MacEwan DJ. TNF receptor subtype signalling: differences and cellular consequences. Cell
Signal. 14: 477–492, 2002.
Machado AV, Cardoso JE, Claser C, Rodrigues MM, Gazzinelli RT, Bruna-Romero O. Longterm protective immunity induced against Trypanosoma cruzi infection after vaccination with
recombinant adenoviruses encoding amastigote surface protein-2 and trans-sialidase. Hum Gene
Ther. 17: 898–908, 2006.
Machado FS, Dutra WO, Esper L, Gollob KJ, Teixeira MM, Factor SM, Weiss LM, Nagajyothi
F, Tanowitz HB, Garg NJ. Current understanding of immunity to Trypanosoma cruzi infection
and pathogenesis of Chagas disease. Semin Immunopathol. 34: 753–770, 2012.
Machado FS, Koyama NS, Carregaro V, Ferreira BR, Milanezi CM, Teixeira MM, Rossi MA,
Silva JS. CCR5 plays a critical role in the development of myocarditis and host protection in
mice infected with Trypanosoma cruzi. J Infect Dis. 191: 627–36, 2005.
Machado FS, Martins GA, Aliberti JC, Mestriner FL, Cunha FQ, Silva JS. Trypanosoma cruziinfected cardiomyocytes produce chemokines and cytokines that trigger potentnitric oxidedependent trypanocidal activity. Circulation. 102: 3003–3008, 2000.
Magalhães LM, Villani FN, Nunes Mdo C, Gollob KJ, Rocha MO, Dutra WO. High interleukin
17 expression is correlated with better cardiac function in human Chagas disease. J Infect Dis;
207: 661–665, 2013.
Mahmoud MF, El Shazly SM, Barakat W. Inhibition of TNF-α protects against hepatic
ischemia-reperfusion injury in rats via NF-κB dependent pathway. Naunyn Schmiedebergs Arch
Pharmacol. 385: 465–471. 2012.
Mahy M, Autenrieth CS, Stanecki K, Wynd S. Increasing trends in HIV prevalence among
people aged 50 years and older: evidence from estimates and survey data. AIDS. 4: S453–459,
2014.
Mandell GL. ARDS, neutrophils, and pentoxifylline Am Rev Respir Dis.138: 1103–1105, 1988.
Mann DL, McMurray JJ, Packer M, Swedberg K, Borer JS, Colucci WS, Djian J, Drexler H,
Feldman A, Kober L, Krum H, Liu P, Nieminen M, Tavazzi L, van Veldhuisen DJ,
Waldenstrom A, Warren M, Westheim A, Zannad F, Fleming T. Targeted anticytokine therapy
in patients with chronic heart failure: results of the Randomized Etanercept Worldwide
Evaluation (RENEWAL). Circulation.109: 1594–1602, 2004.
Mann DL. Inflammatory Mediators and the Failing Heart Past, Present, and the Foreseeable
Future. Circ Res. 91: 988–998, 2002.
Mann DL. The effect of tumor necrosis factor-alpha on cardiac structure and function: a tale of
two cytokines. J Card Fail. 2: S165–172, 1996.
189
Mann DL. Tumor necrosis factor and viral myocarditis: the fine line between innate and
inappropriate immune responses in the heart. Circulation. 103: 626–629, 2001.
Maria-Jesus Pinazo, Maria-Carmen Thomas, Juan Bustamante, Igor Correia de Almeida,
Manuel-Carlos Lopez, Joaquim Gascon. Biomarkers of therapeutic responses in chronic Chagas
disease: state of the art and future perspectives Mem Inst Oswaldo Cruz. 110: 422–432, 2015.
Marinho CR, Nunez-Apaza LN, MartinsSantos R, Bastos KR, Bombeiro AL, Bucci DZ,
Sardinha LR, Lima MR, Alvarez JM: IFN-γ, but not nitric oxide or specific IgG, is essential for
the in vivo control of low-virulence Sylvio X10/4 Trypanosoma cruzi parasites. Scand J
Immunol. 66: 297–308, 2007.
Marin-Neto JA, Cunha-Neto E, Maciel BC, Simões MV. Pathogenesis of chronic Chagas heart
disease. Circulation. 115: 1109–1123, 2007.
Marin-Neto JA, Rassi A Jr, Avezum A Jr, Mattos AC, Rassi A, Morillo CA, Sosa-Estani S,
Yusuf S; BENEFIT Investigators. The BENEFIT trial: testing the hypothesis that trypanocidal
therapy is beneficial for patients with chronic Chagas heart disease. Mem Inst Oswaldo Cruz.
104: 319–324, 2009.
Marin-Neto JA, Rassi A Jr. Update on Chagas heart disease on the first centenary of its
discovery. Rev Esp Cardiol. 62: 1211–1216, 2009.
Marino APMP, Azevedo MIP, Lannes-Vieira J. Differential expression of adhesion molecules
shaping the T-cell subset prevalence during the early phase of autoimmune and Trypanosoma
cruzi-elicited myocarditis. Mem Inst Oswaldo Cruz, 98: 945–952, 2003.
Marino APMP, Silva AA, Pinho RT, Lannes-Vieira J. Trypanosoma cruzi infection: a
continuous invader-host cell cross talk with participation of extracellular matrix, and adhesion
and chemoattractant molecules. Braz J Med Biol Res. 36: 1121–1133, 2003.
Marino APMP, Silva AaA, Santos PVA, Pinto LMO, Gazzinelli RT, Teixeira MM,
LannesVieira J. RANTES antagonist (Met-RANTES) controls the early phase of Trypanosoma
cruzi elicited myocarditis. Circulation. 110: 1443–1449, 2004.
Martin D, Tarleton R. Generation, specificity, and function of CD8+ T cells in Trypanosoma
cruzi infection. Immunol Rev. 201: 304–317, 2004.
Martins GA, Tadokoro CE, Silva RB, Silva JS, Rizzo LV. CTLA-4 blockage increases
resistance to infection with the intracellular protozoan Trypanosoma cruzi. J Immunol. 172:
4893–4901, 2004.
Martins GA, Vieira L Q, Cunha FQ, Silva JS. Gamma interferon Modulates CD95 (Faz) and
CD 95 ligant (Faz-L) Expression and Nitric Oxide- Induced Apoptosis during the Acute Phase
of Trypanossoma cruzi Infection: a Possible Role in Immune Response Control. Infect. Immun.
67: 3864–3871, 1999.
Mathers CD, Ezzati M, Lopez AD. Measuring the burden of neglected tropical diseases: the
global burden of disease framework. Negl Trop Dis. 1: e114, 2007.
Mathers CD, Loncar D. Projections of global mortality and burden of disease from 2002 to
2030. PLoS Med. 3: e442, 2006.
Medeiros GA, Silvério JC, Marino AP, Roffê E, Vieira V, Kroll-Palhares K, Carvalho CE, Silva
AA, Teixeira MM, Lannes-Vieira J. Treatment of chronically Trypanosoma cruzi-infected mice
with a CCR1/CCR5 antagonist (Met-RANTES) results in amelioration of cardiac tissue
damage. Microbes Infect. 11: 264–273, 2009.
190
Mejia AM, Hall BS, Taylor MC, Gómez-Palacio A, Wilkinson SR, Triana-Chávez O, Kelly JM.
Benznidazole-resistance in Trypanosoma cruzi is a readily acquired trait that can arise
independently in a single population. The Journal of Infectious Disease. 206–220, 2012.
Melo L, Caldas IS, Azevedo MA, Gonçalves KR, Nascimento AFS, Figueiredo VP, Diniz
LF, de Lima WG, Torres RM, Bahia MT, Talvani A. Low Doses of Simvastatin Therapy
Ameliorate Cardiac Inflammatory Remodeling in Trypanosoma cruzi -Infected Dogs. Am. J.
Trop. Med. Hyg. 84: 325–331, 2011.
Meneghelli UG. Chagasic enteropathy. Rev Soc Bras Med Trop. 37: 252–60, 2004.
Menezes C, Costa GC, Gollob KJ, Dutra WO. Clinical aspects of Chagas disease and
implications for novel therapies. Drug Dev Res. 72: 471–479, 2011.
Michailowsky M, Celes MRN, Marino AP, Silva AA, Vieira LQ, Rossi MA, Gazzinelli RT,
Lannes-Vieira J and Silva JS. ICAM-1 Deficiency Leads to Impaired Recruitment of T
Lymphocytes and Enhanced Host Susceptibility to Infection with Trypanosoma cruzi. J.
Immunol. 173: 463–470, 2004.
Michailowsky V, Silva NM, Rocha CD, Vieira LQ, Lannes-Vieira J e Gazzinelli RT. Pivotal
role of interleukin-12 and interferon-γ axis in controlling tissue parasitism and inflammation in
the heart and central nervous system during Trypanosoma cruzi infection. Am. J. Pathol.. 159:
1723–1733, 2001.
Miles MA, Feliciangeli MD, de Arias AR. American trypanosomiasis (Chagas' disease) and the
role of molecular epidemiology in guiding control strategies. BMJ. 326: 1444–1448, 2003.
Miles MA, Llewellyn MS, Lewis MD, Yeo M, Baleela R, Fitzpatrick S, Gaunt MW, Mauricio
IL. The molecular epidemiology and phylogeography of Trypanosoma cruzi and parallel
research on Leishmania: looking back and to the future. Parasitology 136: 1509–1528, 2009.
Miller EA, Ernst JD. Anti-TNF immunotherapy and tuberculosis reactivation: another
mechanism revealed. J Clin Invest.119: 1079–1082, 2009.
Ministério da Saúde. Secretaria de Atenção à Saúde. Departamento de Atenção Básica.
Prevenção clínica de doença cardiovascular, cerebrovascular e renal crônica. Brasília; (Cadernos
de Atenção Básica, 14), 2006.
Minoprio P. Parasite polyclonal activators: new targets for vaccination approaches? Int J
Parasitol. 31: 588–591, 2001.
Minoprio P., Eisen H., Forni L., D’Imperio Lima M. R., Joskowicz M., and Coutinho A.
Polyclonal lymphocyte responses to murine Trypanosoma cruzi infection. I. Quantitation of
both T and B cell responses. Scandinavian Journal of Immunolology 24: 661–668, 1986.
Miyahira Y, Takashima Y, Kobayashi S, Matsumoto Y, Takeuchi T, Ohyanagi-Hara M,
Yoshida A, Ohwada A, Akiba H, Yagita H, Okumura K, Ogawa H. Immune responses against a
single CD8+-T-cell epitope induced by virus vector vaccination can successfully control
Trypanosoma cruzi infection. Infect Immun. 73: 7356–7365, 2005.
Miyazaki Y, Hamano S, Wang S, Shimanoe Y, Iwakura Y, Yoshida H. IL-17 is necessary for
host protection against acute-phase Trypanosoma cruzi infection. J Immunol. 185: 1150–1157,
2010.
Molina J, Brener Z, Romanha AJ, Urbina JA. In vivo activity of the bis-triazole D0870 against
drug-susceptible and drug-resistant strains of the protozoan parasite Trypanosoma cruzi. J
Antimicrobial Chemotherapy. 46: 137–140, 2000.
191
Moody AM, Chui D, Reche PA, Priatel JJ, Marth JD, Reinherz EL. Developmentally regulated
glycosylation of the CD8alphabeta coreceptor stalk modulates ligand binding. Cell. 107: 501–
512, 2001.
Moody AM, North SJ, Reinhold B, Van Dyken SJ, Rogers ME, Panico M, Dell A, Morris HR,
Marth JD, Reinherz EL. Sialic Acid Capping of CD8β Core 1-O-Glycans Controls ThymocyteMajor Histocompatibility Complex Class I Interaction. J. Biol. Chem. 278: 7240–7246, 2003.
Moraes-Souza H, Ferreira-Silva MM. O controle da transmissão transfusional. Rev. História
sobre a Doença de Chagas no Brasil. 44: 64–67, 2011.
Moreira OC, Ramírez JD, Velázquez E, Melo MF, Lima-Ferreira C, Guhl F, Sosa-Estani S,
Marin-Neto JA, Morillo CA, Britto C. Towards the establishment of a consensus real-time
qPCR to monitor Trypanosoma cruzi parasitemia in patients with chronic Chagas disease
cardiomyopathy: a substudy from the BENEFIT trial. Acta Trop. 125: 23–31, 2013.
Moura FM, da Silva MCG, Carnut L. Política de Atenção Cardiovascular no âmbito do Sistema
Único de Saúde: breves comentários sobre a literatura científica nacional indexada disponível. J
Manag Prim Health Care. 2: 30–33, 2011.
Muniz-Junqueira MI. Immunomodulatory Therapy Associated to Anti-Parasite Drugs as a Way
to Prevent Severe Forms of Malaria. Current Clinical Pharmacology. 2: 59–73, 2007.
Muñoz-Fernández MA, Fernández MA, Fresno M. Synergism between tumor necrosis factoralpha and interferon-gamma on macrophage activation for the killing of intracellular
Trypanosoma cruzi through a nitric oxide-dependent mechanism. Eur J Immunol. 22: 301–307,
1992.
Nahid P, Pai M, Hopewell PC. Advances in the diagnosis and treatment of tuberculosis. Proc
Am Thorac Soc. 3: 103–110, 2006.
Nakano M, Knowlton AA, Dibbs Z, Mann DL. Tumor necrosis factor-α confers resistance to
injury induced by hypoxic injury in the adult mammalian cardiac myocyte. Circulation. 97:
1392– 1400, 1998.
Neves, D. P.; Melo, A. L.; Linardi, P. M.; Vitor, R. W. A. Parasitologia Humana. 11 ed. São
Paulo: editora Atheneu. 85–108, 2005.
Ngasala BE, Malmberg M, Carlsson AM, Ferreira PE, Petzold MG, Blessborn D, Bergqvist Y,
Gil JP, Premji Z, Björkman A, Mårtensson A. Efficacy and effectiveness of artemetherlumefantrine after initial and repeated treatment in children,5 years of age with acute
uncomplicated Plasmodium falciparum malaria in rural Tanzania: a randomized trial. Clin Infect
Dis. 52: 873–882, 2011.
Nogueira RT, Nogueira AR, Pereira MC, Rodrigues MM, Galler R, Bonaldo MC. Biological
and immunological characterization of recombinant Yellow Fever 17D viruses expressing a
Trypanosoma cruzi Amastigote Surface Protein-2 CD8+T cell epitope at two distinct regions of
the genome. Virol J. 8: 127, 2011.
Nozaki N, Yamaguchi S, Shirakabe M, Nakamura H, Tomoike H. Soluble tumor necrosis
factorreceptors are elevated in relation to severity of congestive heart failure. Jpn Circ J. 61:
657–664, 1997.
Nunes MCP, Barbosa MM, Ribeiro AL, Colosimo EA, Rocha MO. Left atrial volume provides
independent prognostic value in patients with chagas cardiomyopathy. J Am Soc Echocardiogr.
22: 82–88, 2009.
192
Nunes MCP, Barbosa MM, Ribeiro AL, Amorim Fenelon LM, Rocha MO. Predictors of
mortality in patients with dilated cardiomyopathy: relevance of Chagas disease as an etiological
factor. Rev Esp Cardiol. 63: 788–797, 2010.
Oikonomou E, Tousoulis D, Siasos G, Zaromitidou M, Papavassiliou AG, Stefanadis C. The
role of inflammation in heart failure: new therapeutic approaches. Hellenic J Cardiol. 52: 30–40,
2011.
Oliveira MF, Nagão-Dias AT, Pontes VMO, Souza JAS, Coelho HLL, Coelho ICB. Tratamento
etiológico da doença de Chagas no Brasil. Revista de Patologia Tropical. 37: 2009–2228, 2008.
Oliveira TB, Pedrosa RC, Wilhelm-Filho D. Oxidative stress in chronic cardiopathy associated
with Chagas disease. Int J Cardiol. 116: 357–363, 2007.
OPAS - Organización Panamericana de la Salud. Consulta Técnica sobre Información,
Educación y Comunicación (IEC), em Enfermedad de Chagas Congénita. Montevideo,
Uruguay, 2007.
Padilla AM, Bustamante JM, and Tarleton RL CD8+ T cells in Trypanosoma cruzi infection.
Curr Opin Immunol. 21: 385–390, 2009.
Paiva CN, Castelo-Branco MTL, Lannes-Vieira J, and Gattass CR. Trypanosoma cruzi:
Protective Response of Vaccinated Mice Is Mediated by CD8+ Cells, Prevents Signs of
Polyclonal T Lymphocyte Activation, and Allows Restoration of a Resting Immune State after
Challenge. Experimental Parasitology. 91: 7–19, 1999.
Paiva CN, Feijó DF, Dutra FF, Carneiro VC, Freitas GB, Alves LS, Mesquita J, Fortes GB,
Figueiredo RT, Souza HS, Fantappié MR, Lannes-Vieira J, Bozza MT. Oxidative stress fuels
Trypanosoma cruzi infection in mice. J Clin Invest. 122: 2531–2542, 2012.
Pereira ASL, Corrêa BS, Minicucci GP, Lopes GMA, Cunha EC, Reis NA, Teixeira VPA. O
peso do baço em chagásicos crônicos. Revista da Sociedade Brasileira de Medicina Tropical.
32: 167–170, 1999.
Pérez AR, Fontanella GH, Nocito AL, Revelli S, and Bottasso OA. Short treatment with the
tumour necrosis factor-α blocker infliximab diminishes chronic chagasic myocarditis in rats
without evidence of Trypanosoma cruzi reactivation. Clin Exp Immunol. 157: 291–299, 2009.
Pérez AR, Silva-Barbosa SD, Roggero E, Calmon-Hamaty F, Villar SR, Gutierrez FR, Santana
Silva J, Savino W, Bottasso O. Immunoendocrinology of the Thymus in Chagas Disease.
Neuroimmunomodulation. 18: 328–338, 2011.
Perez-Fuentes R, Guegan JF, Barnabe C, Lopez-Colombo A, Salgado-Rosas H, Torres-Rasgado
E, Briones B, Romero-Diaz M, Ramos-Jimenez J, Sanchez-Guillen Mdel C. Severity of chronic
Chagas disease is associated with cytokine/antioxidant imbalance in chronically infected
individuals. Int J Parasitol. 33: 293–299, 2003.
Perez-Fuentes R, López-Colombo A, Ordóñez-Toquero G, Gomez-Albino I, Ramos J, TorresRasgado E, Salgado-Rosas H, Romero-Díaz M, Pulido-Pérez P, Sánchez-Guillén MC.
Correlation of the serum concentrations of tumour necrosis factor and nitric oxide with disease
severity in chronic Chagas disease (American trypanosomiasis). Ann Trop Med Parasitol. 101:
123–132, 2007.
Petersen CA, Krumholz KA, Burleigh BA. Toll-Like receptor-2 regulates interleukin-1betadependent cardiomyocyte hypertrophy triggered by Trypanosoma cruzi. Infect Immun. 73:
6974–6980, 2005.
193
Peterson TC. Pentoxifylline prevents fibrosis in an animal model and inhibits platelet-derived
growth factor-driven proliferation of fibroblasts. Hepatology.17: 486–493, 1993.
Pinazo MJ, Espinosa G, Gallego M, Lopez-Chejade PL, Urbina JA, Gascon J. Successful
treatment with posaconazole of a patient with chronic Chagas disease and systemic lupus
erythematosus. Am.J.Trop Med.Hyg. 82: 583–587, 2010.
Pinazo MJ, MC Thomas, J Bustamante, IC Almeida, Lopez MC, Gascon J. Biomarkers of
therapeutic responses in chronic Chagas disease: state of the art and future perspectives. Mem.
Inst. Oswaldo Cruz. 110: 422–432, 2015.
Pinto AM, Sales PC, Camargos ER, Silva AM. Tumour necrosis factor (TNF)-mediated NF-κB
activation facilitates cellular invasion of non-professional phagocytic epithelial cell lines by
Trypanosoma cruzi. Cell Microbiol. 13: 1518–1529, 2011.
Pipkin ME, Lieberman J. Delivering the kiss of death: progress on understanding how perforin
works. Curr Opin Immunol. 19: 301–308, 2007.
Pissetti CW, Correia D, de Oliveira RF, Llaguno MM, Balarin MA, Silva-Grecco RL,
Rodrigues V Jr. Genetic and functional role of TNF-alpha in the development Trypanosoma
cruzi infection. PLoS Negl Trop Dis. 5: e976, 2011.
Priotto G, Kasparian S, Mutombo W, Ngouama D, Ghorashian S, Arnold U, Ghabri S, Baudin
E, Buard V, Kazadi-Kyanza S, Ilunga M, Mutangala W, Pohlig G, Schmid C, Karunakara U,
Torreele E, Kande V. Nifurtimox-eflornithine combination therapy for second-stage African
Trypanosoma brucei gambiense trypanosomiasis: a multicentre, randomised, phase III, noninferiority trial. Lancet. 374: 56–64, 2009.
Proudfoot AE, Buser R, Borlat F, Alouani S, Soler D, Offord RE, Schröder JM, Power CA,
Wells TN. Amino-terminally modified RANTES analogues demonstrate differential effects on
RANTES receptors. J Biol Chem. 274: 32478–32485, 1999.
Quijano-Hernández IA, Castro-Barcena A, Vázquez-Chagoyán JC, Bolio-González ME,
Ortega-López J, Dumonteil E. Preventive and therapeutic DNA vaccination partially protect
dogs against an infectious challenge with Trypanosoma cruzi. Vaccine. 31: 2246–2252, 2013.
Rassi A Jr, Rassi A, Marcondes de Rezende J. American trypanosomiasis (Chagas disease).
Infect Dis Clin North Am. 26: 275-291, 2012.
Rassi AJr, Rassi A, Marin-Neto JA. Chagas disease. Lancet. 375: 1388–1402, 2010.
Rauchhaus M, Doehner W, Francis DP, Davos C, Kemp M, Liebenthal C, Niebauer J, Hooper J,
Volk HD, Coats AJS, Anker SD. Plasma Cytokine Parameters and Mortality in Patients With
Chronic Heart Failure. Circulation. 102: 3060–3067, 2000.
Rauchhaus M. Anti-cytokine treatment in patients with chronic heart failure-a clinical approach.
Int J Cardiol. 72: 295–296; author reply 297–298, 2000.
Reis DD, Jones EM, Tostes S Jr, Lopes ER, Gazzinelli G, Colley DG, McCurley TL.
Characterization of inflammatory infiltrates in chronic chagasic myocardial lesions: presence of
tumor necrosis factor-alpha cells and dominance of granzyme A, CD8 lymphocytes. Am J Trop
Med Hyg. 48: 637– 644, 1993.
Reis MM, Higuchi Md, Benvenuti LA, Aiello VD, Gutierrez PS, Bellotti G, Pileggi,F. An in
situ quantitative immunohistochemical study of cytokines and IL- 2R+ in chronic human
194
chagasic myocarditis: correlation with the presence of myocardial Trypanosoma cruzi antigens.
Clin.Immunol.Immunopathol. 83:165–172, 1997.
Rey L. Parasitologia: parasitos e doenças parasitárias do homem nos trópicos ocidentais. 4 ed.
Rio de Janeiro: editora Guanabara koogan. 295–343, 2008.
Ribeiro Dos Santos R, Rassi S, Feitosa G, Grecco OT, Rassi A Jr, da Cunha AB, de Carvalho
VB, Guarita-Souza LC, de Oliveira W Jr, Tura BR, Soares MB, Campos de Carvalho AC;
Chagas Arm of the MiHeart Study Investigators. Cell therapy in Chagas cardiomyopathy
(Chagas arm of the multicenter randomized trial of cell therapy in cardiopathies study): a
multicenter randomized trial. Circulation. 125: 2454–2461, 2012.
Ribeiro I, Sevcsik AM, Alves F, Diap G, Don R, Harhay MO, Chang S, Pecoul B. New,
improved treatments for Chagas disease: from the R&D pipeline to the patients. PLoS Negl
Trop Dis. 3: e484, 2009.
Rigato PO, de Alencar BC, de Vasconcelos JR, Dominguez MR, Araújo AF, Machado AV,
Gazzinelli RT, Bruna-Romero O, Rodrigues MM. Heterologous plasmid DNA primerecombinant human adenovírus 5 boost vaccination generates a stable pool of protective longlived CD8(+) T effector memory cells specific for a human parasite Trypanosoma cruzi. Infect
Immun 79: 2120–2130, 2011.
Rivera M, Taléns-Visconti R, Jordán A, Sirera R, Sevilla B, Climent V, Roselló E, Payá R,
Cortés R, Sancho-Tello MJ, Valero R, González-Molina A. Myocardial remodeling and
immunologic activation in patients with heart failure. Rev Esp Cardiol. 59: 911–988, 2006.
Rocha CD, Caetano BC, Machado AV, Bruna-Romero O. Recombinant viruses as tools to
induce protective cellular immunity against infectious diseases. Int Microbiol. 7: 83–94, 2004.
Rocha MO, Teixeira MM, Ribeiro AL. An update on the management of Chagas
cardiomyopathy. Expert Rev Anti Infect Ther. 5: 727–743, 2007.
Rodrigues MM, Alencar BC, Claser C, Tzelepis F. Immunodominance: a new hypothesis to
explain parasite escape and host/parasite equilibrium leading to the chronic phase of Chagas'
disease? Braz J Med Biol Res. 42: 220–223, 2009.
Rodrigues MM, Boscardin SB, Vasconcelos JR, Hiyane MI, Salay G, Soares IS. Importance of
CD8 T cell-mediated immune response during intracellular parasitic infections and its
implications for the development of effective vaccines. An Acad Bras Cienc. 75: 443–468,
2003.
Rodrigues MM, Oliveira AC, Bellio M. The immune response to Trypanosoma cruzi: Role of
Toll-Like Receptors and Perspectives for Vaccine Development. J Prasitol Res. ID 507874,
2012.
Rodrigues MM, Ribeirão M, Pereira-Chioccola V, Renia L, Costa F. Predominance of CD4 Th1
and CD8 Tc1 cells revealed by characterization of the cellular immune response generated by
immunization with a DNA vaccine containing a Trypanosoma cruzi gene. Infect Immun. 67:
3855–3863, 1999.
Rodriguez-Morales AJ. Nuevas perspectivas en el manejo terapéutico de la enfermedad de
Chagas. Rev Peru Med Exp Salud Publica. 22: 123-132, 2005.
Rodríguez-Pérez JM, Cruz-Robles D, Hernández-Pacheco G, Pérez-Hernández N, Murguía LE,
Granados J, Reyes PA, Vargas-Alarcón G. Tumor necrosis factor-alpha promoter polymorphism
in Mexican patients with Chagas' disease. Immunol Lett. 98: 97-102, 2005.
195
Roffê E, Rothfuchs AG, Santiago HC, Marino AP, Ribeiro-Gomes FL, Eckhaus M, Antonelli
LR, Murphy PM IL-10 limits parasite burden and protects against fatal myocarditis in a mouse
model of Trypanosoma cruzi infection. J Immunol. 188: 649–660, 2012.
Ronco MT, Manarin R, Francés D, Serra E, Revelli S, Carnovale C. Benznidazole treatment
attenuates liver NF-κB activity and MAPK in a cecal ligation and puncture model of sepsis. Mol
Immunol. 48: 867–873, 2011.
Ropert C, Ferreira LR, Campos MA, Procópio DO, Travassos LR, Ferguson MA, Reis LF,
Teixeira
MM,
Almeida
IC,
Gazzinelli
RT.
Macrophage
signaling
by
glycosylphosphatidylinositol-anchored mucin-like glycoproteins derived from Trypanosoma
cruzi trypomastigotes. Microbes Infect. 4: 1015–1025, 2002.
Rottenberg ME, Bakhiet M, Olsson T, Kristensson K, Mak T, Wigzell H, Orn A. Differential
susceptibilities of mice genomically deleted of CD4 and CD8 to infections with Trypanosoma
cruzi or Trypanosoma brucei. Infect Immun. 61: 5129-5133, 1993.
Ruddle NH. Lymphotoxin and TNF: how it all began-a tribute to the travelers. Cytokine Growth
Factor Rev. 25: 83–89, 2014.
Russo C, Polosa R. TNF-alpha as a promising therapeutic target in chronic asthma: a lesson
from rheumatoid arthritis. Clin Sci (Lond). 110: 265, 2006.
Saghizadeh M, Ong JM, Garvey WT, Henry RR, Kern PA. The expression of TNF alpha by
human muscle. Relationship to insulin resistance. J Clin Invest. 97: 1111–1116, 1996.
Sakaguchi S, Miyara M, Costantino CM, Hafler DA. FOXP3+ regulatory T cells in the human
immune system. Nat Rev Immunol. 10: 490–500, 2010.
Sales PA Jr, Golgher D, Oliveira RV, Vieira V, Arantes RM, Lannes-Vieira J, Gazzinelli RT.
The regulatory CD4+CD25+ T cells have a limited role on pathogenesis of infection with
Trypanosoma cruzi. Microbes Infect. 10: 680–688, 2008.
Sallusto F, Lenig D, Förster R, Lipp M, Lanzavecchia A. Two subsets of memory T
lymphocytes with distinct homing potentials and effector functions. Nature. 401: 708–712,
1999.
Salomon B, Bluestone JA. Complexities of CD28/B7: CTLA-4 costimulatory pathways in
autoimmunity and transplantation. Annu Rev Immunol. 19: 225–52, 2001.
Salvatella R, Irabedra P, Sánchez D, Castellanos LG, Espinal M. South-south cooperation for
Chagas disease. Lancet. 382: 395–396, 2013.
Samudio M, Montenegro-James S, de Cabral M, Martinez J, Rojas de Arias A, Woroniecky O,
James MA. Differential expression of systemic cytokine profiles in Chagas' disease is associated
with endemicity of Trypanosoma cruzi infections. Acta Trop. 69: 89–97, 1998.
Sanches TL, Cunha LD, Silva GK, Guedes PM, Silva JS, Zamboni DS. The use of a
heterogeneously controlled mouse population reveals a significant correlation of acute phase
parasitemia with mortality in Chagas disease. PLoS One. 9: e91640, 2014.
Schenkman S, Eichinger D, Pereira ME, Nussenzweig V. Structural and functional properties of
Trypanosoma trans-sialidase. Annu Rev Microbiol 48: 499–523, 1994.
Schnapp AR, Eickhoff CS, Sizemore D, Curtiss R, 3rd, Hoft DF. Cruzipain induces both
mucosal and systemic protection against Trypanosoma cruzi in mice. Infect Immun. 70: 5065–
5074, 2002.
196
Scott, P.; Trinchieri, G. The role of natural killer cells in host-parasite interactions. Curr. Opin.
Immunol., v.7, n.1, p.34-40, 1995.
Shaw SM, Shah MK, Williams SG, Fildes JE. Immunological mechanisms of pentoxifylline in
chronic heart failure. Eur J Heart Fail. 11: 113–118, 2009.
Shelby A, Ernst K. Story and science: how providers and parents can utilize storytelling to
combat anti-vaccine misinformation. Hum Vaccin Immunother. 9: 1795–1801, 2013.
Shi L, Mai S, Israels S, Browne K, Trapani JA, Greenberg AH. Granzyme B (GraB)
autonomously crosses the cell membrane and perforin initiates apoptosis and GraB nuclear
localization. J Exp Med. 185: 855–866, 1997.
Shoda LK, Kegerreis KA, Suarez CE, Mwangi W, Knowles DP, Brown WC.
Immunostimulatory CpG-modified plasmid DNA enhances IL-12, TNF-alpha, and NO
production by bovine macrophages. J Leukoc Biol. 70: 103–112, 2001.
Sigmundsdottir H, Butcher EC. Environmental cues, dendritic cells and the programming of
tissue-selective lymphocyte trafficking. Nat Immunol. 9: 981–987, 2008.
Silva AA, Pereira GV, de Souza AS, Silva RR, Rocha MS, Lannes-Vieira J. Induced Central
Nervous System Alterations: From the Entry of Inflammatory Cells to Potential Cognitive and
Psychiatric Abnormalities. Journal of Neuroparasitology. 1: 1–13, 2010.
Silva DT, De Nazareth SLM, Meirelles M, Almeida D, Urbina JA, Pereira MC. Cytoskeleton
reassembly in cardiomyocytes infected by Trypanosoma cruzi is triggered by treatment with
ergosterol biosynthesis inhibitors. Int J Antimicrob Agents. 27: 530–537, 2006.
Silva JG, Vespa MC, Aliberti J, Cunha F. Tumor necrosis factor alpha mediates resistance to
Trypanosoma cruzi infection in mice by inducing nitric oxide production in infected gammainterferonactivated macrophages. Infect. Immun. 63: 4862–4867, 1995.
Silva JS, Machado FS, Martins GA. The role of nitric oxide in the pathogenesis of Chagas
disease. Front Biosci. 8: 314–325, 2003.
Silva SH & Moresco RN. Cardiac biomarkers for assessment of acute coronary syndrome.
Scientia Medica (Porto Alegre). 21: 132–142, 2011.
Silva JS, Morrissey PJ, Grabstein KH, Mohler KM, Anderson D, Reed SG. Interleukin 10 and
interferon gamma regulation of experimental Trypanosoma cruzi infection. J Exp Med. 175:
169–174, 1992.
Silva RR, Mariante RM, Silva AA, dos Santos ALB, Roffê E, Santiago H, Gazzinelli RT,
Lannes-Vieira J. Interferon-Gamma Promotes Infection of Astrocytes by Trypanosoma cruzi.
PLoS ONE 10: e0118600, 2015.
Silva RS, Shrestha-Bajracharya D, Almeida-Leite CM, Leite R, Bahia MT, Talvani A. Shortterm therapy with simvastatin reduces inflammatory mediators and heart inflammation during
the acute phase of experimental Chagas disease. Mem Inst Oswaldo Cruz. 107: 513–521, 2012.
Silva VLC. Subsídios ao processo de certificação do Brasil como área livre da transmissão
transfusional da doença de Chagas. Dissertação (Mestrado em Saúde Coletiva) – Faculdade de
Ciências Médias da Santa Casa de São Paulo. São Paulo. 2010.
Silverio JC, de-Oliveira-Pinto LM, da Silva AA, de Oliveira GM, Lannes-Vieira J. Perforin
expressing cytotoxic cells contribute to chronic cardiomyopathy in Trypanosoma cruzi
infection. Int J Exp Pathol. 91:72–86, 2010.
197
Silverio JC, Pereira IR, Cipitelli M da C, Vinagre NF, Rodrigues MM, Gazzinelli RT, LannesVieira J. CD8+ T-Cells Expressing Interferon Gamma or Perforin Play Antagonistic Roles in
Heart Injury in Experimental Trypanosoma cruzi-Elicited Cardiomyopathy. PLoS Pathog 8:
e1002645, 2012.
Simon V, Ho DD, Abdool Karim Q. HIV/AIDS epidemiology, pathogenesis, prevention, and
treatment. Lancet. 368: 489–504, 2006.
Skudicky D, Bergemann A, Sliwa K, Candy G, Sareli P. Beneficial effects of pentoxifylline in
patients with idiopathic dilated cardiomyopathy treated with angiotensin-converting enzyme
inhibitors and carvedilol: results of a randomized study. Circulation. 103: 1083–1088, 2001.
Sliwa K, Skudicky D, Candy G, Wisenbaugh T, Sareli P. Randomised investigation of effects of
pentoxifylline on left-ventricular performance in idiopathic dilated cardiomyopathy. Lancet.
351: 1091–1093, 1998.
Sliwa K, Woodiwiss A, Candy G, Badenhorst D, Libhaber C, Norton G, Skudicky D, Sareli P.
Effects of pentoxifylline on cytokine profiles and left ventricular performance in patients with
decompensated congestive heart failure secondary to idiopathic dilated cardiomyopathy. Am J
Cardiol. 90: 1118-1122, 2002.
Sliwa K, Woodiwiss A, Kone VN, Candy G, Badenhorst D, Norton G, Zambakides C, Peters F,
Essop R. Therapy of ischemic cardiomyopathy with the immunomodulating agent
pentoxifylline: results of a randomized study. Circulation.109: 750–755, 2004.
Smaill F, Jeyanathan M, Smieja M, Medina MF, Thanthrige-Don N, Zganiacz A, Yin C,
Heriazon A, Damjanovic D, Puri L, Hamid J, Xie F, Foley R, Bramson J, Gauldie J, Xing Z. A
human type 5 adenovirus-based tuberculosis vaccine induces robust T cell responses in humans
despite preexisting anti-adenovirus immunity. Sci Transl Med 5: 205ra134, 2013.
Soares MB, Lima RS, Rocha LL, Takyia CM, Pontes-de-Carvalho L, de Carvalho AC,
Ribeirodos-Santos R. Transplanted bone marrow cells repair heart tissue and reduce myocarditis
in chronic chagasic mice. Am J Pathol. 164: 441–447, 2004.
Soares MB, Silva-Mota KN, Lima RS, Bellintani MC, Pontes-de-Carvalho L, Ribeiro-dosSantos R. Modulation of chagasic cardiomyopathy by interleukin-4: dissociation between
inflammation and tissue parasitism. Am J Pathol. 159: 703–709, 2001.
Sokol CL, Luster AD. Chemokines and chemokine receptors: positioning cells for host defense
and immunity. Annu Rev Immunol. 32: 659–702, 2014.
Souza PE, Rocha MO, Menezes CA, Coelho JS, Chaves AC, Gollob KJ, Dutra WO.
Trypanosoma cruzi infection induces differential modulation of costimulatory molecules and
cytokines by monocytes and T cells from patients with indeterminate and cardiac Chagas'
disease. Infect Immun. 75: 1886–1894, 2007.
Spate U, Schulze PC. Proinflammatory cytokines and skeletal muscle. Curr Opin Clin Nutr
Metab Care. 7: 265–269, 2004.
Starobinas N, Russo M, Minoprio P, Hontebeyrie-Joskowicz M. Is TNF alpha involved in early
susceptibility of Trypanosoma cruzi-infected C3H/He mice? Res Immunol. 142: 117–122, 1991.
Strauss M, Lo Presti MS, Bazán PC, Baez A, Fauro R, Esteves B, Sanchez Negrete O,
Cremonezzi D, Paglini-Oliva PA, Rivarola HW. Clomipramine and benznidazole association
for the treatment of acute experimental Trypanosoma cruzi infection. Parasitol Int. 62: 293–299,
2013.
198
Stumpf C, Lehner C, Yilmaz A, Daniel WG, Garlichs CD Decrease of serum levels of the antiinflammatory cytokine interleukin-10 in patients with advanced chronic heart failure. Clin Sci
(Lond). 105: 45–50. 2003.
Sugamori T, Ishibashi Y, Shimada T, Takahashi N, Sakane T, Ohata S, Kunizawa Y, Inoue S,
Nakamura K, Ohta Y, Shimizu H, Katoh H, Oyake N, Murakami Y, Hashimoto M. Increased
nitric oxide in proportion to the severity of heart failure in patients with dilated cardiomyopathy:
close correlation of tumor necrosis factor-alpha with systemic and local production of nitric
oxide. Circ J. 66: 627–632, 2002.
Takada Y, Sung B, Sethi G, Chaturvedi MM, Aggarwal BB. Evidence that genetic deletion of
the TNF receptor p60 or p80 inhibits Fas mediated apoptosis in macrophages. Biochem
Pharmacol. 74: 1057–64, 2007.
Talvani A, Ribeiro CS, Aliberti JCS, Michailowsky V, Santos PVA, Murta SMF, Romanha AJ,
Almeida IC, Farber J, Lannes-Vieira J, Silva JS and Gazzinelli RT. Kinetics of cytokine gene
expression in experimental chagasic cardiomyopathy: tissue parasitism and endogenous
IFNgama as important determinants of chemokine mRNA expression during infection with
Trypanosoma cruzi. Microbes and Infection. 2: 1–16, 2000.
Talvani A, Rocha MO, Ribeiro AL, Correa-Oliveira R, Teixeira MM. Chemokine receptor
expression on the surface of peripheral blood mononuclear cells in Chagas Disease. J Infect Dis.
189: 214–220, 2004.
Tamminga C, Sedegah M, Regis D, Chuang I, Epstein JE, Spring M, Mendoza-Silveiras J,
McGrath S, Maiolatesi S, Reyes S, Steinbeiss V, Fedders C, Smith K, House B, Ganeshan H,
Lejano J, Abot E, Banania GJ, Sayo R, Farooq F, Belmonte M, Murphy J, Komisar J, Williams
J, Shi M, Brambilla D, Manohar N, Richie NO, Wood C, Limbach K, Patterson NB, Bruder JT,
Doolan DL, King CR, Diggs C, Soisson L, Carucci D, Levine G, Dutta S, Hollingdale MR,
Ockenhouse CF, Richie TL. Adenovirus-5-vectored P. falciparum vaccine expressing CSP and
AMA1. Part B: safety, immunogenicity and protective efficacy of the CSP component. PLoS
One 6: e25868, 2011.
Tanaka T, Hishitani Y, Ogata A. Monoclonal antibodies in rheumatoid arthritis: comparative
effectiveness of tocilizumab with tumor necrosis factor inhibitors. Biologics: Targets and
Therapy. 8: 141–153, 2014.
Tarleton RL, Koller BH, Latour A, Postan M. Susceptibility of β2 microglobulin deficient mice
to Trypanosoma cruzi infection. Nature. 356: 338–340, 1992.
Tarleton RL, Sun J, Zhang L, Postan M. Depletion of T-cell subpopulations results in
exacerbation of myocarditis and parasitism in experimental Chagas' disease. Infect Immun. 62:
1820–9, 1994.
Tarleton RL. Depletion of CD8+ T cells increases susceptibility and reverses vaccine-induced
immunity in mice infected with Trypanosoma cruzi. J Immunol. 15: 717–724, 1990.
Tarleton RL. Immune System Recognition of Trypanosoma cruzi. Curr Opin Immunol. 19:
430–434, 2007.
Tarleton RL. New approaches in vaccine development for parasitic infections. Cell Microbiol.
7: 1379–1386, 2005.
Tartaglia LA, Goeddel DV. Two TNF receptors. Immunol Today. 13: 151–153, 1992.
199
Teixeira ARL, Nitz N, Guimaro MC, Gomes C, Santos-Buch CA. Chagas disease. Postgrad
Med. 82: 788–798, 2006.
Toledo MJ, Bahia MT, Carneiro CM, Martins-Filho OA, Tibayrenc M, Barnabe C, Tafuri WL,
De LM. Chemotherapy with benznidazole and itraconazole for mice infected with different
Trypanosoma cruzi clonal genotypes. Antimicrob. Agents Chemother. 47: 223–230, 2003.
Torre-Amione G, Kapadia S, Lee J, Bies RD, Lebovitz R, Mann DL. Expression and functional
significance of tumor necrosis factor receptors in human myocardium. Circulation. 92: 1487–
1493, 1995.
Tracey D, Klareskog L, Sasso H, Salfeld JG, Tak PP. Tumor necrosis factor antagonist
mechanisms of action: A comprehensive review. Pharmacology & Therapeutics. 117: 244–279,
2008.
Trapani JA, Smyth MJ. Functional significance of the perforin/granzyme cell death pathway.
Nat Rev Immunol. 2: 735–747, 2002.
Trouiller P, Olliaro P, Torreele E, Orbinski J, Laing R, Ford N. Drug development for neglected
diseases: a deficient market and a public-health policy failure. Lancet. 359: 2188–2194, 2002.
Truyens C, Torrico F, Angelo-Barrios A, Lucas R, Heremans H, De Baetselier P, Carlier Y. The
cachexia associated with Trypanosoma cruzi acute infection in mice is attenuated by antiTNFalpha, but not by anti-IL-6 or anti-IFN-gamma antibodies. Parasite Immunol. 17: 561-568,
1995.
Tzelepis F, de Alencar BC, Penido ML, Claser C, Machado AV, Bruna-Romero O, Gazzinelli
RT, Rodrigues MM. Infection with Trypanosoma cruzi restricts the repertoire of parasitespecific CD8+ T cells leading to immunodominance. J Immunol. 180: 1737–1748, 2008.
Tzelepis F, de Alencar BC, Penido ML, Gazzinelli RT, Persechini PM, Rodrigues MM. (2006).
Distinct kinetics of effector CD8+ cytotoxic T cells after infection with Trypanosoma cruzi in
naive or vaccinated mice. Infect Immun. 74: 2477-2481, 2006.
Urbina JA & Docampo R. Specific chemotherapy of Chagas disease: controversies and
advances. Trends Parasitol. 19: 495-501, 2003.
Urbina JA, Payares G, Molina J, Sanoja C, Liendo A, Lazardi K, Piras MM, Piras R, Perez N,
Wincker P, Ryley JF. Cure of short- and long-term experimental Chagas' disease using D0870.
Science. 273: 969–971, 1996.
Urbina JA. Specific chemotherapy of Chagas disease: relevance, current limitations and new
approaches. Acta Trop. 115: 55–68, 2010.
Urbina JA. Chemotherapy of Chagas disease. Curr.Pharm.Des. 8: 287–295, 2002.
Urbina JA. Ergosterol biosynthesis and
Mem.Inst.Oswaldo Cruz. 104: 311–318, 2009.
drug
development
for
Chagas
disease.
Urbina JA. Recent Clinical Trials for the Etiological Treatment of Chronic Chagas Disease:
Advances, Challenges and Perspectives. Journal of Eukaryotic Microbiology. 62: 149–156,
2015.
Vago AR, Andrade LO, Leite AA, Reis DD, Macedo AM, Adad SJ, Tostes S, Moreira MC,
Filho GB, Pena SD. Genetic characterization of Trypanosoma cruzi directly from tissues of
patients with chronic Chagas disease: differential distribution of genetic types into diverse
organs. Am J Pathol 156: 1805–1809, 2000.
200
Vasconcelos JR, Bruna-Romero O, Araújo AF, Dominguez MR, Ersching J, de Alencar BC,
Machado AV, Gazzinelli RT, Bortoluci KR, Amarante-Mendes GP, Lopes MF, Rodrigues MM.
Pathogen induced proapoptotic phenotype and high CD95 (Fas) expression accompany a
suboptimal CD8+T cell response: reversal by adenoviral vaccine. PLoS Pathog 8: e1002699,
2012.
Vilas-Boas F, Feitosa GS, Soares MB, Mota A, Pinho-Filho JA, Almeida AJ, Andrade MV,
Carvalho HG, Dourado-Oliveira A, Ribeiro-dos-Santos R. Early results of bone marrow cell
transplantation to the myocardium of patients with heart failure due to Chagas disease. Arq Bras
Cardiol. 87: 159–66, 2006.
Viotti R, Vigliano C, Lococo B, Bertocchi G, Petti M, Alvarez MG, Postan M, Armenti A.
Long-term cardiac outcomes of treating chronic Chagas disease with benznidazole versus no
treatment: a nonrandomized trial. Ann.Intern.Med. 144: 724–734, 2006.
Vitelli-Avelar DM, Sathler-Avelar R, Dias JC, Pascoal VP, Teixeira-Carvalho A, Lage PS,
Elói-Santos SM, Corrêa-Oliveira R, Martins-Filho OA. Chagasic patients with indeterminate
clinical form of the disease have high frequencies of circulating CD3+CD16-CD56+ natural
killer T cells and CD4+CD25High regulatory T lymphocytes. Scand J Immunol. 62: 297–308,
2005.
Vitelli-Avelar DM, Sathler-Avelar R, Teixeira-Carvalho A, Pinto Dias JC, Gontijo ED, Faria
AM, Elói-Santos SM, Martins-Filho OA. Strategy to assess the overall cytokine profile of
circulating leukocytes and its association with distinct clinical forms of human Chagas disease.
Scand J Immunol. 68: 516–525, 2008.
Waghabi MC, Coutinho CM, Soeiro MN, Pereira MC, Feige JJ, Keramidas M, Cosson A,
Minoprio P, Van Leuven F, Araújo-Jorge TC. Increased Trypanosoma cruzi invasion and heart
fibrosis associated with high transforming growth factor beta levels in mice deficient in
alpha(2)-macroglobulin. Infect Immun. 70: 5115–5123, 2002.
Waghabi MC, de Souza EM, de Oliveira GM, Keramidas M, Feige JJ, Araujo-Jorge TC, Bailly
S. Pharmacological Inhibition of Transforming Growth Factor β Signaling Decreases Infection
and Prevents Heart Damage in Acute Chagas’ Disease. Antimicrobial Agents And
Chemotherapy. 53: 4694–4701, 2009.
Waters JP, Pober JS and Bradley JR.Tumour necrosis factor in infectious disease. J Pathol. 230:
132–147, 2013.
Weaver C.T., Hatton R.D., Mangan P.R., Harrington L.E. IL-17 family cytokines and the
expanding diversity of effector T cell lineages.Annu. Rev. Immunol. 25: 821–852, 2007.
Wen, J.J.; Vyatkina, G.; Garg, N. Oxidative damage during chagasic cardiomyopathy
development: Role of mito chondrial oxidant release and inefficient antioxidant defense. Free
Radical Biology and Medicine. v. 37, p. 1821-1833, 2004.
WHO. Chagas disease (American trypanosomiasis) fact sheet (revised in June 2010). Wkly
Epidemiol Rec. 85: 334–336, 2010.
Wicovsky A, Henkler F, Salzmann S, Scheurich P, Kneitz C, Wajant H. Tumor necrosis factor
receptor-associated factor-1 enhances proinflammatory TNF receptor-2 signaling and modifies
TNFR1-TNFR2 cooperation. Oncogene. 28: 1769–1781, 2009.
Windmeier C, Gressner AM. Effect of pentoxifylline on the fibrogenic functions of cultured rat
liver fat-storing cells and myofibroblasts. Biochem Pharmacol. 51: 577–584, 1996.
201
Wizel B, Garg N, Tarleton RL. Vaccination with trypomastigote surface antigen 1encoding
plasmid DNA confers protection against lethal Trypanosoma cruzi infection. Infect Immun. 66:
5073–5081, 1998.
Wong M, Ziring D, Korin Y, Desai S, Kim S, Lin J, Gjertson D, Braun J, Reed E, Singh RR.
TNF alpha blockade in human diseases: mechanisms and future directions. Clinical
Immunology. 126: 121–136, 2008.
WHO – World Health Organization (2014) Fact Sheet N°340 – Chagas disease (American
trypanosomiasis).
Disponível
em
http://www.who.int/mediacentre/factsheets/fs340/en/index.html.
World Health Organization. Chagas disease (American trypanosomiasis). Disponível em:
<http://www.who.int/mediacentre/factsheets/ fs340/en/index.html>
Zacks MA, Wen JJ, Vyatkina G, Bhatia V, Garg N. An overview of chagasic cardiomyopathy:
pathogenic importance of oxidative stress. Annals of the Brazilian Academy of Sciences. 77:
695–715, 2005.
Zhang XD, Hou JF, Qin XJ, Li WL, Chen HL, Liu R, Liang X, Hai CX.Pentoxifylline inhibits
intercellular adhesion molecule-1 (ICAM-1) and lung injury in experimental phosgene-exposure
rats. Inhal Toxicol. 22: 889–895, 2010.
Zhu FC, Hou LH, Li JX, Wu SP, Liu P, Zhang GR, Hu YM, Meng FY, Xu JJ, Tang R, Zhang
JL, Wang WJ, Duan L, Chu K, Liang Q, Hu JL, Luo L, Zhu T, Wang JZ, Chen W. Safety and
immunogenicity of a novel recombinant adenovirus type-5 vector-based Ebola vaccine in
healthy adults in China: preliminary report of a randomised, double-blind, placebo-controlled,
phase 1 trial. The Lancet. S0140-6736(15)60553-0, 2015.
Zingales B, Andrade SG, Briones MRS, Campbell DA, Chiari E, Fernandes O, Guhl F,
LagesSilva E, Macedo AM, Machado CR, Miles MA, Romanha AJ, Sturm NR, Tibayrenc M,
Schijman AG. A new consensus for Trypanosoma cruzi intraspecific nomenclature: second
revision meeting recommends TcI to TcVI. Mem Inst Oswaldo Cruz. 104: 1051–1054, 2009.
Zingales B, Miles MA, Campbell DA, Tibayrenc M, Macedo AM, Teixeira MM, Schijman AG,
Llewellyn MS, Lages-Silva E, Machado CR, Andrade SG, Sturm NR. The revised
Trypanosoma cruzi subspecific nomenclature: rationale, epidemiological relevance and research
applications. Infect Genet Evol. 12: 240–53, 2012.
Zingales B, Miles MA, Moraes CB, Luquetti A, Guhl F, Schijman AG, Ribeiro I. Drug
discovery for Chagas disease should consider Trypanosoma cruzi strain diversity Mem Inst
Oswaldo Cruz. 109: 828–833, 2014.
202
9. Anexos
___________________________________________________________________________________
203
Durante a realização desta tese, participei das seguintes publicações:
Navarro IC, Ferreira FM, Nakaya HI, Baron MA, Vilar-Pereira G, Pereira IR, Silva
AM, Real JM, De Brito T, Chevillard C, Lannes-Vieira J, Kalil J, Cunha-Neto E,
Ferreira LR. MicroRNA Transcriptome Profiling in Heart of Trypanosoma cruziInfected Mice: Parasitological and Cardiological Outcomes. PLoS Negl Trop Dis. 2015
Jun 18;9(6):e0003828.
Daliry A, Pereira IR, Pereira-Junior PP, Ramos IP, Vilar-Pereira G, Silvares RR,
Lannes-Vieira J, Campos De Carvalho AC. Levels of circulating anti-muscarinic and
anti-adrenergic antibodies and their effect on cardiac arrhythmias and dysautonomia in
murine models of Chagas disease. Parasitology. 2014 Nov;141(13):1769-78.
Vilar-Pereira G, Silva AA, Pereira IR, Silva RR, Moreira OC, de Almeida LR, de
Souza AS, Rocha MS, Lannes-Vieira J. Trypanosoma cruzi-induced depressive-like
behavior is independent of meningoencephalitis but responsive to parasiticide and TNFtargeted therapeutic interventions. Brain Behav Immun. 2012 Oct;26(7):1136-49.
Carvalho CM, Silverio JC, da Silva AA, Pereira IR, Coelho JM, Britto CC, Moreira
OC, Marchevsky RS, Xavier SS, Gazzinelli RT, da Glória Bonecini-Almeida M,
Lannes-Vieira J. Inducible nitric oxide synthase in heart tissue and nitric oxide in serum
of Trypanosoma cruzi-infected rhesus monkeys: association with heart injury. PLoS
Negl Trop Dis. 2012;6(5):e1644.
Silverio JC, Pereira IR, Cipitelli Mda C, Vinagre NF, Rodrigues MM, Gazzinelli RT,
Lannes-Vieira J. CD8+ T-cells expressing interferon gamma or perforin play
antagonistic roles in heart injury in experimental Trypanosoma cruzi-elicited
cardiomyopathy. PLoS Pathog. 2012;8(4):e1002645.
Lannes-Vieira J, Pereira IR, Vinagre NF, Arnez LE. TNF-α and TNFR in Chagas
disease: from protective immunity to pathogenesis of chronic cardiomyopathy. Adv Exp
Med Biol. 2011;691:221-30.
204
205
206
207
208
209
210
211
212
213
214
215
216
217
218
219
220
221
222
223
224
225