Universidade de São Paulo
Instituto de Ciências Biomédicas
Disciplina de MICROBIOLOGIA
Profa. Dra. Beatriz L. Fernandes
Clostridium sp
Adriana Dati
Ana Carolina Soares
Elisabete Maia
Fernanda Machado
Fernanda Palone
Juliana Duarte
Priscila Losano
Talita Carnaval
Soraya Akemi
ODONTOLOGIA - DIURNO
Clostridium sp
Generalidades
A palavra Clostrídio origina-se do latim clostridium = fuso.
Os clostrídios são bastonetes, a maioria anaeróbios obrigatórios, mas algumas crescem em condições
microaerófilas. São Gram positivos, móveis e grandes. Muitos decompõem proteínas e/ou formam toxinas.
Habitat
Distribuição ubíqua. Têm como habitats preferenciais o trato gastro-intestinal de animais e seres humanos e
em pele e tecidos moles.
Característica do crescimento
Por ser anaeróbio, é incapaz de utilizar o O2 como aceptor final de hidrogênio. Estes organismos carecem
de citocromo e de citocromo-oxidase sendo incapazes de degradar o peróxido de hidrogênio, uma vez que não
possuem catalase. Dessa forma, o peróxido tende a acumular-se em concentrações tóxicas quando na presença
de O2.
Os clostrídios também carecem de superóxido desmutase permitindo o acúmulo do ânion tóxico
superóxido.
Esses microorganismos só conseguem realizar seu metabolismo normal quando sujeitos a um potencial de
redução negativo, isto é, fortemente redutor (ex: ausência de O2).
Podem fermentar açúcares, digerir proteínas e ainda formar toxinas.
Cultura
Crescem apenas em condições anaeróbias de cultura:
1. Placas de ágar ou tubo de cultura são colocados em ambientes hermeticamente fechados nos quais o ar
é substituído por nitrogênio com CO2 a 10% (o O2 também pode ser eliminado por outros métodos como
Gaspack).
2. Meios líquidos colocados em tubos profundos contendo tecido animal ou ágar de um agente redutor como
o tioglicolato. Dessa forma o crescimento bacteriano se dará de baixo para cima, já que a superfície está
exposta ao ar.
Formas de colônias
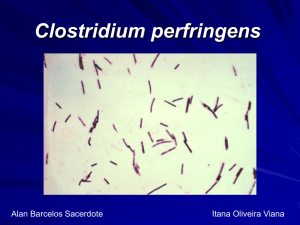
Colônias elevadas com margens bem delimitadas (Clostridium perfringens)
Colônias menores que se estendem em redes de filamentos finos (Clostridium tetani)
Muitos clostrídios deixam no meio de cultura, zona de hemólise (Clostridium perfringens no ágar sangue)
Motilidade
A maioria dos Clostrídios é móvel possuindo flagelos peritríquios. Exceção: Clostridium perfringens.
Formação de endoesporos
Normalmente o esporo tem um diâmetro maior que o bastonete dos quais se formaram. Pode ter
localização central, subterminal ou terminal.
Esporulação
1. Material nuclear espalhado
2. Formação do filamento de DNA
3. Invaginação da membrana citoplasmática para formar o pré-esporo
4. Septo do pré-esporo completo
5. Desenvolvimento completo do pré-esporo
6. Capa do esporo sintetizada e córtex completo
7. Lise da célula mãe (esporângio)
8. Os esporos livres germinam e crescem para formar a célula vegetativa.
Quando os esporos são liberados da célula mãe, podem sobreviver ao calor, ao dessecamento intenso e a
exposição a diversos compostos químicos tóxicos. O que leva a essa resistência tem sido alvo de diversas
pesquisas. No entanto, acredita-se que os fatores que conferem a resistência são:
Presença de enzimas termoestáveis
Ausência de água livre
Alto conteúdo de minerais como o cálcio
Presença de ácido dipicolínico (DPA).
O processo de esporulação pode ser induzido por:
Ligeira variação de temperatura e pH em relação aos valores ótimos para o crescimento da célula
vegetativa
Aumento da disponibilidade de O2.
Composição do esporo (de fora pra dentro)
- Exósporo
Uma camada fina e delicada, a mais externa.
- Capa do esporo
Camada formada por varias proteínas
- Córtex
Formado por peptideoglicano fracamente cruzado
- Core
Segue-se à parede celular, à membrana plasmática e ao nucleóide.
Transformação do esporo em célula vegetativa – germinação
Este processo é dividido em 3 estágios:
1. Ativação: quando ativado pelo calor ou substâncias químicas ocorre a quebra da permeabilidade do
esporo, ruptura química da capa e do córtex e a ativação do metabolismo de carboidratos.
2. Germinação: um sulco é criado na capa do esporo servindo para a entrada de água. Esta causa a
oxidação da glicose, o consumo de O2 e a eliminação de parte da massa seca do esporo. Ocorre a perda
de resistência do esporo.
3. Crescimento: significativo intumescimento do esporo, com formação de membrana e parede celular. A
célula recém formada emerge da capa e alonga-se.
TÉTANO
Agente Etiológico: Clostridium tetani.
É um bacilo móvel, Gram positivo encontrado no solo de todas as partes do mundo e no trato gastrointestinal de muitos animais, incluindo os seres humanos.
Produz endósporo oval terminal, o que lhe confere uma forma inquestionável de raquete.
Sua temperatura ótima de crescimento é de 37ºC. São metabolicamente inativos e têm uma extrema
sensibilidade à toxicidade do oxigênio, o que torna o crescimento e identificação do microorganismo difícil.
Patogenia
O Clostridium tetani produz duas toxinas: uma hemolisina oxigênio-lábil (tetanolisina) e uma neurotoxina
termolábil (tetanospasmina).
A tetanospasmina é sintetizada durante a fase estacionária de crescimento, liberada quando a célula é
lisada e é a responsável pelas manifestações clínicas do tétano. Essa neurotoxina é codificada por plasmídeos e
sintetizada como um polipeptídio de cadeia simples, com 150KDa. Esse polipeptídio é clivado por proteases
bacterianas e do hospedeiro em duas cadeias, uma de 100KDa que é dita pesada, e outra de 50KDa e é dita
leve.
A cadeia pesada liga-se a um receptor de superfície sobre a membrana neuronal e atua bloqueando a
liberação de neurotrasmissores e sinapses inibitórias, causando assim uma desregulação da atividade sináptica
excitatória (paralisia espástica). A ligação da toxina é irreversível, de modo que a recuperação depende da
formação de novas terminações axoniais. Porém, ao contrário do Clostridium botulinum, não há interferência na
transmissão da acetilcolina.
A cadeia leve da toxina é internalizada em compartimentos semelhantes ao endossoma e transportada das
terminações nervosas periféricas para o sistema nervoso central por transporte axonal retrógrado.
A doença ocorre após a introdução dos esporos na lesão, que em baixo potencial redox são capazes de
germinar e multiplicar-se. A toxina é liberada no organismo após a lise celular e então se liga a junções
neuromusculares dos neurônios motores para então serem endocitadas. Por transporte retrógrado, através dos
axônios, a tetanospasmina chega ao sistema nervoso central e então impede a liberação de neurotrasmissores
bloqueando os impulsos inibitórios aos neurônios motores, e conseqüentemente levando a uma paralisia
espástica.
Sintomatologia / Manifestações Clínicas
O período de incubação do tétano varia de poucos dias a algumas semanas, e a duração desse período
está diretamente relacionada à distância entre a infecção primária da ferida e o sistema nervoso central.
Existem várias formas de tétano:
Generalizado, que é a forma mais comum. Na maioria dos casos o primeiro sinal e o comprometimento do
músculo masseter que recebe o nome de trismo. O riso sardônico, devido à contração contínua dos
músculos faciais também é outra característica marcante. Outros sinais como sudorese, salivação
irritabilidade e espasmos dorsais persistentes (opostótono), são características marcantes do tétano
generalizado. No caso de doença mais grave, o sistema nervoso também é afetado, e os sinais e
sintomas incluem arritmias cardíacas, flutuação da pressão arterial, sudorese acentuada e desidratação.
Localizado, em que a doença permanece restrita à musculatura no local da infecção primária.
Cefálico, em que a cabeça é o local primário da infecção.
Neonatal, a infecção inicial ocorre no coto-umbilical e progride a uma infecção generalizada.
Diagnóstico
O diagnóstico do tétano é estabelecido com base nas manifestações clínicas. A detecção microscópica ou o
isolamento do Clostridium tetani são úteis, mas freqüentemente não tem êxito, pois uma porcentagem muito
pequena dos infectados, apenas 30%, apresenta cultura positiva, visto que a doença pode ser causada por um
número relativamente pequeno de microorganismos e as bactérias de crescimento lento são rapidamente
destruídas quando expostas ao ar.
O tétano também pode ser confundido com afecções da boca que se fazem acompanhar de trismo como
abscesso dentário, periostite alvéolo-dentária, erupção viciosa do dente do terceiro molar, fratura e/ou
osteomielite da mandíbula, abscesso amidaliano e/ou retrofaríngeo.
Prevenção e Tratamento
O tratamento do tétano requer desbridamento da ferida primária, administração de metronidazol,
inumização passiva com imunoglobulina antitetânica humana e vacinação com toxóide tetânico. Os cuidados
com a ferida e o tratamento com metronidazol eliminam as bactérias vegetativas que produzem toxinas,
enquanto os anticorpos antitoxina ligam-se às moléculas de tetanospasmina livre. A toxina ligada às terminações
nervosas é protegida dos anticorpos. Por conseguinte, os efeitos tóxicos devem ser controlados
sintomaticamente até o restabelecimento da regulação normal da transmissão sináptica. A vacinação com uma
série de três doses de toxóide tetânico e doses de reforço a cada dez anos é altamente eficaz na prevenção do
tétano.
O tétano é uma doença que não pode ser transmitida de um doente para outro, tão pouco confere
imunidade. Para evitar essa doença, a população deve ser adequadamente vacinada.
BOTULISMO
Agente Etiológico
É uma doença causada por exotoxinas produzidas pelo Clostridium botulinum, um bacilo Gram-positivo
anaeróbio, formador de esporos ovais e subterminais e que apresenta flagelos peritríquios. Tem como hábitat
natural o solo, a poeira e sedimentos marinhos, podendo ser encontrados em agroprodutos frescos ou
industrializados. Essa espécie produz oito tipos de toxina, de natureza protéica, denominadas A, B, C1, C2, D, E,
F e G, sendo apenas os tipos A, B, E e F causadores da doença no homem.
Atualmente, são conhecidas três formas de botulismo:
Botulismo clássico, causado pela ingestão de alimentos contendo as neurotoxinas;
Botulismo de lesões, doença infecciosa causada pela proliferação e conseqüente liberação de toxinas
em lesões infectadas com o C. botulinum;
Botulismo infantil, também uma doença infecciosa causada pela ingestão de esporos do C. botulinum e
subseqüente germinação, multiplicação e produção da toxina no intestino de crianças com menos de um
ano de idade.
De modo geral, uma cepa de C. botulinum produz somente um tipo de toxina. A produção desta ocorre
durante a multiplicação bacteriana, mas apenas uma pequena quantidade é liberada para o ambiente nesta fase.
A liberação é maior e significativa quando se inicia o processo de lise da célula bacteriana.
Toxina / Patogenia
As toxinas do C. botulinum estão entre as substâncias mais tóxicas conhecidas. São destruídas pelo calor a
100ºC durante vinte minutos e, sua a dose letal para o ser humano é próxima a 1-2 g.
São proteínas neurotóxicas de estrutura e ação semelhantes, constituídas de cadeias pesadas e leves,
unidas por uma ligação de dissulfeto. Com exceção da toxina C2, as demais apresentam ação neurotóxica.
A toxina age através do bloqueio da liberação do neurotransmissor nas junções neuromusculares, sem
interferir na função sensorial do hospedeiro. Tanto os sistemas colinérgicos quanto os adrenérgicos são afetados,
sendo necessária uma concentração maior de toxina para inibir a liberação de noradrenalina comparada à de
acetilcolina.
O mecanismo neurotóxico tem início com a ligação da toxina aos sítios receptores na membrana présináptica, seguida pela internalização da toxina e bloqueio da liberação do neurotransmissor. Depois que a toxina
sofre a internalização, não é mais possível bloquear seu efeito neurotóxico.
A toxina botulínica tem sido usada para tratamento de doenças relacionadas a contrações musculares
indesejáveis e para o tratamento estético, Botox, em concentrações muito menores àquelas que causam a
doença.
Sintomatologia
O botulismo apresenta quatro quadros clínicos denominados: período de incubação (assintomático),
período de invasão (nervoso, respiratório, digestivo ou misto), período de estado e período de declínio.
O de origem alimentar e o de lesões produzem sintomas que afetam o sistema nervoso, mas as pessoas
mantêm um estado mental claro até pouco antes da morte. Os sintomas podem incluir visão embaçada ou visão
dupla, sensação de boca seca, dificuldades para engolir, diminuição da pressão arterial e retenção de líquidos.
Fraqueza e paralisa muscular são sintomas que indicam o início da ação da neurotoxina.
Em algumas pessoas, a doença causa paralisia respiratória e pode provocar a morte. Bebês com botulismo
freqüentemente apresentam prisão de ventre, param de comer e ficam apáticos, podendo apresentar sintomas
mais graves do sistema nervoso posteriormente.
Diagnóstico
História alimentar e exame físico do paciente nem sempre são suficientes para estabelecer o diagnóstico,
pois existem outras doenças parecidas com o botulismo. A forma mais direta para se confirmar a doença é
demonstrar a presença da toxina botulínica através da injeção das fezes no caso do botulismo alimentar e infantil
e do soro, no caso do botulismo por lesões em camundongos. Depois, observa-se o desenvolvimento de
sintomas nesses animais.
A coleta do sangue do paciente para investigação da toxina deve ser feita precocemente, pois, se tardia,
pode impedir a detecção da toxina, que é rapidamente absorvida pelos tecidos (após oito dias do início da
doença a toxina não é mais encontrada).
Tratamento
O tratamento deverá ser realizado em unidade de terapia intensiva e divide-se em duas fases igualmente
importantes: o tratamento específico e o geral.
O específico é realizado com o uso de soro antibotulínico - caso a doença seja diagnosticada precocemente
- com antitoxina tri, penta ou heptavalente, que atua contra a toxina circulante e não contra aquela que já se fixou
no sistema nervoso.
O tratamento geral inclui medidas para eliminar a toxina do aparelho digestivo, antibióticos (essa terapia
com agentes antimicrobianos é questionada uma vez que a lise da bactéria no intestino poderia aumentar a
disponibilidade de toxina), hidratação e alimentação balanceadas e assistência respiratória entre outras.
A recuperação da doença é lenta e não existem remédios ou soro que eliminem a toxina do organismo.
Prevenção
A prevenção do botulismo consiste na realização de educação sanitária: os alimentos que serão
conservados deverão estar absolutamente limpos; as carnes devem provir de animais sacrificados e preparados
com as mais rigorosas medidas higiênicas; quando conservados em salmoura, a concentração de NaCl deve ser
superior a 15% e quando em ácido acético, a concentração deste não deve ser inferior a 2%; a esterilização
industrial deve ser feita em autoclave a 120ºC, durante prazo variável.
No indivíduo exposto deve-se provocar o vômito e a evacuação intestinal imediata, seguidos por soroterapia
por via intramuscular.
BOTOX
As marcas da expressão aparecem na face, na forma de sulcos ou rugas e são provocadas pela ação dos
músculos. Estes, sendo contraídos repetidas vezes, ficam atrofiados e com a tonicidade aumentada, formando os
sulcos e as rugas. A toxina Botox é usada então, em pequenas doses, para corrigir essas marcas.
A técnica consiste em injetar a substância no músculo, obtendo-se assim uma paralisia temporária, de
músculos desnecessários, com o desaparecimento das rugas mais leves e atenuação das mais profundas.
A duração deste efeito é de seis meses e a aplicação pode então ser repetida.
INTOXICAÇÃO ALIMENTAR E INFECÇÃO INVASIVA
Agente etiológico: Clostridium perfringens
É um grande bacilo, Gram positivo, cujos esporos são raramente observados; é um dos poucos clostrídios
imóveis, cresce rapidamente em tecidos e culturas (sendo favorecido por um ambiente anaeróbio), é hemolítico e
metabolicamente ativo. A produção de quatro toxinas letais principais de C. perfringens (toxinas alfa, beta,
épsilon e iota) é utilizada para subdividir os microorganismos isolados em cinco tipos (A a E).
O do tipo A é o responsável pela maioria das infecções humanas, como gangrena gasosa, infecções dos
tecidos moles e intoxicação alimentar. Habita comumente o trato intestinal dos seres humanos e animais, sendo
amplamente distribuído na natureza, sobretudo no solo e água contaminada com fezes. Este microrganismo
forma esporos sobrevivendo por longos períodos em condições ambientais adversas.
As cepas do tipo B a E não sobrevivem no solo, mas colonizam o trato intestinal de animais e, em certas
ocasiões, do homem.
Toxinas e Patogenia
O potencial patogênico de C. perfringens é atribuído principalmente às doze toxinas e enzimas produzidas
por esse microrganismo.
A toxina alfa é a mais importante, produzida por todos os tipos de C. perfringens. É uma lecitinase
(fosfolipase C) que provoca a lise dos eritrócitos, plaquetas, leucócitos e células endoteliais. Esta toxina está
associada ao aumento da permeabilidade vascular, com hemólise maciça e sangramento, destruição tecidual,
hepatotoxicidade e disfunção do miocárdio. As maiores quantidades da toxina alfa são produzidas por C.
perfringens do tipo A.
A toxina beta é responsável pela produção das lesões necróticas na enterite necrotizante.
A toxina épsilon é uma pró-toxina, que ativada, aumenta a permeabilidade vascular da parede
gastrintestinal.
A toxina iota possui atividade necrótica e aumenta a permeabilidade vascular.
A enterotoxina é uma proteína produzida no cólon e liberada durante a formação de esporos. É produzida
basicamente por cepas do tipo A, mas também por algumas cepas do tipo C e D. Interrompe o transporte de íons
no íleo e jejuno através da sua inserção na membrana celular, alterando sua permeabilidade. Muitas células
vegetativas devem ser ingeridas com o alimento contaminado para produzir os efeitos enterotóxicos.
Gangrena Gasosa
É uma doença potencialmente fatal, caracterizada por dor intensa, observada dentro de uma semana após
a introdução dos clostrídios nos tecidos em conseqüência de traumatismos ou cirurgia. Este evento é
rapidamente seguido de extensa necrose muscular, choque, insuficiência renal e morte freqüentemente dentro de
dois dias após o início. A presença de gás no tecido ocorre em decorrência da atividade metabólica da bactéria
em rápida divisão. As toxinas do microrganismo causam hemólise e sangramento. É mais comumente causada
por C. perfringens, porém outras espécies de clostrídios podem causar a doença.
Quando não ocorre comprometimento muscular, o processo destrutivo e rapidamente progressivo em que
os microrganismos se disseminam através dos planos fasciais é chamado fasciite. Estes microrganismos
também podem iniciar a celulite, embora algumas espécies de clostrídios possam colonizar feridas e a pele sem
nenhuma conseqüência clínica.
Intoxicação Alimentar
É uma doença bacteriana relativamente comum, caracterizada por um curto período de incubação (8 à 24
horas), as manifestações clínicas consistem em cólicas abdominais e diarréia aquosa na ausência de febre,
náusea ou vômitos e evolução clínica de menos de 24 horas. A doença é produzida pela ingestão de carne
contaminada com grandes números de C. perfringens do tipo A (108 a 109 microrganismos). São freqüentes os
surtos em instituições como em escolas, hospitais, prisões etc, onde há larga produção de alimentos preparados
com muita antecedência antes de serem servidos, favorecendo a multiplicação de C. perfringens. A enterotoxina
produzida após a germinação dos esporos atua como superantígeno, estimulando a liberação de citocinas dos
linfócitos. A refrigeração do alimento após sua preparação evita a produção de enterotoxina. Por outro lado, o
reaquecimento pode destruir a toxina.
Enterite Necrosante
É um processo necrosante agudo, raro, do jejuno caracterizado por dor abdominal, diarréia sanguinolenta,
choque e peritonite. É causada por C. perfringens do tipo C, que produz toxina beta, e, a taxa de mortalidade em
pacientes com esta infecção atinge quase 50%.
A beta toxina pode ser inibida por proteases pancreáticas.
Tratamento
A gangrena gasosa e a fasciite podem ser tratadas agressivamente com desbridamento cirúrgico e altas
doses de penicilina. Apesar de todos os esforços terapêuticos, a taxa de mortalidade varia de 40 a quase 100%.
As doenças por clostrídios localizadas e menos graves podem ser tratadas, com êxito, com penicilina,
sendo o desenvolvimento de resistência raramente registrado, porém quando ocorrido utiliza-se metronidazol ou
imipenem. Não há necessidade de antibioticoterapia para a intoxicação alimentar causada por clostrídios.
Conclusão
Botulismo
Tétano
Paralisia Flácida
Paralisia Espástica
Inibição de sinapses excitatórias
Inibição de sinapses inibitórias
Inibição de sinapses excitatórias
Inibição de sinapses inibitórias
Inibe a liberação do
neurotransmissor da junção
neuromuscular: acetilcolina
Inibe neurotransmissores
adrenérgicos e colinérgicos (não
impede a acetilcolina)
Bibliografia
Microbiologia TRABULSI – 4ª edição
Microbiologia, conceitos e aplicações – volume 1, capítulo 4
Tratado de Infectologia – Ricardo Verones e Roberto Focaccia – 2ª edição – Ed. Atheneu
Microbiologia Médica – Morraiy, P. R.; 3ª edição – Ed Guanabara
www.unificado.com.br/biologia/parasitismo/tetano.vacina.htm
www.saudesergipe.com.br/doencas/botulismo.htm
www.saude.discovery.com
http://microvet.arizona.edu/Courses/MIC420/lecture_notes/clostridia/clostridia_neurotox/movie/botulinum_movie.html
Revista Prática Hospitalar – ano 6 – set/out 2004