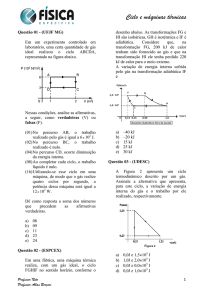
01 - (FUVEST SP/2016)
Uma garrafa tem um cilindro afixado em sua boca, no qual um
êmbolo pode se movimentar sem atrito, mantendo constante a
massa de ar dentro da garrafa, como ilustra a figura.
Inicialmente, o sistema está em equilíbrio à temperatura de 27
3
ºC. O volume de ar na garrafa é igual a 600cm e o êmbolo tem
2
uma área transversal igual a 3 cm . Na condição de equilíbrio,
com a pressão atmosférica constante, para cada 1 ºC de
aumento da temperatura do sistema, o êmbolo subirá
aproximadamente
A respeito dessas transformações, afirmou-se o seguinte:
I. O trabalho total realizado no ciclo ABCA é nulo.
II. A energia interna do gás no estado C é maior que no estado
A.
III. Durante a transformação A B, o gás recebe calor e realiza
trabalho.
Está correto apenas o que se afirma em
Note e adote:
o gás deve ser tratado com ideal;
a transformação B C é isotérmica.
a) 0,7 cm
b) 1,4 cm
c) 2,1 cm
d) 3,0 cm
e) 6,0 cm
Note e adote:
0 ºC = 273 K
Considere o ar da garrafa como um gás ideal.
a)
b)
c)
d)
e)
I
II
III
I e II
II e III
04 - (UEL PR/2015)
Analise o gráfico a seguir, que representa uma transformação
cíclica ABCDA de 1 mol de gás ideal.
02 - (UNESP/2016)
Determinada massa de nitrogênio é armazenada a 27 ºC dentro
de um cilindro fechado em sua parte superior por um êmbolo de
massa desprezível, sobre o qual está apoiado um corpo de 100
kg. Nessa situação, o êmbolo permanece em repouso a 50 cm
de altura em relação à base do cilindro. O gás é, então, aquecido
isobaricamente até atingir a temperatura de 67 ºC, de modo que
o êmbolo sofre um deslocamento vertical h , em movimento
uniforme, devido à expansão do gás.
a) Calcule o trabalho realizado pelo gás durante o ciclo ABCDA.
b) Calcule o maior e o menor valor da temperatura absoluta do
J
gás no ciclo (considere R 8
).
Kmol
Justifique sua resposta apresentando todos os cálculos
realizados.
2
Desprezando o atrito, adotando g = 10 m/s e sabendo que a
2
área do êmbolo é igual a 100 cm , que a pressão atmosférica
5
2
local vale 10 N/m e considerando o nitrogênio como um gás
ideal, calcule o módulo, em N, da força vertical que o gás exerce
sobre o êmbolo nesse deslocamento e o trabalho realizado por
essa força, em J, nessa transformação.
05 - (IFSC/2015)
O gráfico a seguir representa a transformação gasosa sofrida por
um gás, quando passa do estado A para o estado C, passando
também pelo estado B. Admitindo o gás como ideal e tendo o
gráfico como base, assinale no cartão-resposta a soma da(s)
proposição(ões) CORRETA(S).
03 - (FUVEST SP/2015)
Certa quantidade de gás sofre três transformações sucessivas,
AB, BC e CA, conforme o diagrama p-V apresentado na
figura abaixo.
Córtex Vestibulares Rua T38, nº 61, Setor Bueno. Fone: (62)3609-9354
1
a)
b)
c)
d)
01. De A para B, o gás sofre uma transformação isobárica, na
qual quantidade de calor trocado é maior que o trabalho
associado a esta transformação.
2
02. O trabalho realizado de A para C é de 1,4 10 J.
04. A temperatura absoluta do gás no estado A é o dobro da
temperatura no estado C e metade da temperatura no estado B.
08. Admitindo que na transformação de A para C o gás cede uma
quantidade de calor igual a 120J, a sua energia interna varia em
–310J.
16. O fato de a pressão diminuir do estado A para o estado C é
consequência de um vazamento de gás para o meio externo.
32. A transformação de B para C é uma adiabática, pois a
temperatura diminuiu devido à energia gasta na forma de
trabalho pelo gás.
06 - (UNIMONTES MG/2015)
Num processo isocórico, três moles de gás ideal recebem
3
7,510 J de calor ao variar sua temperatura de 300 K para 500
K. Num processo isobárico, essa mesma amostra de gás recebe
3
12,510 J de calor para sofrer a mesma variação de
temperatura. O trabalho feito pelo gás, no processo isobárico, é
igual a
a)
b)
c)
d)
3
08 - (UFSC/2016)
A busca por alternativas energéticas para o futuro ou para locais
com poucos recursos econômicos tem levado à proposição de
inovações cada vez mais criativas, como a Soccket, mostrada na
figura abaixo. A Soccket é uma bola de futebol com um pequeno
pêndulo no interior que aproveita a energia cinética do seu
movimento através de um gerador elétrico conectado a uma
bateria recarregável. A energia armazenada pode ser usada para
os mais diversos fins, como o acendimento de lâmpadas e a
recarga de baterias e dispositivos eletrônicos.
Disponível em: <http://www.greenprophet.com/2012/12/socket-afun-powered-energy-ball-kids-kick-for-power/>. [Adaptado].
Acesso em: 24 set. 2015.
Com base no exposto acima e no Princípio de Conservação de
Energia, é CORRETO afirmar que:
01. quando a Soccket é chutada, realiza-se um trabalho
mecânico sobre ela.
02. apenas o trabalho mecânico determina a quantidade de
energia que é transferida ou retirada da Soccket.
04. toda energia recebida pela Soccket durante um chute é
convertida em energia elétrica.
08. a energia armazenada na Soccket é transferida para outros
dispositivos eletrônicos pelo trabalho elétrico.
16. a transformação da energia cinética em energia elétrica no
gerador elétrico da Soccket é explicada pela Lei de Faraday.
32. a função da bateria da Soccket é de aumentar a energia
elétrica produzida.
5,010 J.
3
2,010 J.
3
4,010 J.
3
1,010 J.
07 - (PUC GO/2016)
Mulher proletária
Mulher proletária — única fábrica
que o operário tem (fábrica de filhos),
tu
na tua superprodução de máquina humana
forneces anjos para o Senhor Jesus,
forneces braços para o senhor burguês.
Mulher proletária,
o operário, teu proprietário
há de ver, há de ver:
a tua produção,
a tua superprodução,
ao contrário das máquinas burguesas
salvar teu proprietário.
(LIMA, Jorge de. Melhores poemas.
3. ed. São Paulo: Global, 2006. p. 69.)
O texto faz referência a máquinas. Suponha que uma
Máquina Térmica de Carnot, com eficiência de 32%, receba a
cada ciclo 5000 joules de energia de uma fornalha a 227 ºC.
Com base nessas informações, analise as afirmações a seguir:
Adote 0ºC igual a 273 K.
I. O trabalho por ciclo realizado por essa máquina é igual a
1600 joules.
II. A fonte fria que recebe o calor expelido se encontra a 87 ºC.
III. Se a fonte fria estivesse a 182 ºC, a eficiência dessa máquina
cairia para 9%.
IV. Se os ciclos dessa máquina se repetem a uma taxa de 0,25
Hz, então ela produz 300 W de potência útil.
Marque a alternativa que apresenta todos os itens corretos:
Colégio Córtex
I e II.
I e III.
I e IV.
II e IV.
09 - (UEL PR/2015)
Além do flogístico, outro conceito que surge na origem da
compreensão da termodinâmica é o calórico, fluido elástico que
permearia todas as substâncias e se moveria de um corpo a
outro através de processos de atração e repulsão. Conde
Rumford, ao estudar a perfuração de canhões sob a água,
concluiu que aparentemente haveria calórico ilimitado sendo
expelido dos blocos metálicos ao longo do processo de
usinagem, fato que contraria a premissa de que tal substância
não poderia ser criada, somente conservada. Tais observações
iniciaram a derrocada do conceito de calórico.
De acordo com a Física atual, é correto afirmar que o fenômeno
observado por Rumford diz respeito à
a)
b)
c)
d)
e)
combustão das moléculas da água.
combustão dos blocos de metal.
conversão de flogístico em calórico.
conversão de energia cinética em calor.
troca de calor entre a água e o metal.
10-(ENEM 2015)
O ar atmosférico pode ser utilizado para armazenar o excedente
de energia gerada no sistema elétrico, diminuindo seu
desperdício, por meio do seguinte processo: água e gás
carbônico são inicialmente removidos do ar atmosférico e a
massa de ar restante é resfriada até –198 ºC. Presente na
Rua T53, nº 929, Setor Bueno. Fone: (62)3251-3477
proporção de 78% dessa massa de ar, o nitrogênio gasoso é
liquefeito, ocupando um volume 700 vezes menor. A energia
excedente do sistema elétrico é utilizada nesse processo, sendo
parcialmente recuperada quando o nitrogênio líquido, exposto à
temperatura ambiente, entra em ebulição e se expande, fazendo
girar turbinas que convertem energia mecânica em energia
elétrica.
MACHADO, R. Disponível em: www.correiobraziliense.com.br.
Acesso em: 9 set. 2013 (adaptado).
No processo descrito, o excedente de energia elétrica é
armazenado pela
a) expansão do nitrogênio durante a ebulição.
b) absorção de calor pelo nitrogênio durante a ebulição.
c) realização de trabalho sobre o nitrogênio durante a
liquefação.
d) retirada de água e gás carbônico da atmosfera antes do
resfriamento.
e) liberação de calor do nitrogênio para a vizinhança durante a
liquefação.
11 - (ENEM/2014)
Um sistema de pistão contendo um gás é mostrado na figura.
Sobre a extremidade superior do êmbolo, que pode movimentarse livremente sem atrito, encontra-se um objeto. Através de uma
chapa de aquecimento é possível fornecer calor ao gás e, com
auxílio de um manômetro, medir sua pressão. A partir de
diferentes valores de calor fornecido, considerando o sistema
como hermético, o objeto elevou-se em valores h, como
mostrado no gráfico. Foram estudadas, separadamente,
quantidades equimolares de dois diferentes gases, denominados
M e V.
a) O trabalho realizado pela máquina térmica em questão em
4
um ciclo completo é igual a 2,5 10 J.
b) A variação da energia interna em um ciclo completo é igual a
4
5,0 10 J.
c) Se a temperatura do gás em I for igual a T0, a temperatura do
gás em K será igual a 2T0.
d) No trecho de I para J, não há perda de calor.
13 - (UniCESUMAR SP/2015)
2
Um gás perfeito, submetido a uma pressão de 35 N/m ,
3
apresenta um volume inicial de 10 m . Em uma transformação
isobárica, esse gás sofreu uma variação em sua energia interna
de 750 J após receber 2500 J de energia térmica de uma fonte
de calor. Encerrada a transformação, podemos afirmar que o
3
volume final do gás, em m , passou a ser de:
a)
b)
c)
d)
e)
80
60
50
40
10
14 - (IFGO/2014)
Considerando duas expansões gasosas ideais, uma isobárica e
outra adiabática, é correto afirmar que:
A diferença no comportamento dos gases no experimento
decorre do fato de o gás M, em relação ao V, apresentar
a)
b)
c)
d)
e)
maior pressão de vapor.
menor massa molecular.
maior compressibilidade.
menor energia de ativação.
menor capacidade calorífica.
12 - (ESCS DF/2015)
A figura acima ilustra um diagrama P V de uma máquina
térmica. Considerando que n moles de um gás monoatômico
ideal percorre o ciclo IJKL nesse diagrama, assinale a opção
correta.
a) Na expansão isobárica, haverá uma redução da energia
interna do gás.
b) Na expansão adiabática, o volume e a temperatura sofrem
redução.
c) Em ambas as expansões, a temperatura sofre aumento.
d) Na expansão adiabática, não há trocas de calor e a energia
interna do gás sofre redução.
e) Na expansão adiabática, o produto da pressão pelo volume
se mantém constante.
15 - (UECE/2015)
O biodiesel é um combustível biodegradável que pode ser
produzido a partir de gorduras animais ou óleos vegetais. Esse
combustível substitui total ou parcialmente o óleo diesel de
petróleo em motores ciclo diesel automotivos. Considere que a
queima de 1,0 g de biodiesel libera x Joules de energia e o
rendimento do motor é de 15%. Qual o trabalho mecânico
realizado pelo motor, em Joules, resultante da queima de 10 g
desse combustível?
a)
b)
c)
d)
1,5x/100.
150x/10.
15x/100.
15x/10.
16 - (UECE/2015)
Em um motor de carro o processo de combustão gera 300 J de
energia térmica. Deste valor, 200 J são perdidos sob a forma de
calor. Qual a eficiência desse motor?
a)
b)
c)
d)
Colégio Córtex
300/3.
100/3.
200/3.
500/2.
Rua T53, nº 929, Setor Bueno. Fone: (62)3251-3477
17 - (FUVEST SP/2015)
A energia necessária para o funcionamento adequado do corpo
humano é obtida a partir de reações químicas de oxidação de
substâncias provenientes da alimentação, que produzem
aproximadamente 5 kcal por litro de O2 consumido. Durante uma
corrida, um atleta consumiu 3 litros de O2 por minuto.
Determine
a) a potência P gerada pelo consumo de oxigênio durante a
corrida;
b) a quantidade de energia E gerada pelo consumo de oxigênio
durante 20 minutos da corrida;
c) o volume V de oxigênio consumido por minuto se o atleta
estivesse em repouso, considerando que a sua taxa de
metabolismo basal é 100 W.
Note e adote: 1 cal = 4J.
18 - (IFGO/2015)
As máquinas térmicas e as máquinas frigoríficas funcionam
ciclicamente obedecendo aos princípios da termodinâmica.
Sobre essas máquinas, é correto afirmar que
a) o rendimento de uma máquina térmica idealizada que
funciona em acordo com o ciclo de Carnot depende
exclusivamente das temperaturas das fontes ―quente‖ e ―fria‖.
b) uma máquina frigorífica essencialmente converte calor em
trabalho.
c) uma máquina térmica pode converter integralmente calor em
trabalho.
d) as máquinas frigoríficas se utilizam de uma fonte de energia
externa para converter calor em trabalho.
e) quanto menor a diferença de temperatura entre a fonte
―quente‖ e a fonte ―fria‖ de uma máquina a vapor idealizada que
funcione em acordo com o ciclo de Carnot, maior será seu
rendimento.
19 - (UNIMONTES MG/2015)
Uma máquina térmica opera segundo o ciclo representado no
diagrama PV da figura a seguir. O produto P1V1 = 12 J e a
eficiência dessa máquina é de 40 %. O trabalho realizado por
ciclo e o calor rejeitado por essa máquina, em Joules, são,
respectivamente:
a)
b)
c)
d)
No Ciclo de Carnot um gás ideal sofre quatro transformações
reversíveis: duas isotérmicas (AB e CD) e duas adiabáticas (BC
e DA). A respeito da máquina e do Ciclo de Carnot, é correto
afirmar que
a) na transformação BC a máquina cede calor ao meio externo.
b) na transformação CD o gás sofre uma compressão e é
aquecido.
c) o trabalho total realizado em cada ciclo é nulo.
d) o gás só troca calor com o meio externo nas transformações
AB e CD.
e) na expansão AB o meio externo realiza trabalho sobre o gás.
21 - (UFU MG/2014)
As máquinas a combustão interna do tipo Otto e Diesel,
inventadas no final do século XIX, são compostas de, no mínimo,
um cilindro, contendo um êmbolo móvel (pistão) e diversas peças
móveis e representam a maioria dos motores dos veículos
atuais.
A figura 1 apresenta os quatro tempos de uma máquina térmica
do tipo Otto. O ciclo ideal que mais se aproxima do que
efetivamente ocorre em máquinas do tipo Otto ou Diesel é o ciclo
composto Otto-Diesel, representado na figura 2, por meio de um
diagrama pressão versus volume. No diagrama da figura 2, as
linhas curvas representam transformações adiabáticas.
36 e 54.
72 e 180.
72 e 108.
36 e 90.
20 - (UEA AM/2013)
Em 1824 o engenheiro francês Nicolas Léonard Sadi Carnot
demonstrou que se uma máquina térmica, operando entre duas
temperaturas constantes T1 e T2 (com T1 > T2), trabalhasse em
ciclos segundo o gráfico mostrado, apresentaria o maior
rendimento possível para essas temperaturas. Esse ciclo passou
a se chamar Ciclo de Carnot e essa máquina, máquina ideal ou
máquina de Carnot.
Silveira, F. L. Máquinas térmicas à combustão interna de Otto e Diesel. Disponível
em <http://www.if.ufrgs.br/~lang/maqterm.pdf>. Acesso em: 11 fev. 2014.
(adaptados).
a) Dentre as transformações mostradas na figura 2, quais são
isovolumétricas e quais são isobáricas?
Colégio Córtex
Rua T53, nº 929, Setor Bueno. Fone: (62)3251-3477
b) Descreva e explique o que ocorre com a temperatura da
mistura gasosa dentro do cilindro da máquina durante a
expansão e-f, mostrada no diagrama da figura 2.
c) Durante o ciclo termodinâmico apresentado na figura 2,
energia é acrescida ao sistema para o funcionamento da
máquina (motor a explosão). Explique a origem desse acréscimo
de energia ao sistema e a forma pela qual esse acréscimo
ocorre, relacionando-o com o ciclo da figura 1 e o diagrama da
figura 2.
22 - (UFG GO)
A figura a seguir representa o ciclo de Otto para motores a
combustão interna. Nesse tipo de motor, a vela de ignição gera
uma faísca que causa a combustão de uma mistura gasosa.
Considere que a faísca seja suficientemente rápida, de modo
que o movimento do pistão possa ser desprezado.
I. Nenhuma máquina térmica operando em ciclos pode retirar
calor de uma fonte e transformá-lo integralmente em trabalho.
II. A segunda lei da Termodinâmica se aplica aos refrigeradores,
porque esses transferem calor da fonte fria para a fonte quente.
III. O rendimento de uma máquina térmica que opera em ciclos
pode ser de 100%.
Após a análise feita, verifica-se que é(são) correta(s) apena(s)
a(s) proposição(ões)
a) II e III.
b) II.
c) III.
d) I.
e) I e II.
25 - (UFG GO)
A figura abaixo mostra o comportamento de n mols de um gás
ideal numa expansão adiabática AB entre as isotermas TA e TB.
C
5
Dado: P
CV 3
A faísca e a liberação dos gases pelo escapamento ocorrem,
respectivamente, nos pontos
a)
b)
c)
d)
e)
A e C.
B e A.
D e A.
D e B.
O e C.
Com base no gráfico, calcule:
a) A pressão pB.
b) A temperatura TB.
23 - (UFG GO)
A máquina térmica é um dispositivo que pode tanto fornecer
energia para um sistema quanto retirar.
____________________________________________________
GABARITO:
1) Gab: A
2) Gab: Fgás = 2,0 103 N e
Considere que a máquina térmica opera com um gás ideal em
um sistema fechado, conforme o ciclo ilustrado na figura acima.
De acordo com o exposto.
a) calcule o trabalho total em um ciclo;
b) explique como ela opera, ou seja, qual é a sua função?
Justifique sua resposta;
c) calcule a temperatura no ponto C, considerando que a
temperatura no ponto A é de 300k.
24 - (UEPB/2010)
A Revolução Industrial consistiu em um conjunto de mudanças
tecnológicas com profundo impacto no processo produtivo em
nível econômico e social. Iniciada na Inglaterra em meados do
século XVIII, expandiu-se pelo mundo a partir do século XIX.
James Hargreaves, 1764, na Grã-Bretanha, inventa a fiadora
―spinning Jenny‖, uma máquina de fiar rotativa que permitia a um
único artesão fiar oito fios de uma só vez.; James Watt, 1768,
inventa a máquina a vapor; Gottlieb Daimler, 1885, inventou um
motor a explosão etc.
Acerca do assunto tratado no texto, em relação às máquinas
térmicas, de acordo com a segunda lei da Termodinâmica,
podemos afirmar:
Colégio Córtex
400
J
3
3) Gab: E
4) Gab:
a) O trabalho no ciclo ABCDA não é nulo somente ao longo das transformações
isobáricas, sendo igual à soma dos trabalhos de cada segmento do ciclo. Desse
modo,
BC = pV = 15 (6 – 2)J = 60J
enquanto
DA = 5 (2 – 6)J = –20J
sendo o valor do trabalho no ciclo
= 40 J
que também corresponde à área do retângulo que define o ciclo.
b) A equação de estado de um gás ideal é dada por
pV = nRT
Para 1 mol de um gás ideal, tem-se
T
pV
R
de onde segue que o maior valor da temperatura é
T
15 6 45
11,25K
8
4
enquanto o menor valor é
T
5 2 5
1,25K
8
4
5) Gab: 13
6) Gab: A
7) Gab: B
8) Gab: 25
9) Gab: D
10) Gab: C
11) Gab: E
12) Gab: A
13) Gab: B
14) Gab: D
15) Gab: D
16) Gab: B
17) Gab:
a) P = 15 kcal/min ou P = 1 kW
b) E = 300 kcal ou 1200 kJ
c) V = 0,3 L
18) Gab: A
Rua T53, nº 929, Setor Bueno. Fone: (62)3251-3477
19) Gab: A
20) Gab: D
21) Gab:
a) Isovolumétricas: compressão c-d, onde ocorre a explosão do combustível; e
descompressão f-b, onde ocorre a descarga dos gases provenientes da combustão.
Isobáricas: a-b e b-a, onde ocorre a admissão do combustível e a exaustão dos
gases provenientes da combustão; e d-e, onde ocorre uma expansão ainda sobre
os efeitos da explosão do combustível.
b) A temperatura diminui. A expansão e-f é adiabática, isto significa que não há
troca calor com o ambiente. Deste modo, pela 1ª lei da termodinâmica, o trabalho
realizado pelo gás deve ser igual a variação da energia interna do gás com o sinal
trocado:
Q = + U = 0
= –U
Como o trabalho realizado é positivo, por ser uma expansão, a variação da energia
interna do gás é negativa. Por fim, sabendo que a energia interna do gás é
proporcional a sua temperatura, conclui-se que a redução da energia interna é
acompanhada de uma redução na temperatura.
c) A energia acrescida ao sistema é proveniente da queima do combustível. A
energia que estava armazenada nas ligações químicas do combustível é liberada
durante a explosão do mesmo dentro do cilindro do motor.
Esta explosão, com energia sendo acrescida ao sistema, ocorre na transformação
c-d, ao fim da compressão da mistura gasosa dentro do cilindro, no início do 3º
tempo. Esta explosão é rápida e produz um aumento rápido da pressão
caracterizando uma transformação isovolumétrica. A expansão resultante que
ocorre em seguida é inicialmente isobárica (d-e) e em seguida adiabática (e-f)
finalizando o 3º tempo do ciclo.
22) Gab: D
23) Gab:
a) W = −Área = −125 kJ
b) Opera como um refrigerador porque está sendo realizado trabalho sobre o
sistema (trabalho negativo).
c) TC = 1500 K
24) Gab: E
25) Gab: a) PB
1
0,25atm
4
b) TB = 100 K
Colégio Córtex
Rua T53, nº 929, Setor Bueno. Fone: (62)3251-3477