Feito por André Silva Franco
Visão Geral da Aula
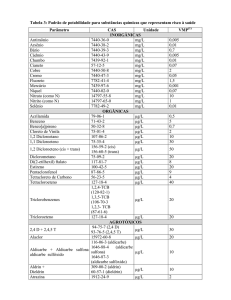
Cátions (Metais – carga +) Ânions (Ametais – carga -)
Adicionar “-eto”
Manter nome do metal
Li
F
Lítio:
Fluoreto:
Na
Sódio:
Cl
Cloreto:
K
Potássio:
Br
Brometo:
Be 2
Berílio:
I
Iodeto:
Mg 2
Magnésio:
2
S
Sulfeto:
Ca 2
Cálcio:
3
N
Nitreto:
Estrôncio:
Sr 2
H
Hidreto:
2
Bário:
Ba
2
Óxido:
2
3
O
Mangânes (II, III...): Mn e Mn
Hidróxido:
OH
Ferro (II, III):
Fe 2 e Fe3
Peróxido:
Cobre (I, II):
O22
Cu e Cu 2
Ouro (I, III):
Superóxido: O2
Au e Au 3
Alumínio:
Cianeto:
Al 3
CN
!
Chumbo (II, IV):
Pb 2 e Pb 4
x
y
M A M y Ax
Compostos Iônicos
Nome do ânion + Nome do Cátion
Óxidos – apresentam como ânion o oxigênio
divalente, e como cátion, um metal.
CaO : Óxido de cálcio
Li2O :
Óxido de lítio
Na2O : Óxido de sódio
K 2O : Óxido de potássio
Mn2O3 : Óxido de manganês (III)
MnO :
MgO :
Fe2O3 :
Óxido de manganês (II)
Óxido de magnésio
Óxido de ferro (III)
CrO3 : Óxido de cromo (VI)
Muitas vezes chamado erroneamente
de Trióxido de cromo!!!
Compostos Iônicos
M x A y M y Ax
Nome do ânion + Nome do Cátion
Hidretos – hidrogênio como ânion ligado a um metal de
família IA ou IIA
NaH : Hidreto de sódio
LiH : Hidreto de lítio
CaH 2 :Hidreto de cálcio
Hidrácidos gasosos– ametais como ânion e hidrogênio
como cátion.
HF :
Fluoreto de hidrogênio
HCl : Cloreto de hidrogênio
HBr : Brometo de hidrogênio
HI :
Iodeto de hidrogênio
H 2 S : Sulfeto de hidrogênio
HCN : Cianeto de hidrogênio
x
y
M A M y Ax
Compostos Iônicos
Hidrácidos aquosos – hidrogênio como cátion ligado
a um ânion
Ácido + nome do elemento(+ídrico)
HF :
Ácido fluorídrico
HCl :
Ácido clorídrico
HBr :
Ácido bromídrico
HI :
Ácido iodídrico
H2S :
Ácido sulfídrico
HCN :
Ácido cianídrico
Compostos Iônicos
x
y
M A M y Ax
Bases – hidroxila (hidróxido) como ânion, ligado a
um cátion de metal.
Hidróxido de + nome do metal
NaOH :
Hidróxido de sódio
KOH :
Hidróxido de potássio
Ba (OH ) 2 :
Hidróxido de bário
Fe(OH )3 :
Hidróxido de ferro (III)
Au (OH )3 :
Hidróxido de ouro (III)
CuOH :
Hidróxido de cobre (I)
Zn(OH ) 2 :
Hidróxido de zinco
NH 4OH :
Hidróxido de amônio
Oxiácidos
Ácidos que possuem um elemento principal ligado a
oxigênio e hidroxilas.
Oxiácidos -chave: Ácido + nome do elemento (+ico)
H 3 BO3
Ácido bórico
H 2CO3
Ácido carbônico
HNO3
Ácido nítrico
H 3 PO4
Ácido fosfórico
H 2 SO4
Ácido sulfúrico
HClO3
Ácido clórico
HBrO3
Ácido brômico
HIO3
Ácido iódico
“Bacana passa cola e briga com o inspetor”
Derivados dos oxiácidos-chave
Adição de um átomo de oxigênio
Ácido + per(+nome do ácido).
HClO4 : Ácido perclórico
HIO4 : Ácido periódico
Remoção de um átomo de oxigênio
Ácido + nome do elemento(+oso)
HNO2 : Ácido nitroso
H 2 SO3 : Ácido sulfuroso
HClO2 : Ácido cloroso
Remoção de dois átomos de oxigênio
Ácido + (hipo)nome do elemento(+oso)
HBrO : Ácido hipobromoso
HIO :
Ácido hipoiodoso
HClO : Ácido hipocloroso
Derivados de Oxiácidos
Oxiânions: trocar “ico” por “ato”, e “oso” por “ito”
CO32
Carbonato
NO3
Nitrato
PO43
SO42
Nitrito
Fosfato
NO2
SO32
Sulfito
Sulfato
ClO2
Clorito
ClO3
Clorato
Hipobromito
BrO3
BrO
Bromato
IO
Hipoiodito
ClO
Hipoclorito
IO3
Iodato
ClO4
Perclorato
IO4
Periodato
“Teimoso mosquito no bico do pato”
M x A y M y Ax
Sais
De modo geral, nome do ânion + nome do cátion
Cloreto de cálcio
CaCl2
FeS
Sulfeto de ferro (II)
Na2CO3
Carbonato de sódio
Mg 3 PO4 2
Fosfato de magnésio
KNO2
Nitrito de potássio
LiClO4
Perclorato de lítio
Cianeto de sódio
NaCN
AlF3
Fluoreto de alumínio
Mn2O3
Óxido de manganês (III)
Compostos Moleculares
Ax By
Prefixo grego + nome de B (ânion) + (prefixo grego)
+ nome de A
CO : Monóxido de carbono
Prefixo
Significado
Mono
1
Di
2
N 2O4 : Tetróxido de dinitrogênio
Tri
3
Tetra
4
P4O10 : Decóxido de tetrafósforo
Penta
5
Hexa
6
Hepta
7
Octa
8
Nona
9
Deca
10
CO2 : Dióxido de carbono
SO3 :
Trióxido de enxofre
PCl5 : Pentacloreto de fósforo
XeF4 : Tetrafluoreto de xenônio
CI 4 :
Tetraiodeto de carbono
SF6 : Hexafluoreto de enxofre
Compostos moleculares
Atenção para os seguintes nomes de hidretos
moleculares:
NH 3 :
H 2O :
PH 3 :
Amônia
Água
Fosfina
SiH 4 :
Silano
H 2O2 :
Peróxido de hidrogênio
Ax By
Casos Especiais
NH
e
NH
Amônia e Amônio:
3
4
Hidróxido de amônio, cloreto de amônio, fosfato de amônio
NH 4OH , NH 4Cl , NH 4 3 PO4
Cromato, Dicromato: CrO42 e Cr2O72
Cromato de sódio, dicromato de potássio, cromato de bário,
dicromato de amônio...
Na2CrO4 , K2Cr2O7 , BaCrO4 , NH 4 2 Cr2O7
Sais hidratados
Adicionar “prefixo grego + hidratado após o nome do sal.
Sulfato de cobre pentaidratado CuSO4 .5H 2O
LiF .H 2O
Cloreto de cálcio diidratado
Fluoreto de lítio monoidratado
CaCl2 .2H 2O
Casos Especiais
Peróxidos: O 2
2
Só ocorre com cátions das famílias IA e IIA.
Na2O2 : Peróxido de sódio
K 2O2 : Peróxido de potássio
CaO2 : Peróxido de cálcio
SnO2 : Óxido de estanho
Oxiácidos ionizados parcialmente:
HCO3
Bicarbonato = hidrogenocarbonato
Bisulfito = hidrogenosulfito
HSO3
Diidrogenofosfato
H 2 PO4
Hidrogenofosfato
HPO 2
4
Permanganato: MnO4
Permanganato de potássio KMnO
4
Fórmula
Nome ordinário
Nome IUPAC
H2O
Água
Óxido de diidrogênio
H2O2
Água-oxigenada
Peróxido de hidrogênio
CO2
Gelo-seco
Dióxido de carbono
NaCl
Sal de cozinha(marinho)
Cloreto de sódio
N2O
Gás hilariante, óxido nitroso
Monóxido de dinitrôgênio
CaCO3
Calcário, mármore
Carbonato de cálcio
CaO
Cal virgem (viva)
Óxido de cálcio
Ca(OH)2
Cal queimada (apagada)
Hidróxido de cálcio
Mg(OH)2
Leite de Magnésia
Hidróxido de magnésio
CaSO4
Gesso
Sulfato de cálcio
Na2CO3
Soda
Carbonato de sódio
NH4OH
Amoníaco
Hidróxido de amônio
KNO3/NaNO3
Salitre/Salitre do Chile
Nitrato de potássio/ de sódio
HCl
Ácido Muriático
Ácido Clorídrico
NO
Óxido nítrico
Monóxido de nitrogênio
Agradecimentos
Boa sorte nos exames! Estudem bastante!
“A questão Primordial não é o que sabemos, mas
como sabemos”
Aristóteles