Programa de Pós-Graduação em Biociência Animal
Área de Concentração Saúde Animal
MARIANA BUENO CARVALHO
TRATAMENTO DA PITIOSE CUTÂNEA EM MEMBROS DE EQUINOS POR MEIO
DE PERFUSÃO REGIONAL INTRAVENOSA
Cuiabá, 2013
MARIANA BUENO CARVALHO
TRATAMENTO DA PITIOSE CUTÂNEA EM MEMBROS DE EQUINOS POR MEIO
DE PERFUSÃO REGIONAL INTRAVENOSA
Dissertação de Mestrado apresentada ao Programa de Pósgraduação em Biociência Animal, da Universidade de Cuiabá –
UNIC como requisito parcial para obtenção do Título de Mestre.
Orientador: Prof. Dr. Luciano A. Pimentel
Cuiabá, 2013
FICHA CATALOGRÁFICA
Dados Internacionais de Catalogação na Publicação (CIP)
C331t
Carvalho, Mariana Bueno
Tratamento da pitiose cutânea em membros de equinos por meio de
perfusão regional intravenosa. / Mariana Bueno Carvalho. – Cuiabá, 2013.
78 f. : il.
Dissertação apresentada à Universidade de Cuiabá, para obtenção do título
de Mestre em Biociência Animal.
Orientador: Prof. Dr. Luciano A. Pimentel
1. Veterinária. 2. Patologia. 4. Fungo. 5. Pitiose Equina I. Título. II.
Universidade de Cuiabá.
CDD 571.995
Normalização e Catalogação na fonte
Bibliotecária Valéria Oliveira dos Anjos - CRB1/1713
MARIANA BUENO CARVALHO
TRATAMENTO DA PITIOSE CUTÂNEA EM MEMBROS DE EQUINOS POR MEIO
DE PERFUSÃO REGIONAL INTRAVENOSA
Dissertação de Mestrado apresentada ao Programa de Pós-graduação em
Biociência Animal, da Universidade de Cuiabá – UNIC como requisito parcial para
obtenção do Título de Mestre.
Orientador Prof. Dr. Luciano A. Pimentel
BANCA EXAMINADORA
___________________________________________________
Orientador: Prof. Dr Luciano A. Pimentel - UNIC
___________________________________________________
Membro Titular: Prof. Dr. Armando de Mattos Carvalho - UNIC
___________________________________________________
Membro Titular: Prof. Dr. Edson Moleta Colodel - UFMT
Cuiabá, 01 de novembro de 2013.
Conceito Final: _____________
Dedico este trabalho á minha família que tanto me
incentivou, pois sem eles nada seria possível. Em
especial ao meu pai que mesmo com problemas de
saúde não mediu esforços, dedicação e
compreensão.
AGRADECIMENTOS
À Deus por te me dado forças e iluminado meu caminho para que pudesse concluir
mais uma etapa da minha vida.
A minha co- orientadora, Prof. Dra. Renata Gebara Sampaio Dória, por me aceitar
com sua orientada, e mesmo estando distante não mediu esforços.
Ao meu orientador Luciano A. Pimentel que me orientou cada passo deste trabalho,
por acreditar na minha capacidade e mostrar que sou capaz de chegar onde eu
desejo.
Aos professores Marco Aurélio M. Pires, Luciane M. Laskoski, Djeison Raimundo,
Lívia Saab Muraro pela dedicação dispensado no auxílio a concretização deste
trabalho.
Armando de Mattos Carvalho, Michelle Igarashi e Edson Moleta Colodel pela
disposição, presença e sugestões feitas na banca de qualificação e defesa de tese
de mestrado, certamente com o objetivo de enriquecer o trabalho.
A minha mãe Ana Clara C. B. Carvalho e meu pai Carlos Roberto de Carvalho, por
estarem torcendo e rezando para que meus objetivos sejam alcançados, por todo
amor que ambos me dedicaram, meu eterno amor e agradecimento. Ao meu irmão
Gabriel pelo carinho e atenção que teve comigo.
Ao meu namorado Diego Santos, pelo imenso apoio, esforço, compreensão e
companheirismo diário.
Ao Programa de Pós-Graduação em Biociência Animal, ao Departamento de Clínica
e Cirurgia Veterinária e ao Hospital Veterinário da UNIC, pela oportunidade e apoio à
realização de pesquisas científicas.
Aos amigos que fiz durante a realização do projeto, pela verdadeira amizade que
construímos em particular aqueles que estavam sempre ao meu lado (Luciana Palu,
Sidney, Vinicius e Rafael).
À Universidade de Cuiabá (UNIC), Faculdade de Medicina Veterinária e Hospital
Veterinário da UNIC, por fomentar este projeto de pesquisa.
À Universidade Federal do Mato Grosso (UFMT), Laboratório de Patologia
Veterinária, pela colaboração com a realização do método de imuno-histoquímica.
À Fundação de Amparo à Pesquisa do Estado de Mato Grosso (FAPEMAT) que
acreditou e auxiliou no desenvolvimento deste estudo experimental.
À Cristália Produtos Químicos e Farmacêuticos que apoiou este estudo
experimental, fornecendo a anfotericina B.
O maior respeito que você pode ter por um adversário é entrar e ganhar dele.
(autor desconhecido)
RESUMO
CARVALHO, Mariana Bueno. Tratamento da pitiose cutânea em membros de
equinos por meio de perfusão regional intravenosa. 2013. 78 f. Dissertação
(Mestrado em Biociência Animal) – Coordenação de Pós-Graduação e Pesquisa,
Universidade de Cuiabá, Cuiabá, 2013.
A pitiose é uma doença cutânea, gastrintestinal ou multissistêmica, granulomatosa,
que atinge equinos, caninos, bovinos, ovinos, felinos e humanos e ocorre em áreas
tropicais, subtropicais ou temperadas, causada pelo oomiceto Pythium insidiosum.
Este organismo filamentoso encontra-se em ambientes aquáticos, especialmente em
regiões pantanosas, com temperaturas superiores a 25º C, como o Pantanal MatoGrossense. Em equinos, a enfermidade caracteriza-se pela formação de granulomas
eosinofílicos, com a presença de massas necróticas denominadas “kunkers”.
Tradicionalmente, o diagnóstico da pitiose no Brasil baseia-se nos dados clínicoepidemiológicos, exame histopatológico e/ou micológico sendo confirmado pela
imuno-histoquímica. A pitiose causa prejuízos significativos na criação de equinos no
Brasil, seja pela morte dos animais, pela perda de função ou pelos gastos com
tratamentos. Vários métodos terapêuticos têm sido utilizados, principalmente em
equinos, incluindo tratamento medicamentoso (antimicóticos), cirúrgico e
imunoterápico. Existe dificuldade no tratamento devido às características deste
oomiceto, que não apresenta esteróis de membrana, sendo, portanto, resistente à
maioria dos antimicóticos.
Palavras-chave: Dermatologia. Infecção. Fungo.
ABSTRACT
CARVALHO, Mariana Bueno. Pythiosis treatment cutaneous of equine limb by
means of intravenous regional perfusion. 2013. 78 f. Dissertation (MSc Animal
Bioscience) - University of Cuiabá, Cuiabá, 2013.
Pythiosis is a cutaneous, gastrointestinal or multisystem granulomatous affecting
horses, dogs, cattle, sheep, cats and humans and occurs in tropical, subtropical and
temperate caused by oomycete Pythium insidiosum). This filamentous organism
found in aquatic environments, especially in marshlands, with temperatures above 25
º C, as the Pantanal of Mato Grosso. In horses, the disease characterized by
eosinophilic granuloma formation in the presence of necrotic masses called
"kunkers". Traditionally, the diagnosis of pythiosis in Brazil is based on clinical,
epidemiological, histopathological and / or mycological, was confirmed by
immunohistochemistry. Pythiosis cause significant damage in the creation of horses
in Brazil, is the death of the animals, the loss of function or by spending on
treatments. Several therapeutic methods have been used primarily in horses,
including drug treatment (antifungal), surgical and immunotherapy. There is some
difficulty in handling due to the characteristics of the oomycete that has no
membrane sterols, therefore, resistant to most antimycotics.
Key words: Dermatology. Infection. Fungus.
LISTA DE QUADROS
Quadro 1. Valores referentes ao número e porcentagem (%) de equinos que
apresentavam feridas grandes (> 25 cm2) e feridas pequenas (< 25
cm2), submetidos à técnica de perfusão regional intravenosa do
membro com anfotericina B e DMSO e de equinos do grupo controle... 63
Quadro 2. Discriminação da localização anatômica, tempo de evolução e
dimensões da ferida (cm2) na primeira avaliação (D0) dos equinos
submetidos à técnica de perfusão regional intravenosa do membro
com anfotericina B e DMSO e nos equinos do grupo controle. .............. 64
LISTA DE FIGURAS
Figura 1. Ilustração do progresso da condição corporal de equinos do grupo
tratado com anfotericina B e DMSO, aplicada pela técnica de perfusão
regional intravenosa do membro, entre a primeira (D0) e a terceira
semana (D21) avaliação........................................................................... 60
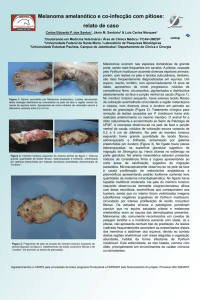
Figura 2. A - Derme, área focal de necrose (Kunkers) e dermatite eosinofilica,
neutrofílica e tecido de granulação H&E 10x. B - área de central de
necrose com imagens (negativas) não coradas, tubulares, ramificadas
e irregulares (hifas) H&E 40x. C - Hifas irregulares e ramificadas no
centro ou na periferia dos “kunkers”, Gömori (GMS) 40x. D imunomarcação positiva com uso do kit (LSAB - DAKO) para Pythium
insidiosum 40x. ......................................................................................... 62
Figura 3. Ilustração da evolução da cicatrização de feridas de pitiose de eqüinos
tratados com aplicação única de anfotericina B e DMSO, pela técnica
de perfusão regional intravenosa do membro, no primeiro dia (D0) e
nos dias 7. ................................................................................................ 65
Figura 4. Ilustração da evolução da cicatrização de feridas de pitiose de equinos
tratados com anfotericina B e DMSO, aplicada pela técnica de
perfusão regional intravenosa do membro, na primeira avaliação (D0)
e no último dia (D60) do período pós-operatório. ..................................... 66
SUMÁRIO
1 INTRODUÇÃO ....................................................................................................... 13
2 ARTIGO 1 - REVISÃO DA LITERATURA ............................................................. 15
2.1 HISTÓRICO ........................................................................................................ 15
2.2 ETIOLOGIA ......................................................................................................... 16
2.3 EPIDEMIOLOGIA ................................................................................................ 17
2.4 PATOGENIA ....................................................................................................... 19
2.5 SINAIS CLÍNICOS ............................................................................................... 21
2.6 DIAGNÓSTICO ................................................................................................... 23
2.6.1 Diagnóstico Laboratorial da Pitiose Equina ................................................ 23
2.6.2 Imuno-histoquímica ....................................................................................... 24
2.6.3 Sorologia ......................................................................................................... 24
2.6.4 Isolamento ...................................................................................................... 25
2.7 TRATAMENTO.................................................................................................... 26
2.7.1 Imunoterapia ................................................................................................... 32
3 CONCLUSÃO ........................................................................................................ 35
REFERÊNCIAS ......................................................................................................... 36
4 ARTIGO 2 .............................................................................................................. 48
TRATAMENTO DA PITIOSE EM MEMBROS DE EQUINOS POR MEIO DE
PERFUSÃO REGIONAL INTRAVENOSA COM ANFOTERICINA B ASSOCIADA
AO DIMETILSULFÓXIDO ......................................................................................... 49
4.1 INTRODUÇÃO .................................................................................................... 51
5 MATERIAL E MÉTODOS ...................................................................................... 54
5.1 AVALIAÇÃO CLÍNICA ......................................................................................... 54
5.2 AVALIAÇÃO HISTOPATOLÓGICA ..................................................................... 54
5.3 TÉCNICA DE IMUNO-HISTOQUÍMICA .............................................................. 55
5.4 PROCEDIMENTO EXPERIMENTAL................................................................... 57
5.5 AVALIAÇÃO DAS FERIDAS ............................................................................... 58
6 RESULTADOS ....................................................................................................... 60
6.1 AVALIAÇÃO DA DOSE DE ANFOTERICINA B .................................................. 66
7 DISCUSSÃO .......................................................................................................... 67
8 CONCLUSÕES ...................................................................................................... 72
REFERÊNCIAS ......................................................................................................... 73
APÊNDICE ................................................................................................................ 77
APÊNDIA A - DISCRIMINAÇÃO DAS CIDADES DE ORIGEM, RAÇA, SEXO,
IDADE E PESO (KG) DOS EQUINOS QUE FORAM TRATADOS COM
ANFOTERICINA B E DMSO, APLICADA PELA TÉCNICA DE PERFUSÃO
REGIONAL INTRAVENOSA DO MEMBRO E DOS EQUINOS DO GRUPO
CONTROLE .............................................................................................................. 78
13
1 INTRODUÇÃO
A
zigomicose
denominada
Pitiose
é
uma
doença
multissistêmica,
piogranulomatosa causada pelo oomiceto Pythium insidiosum e que afeta equinos,
caninos, bovinos, ovinos, felinos e humanos (DE COCK et al., 1987; LEAL et al.,
2001b; SANTURIO et al., 1998).
A pitiose ocorre em regiões de clima tropical, subtropical e temperado, em
áreas alagadiças ou com histórico de inundação e temperaturas médias de 25ºC
(ALEXOPOULOS; MIMS; BLACKWELL, 1996). No mundo, o Pantanal brasileiro é o
local de maior incidência de pitiose equina, apesar de não se ter dados completos
sobre a incidência da pitiose no Brasil, esta representa um grande problema na
criação de equinos (LEAL et al., 2001).
Nas porções norte e sul do Pantanal, onde a doença tem maior ocorrência e
é conhecida como "ferida-brava" ou "ferida-da-moda" (CARVALHO et al., 1984;
MEIRELES et al., 1993), certamente a enfermidade causa perdas econômicas de
grandes proporções na equinocultura (SANTURIO et al., 2004). Atribui-se estas
observações, principalmente, pelo fato do pantanal ser uma planície inundável de
aproximadamente 140.000 km², situada na região centro-oeste do Brasil e figura
como a maior área de planície inundável do mundo, fatores estes que predispõem
há ocorrência da pitiose (SILVA; ABDON, 1998).
Nesta região a enfermidade vem sendo estudada devido pantanal MatoGrossense ser uma das regiões predominantes para a ocorrência de pitiose no
Brasil, devido seu clima quente e úmido particular e a existência de muitas lagoas,
lagos, pântanos e áreas alagadas proporcionando um ambiente favorável para o P.
insidiosum (CHAFFIN; SCHUMACHER; McMULLAN, 1995).
No Pantanal Sul-Mato-Grossense, a maioria dos casos de pitiose equina é
registrada entre os meses de fevereiro e maio (verão-outono), período que
corresponde ao ápice das cheias, acarretando prejuízos significativos, direta ou
indiretamente. O prejuízo provocado pela pitiose é bem documentado e inclui
disfunção, custos de tratamento e mortes (FREY JR et al., 2007; LEAL et al., 2001;
MENDOZA; ALFARO, 1986).
Estudos mais recentes visaram métodos de tratamento adequado e de
eficácia satisfatória, pois os métodos convencionais não produzem bons resultados.
Nesta casuística, foi demonstrado que, em associação com a excisão cirúrgica do
14
tecido de granulação, a infecção causada por P. insidiosum, utilizando perfusão
intravenosa regional de 50 mg de anfotericina B foi uma técnica eficaz para o
tratamento da pitiose em membros de equinos, com efeitos colaterais mínimos
(DÓRIA et al., 2012).
Um dos principais fatores para o insucesso no tratamento é o diagnóstico
tardio, pois com lesões iniciais consegue-se promover terapêutica adequada (LEAL
et al., 2001). Do contrário, os animais enfermos evoluem, por alterações
consequentes, para a morte ou são encaminhados para eutanásia.
O presente estudo será dividido em dois capítulos. O capítulo 1 tem por
objetivo fazer uma revisão da epidemiologia, sinais clínicos, patologia, formas de
controle e profilaxia da pitiose equina no Brasil. O capítulo 2 trata-se de um estudo
do tratamento cirúrgico e farmacológico das lesões de membros de equinos com
diagnóstico de pitiose, que ingressaram ao Hospital Veterinário da Universidade de
Cuiabá (UNIC), Cuiabá, MT.
15
2 ARTIGO 1 - REVISÃO DA LITERATURA
2.1 HISTÓRICO
Os primeiros relatos de pitiose foram creditados a Smith, em 1884 e Drouin,
em 1896, quando comentaram a presença de hifas em lesões de equinos. A primeira
evidência definitiva da causa ser um fungo foi feita por Fish, em 1895 quando
descreveu hifas com características de um ficomiceto em cortes histológicos de
lesões cutâneas, em equinos, na Flórida.
O agente da pitiose Pythium insidiosum é um pseudo-fungo. O primeiro
isolamento desse organismo filamentoso foi realizado em 1901 por Haan e
Hoogkamer, a partir de granulomas subcutâneos em equinos. Esses autores
chamaram a doença de "hyphomycoses destruens", porém não conseguiram
classificar o agente. Somente em 1961 o agente foi identificado, recebendo o nome
de Hyphomyces destruens (MENDOZA et al., 1996).
Austwick e Copland (AVEMANN, 1974) verificaram a capacidade desse
agente em produzir zoósporos biflagelados, permitindo classificá-lo como um fungo
da família Pythiaceae, ordem Peronosporales, que deveria ser incluído no gênero
Pythium. No entanto, a denominação Hyphomyces destruens continuou sendo
utilizada nas descrições da doença (MCMULLAN et al.,1977; MURRAY et al.,1978).
Ichitani e Amemiya (1980) compararam as características reprodutivas de
diferentes espécies de Pythium e classificaram um isolado de equino como Pythium
gracile (MIDDLETON, 1943). De Cock et al. (1987) analisaram isolados de equinos,
bovinos, cães e humanos e concluíram que se tratava do mesmo organismo, o qual
foi denominado Pythium insidiosum e que essa nova espécie era igual as
anteriormente descritas (Pythium sp - Austwick e Copland; Pythium gracile – Ichitani
e Amemiya e Hyphomyces destruens – Bridges e Emmons).
Embora o nome do agente tenha sido estabelecido, a sua classificação
taxonômica continuou sendo discutida nos anos seguintes. Segundo De Cock et al.
(1987), os oomicetos são seres eucariotas produtores de zoósporos biflagelos,
característica comum ao Pythium insidiosum, incluindo-o na ordem Peronospolares,
filo Oomycota e reino Protista. Mendoza et al. (1996), apresentaram o P. insidiosum
como um organismo do reino Chromista, filo Pseudo-fungi, classe Oomycetes,
ordem Pythiales, e família Pythiaceae. Entretanto, estudos detalhados sobre a
16
classificação dos fungos dividiram os organismos anteriormente classificados como
fungos em três reinos: Fungi, Stramenopila e Protista (ALEXOPOULOS; MIMS;
BLACKWELL, 1996). Baseado nessa classificação, o agente etiológico da pitiose
pertence ao reino Stramenopila, filo Oomycota, família Pythiaceae, gênero Pythium e
espécie P. insidiosum.
2.2 ETIOLOGIA
As zigomicoses constituem um conjunto de afecções micóticas de estreita
semelhança anatomopatológica, que acomete a pele e o tecido subcutâneo, o trato
digestório e o respiratório, especialmente de equinos (BIAVA et al., 2007;
RODRIGUES e LUVIZOTTO, 2000). Constituem ainda um grupo complexo de
doenças piogranulomatosas que inclui a pitiose, a conidiobolomicose e a
basidiobolomicose causadas pelo Pythium insidiosum, Conidiobolus coronatus e
Basidiobolus haptosporus (Basidiobolus ranarum), respectivamente (BIAVA et al.,
2007; MENDOZA et al., 1996; UBIALAI et al., 2012).
O gênero P. insidiosum possuem reprodução assexuada, reprodução
sexuada oogâmica, parede celular composta de ß-glucanos, celulose e hidroxipolina,
talo diplóide, mitocôndria com crista tubular e características moleculares e
bioquímicas próprias, destacando-se uma rota alternativa para a síntese de lisina
(MOORE-LANDECKER, 1996), particularidades que os diferenciam dos fungos
verdadeiros.
A ausência de componentes esteróides na membrana plasmáticas dos
oomicetos tem importância clínica porque as maiorias das drogas antifúngicas atuam
na molécula do ergosterol (SANTURIO et al., 2004).
O P. insidiosum é a única espécie do gênero que além de plantas pode
infectar animais mamíferos, incluindo o homem. A infecção no homem e em animais,
no entanto, é casual e não tem importância na manutenção do agente no ambiente.
Nos animais há somente crescimento vegetativo das hifas, sem produção das
formas propagativas infectantes (oósporos e zoósporos). Também não há relatos de
transmissão entre os animais e o homem (MENDOZA et al., 1993).
17
2.3 EPIDEMIOLOGIA
A pitiose é considerada uma doença emergente (VANITTANAKOM et al.,
2004), caracterizada como uma enfermidade crônica, que acometi animais de todas
as idades, sexo e raças. Tem ocorrência cosmopolita em áreas temperadas,
tropicais e subtropicais, com relatos na Argentina, Austrália, Brasil, Colômbia, Costa
Rica, Estados Unidos, Haiti, Índia, Indonésia, Japão, Nova Zelândia, Papuá Nova
Guiné, Tailândia (CHAFFIN; SCHUMACHER; McMULLAN, 1995; FOIL, 1996;
MENDOZA et al., 1996, MENDONZA; NEWTON 2005), Venezuela (PÉREZ et al.,
2005) e África (RIVIERRE et al., 2005) afetando diversas espécies domésticas,
selvagens e também humanos (MARQUES et al., 2006).
Das espécies domésticas a maioria dos casos corresponde a lesões
cutâneas em equinos (SANTURIO et al., 2006) porém vem sendo registrados casos
em bovinos (GABRIEL et al. 2008, GRECCO et al., 2009), ovinos (TABOSA et al.,
2004) e caninos (PEREIRA et al., 2010).
Nos últimos anos, é crescente também o número de relatos de Pitiose em
espécies não-domésticas como urso, jaguar, camelo e tigre (CAMUS et al., 2004;
GROOTERS, 2003).
No Brasil, o primeiro relato, em equinos, ocorreu no Rio Grande do Sul, por
Santos e Londero (1974), apartir desse momento, os relatos de Pitiose no país,
somam em estados como o Rio Grande do Sul, Paraná, Mato Grosso do Sul, Mato
Grosso, Pará, São Paulo, Rio de Janeiro, Minas Gerais, Bahia, Paraíba e
Pernambuco (CARVALHO et al., 1984; FREY JR et al., 2007; HEADLEY; ARRUDA,
2004; LEAL et al., 2001a,b; LUVIZARI et al., 2002; MEIRELES et al., 1993; REIS JR;
NOGUEIRA, 2002; SALLIS et al., 2003; SANTOS et al., 1987; TABOSA et al., 1999;
TÚRY; COROA, 1997) e em bezerros do Pantanal mato - grossense (SANTURIO et
al., 1998).
Nas infecções pelo microorganismo P. Insidiosum não há relatos de
transmissão direta entre os animais ou entre animais e humanos (MENDONZA et al.,
1996). Comumente, os animais afetados permanecem por longos períodos em
contato com águas paradas em lagos, açudes ou locais pantanosos (CHAFIN et al.,
1995).
Portantoas condições ambientais são fundamentais para o desenvolvimento
do organismo no meio ambiente. Para a produção de zoósporos são necessárias
18
temperaturas entre 30º e 40º e o acúmulo de água em banhados e lagoas, já que a
maioria dos casos de infecção por pitiose ocorre durante ou após a estação
chuvosa, entre os meses de fevereiro e maio (verão-outono), período máximo das
cheias do Pantanal, (MILLER; CAMPBELL, 1982).
Em águas estagnadas a temperatura é variável de acordo com a
profundidade do solo, com a irradiação solar, com a nebulosidade, com a
temperatura ambiente, com a hora do dia e com a presença de ventos. Visto que a
temperatura em águas paradas é superior a do ar, tanto em dias de alta irradiação
solar como em dias nublados ou chuvosos. Além disso, a água tem capacidade de
reter calor contribuindo para que as flutuações térmicas sejam bem mais atenuadas
do que as flutuações térmicas do ar (ANGELOCCI; VILLA NOVA; 1995). Isso sugere
que mesmo que a temperatura do ambiente seja inferior a 30°C ou que tenha
variações durante as várias horas do dia, as águas onde P. insidiosum está presente
podem ter a temperatura ideal para a zoosporogênese (ANGELOCCI; VILLA NOVA;
1995). Este fato poderia explicar o aparecimento de lesões de pitiose nos meses
mais frios do ano.
Essas características epidemiológicas foram observadas no Pantanal mato grossense, onde a maioria dos casos de pitiose equina ocorrem entre os meses de
fevereiro e maio, que corresponde as estações do verão e outono, (LEAL et al.,
2001). Provavelmente, o Pantanal brasileiro seja o local de maior ocorrência e
prevalência de pitiose equina no mundo, constituindo-se planície inundável de,
aproximadamente, 140.000 km2, com população estimada em 140.000 equinos,
sendo a pitiose um problema frequente para a criação de equinos (MENDOZA et
al.,1996; SANTURIO et al., 2006ª; SILVA et al, 1995).
Situações
epidemiológicas
com
características
semelhantes
foram
observadas em alguns estudos da enfermidade, tais como na Paraíba por Tabosa et
al. (1999), ocorrendo nos meses de julho a outubro, sete a dez meses após o início
das chuvas, e por Santos et al. (1987) no Rio Grande do Sul descreveram a
ocorrência de 12 casos de pitiose equina nos meses mais quentes do ano (janeiro –
março).
Diferentes estudos de prevalência da pitiose nas espécies domésticas
apontam que a espécie equina é mais frequentemente afetada. De acordo com
Santos et al. (2011), a incidência de pitiose em equinos em seu estudo foi 57,23
vezes a observada em bovinos. Mesmo sendo exposto às mesmas condições
19
ambientais, o padrão de comportamento das espécies provavelmente influencia a
ocorrência da patologia. Equinos se mantêm mais tempo nos locais alagadiços,
quando comparados com os bovinos, os quais preferem, ou são conduzidos às
coxilhas nas situações de alagamentos. Desta forma os equinos têm maior risco de
contato com as formas infectantes do pseudo-fungo. (MENDOZA et al., 1996;
SANTURIO et al. 2006).
Embora não haja dados epidemiológicos bem definidos estima-se que a
incidência de 1% entre os aproximadamente 120 mil equinos, somente a região do
Pantanal, acarretaria em custos com a perda de animais doentes que poderiam
alcançar R$ 1.000.000,00 para o ano de 2009 (TOMICH et al., 2010). Santos et al.,
(2011d) observaram em uma população de 3205 equinos, entre 2009 e 2010, na
região do Pantanal norte, incidência de 5,88 a 28,57% de casos de pitiose, com
índices de mortalidade e letalidade (similares) variando de 40% a 100% e risco para
equinos de 12,5%.
2.4 PATOGENIA
Os zoósporos são biflagelados, procedentes de esporângios filamentosos
que são a forma de propagação do agente. O agente habita água estagnada
infectando plantas aquáticas. Reproduz-se de forma sexuada, por esporangiósporos
móveis, liberados dos esporângios, que se aderem em plantas aquáticas e/ou restos
vegetais em decomposição. Nos animais, a instalação desses oomiceto ocorre,
principalmente, em soluções de continuidade na pele (BIAVA et al., 2007;
MENDOZA et al., 1993; MILLER, 1983).
Eles são liberados periodicamente em águas pantanosas e infectam equinos
e outros mamíferos que frequentam esses locais. Os zoósporos móveis são atraídos
para o pêlo dos animais, penetram na pele através de lesão preexistentes
produzindo a enfermidade (MILLER; CAMPBELL,1982), comprovado pela análise in
vitro que evidencia a atração dos zoóporos por substâncias presentes nos pêlos e
tecidos de animais e vegetais, essas substâncias atuam com um adesivo para o
zoóporo permitindo a formação do tubo germinativo (MENDOZA et al.,1993).
Essas observações sustentaram a teoria de infecção, sugerindo que os
eqüinos em contato com água contaminada poderiam atrair os zoósporos
(MENDOZA et al., 1993; MILLER, 1983).
20
Outros autores sugeriram a possibilidade de penetração dos zoósporos
através dos folículos pilosos, baseados na detecção de hifas no interior do folículo
de bovinos infectados naturalmente ou no fato da quimiotaxia ser mais ativo na
região do pêlo encontrada dentro do folículo piloso (SANTURIO et al.,1998). Essa
observação pode questionar a necessidade de lesão na pele para que ocorra a
germinação dos zoósporos. Além disso, diferenças individuais de suscetibilidade, ao
exemplo do que ocorre em humanos (talassemia), parecem ocorrer também em
equinos.
Macroscopicamente, a lesão demonstra intensa proliferação de tecido
esbranquiçado em forma sinuosa, com ramificação com bordas escuras e repletas
internamente de material amarelado em forma de coral marinho conhecido como
“kunkers”. Apresentando ainda material necrótico friável, observado somente em
eqüinos. Ao ser pressionada a lesão, facilmente consegue-se extrair “kunkers” com
facilidade de onde foram isoladas estruturas posteriormente identificadas como P.
insidiosum. Os eqüinos com tais lesões atípicas de pitiose não apresentam
emagrecimento progressivo e, após um ano de observação as lesões permanecem
do mesmo aspecto e tamanho (CHAFFIN; SCHUMACHER; McMULLAN, 1995;
MARTINS et al., 2006; MENDONZA; AJELLO, 1996),
Microscopicamente, os kunkers são grandes massas eosinofílicas, formadas
ainda por celulares necróticos, inclusive colágenos e as hifas do P. insidiosum
localizam-se nas margens dessas estruturas. A principal manifestação clínica desse
distúrbio
é
a
eliminação
abundante
de
corrimento
serossanguinolento,
mucopurulento e filamentoso, sendo esses chamados de sanguessugas em função
de seu aspecto serpejante, cujos trajetos drenantes representam os núcleos de
necrose contendo o organismo (TABOSA et al., 1999).
Em cortes histológicos corados com coloração especial de prata, é possível
observar as hifas com paredes espessas, esparsamente septadas, irregularmente
ramificadas (normalmente em ângulo reto) e medindo de 2 a 6 um de diâmetro
(BROWN et al., 1988; CHAFFIN; SCHUMACHER; McMULLAN, 1995; MILLER;
CAMPBELL, 1984). Os achados histopatológicos variaram de tecido conjuntivo
fibroso com áreas de necrose de coagulação e focos de mineralização (sem
infiltrado eosinofílico) à granuloma eosinofílico crônico, porém sem a observação de
“kunkers” (ALLISON; GILLIS, 1990; MORTON et al., 1991; PURCELL et al., 1994).
21
2.5 SINAIS CLÍNICOS
Os equinos são os mamíferos mais atingidos pela pitiose, não havendo
predisposição pela idade, raça ou sexo. As lesões mais características são
subcutâneas, que atingem principalmente as extremidades distais dos membros e
porção ventral da parede toraco-abdominal, provavelmente devido ao contato com
águas contaminadas com zoóporos (REIS et al., 2003; SANTOS et al., 2011c;
SANTOS et al., 2011d).
As lesões podem aparecer isoladas ou múltiplas (KAUFMAN, 1990;
TABOSA et al., 1999), iniciando pequenas e com aspecto inofensivo, de forma
circular, podendo aumentar sobre uma área que estava apenas tumefeita, de
maneira ulcerativa.
Os sinais clínicos da pele caracterizam-se por lesões ulcerativas, tem forma
irregular, ramificada, com aspecto arenoso e penetram no tecido granular, dentro de
seios formados ao longo do seu trajeto. O tamanho das lesões depende do local e
duração
da
infecção
e
apresenta
secreção
serossanguinolenta,
mucossanguinolenta, hemorrágica e, às vezes, muco-purulenta e fétida, que drenam
dos tecidos piogranulomatosos e necróticos, semelhantes a corais chamadas
internacionalmente, de “kunkers”, que variam o tamanho de 2 a 10 mm de diâmetro.
A lesão alastra-se rapidamente pelos tecidos, ocasionando à formação de tecido de
granulação e hemorragias. Essa perda sanguínea pode ser suficiente para causar
anemia nos animais acometidos (KNOTTEMBELT; PASCOE, 1998; LUVIZARI et al.,
2002). Na maioria dos casos, cada animal apresenta foco único da lesão, porém,
lesões cutâneas multifocais já foram relatadas (CHAFFIN; SCHUMACHER;
McMULLAN, 1992; MILLER; CAMPBELL, 1982).
Já a pitiose intestinal apresenta como a segunda forma mais comum da
doença nos equinos e caracteriza-se por episódios de cólica devido a presença de
massas tumorais que causam a diminuição ou obstrução do lúmen intestinal. Os
dados de excisão cirúrgica e necropsia mostram ulceração intestinal e massas
nodulares que podem atingir ate 20 cm de diâmetro localizadas na parede do jejuno
(SANTURIO; FERREIRO, 2008).
A claudicação é comum entre os cavalos com lesões nos membros, além de
apresentarem prurido, dor, apatia, inapetência, perda de peso e hipoproteinemia
sendo que a claudicação é frequente em animais afetados nos membros havendo na
22
maioria das vezes necessidade de eutanásia (CHAFFIN; SCHUMACHER;
McMULLAN, 1995). O prurido e a dor levam os animais à automutilação, como
mordidas e traumas se debatendo contra objetos rígidos na tentativa de aliviar o
desconforto.
No entanto, há descrição de lesões cutâneas multifocais (SANTOS et al.,
2011c; SANTOS et al., 2011d; SANTURIO; FERREIRO, 2008), disseminação para
órgãos internos (REIS JR. et al., 2003) e casos atípicos no Pantanal brasileiro em
que os animais com pitiose apresentam emagrecimento progressivo, com lesões
deformantes recobertas com pele escurecida e espessa, mas sem a constante saída
de secreções e manutenção do aspecto e tamanho após um ano de observação
(SANTURIO; FERREIRO, 2008; SANTOS et al., 2011d).
Muitas lesões ósseas, na maioria das vezes são limitadas aos ossos
adjacentes ás lesões subcutâneas crônicas dos membros, comumente são
refratárias aos tratamentos convencionais, caracterizando-se por exostoses, áreas
de osteólise, sinais de osteomielite ao exame radiológico e presença de granulomas
eosinofílicos, além de identificação de hifas em áreas de necrose ao exame
histopatológico (POOLE; BRASHIER, 2003).
Já foram relatados casos de metástase via linfática para os pulmões e
linfonodos regionais (cervicais inferiores, inguinais e submandibulares), onde
apresentavam “kunkers”, e sendo possível o isolamento do fungo. Na grande
maioria, os linfonodos regionais encontram-se aumentados de volume, porém isso
nem sempre caracteriza metástase (GOAD, 1984; LEAL et al., 1997; MURRAY et al.,
1978).
23
2.6 DIAGNÓSTICO
2.6.1 Diagnóstico Laboratorial da Pitiose Equina
Embora
o
P.
insidiosum
possua
semelhança
estrutural
com
os
microorganismos fúngicos, acaba tendo características específicas em seu ciclo
biológico, fazendo com que a maioria dos laboratórios não disponha de estrutura
funcional correta para sua identificação. No entanto, a identificação precoce da
doença, torna-se difícil. O diagnóstico diferencial inclui habronemose, neoplasia,
tecido de granulação exuberante e granulomas fúngicos ou bacterianos (CHAFFIN;
SCHUMACHER; McMULLAN, 1992).
O isolamento do P. insidiosum pode ocorrer mediante o aspecto das
colônias e das características das hifas (BROWN et al., 1988; FISCHER et al., 1994;
HOWERTH; BROWN; CROWER, 1989; PURCELL et al., 1994). Este isolamento
requer colheita de material adequado e pode ser dificultado por contaminações
secundárias da lesão.
Na avaliação microscópica com emprego de KOH 10% (exame direto),
realizada geralmente da extração de Kunkers (massas necróticas), observa-se P.
insidiosum desenvolvendo hifas hialinas e eventualmente septadas, morfologia que
facilmente pode ser confundida com a maioria dos fungos filamentosos
(MENDONZA et al., 2009). O crescimento das hifas pode ser visto a partir de 24
horas após a incubação a 37 C, e estas se apresentam submersas no meio e com
coloração branca e hialina (GROOTERS; GEE, 2002). Uma vez que P. insidiosum
não produz estruturas reprodutivas nos meios tradicionais de cultura, a indução da
zoosporogênese (formação assexuada de zoósporo) pode ser obtida a partir do
cultivo de P. insidiosum em folhas de grama estéreis que posteriormente são
transferidas para uma solução de sais minerais, que deve incluir (PEREIRA et al.,
2008).
Na histologia observa inflamação granulomatosa e granulocítica, os
“kunkers” de tamanho variado, forma circular e contonos irregulares, contendo hifas,
colágeno, arteríolas e infiltrado inflamatório principalmente eosinofílico.
Já nos casos de pitiose equina que o animal não se encontra perto dos
laboratórios de referência, o envio de soro para realização de ELISA, de Kunkers e
tecidos para cultivo microbiológico e análise histopatológica estão caracterizadas
24
como as principais formas utilizadas de diagnóstico.
2.6.2 Imuno-histoquímica
O diagnóstico precoce da pitiose pode ser feito com métodos imunohistoquímica (TROST et al., 2009) ou pelos testes sorológicos para detecção de
anticorpos, como imunodifusão em gel de Agar, Enzyme – Linked Immunosorbent
Assay (ELISA), Western blot, aglutinação em látex e testes imunocromatógráficos
(BOTTON et al., 2011).
A técnica de imuno-histoquímica foi descrita pela primeira vez em 1988,
desde então está sendo utilizada por vários autores, com inúmeras vantagens, pois
possibilita a diferenciação do P. insidiosum de outros fungos, pela utilização de
coloração seletiva com a metodologia da peroxidase indireta, com uma alta
especificidade no diagnóstico (REIS JR., NOGUEIRA, 2002; BIAVA; et al., 2007).
2.6.3 Sorologia
A utilização de técnicas sorológicas foi impulsionada por Miller e Campbell
(1982), que desenvolveram as técnicas de imunodifusão em gel de ágar, fixação do
complemento e hipersensibilidade intradérmica, para o diagnóstico e monitoramento
da resposta imunológica em eqüinos afetados. Os testes realizados em eqüinos com
pitiose clínica, demonstraram que apresenta alta sensibilidade e especificidade para
a detecção de anticorpos anti-P. insidiosum (MILLER; CAMPBELL, 1982).
Kaufman, Mendoza e Standard (1990), demonstraram a eficiência da
imunodifusão em gel de ágar para o soro-diagnóstico e diagnóstico diferencial das
entomoftoromicoses causadas por Basidiobolus ranarum e Conidiobolus coronatus
em humanos e animais, assim como para pitiose, Mendoza et al. (1997)
desenvolveram um teste de ELISA para o soro-diagnóstico de pitiose em humanos e
animais, utilizando antígeno solúvel de hifas. Os resultados indicaram que o ELISA é
eficiente para o diagnóstico da pitiose e possui especificidade semelhante à
imunodifusão em gel de ágar, porém com maior sensibilidade.
No Brasil, Rosa et al. (1999) desenvolveram um teste de ELISA para
diagnóstico da pitiose eqüina e Pinto et al. (1999) descreveram a padronização de
teste ELISA para detecção de IgG em coelhos imunizados com antígenos de P.
25
insidiosum. Um teste de “dot-blot” modificado foi desenvolvido para detecção de IgG
anti-pythium em coelhos e eqüinos (ROSA et al., 1999).
A técnica desenvolvida utilizou sistema de luminescência química para
visualização da reação, no entanto, pode ser adaptada para um sistema de
visualização direta na membrana, podendo ser utilizada como um teste de campo,
possuindo boa especificidade, sensibilidade, praticidade e baixo custo (LÜBECK et
al., 1999).
2.6.4 Isolamento
O sucesso no isolamento de P. insidiosum é alto quando as amostras de
biópsias forem armazenadas ou transportadas à temperatura ambiente, com o
acréscimo de antibióticos, entre 1 e 3 dias antes de seu processamento no
laboratório. Quando o meio de transporte da biópsia não contiver antibióticos é
melhor transportá-la a 4ºC. Estes dados sugerem que a inibição do crescimento
bacteriano, que contamina a amostra, aumenta as chances de isolamento de P.
insidiosum dos tecidos infectados (MILLER, 1983).
Os procedimentos de diagnósticos da pitiose segundo (QUINN et al., 2005),
segue os seguintes itens:
1.
A natureza e a distribuição das lesões e o histórico de acesso á água
estagnada em regiões onde a pitiose ocorre podem sugerir a doença;
2.
Os espécimes, incluído material de biópsia e amostras de lesões
cutâneas em equinos;
3.
Cortes de tecidos são usados para demonstrar formas de hifas;
4.
Técnicas de imunofluorescência ou imunoperoxidase podem ser
usadas para identificar P. insidiosum nos cortes de tecidos;
5.
Agar dextrose Sabouraud, inoculado com material das lesões, é
incubado aerobiamente a 37º C por 24 a 48 horas. As colônias, que
são planas esbranquiçadas e radiadas, podem ter até 20µm de
diâmetro após 24 horas;
6.
Critérios para identificação dos isolados: morfologia colonial, hifas
asseptadas;
7.
Identificação especifica deve ser realizada em um laboratório de
referência;
26
8.
Teste sorológicos, tais como Difusão em Ágar-gel e ELISA, tem sido
usados para diagnósticos em animais.
2.7 TRATAMENTO
A maioria dos antifúngicos não possuem uma reposta adequada no
tratamento de infecções pelo P. insidiosum, tanto em animais quanto em humanos,
sendo
considerados
ineficientes
pela
maioria
dos
autores
(FOIL,
1996;
SATHAPATAYAVONGS et al., 1989). A explicação para tal fato é inerente às
características
do
agente,
implicado pela
composição
da parede
celular,
principalmente pela ausência de algumas substâncias encontradas na constituição
dos fungos comuns, como exemplo, a ausência de quitina na parede e de esteroides
(ergosterol) na membrana celular, que são alvos pelos princípios ativos (FOIL,
1996).
Já evidenciado a dificuldade em obter êxito no tratamento, diversas
tentativas e alternativas estão sendo desenvolvidas como a utilização de
antimicótico, cirurgias e a imunoterapia (CHAFFIN; SCHUMACHER; McMULLAN,
1992; FOIL, 1996; SANTURIO et al., 2006a). Além disso, o sucesso depende de
fatores ligados ao animal e a história natural da doença, como o tamanho e
localização da lesão, o tempo de instalação, a idade e estado nutricional do animal
(MEDONZA et al., 1997).
No tratamento químico, as drogas mais utilizadas até o momento foram a
anfotericina B, cetoconazole, miconazole, fluconazole e itraconazole, além dos
compostos iodínicos como iodeto de potássio e sódio (SHENEP et al., 1998). Não
observando resultados satisfatórios.
Em estudos realizados demonstrando a eficácia dos medicamentos para o
tratamento observaram que a anfotericina B não obteve atividade satisfatório, já o
fluconazol, cetoconazol e miconazol inibiram o cresimento in vitro de P. insidiosum.
Em outro teste, todos os fármacos testados (anfotericina B, flucitosina, miconazol e
griseofulvina) não inibiram o crescimento do oomiceto, porém, o itraconazol
apresentou atividade moderada, e apenas a terbinafina foi ativa, entretanto, a
associação deste dois obteve efeito sinérgivo e eficaz em infecção facial no homem
(SEKHNON; PADHYE; GARG, 1992).
Uma terapia complementar importante é a administração sistêmica de
27
antimicrobianos, porém a administração local e regional permite atingir picos maiores
de concentrações, muito superiores à administração sistêmica e além de oferecer
vantagens como: maior segurança de que o antimicrobiano alcance concentrações
terapêuticas no local de infecção; concentrações do antimicrobiano, locais e
regionais, superiores à concentração inibitória mínima, o que reduz o aparecimento
de resistência emergente; diminuição ou eliminação do risco de desenvolvimento de
efeitos adversos sistêmicos, como a nefrotoxicidade, a ototoxicidade e a
neurotoxicidade e custo econômico reduzido, o que possibilita a utilização de
fármacos onerosos em animais de grande porte, como os equinos (BERTONE;
CAPRILE; DAVIS, 1990). O grande determinante para uma resposta clínica à terapia
com antimicrobianos é que a concentração inibitória mínima deste fármaco seja
atingida no tecido infectado. Dessa forma, os tecidos infeccionados apresentam,
normalmente, trombose vascular e isquemia, limitando a entrega dos antibióticos
sistêmicos aos tecidos infectados, em concentrações suficientes para efeito
bactericida (McILWRAITH, 1983). Já a perfusão regional é uma técnica que produz
maiores concentrações de antimicrobianos nas porções distais dos membros
quando comparada à administração sistêmica (BUTT et al., 2001).
Existe algumas técnicas para a administração local ou regional de
medicamentos,
como:
a
administração
intra-articular,
os
implantes
de
polimetilmetacrilato (PMMA) ou de polímeros biodegradáveis impregnados com
antibióticos, as bombas de infusão e a perfusão regional intraóssea e intravenosa
(ERRICO et al., 2008; GILLIAM et al., 2008; MARTÍNEZ, 2004; WERNER; HARDY;
BERTONE, 2003).
Dessas técnicas a de escolha é a perfusão regional, sendo de fácil
realização e baixo custo, onde promove a difusão local do medicamento aos tecidos,
pelo sistema venoso regional, utilizando-se de uma veia superficial. Para a
realização desta técnica, um garrote (torniquete) é colocado proximal ao local de
infecção (ou lesão) e um antimicrobiano é injetado, sob pressão, no sistema venoso,
de forma que a pressão utilizada durante a infusão intravenosa do fármaco resulte
em difusão do antibiótico ao tecido afetado (BUTT et al., 2001; GAGNON et al.,
1994; MURPHEY; SANTSCHI; PAPICH, 1994; MURPHEY; SANTSCHI; PAPICH,
1999).
Muitos estudos buscam a dose apropriada do fármaco, melhor volume de
administração, o intervalo apropriado entre as perfusões e o número de perfusões
28
necessárias para conter condições sépticas nas porções distais dos membros de
equinos. Já foi demonstrado que doses inadequadas podem, em excesso, promover
necrose de tecidos moles na região perfundida (SANTSCHI; ADAMS; MURPHEY,
1998). Da mesma forma, não existem dados informando o volume de perfusão ideal
para que se alcance a completa difusão do fármaco no tecido afetado.
Presumivelmente, o volume a ser infundido deve estar correlacionado com o
tamanho do membro (BUTT et al., 2001).
Whitehair et al. (1992c) demonstraram em seus estudos que a realização da
perfusão regional do membro, em equinos adultos, com um grama de gentamicina
promoveu a concentração de 221,2 ± 71,4 µg/mL deste fármaco no líquido sinovial,
24 horas após o procedimento e que quatro administrações de 2,2 mg/kg, a cada
seis 31 horas, via intravenosa, deste mesmo antibiótico, promoveu a concentração
de apenas de 7,6 ± 1,6 µg/mL, intra-articular. Atualmente, há pesquisas que
comprovam que a técnica de perfusão regional do membro de equinos com
antibióticos, como gentamicina, ceftiofur, amicacina, vancomicina e enrofloxacina
promove concentrações ósseas, intra-articulares, peri-articulares e nos tecidos
perfundidos pelo fármaco, várias vezes maiores que a concentração inibitória
mínima dos patógenos, durante várias horas (ERRICO et al., 2008; GILLIAM et al.,
2008; MARTÍNEZ, 2004; MURPHEY; SANTISCHI; PAPICH, 1999; PILLE et al.,
2005; WERNER; HARDY; BERTONE, 2003).
A perfusão regional tem sido considerada mais eficaz que a administração
sistêmica para o tratamento de artrite infecciosa e osteomielite (KETTNER;
PARKER; WATROUS, 2003; WHITEHAIR et al., 1992a,b,c), permitindo a eliminação
de infecções resistentes à terapia convencional e sua aplicação, em combinação
com a antibioticoterapia sistêmica, incrementa as taxas de sobrevivência até valores
maiores que 70% (FINSTERBUSH; ARGAMAN; SACKS, 1970; PALMER; HOGAN,
1999; SANTSCHI; ADAMS; MURPHEY, 1998).
Outras afecções dos equinos que tem sido tratadas com resultados
satisfatórios são a laminite séptica, a osteíte séptica da falange distal e dos ossos
sesamoideos proximais, a artrite séptica das articulações dos dedos, a tenossinovite
séptica, a bursite séptica do sesamóide distal e feridas no casco (SANTSCHI;
ADAMS; MURPHEY, 1998). Os ossos da porção isolada pelo torniquete também
são perfundidos e, neles, a concentração do antibiótico também é elevada
(BERTONE, 2003).
29
A anfotericina B é um antimicótico pertencente ao grupo dos antibióticos
macrolídeos poliênicos, seu nome deriva da característica anfotérica de sua
estrutura molecular, formando tanto sais solúveis em meio ácido como em meio
básico
(ASHER;
SCHURARTZMAN,
1977).
Produzido
naturalmente
pelo
actinomiceto Streptomyces nodosus cujo mecanismo de ação se baseia na ligação
com os esteróis da membrana celular, provocando alteração funcional com saída de
metabólitos essenciais, nucleotídeos e proteínas, levando à morte celular
(RICHARDSON; WARNOCK, 1993; SANDE; MANDELL, 1987). Foi isolada em
meados de 1955 (GOLD; STOUT; PAGANO, 1956; VANDEPUTTE; WACHTEL;
STILLER, 1956) e, desde então, apenas poucos agentes com ação antimicótica
foram descobertos e tornaram-se viáveis para o tratamento das micoses sistêmicas.
A atividade da anfotericia B é máxima na faixa de pH 6,0 a 7,5 e a ação
pode ser fungistática ou fungicida, dependendo da concentração sérica e tecidual do
antimicótico e da suscetibilidade do patógeno (FILIPPIN; SOUZA, 2006). No final
dos anos 50, em 1965, a anfotericina B foi aprovado pela United States Food and
Drug Administration (U.S. FDA) como o primeiro agente antimicótico (WU, 1994;
DISMUKES, 2000).
A anfotericina B possui atividade contra a maioria das espécies de Candida
spp (BURGESS et al., 2000; CLANCY; NGUYEN, 1999; DAVEY et al., 1998;
PFALLER et al., 2002), fungos filamentosos, incluindo o Aspergillus fumigatus,
Aspergillus flavus, Fusarium oxysporum, Fusarium solani, Rhizopus arrhizuz e
Paracoccidioides brasiliensis (HAHN; HAMDAN, 2000).
A anfotericina B também possui atividade contra Histoplasma capsulatum
(GONZALES et al., 2000; LI et al., 2000), Cryptococcus neoformans (DAVEY et al.,
1998), Coccidioides immits e Blastomyces dermatitidis (LI et al., 2000). Sua atividade
foi considerada limitada contra algumas cepas de Fusarium spp (ESPINELINGROFF et al., 1997). Cepas de Leishmania (Viannia) braziliensis também foram
suscetíveis a ação da anfotericina B, sendo também empregada na terapia de
leishmaniose visceral (DAVIDSON et al., 1991; DURAND et al., 1998) e
mucocutânea (AMATO et al., 2000).
A anfotericina B é pouco solúvel na maioria dos solventes, com exceção do
dimetilsulfóxido (DMSO) e da dimetilformamida, é praticamente insolúvel em
soluções aquosas de pH neutro (LEGRAND et al., 1992). Sendo assim interage
especificamente com o ergosterol, esteróide constituinte exclusivo da parede celular
30
fúngica, visto que muitos dos efeitos tóxicos que lhe são atribuídos são resultados
da sua capacidade em ligar-se ao colesterol e outros constituintes da membrana
celular de mamíferos (BOLARD; JOLY; YENI, 1993; HUANG et al., 2002; MORIBE;
MARUYAMA; IWATSURU, 1999; WHITE; PETERSON; HARTSEL, 1989). Do ponto
de vista bioquímico, a resistência aos antibióticos poliênicos poderia estar associada
ao aumento ou diminuição dos esteróides da membrana, especialmente ergosterol e
seus precursores.
Na ação da anfotericina B existem mudanças nas propriedades de
leucócitos, como na inibição da quimiotaxia (BERNAUDIN et al., 1987), na produção
de
anticorpos
(BOGGS;
CHANG;
GOUNDALKAR,1991),
nas
propriedades
funcionais dos leucócitos polimorfonucleares (PMN) (JULLIEN et al., 1991), na
diminuição significativa da fagocitose e na destruição de Candida albicans
(PALLISTER; WARNOCK, 1989), quando altas doses de anfotericina B foram
utilizadas (BERNAUDIN et al., 1987).
Várias são as reações adversas agudas da anfotericina B, no homem, são:
febre, calafrios (MORA-DUARTE et al., 2002), tremores, náusea (NUCCI et al.,
1999), vômitos e dor de cabeça (WALSH et al., 1999) e frequentemente, estão
relacionados à infusão intravenosa. Hipocalemia, hipernatremia, diurese aumentada
(GERBAUD et al., 2003), hipomagnesemia, disfunção renal e efeitos tóxicos sobre a
medula óssea (anemia, leucopenia e trombocitopenia) estão associados com
administrações repetidas (SCHÖFFSKI et al., 1998).
O tratamento sistêmico com anfotericina B quase sempre resulta em algum
grau de disfunção renal, total (MORA-DUARTE et al., 2002). Efeitos neurotóxicos
são raros (RACIS et al., 1990), a cardiotoxidade foi descrita (CRAVEN;
GREMILLION, 1985; SCHÖFFSKI et al., 1998).
O antibióticos quando manipulados de forma correta, possuem uma efeito de
cura excelente. Até agora, a anfotericina B constitui a base terapêutica das infecções
fúngicas graves (FILIPPIN; SOUZA, 2006).
O tratamento cirúrgico apresenta bons resultados em lesões pequenas e
superficiais, nas quais seja possível a retirada de toda área afetada, em lesões
maiores é necessário associar a administração de medicamentos, porém a
recorrência é comum (MILLER, 1981).
A excisão cirúrgica deve atingir as bordas da pele, ao redor da região
ulcerada, que, aparentemente, encontra-se íntegra. Em muitos dos casos ocorrem
31
hemorragias que são contidas por cauterização, ligadura dos vasos ou bandagens
compressivas (BIAVA et al., 2007).
De acordo com alguns autores, é importante a associação da excisão
cirúrgica com medicamento, como observado por Gonzales et al. (1979) e Chaffin,
Schumacher e McMullan (1992) que o o iodeto de potássio é mais eficiente quando
utilizado após a extirpação cirúrgica do granuloma.
Dória, Freitas e Linardi (2012) descrevem casos de perfusão regional com
Anfotericina B (50 mg) nos membros de eqüinos, em uma ou duas aplicações,
associada à remoção cirúrgica, promove a remissão da infecção por Pythium
insidiosum, embora isso causou inflamação local na administração local em alguns
cavalos. Os efeitos secundários, como a inflamação, edema e dor poderia ter sido
causado por inflamação vascular comumente induzida pelo fungo. Para minimizar
tais efeitos secundários, a Anfotericina B, foi diluído em solução de ringer com
lactato com pH neutro a infusão com poucas reações adversas sobre os tecidos
diretamente expostos ao fármaco, constituindo-se uma alternativa terapêutica, viável
e eficaz, para o tratamento de pitiose em membros de eqüinos, promovendo
cicatrização completa das feridas.
Sedrish et al. (1997) relataram o sucesso do uso de raio laser vermelho de
alumínio, neodímio e ítrio como tratamento suplementar após a remoção cirúrgica de
lesões de pitiose equina. Apesar da taxa de recidiva ser relativamente alta, a excisão
cirúrgica é a mais utilizada e a que apresenta os melhores resultados, quando
realizada o mais precocemente possível e de forma abrangente.
32
2.7.1 Imunoterapia
Atualmente, tem sido proposta a imunoterapia empregando-se culturas de
fungo fenolizadas, expostas às ondas ultrassônicas, onde as hifas são maceradas e
liofilizadas (BIAVA et al., 2007; MARIELLO; DE BOER, 2000). A imunoterapia pode
ser realizada utilizando-se vários antígenos derivados de Pythium insidiosum. Esta
modalidade terapêutica constitui uma alternativa concreta para o controle da doença
e tem apresentado resultados promissores (BIAVA et al., 2007; LEAL et al., 2001b;
MILLER, 1981). Porém, o diagnóstico precoce e a intervenção cirúrgica, associado
ao tratamento imunoterápico, são fundamentais para a eficácia do tratamento
(MENDOZA; HERMANDEZ; AJELLO, 1993).
Uma alternativa para o tratamento da pitiose eqüina foi proposto por Miller,
em 1981, que desenvolveu um imunoterápico a partir de culturas do próprio agente
(hifas). Monteiro (1999) testou um imunobiológico produzido a partir de culturas do
Pythium insidiosum, baseando-se na metodologia descrita por Miller (1981), obtendo
índices de cura entre 50% e 83,3%.
Nas décadas de 80 e 90, vários autores utilizaram a imunoterapia. Mendoza
e Alfaro (1986) utilizaram o sobrenadante das culturas como antígeno e obtiveram
recuperação de 3 entre 5 animais tratados. Mendoza, Hermandez e Ajello (1993)
compararam vacinas produzidas com massa celular e com antígeno solúvel
concentrado,
em
71
eqüinos
afetados,
obtendo
60%
e
70%
de
cura,
respectivamente.
Segundo Mendoza, Hermandez e Ajello (1993), o soro de eqüinos
infectados, testado pelo immunoblot, reagiu contra três proteínas (28, 30 e 32 kDa)
imunodominantes e amostras de soro eqüino, obtidas um ano após a cura pela
imunoterapia, também apresentaram anticorpos contra esses três antígenos.
Estudos recentes com Western immunoblot sugerem a presença de cinco
antígenos imunodominantes no P. insidiosum e avaliação de soro eqüino pré e póstratamento (com imunoterápico) não revelou alterações no perfil de imunoglobulinas
G durante a imunoterapia. Isso permite um questionamento sobre a real importância
desses antígenos na cura dos animais (LEAL et al., 1997).
Mendoza, Ajello e McGinnis (1996) acredita que os mecanismos envolvidos
na cura pela imunoterapia, baseiam-se principalmente na resposta celular. Isto é
sustentado pelas alterações teciduais após início da imunoterapia, com mudança de
33
inflamação eosinofílica no início para uma resposta mononuclear, mediada por
macrófagos e linfócitos T. Os autores acreditam que os antígenos presentes no
imunógeno induziriam esta alteração no padrão inflamatório, culminando com a cura
dos animais. Entretanto, Newton e Ross (1993) verificaram que o nível de anticorpos
anti-Pythium aumenta em eqüinos doentes submetidos à imunoterapia. De acordo
com os autores, o aumento do nível de anticorpos auxiliaria na cura.
Todos os animais apresentaram reação inflamatória moderada a severa no
local da injeção subcutânea da vacina e formação de abscesso estéril em 30% dos
casos. 7 a 10 dias após a primeira injeção do imunoterápico os animais
apresentaram redução do prurido, drenagem na superfície da lesão, expulsão dos
“kunkers” e fibrose dos granulomas. Na Costa Rica, com um imunobiológico obtido a
partir do sobrenadante da cultura visando diminuir a reação no local de aplicação
três de cinco animais foram curados.
Duas características dos imunoterápicos produzidos até então; necessidade
de serem mantidos a 4º C e tempo de armazenagem relativamente curto,
praticamente impediam seu uso no Pantanal devido as condições inerentes a região.
Para viabilizar o uso da imunoterapia no tratamento da pitiose eqüina no Pantanal foi
produzido, a partir de culturas de isolados do agente, um imunoterápico liofilizado
que possibilitasse armazenagem por um período longo em temperatura ambiente
(ALEXOPOULOS; MIMS; BLACKWELL, 1996).
Entre os anos de 2001 e 2006 mais de 2800 doses do imunoterápico tem
sido utilizada em 18 estados brasileiros localizados nas regiões Sul, Sudeste, Centro
Oeste, Norte e Nordeste (TRISCOTT; WEEDON; CABANA, 1993).
Exceto em algumas regiões, como no Pantanal, onde a doença é mais
prevalente e os veterinários e mesmo os proprietários estão familiarizados com a
doença, de modo geral, as solicitações do imunoterápico é realizada após o
insucesso com outras abordagens terapêuticas. A aplicação do imunoterápico
baseada muitas vezes apenas no diagnóstico clínico não conclusivo e o não
acompanhamento dos casos, contudo, não permite avaliar a eficiência do
imunoterápico nas diferentes regiões do país (THITITHANYANONT et al., 1998).
O prognóstico da pitiose, em equinos, depende do comprometimento de
estruturas adjacentes à ferida, como tendões, articulações, fáscias e tecido ósseo,
além da linfadenopatia regional ser também frequente, proporcionando a
disseminação do agente a regiões distantes como trato gastrintestinal e pulmões
34
(BIAVA et al., 2007; RODRIGUES; LUVIZOTTO, 2000). A evolução é rápida, pois,
devido ao prurido, os animais dilaceram a ferida, causando sangramento profuso,
levando ao emagrecimento e debilidade orgânica (BIAVA et al., 2007; LEAL et al.,
2001a).
35
3 CONCLUSÃO
Com base na revisão de literatura realizada, conclui-se que novas terapias
alternativas devem ser estudadas, sendo assim conhecer as características do
agente em questão é fundamental para diagnóstico da doença. Embora exista
diferentes técnicas para o tratamento da pitiose em equinos, atualmente poucos
resultados satisfatórios são descritos no curso da doença.
36
REFERÊNCIAS
ABRAHAMSEN, E. et al. Tourniquet-induced hypertension in a horse. Journal of
American Veterinary Medical Association, v.194, p.386-8, 1989.
ALEXOPOULOS, C. J.; MIMS, C. W.; BLACKWELL, M. Phylum Oomycota.
In:______. Introductory Mycology. 4. ed. New York: John Wiley & Sons, 1996, p.
683-737.
ALFARO, A. A.; MENDOZA L. Four cases of equine bone lesions caused by Pythium
insidiosum. Equine Veterinary Journal, v. 22, p. 295-7, 1990.
ALLISON, N.; GILLIS, J. P. Enteric pythiosis in a horse. Journal of the American
Veterinary Medical Association, v. 196, p. 462-4, 1990.
AMATO, V. S. et al. Mucocutaneous leishmaniasis associated with HIV infection
treated successfully with liposomal amphotericin B (AmBisome). Journal of
Antimicrobial Chemotherapy, v. 46, p. 341-2, 2000.
ANGILOCCI, E. V. Technika mistni mitrozilin na distalinch castech koncetin u skotu.
Veterinary Medicine, v. 7, p. 413-20, 1974.
ASHER, I.M.; SCHUWARTZMAN, G. Amphotericin B. Analytical Profiles of Drug
Substances, v. 6, p.1-42, 1977.
AVEMANN, M. Prüfung des von Antalovsky angegebenen Verfahrens zur
intravenösen regionalen Betäubung im Zehenbereich des Rindes auf Seine
Praktische Brauchbarkeit. 1974. (Tesis). Hannover: Tierärztliche Hochschule
Hannover, 1974.
BERNAUDIN, F. E et al. Effet in vitro de l’amphotéricine B sur le chimiotactisme des
polynucléaires et des “large granular lymphocytes” à activité “natural killer”.
Pathologie Biologie, v. 35, p. 1403-7, 1987.
BERTONE, A. L. Infectious arthritis. In: ROSS, M. W.; DYSON, S. J. Diagnosis and
Management of Lameness in the Horse. Philadelphia: W.B. Saunders, 2003. p.
598-605.
BERTONE, A. L.; CAPRILE, K. A.; DAVIS, D. M. Serum and synovial concentrations
of gentamicin administered chronically to horses with experimentally-induced
infectious arthritis. Veterinary Surgery, v. 19, p. 57, 1990.
BIAVA, J. S. et al. Zigomicose em eqüino: revisão. Revista Acadêmica, v. 5, p. 22530, 2007.
BOGGS, J. M.; CHANG, N. H.; GOUNDALKAR, A. Liposomal amphothericin B
inhibits in vitro T- lymphocyte response to antigen. Antimicrobial Agents and
Chemotherapy, v. 35, p. 79-885, 1991.
BOLARD, J.; JOLY, V.; YENI, P. Mechanism of action of amphotericin B at the
cellular level. It’s modulation by delivery system. Journal of Liposome Research. v.
3, p. 409-27, 1993.
37
BOTTON, S. A. et al. Identification of Pythium insidiosum by Nested PCR in
cutaneous lesions of brazilian horses and rabbits. Curr Microbiol., v. 62, p. 1225-9,
2011.
BRAJTBURG, J. et al. Interaction of plasma proteins andlipoproteins with
amphotericin B. Journal of Infectious Diseases, v. 149, p. 986-97, 1984.
BRAJTBURG, J. et al. Involvement of oxidative damage in erythrocyte lysis induced
by amphotericin B. Antimicrobrial Agents and Chemotherapy, v. 29, p. 172-6,
1985.
BROWN, C. C. et al. Use of imunohistochemical methods for diagnosis equine
pytiosis. American Journal of Veterinary Research, v. 49, p. 1866-8, 1988.
BROWN, C. C.; ROBERTS, E. D. Intestinal pythiosis in a horse. Australian
Veterinary Journal, v. 65, p. 88-9, 1988.
BURGESS, D. S. et al. Pharmacodynamics of fluconazole, itraconazole, and
amphotericin B against Candida albicans. Diagnostic Microbiology and Infectious
Disease, v. 36, p. 13-8, 2000.
BUTT, T. D. et al. Comparison of 2 techniques for regional antibiotic delivery to the
equine forelimb: intraosseous perfusion vs. intravenous perfusion. Canadian
Veterinary Journal, v. 42, p. 617-22, 2001.
CAMUS, A. Poliartritis y osteomielitis. Sevilla, España: Jornadas Técnicas
Veterinarias del Salón Internacional del Caballo, 2004.
CARVALHO, E. C. Q. et al. “Hyphomyces destruens”. Agente da “ferida brava”
(Hifomicose) em eqüinos do Pantanal de MT. In: CONGRESSO BRASILEIRO DE
MEDICINA VETERINÁRIA, 19., 1984. Cuiabá, Mato Grosso. Anais... Cuiabá:
Sociedade de Veterinária do Mato Grosso, 1984. p. 311.
CHAFFIN, M. K.; SCHUMACHER, J.; HOOPER, N. Multicentric cutaneous pythiosis
in a foal. Journal of the American Veterinary Medical Association, v. 201, p. 3102, 1992.
CHAFFIN, M. K.; SCHUMACHER, J.; McMULLAN, W. C. Cutaneous pythiosis in the
horse. Veterinary Clinics of North America: Equine Practice, v. 11, p. 91-103,
1995.
CLANCY, C. J.; NGUYEN, H. Correlation between in vitro susceptibility determined
by Etestand response to therapy with amphotericin B: results from a multicenter
prospectivestudy of candidemia. Antimicrobial Agents and Chemotherapy, v. 43,
p. 1289-90, 1999.
CRAVEN, P. C.; GREMILLION, D. H. Risk factors of ventricular fibrillation during
rapid amphotericin B infusion. Antimicrobial Agents and Chemotherapy, v. 27, p.
868-71, 1985.
DAVEY, K. G. et al. Comparative evaluation of FUNGITEST and broth microdilution
methods for antifungal drug susceptibility testing of Candida species and
38
Cryptococcus neoformans. Journal of Clinical Microbiology, v. 36, p. 926-30,
1998.
DAVIDSON, R. N. et al. Liposomal amphotericin B in drug-resistant visceral
leishmaniasis. Lancet, v. 337, p. 1061-2, 1991.
DE COCK, A. W. A. M. et al. Pythium insidiosum sp. The etiologic agent of pythiosis.
Journal of Clinical Microbiology, v. 25, p. 344-9, 1987.
DIETZ, O.; KEHNSCHERPER, G. Intravenöse Stauungsantibiose bei pyogenen
Infektionen der distalen Gliedmassenabschnitte des Pferdes. Der Praktische
Tierarzt, v. 8, p. 30-3, 1990.
DISMUKES, W. E. Introdution to antifungical drugs. Clinical Infectious Disease, v.
30, p. 653-7, 2000.
DÓRIA, R. G. S.; FREITAS, S. H.; LINARDI, R. L. Treatment of pythiosis in equine
limbs using intravenous regional perfusion of amphotericin B. Vet Surg., v. 41, p.
759-65, 2012.
DRUMMOND, D. C. et al. The effects of amphotericin B, fluconazole and miconazole
on neutrophil and lymphocyte function in a guinea pig model. Journal of
Antimicrobial Chemotherapy, v. 36, p. 375-84, 1995.
DURAND, R. et al. Leishmania infantum: lack of parasite resistance to amphotericin
B in a clinically resistant visceral leishmaniasis. Antimicrobial Agents and
Chemotherapy, v. 42, p. 2141-3, 1998.
ERRICO, J. A. et al. Comparison of two indirect techniques for local delivery of a high
dose of an antimicrobial in the distal portion of forelimbs of horses. American
Journal of Veterinary Research, v. 69, p. 334-42, 2008.
ESPINEL-INGROFF, A. et al. Multicenter evaluation of proposed standardized
procedure for antifungal susceptibility testing of filamentous fungi. Journal of
Clinical Microbiology, v. 35, p. 139-43, 1997.
FESSL, L.; AWAD-MASALMEH, M. Antibiotische Versorgung der distalen
Extremitäten beim Rind mittels Applikation in eine gestaute Digitalvene. Wien
tierärztl Mschr, v. 62, p. 51-3, 1975.
FILIPPIN, F. B.; SOUZA, L. C. Eficiência terapêutica das formulações lipídicas de
anfotericina B. Revista Brasileira de Ciências Farmacêuticas, v. 42, p. 167-94,
2006.
FINSTERBUSCH, A.; ARGAMAN, M.; SACKS, T. Bone joint perfusion with
antibiotics inthe treatment of experimental Staphylococcal infection in rabbits.
Journal of Bone and Joint Surgery, v. 52, p. 1424-32, 1970.
FINSTERBUSCH, A.; WEINBERG, H.; Venous perfusion of the limb with antibiotics
for osteomyelitis and other chronic infections. The Journal of Bone and Joint
Surgery, v. 54, p. 1227-34, 1972.
39
FISCHER, J. R. et al. Gastrointestinal pythiosis in Missouri dogs: eleven cases.
Journal of Veterinary Diagnostic Investigation, v. 6, p. 380-2, 1994.
FOIL, C. S. Update on pythiosis (Oomycosis). In: THE NORTH AMERICAN
VETERINARY CONFERENCE, 1996, Orlando, EUA. Proceedings... Orlando: Bayer
Animal Health, 1996. p. 57-63.
FREY JR., F. et al. Pitiose eqüina na região sul do Brasil. Revista Portuguesa de
Ciências Veterinárias, v. 102, p. 561-2, 2007.
GAGNON, H. et al. Single dose phamacokinetics of cefazolin in bovine synovial fluid
after intravenous regional injection. Journal of Veterinary Pharmacological
Therapy, v. 17, p. 31-7, 1994.
GANIS, P. et al. Polyene macrolide antibiotic amphotericin B. Crystal structure of the
N-iodo-acetyl derivative. Journal of the American Chemical Society, v. 93, p.
4560-4, 1971.
GARCIA, A.; ADLER-MOORE, J. P.; PROFFITT, R. Single-dose AmBisome
(liposomal amphotericin B) as prophylaxis for murine systemic candidiasis and
histoplasmosis. Antimicrobial Agents and Chemotherapy, v. 44, p. 2327-32, 2000.
GERBAUD, E. et al. Persistent acute tubular toxicity after switch from conventional
amphotericin B to liposomal amphotericin B (AmBisome). Journal of Antimicrobial
Chemotherapy, v. 51, p. 473-5, 2003.
GILLIAM, J. N. et al. Pharmacokinetics of florfenicol in serum and synovial fluid after
regional intravenous perfusion in the distal portion of the hind limb of adult cows.
American Journal of Veterinary Research, v. 69, p. 997-1004, 2008.
GOAD, M. E. P. Pulmonary pythiosis in a horse. Veterinary Pathology, v. 21, p.
261-2, 1984.
GOLD, N.; STOUT, H. A.; PAGANO, J. F. Amphotericin A and B, antifungal
antibiotics produced by a streptomycete I. In vivo studies. Antibiot Annu., 1956, p.
579-86.
GONZALES, C. A. et al. Endogenous endophthalmitis caused by Histoplasma
capsulatum var. capsulatum. A case report and a literature review. Ophthalmology,
v. 107, p. 725-9, 2000.
GONZÁLES, H. E. et al. Tratamiento de la ficomicosis equina subcutanea
empleando yoduro de potasio. Revista IICA, v. 14, p. 115-22, 1979.
GRAYBILI, J. R.; BOCANEGRA, R. Liposomal amphotericin B therapy of murine
histoplasmosis. Antimicrobial Agents and Chemotherapy, v. 39, p. 1885-7, 1995.
GROOTERS, A. M.; GEE, M. K. Development of a nested polymerase chain reaction
assay for the detection and identification of Pythium insidiosum. Journal of
Veterinary Internal Medicine, v. 16, p. 147-52, 2002.
HAHN, R. C.; HAMDAN, J. S. Effects of amphotericin B and three azole derivatives
40
on the lipids of yeast cells of Paracoccidioides brasiliensis. Antimicrobial Agents
and Chemotherapy, v. 44, p. 1997-2000, 2000.
HEADLEY, S. A. et al. Cutaneous pythiosis in a slaughtered horse: a case report.
Arquivo do Instituto Biológico, v. 69, p. 109-12, 2002.
HEADLEY, S. A.; ARRUDA JR., H. N. Pitiose cutânea eqüina: um relato de quatro
casos. Ciência Rural, v. 34, p. 289-92, 2004.
HOWERTH, E. W.; BROWN, C. C.; CROWER, C. Subcutaneous pythiosis in a dog.
Journal of Veterinary Diagnostic Investigation, v. 1, p. 81-3, 1989.
HUANG, W. et al. Ion channel behavior of amphotericin B in sterol-free and
cholesterol- or ergosterolcontaining supported bilayer model membranes investigated
by electrochemistry and spectroscopy. Biophysical Journal, v. 83, p. 3245-55,
2002.
JULLIÈN, S. et al. Effects of polyene antibiotics on the activation of human
polymorphonuclear leukocytes. Biochemical Pharmacology, v. 41, p. 2037-40,
1991.
KAUFMAN, L.; MENDOZA, L.; STANDARD, P. G. Immunodiffusion test for
serodiagnosing subcutaneous zygomycosis. Journal of Clinical Microbiology, v.
28, p. 1887-90, 1990.
KETTNER, N. U.; PARKER, J. E.; WATROUS, B. J. Intraosseous regional perfusion
for treatment of septic physitis in a two-week-old foal. Journal of the American
Veterinary Medical Association, v. 222, p. 346-50, 2003.
KNOTTEMBELT, D. C.; PASCOE, R. R. Afecções e distúrbios do cavalo. Barueri:
Manole, 1998. 432 p.
LAMY-FREUND, T. M. et al. Characterization and time dependence of amphotericin
B: deoxycholate aggregation by quasielastic light scattering. Journal of
Pharmaceutical Sciences, v. 80, n. 3, p. 262-6, 1991.
LEAL, A. B. M. et al. Pitiose eqüina no Pantanal brasileiro: aspectos clínicos
patológicos de casos típicos e atípicos. Pesquisa Veterinária Brasileira, v. 21, p.
151-6, 2001a.
LEAL, A. T. et al. Pitiose eqüina com envolvimento de linfonodos. In: JORNADA
INTEGRADA DE PESQUISA, EXTENSÃO E ENSINO, 4., 1997. Santa Maria, RS.
Anais...Santa Maria: Jornada Integrada de Pesquisa, Extensão e Ensino, 1997. p.
729.
LEAL, A.T. et al. Pitiose. Ciência Rural. v. 31, p. 735-43, 2001b.
LEGRAND, P. et al. Effects of aggregation and solvent on the toxicity of amphotericin
B to human erythrocytes. Antimicrobial Agents and Chemotherapy, v. 36, p. 251822, 1992.
LI, R. et al. In vitro activities of voriconazole, itraconazole, and amphotericin B
41
against Blastomyces dermatitidis, Coccidioides immitis, and Histoplasma
capsulatum. Antimicrobial Agents and Chemotherapy, v. 44, p. 1734-6, 2000.
LLOYD, K. C. et al. Synovial fluid pH, cytologic characteristics and gentamicin
concentration after intra-articular administration of the drug in an experimental model
of infectious arthritis in horses. American Journal of Veterinary Research, v. 51, p.
1363-9, 1990.
LÜBECK, I. et al. Desenvolvimento de um teste de Dot-blot modificado. In:
JORNADA ACADÊMICA INTEGRADA, 14., 1999, Santa Maria, RS. Anais... Santa
Maria: Universidade Federal de Santa Maria, 1999. p. 609.
LUVIZARI, F. H.; LEHMKUHL, R. C.; SANTOS, I. W. Pitiose eqüina no estado do
Paraná: primeiro relato de caso. Archives of Veterinary Science, v. 7, p. 99-102,
2002.
MALECAZE, F. et al. Diffusion intraoculaire des antifongiques et consequences
thérapeutiques dans lês mycoses oculaires. Journal de Mycologie Médicale, v. 2,
p. 73-6, 1992.
MARIELLO, K. A.; DE BOER, D. J. Enfermidades da pele. In: REED, S. M.; BAYLY,
W. M. Medicina interna eqüina. Rio de Janeiro: Guanabara, 2000. p. 460-1.
MARQUES, S. A. et al. Pythium insidiosum: relato do primeiro caso de infecção
humana no Brasil. Anais Brasileiro de Dermatologia, v. 81, p. 483-5, 2006.
MARTÍNEZ, L. R. Valoración de la perfusion regional de la porción distal de La
extremidade anterior del caballo con vancomicina: estudio experimental. 175 f.
Tese (Doutorado em Veterinaria) - Facultad de Veterinaria, Universidad
Complutense de Madrid, Madrid, España, 2004.
MARTÍNEZ, L. R.; CRUZ, A. M. Antimicrobial regional limb perfusion in horses.
Journal of American Veterinary Medical Association, v. 228, p. 706-12, 2006.
MARZZULLO, L.; SOUZA, L. C.; CAMPA, A. Effect of amphotericin B associated with
alipid emulsion on the oxidative burst of human polymorphonuclear leukocytes.
General Pharmacology, v. 27, p. 203-7, 1997.
McILWRAITH, C. W. Treatment of infectious arthritis. Veterinay Clinics of North
American Large Animal Practice, v. 5, p. 363-79, 1983.
McMULLAN, W. C.; JOYCE, J. R.; HANSELKA, D. V. Anfotericin B for the treatment
of localized subcutaneous phycomycosis in the horse. Journal of the American
Veterinary Medical Association, v. 170, p. 1293-7, 1977.
MEIRELES, M. C. A. et al. Cutaneous pytiosis in horses from Brazil. Mycoses, v. 36,
p. 139-42, 1993.
MENDONZA, L. et al. Serodiagnosis of human and animal pythiosis using an
enzyme-linked immunosorbent assay. Clinical and Diagnostic Laboratory
Immunology, v. 4, p. 715-8, 1997.
42
MENDONZA, L.; HERMANDEZ, F.; AJELLO, L. Life cycle of the human and animal
oomycetus pathogen Pythium insidiosum. Journal of Clinical Microbiology, v. 31,
p. 2967-73, 1993.
MENDOZA, L. et al. Evaluation of two vaccines for the treatment of pythiosis insidiosi
in horses. Mycopathologia, v. 119, p. 89-95, 2009.
MENDOZA, L.; AJELLO, L.; McGINNIS, M. R. Infections caused by the oomycetus
pathogen Pythium insidiosum. Journal of Medical Mycology, v. 6, p. 151-64, 1996.
MENDOZA, L.; ALFARO, A. A. Equine pythiosis in Costa Rica: report of 39 cases.
Mycopathologia, v. 94, p. 123-9, 1986.
MENDOZA, L.; KAUFMAN, L.; STANDARD, P. Antigenic relationship between the
animal and human pathogen Pythium insidiosum and nonpathogenic Pythium
species. Journal of Clinical Microbiology, v. 25, p. 2159–62, 2004.
MENDOZA, L.; NEWTON, J. C.Immunology and immunotherapy of the infections
caused by Pythium insidiosum. Med. My, v. 43, n. 6, p. 477-86, 2005.
MILLER, R. I. Investigations into the biology of three phycomycotic agents
pathogenic for horses in Australia. Mycopathologia, v. 81, p. 23-8, 1983.
MILLER, R. I. Treatment of equine phycomycosis by immunotherapy and surgery.
Australian Veterinary Journal, v. 57, p. 377-82, 1981.
MILLER, R. I.; CAMPBELL, R. S. F. Clinical observations on equine phycomycosis.
Australian Veterinary Journal, v. 58, p. 221-6, 1982.
MILLER, R. I.; CAMPBELL, R. S. F. The comparative pathology of equine cutaneous
phycomycosis. Veterinary Pathology, v. 21, p. 325-32, 1984.
MONTEIRO, A. B. Imunoterapia da pitiose equina: teste de eficácia de um
imunobiológico e avaliação leucocitária em animais infectados naturalmente pelo
Pythium insidiosum. 52 f. 1999. Dissertação (Mestrado em Medicina Veterinária) –
Programa de Pós-graduação em Medicina Veterinária, Universidade Federal de
Santa Maria, RS, Brasil, 1999.
MOORE, R. D.; LIETMAN, P. S.; SMITH, C. R. Clinical response to aminoglycoside
therapy: Importance of the ratio of peak concentration to minimal inhibitory
concentration. Journal of Infectious Disease, v. 155, p. 93-9, 1987.
MOORE-LANDECKER, J. Zoosporic fungi. In:______. Fundamentals of the fungi.
4. ed. New Jersey: Prentice Hall, 1996. p. 33-81.
MORA-DUARTE, J. et al. Comparison of caspofungin and amphotericin B for
invasive candidiasis. The New England Journal of Medicine, v. 347, p. 2020-9,
2002.
MORIBE, K.; MARUYAMA, K.; IWATSURU, M. Molecular localization and state of
amphotericin B in PEG liposomes. International Journal of Pharmacology, v. 193,
p. 97-106, 1999.
43
MORTON, L. D. et al. Chronic eosinophilic enteritis attributed to Pythium sp in a
horse. Veterinary Pathology, v. 28, p. 542-4, 1991.
MURPHEY, E. D.; SANTSCHI, E. M.; PAPICH, M. G. Local antibiotic perfusion of the
distal limb of horses. In: ANNUAL CONVENTION OF THE AMERICAN
ASSOCIATION OF EQUINE PRACTITIONER, 40., 1994, Vancouver, Canadá.
Proceedings… Lexington: American Association of Equine Practitioners. p. 141-2,
1994.
MURPHEY, E. D.; SANTSCHI, E. M.; PAPICH, M. G. Regional intravenous perfusion
of the distal limb of horses with amikacin sulfate. Journal of Veterinary
Pharmacological Therapy, v. 22, p. 68-77, 1999.
MURRAY, D. R. et al. Metastatic phycomycosis in a horse. Journal of the American
Veterinary Medical Association, v. 172, p. 834-6, 1978.
NEWTON, J.; SCHUMACHER, J. Pythiosis. In: ROBINSON, N. E. Current Therapy
in Equine Medicine. Philadelphia: WB. Saunderrs Company, 1997. p. 396-7.
NOBRE, M. O. et al. Drogas antifúngicas para pequenos e grandes animais. Ciência
Rural, v. 32, p. 175-84, 2002.
NUCCI, M. et al. Comparison of the toxicity of amphotericin B in 5% dextrose with
that of amphotericin B in fat emulsion in a randomized trial with cancer patients.
Antimicrobial Agents and Chemotherapy, v. 43, p. 1445-8, 1999.
PALLISTER, C. J.; WARNOCK, D. W. Effect of antimicrobial and antineoplastic
drugsalone and in combination on the phagocytic and candidacidal function of human
polymorphonuclear leucocytes. Journal of Antimicrobial Chemotherapy, v. 23, p.
87-94, 1989.
PALMER, S. E.; HOGAN, P. M. How to perform regional limb perfusion in the
standing horse. In: ANNUAL CONVENTION OF AMERICAN ASSOCIATION OF
EQUINE PRACTITIONER, 45., 1999, Albuquerque, Novo México. Proceedings…
Lexington: American Association of Equine Practitioners, 1999. p.124-7.
PEREIRA, D. I. B. et al. Zoosporogênese in vitro entre isolados do oomiceto Pythium
insidiosum. Ciência Rural, v. 38, p. 143-7, 2008.
PFALLER, M. A. et al. Trends in antifungal susceptibility of Candida spp. isolated
from pediatric and adult patients with bloodstream infections: SENTRY antimicrobial
surveillance program, 1997 to 2000. Journal of Clinical Microbiology, v. 40, p. 8526, 2002.
PILLE, F. et al. Synovial fluid and plasma concentrations of ceftiofur after regional
intranous perfusion in the horse. Veterinary Surgery, v. 34, p. 610-7, 2005.
PINTO, A. M. et al. Padronização de um teste ELISA para pitiose. In: JORNADA
ACADÊMICA INTEGRADA, 14., 1999, Santa Maria, RS. Anais... Santa Maria:
Universidade Federal de Santa Maria, 1999. p. 695.
PONCE, E.; PECHÉRE, J. C. Activity of amphotericin B and itraconazole against
44
intraphagocytic Candida albicans. European Journal of Clinical Microbiology and
Infectious Diseases, v. 9, p. 738-44, 1990.
POOLE, H. M.; BRASHIER, M. K. Equine Cutaneous Pythiosis. Compendium, v. 25,
p. 229-35, 2003.
PURCELL, K. L. et al. Jejunal obstruction caused by a Pythium insidiosum
granuloma in a mare. Journal of the American Veterinary Medical Association, v.
205, p. 337-9, 1994.
QUINN, P. J. et al. Microbiologia veterinária e doenças infecciosas. Porto Alegre:
Artmed, 2005. p. 115-130.
RACIS, S. P. et al. Comparative toxicities of amphotericin B and its monomethyl ester
derivative on glial cells in culture. Antimicrobial Agents and Chemotherapy, v. 34,
p. 1360-5, 1990.
RAMOS, H. et al. Effect of ketoconazole on lethal action of amphotericin B on
Leishmania mexicana promastigotes. Antimicrobial Agents and Chemotherapy, v.
38, p. 1079-84, 1994.
REIS JR., J. L. et al. Disseminated pythiosis in three horses. Veterinary
Microbiology, v. 96, p. 289-95, 2003.
REIS JR., L.; NOGUEIRA, R. H. G. Estudo anatomopatológico e imunoistoquímico
da pitiose em eqüinos naturalmente infectados. Arquivo Brasileiro de Medicina
Veterinária e Zootecnia, v. 54, p. 358-65, 2002.
RICHARDSON, M. D.; WARNOCK, D. W. Antifungal drugs. In:_____. Fungal
Infection: diagnosis and management. London: Blackwell, 1993. p. 17-43.
RODRIGUES, C. A.; LUVIZOTTO, M. C. R. Zigomicose e pitiose cutânea em
eqüinos: diagnóstico e tratamento. Revista de Educação Continuada do CRMVSP, v. 3, p. 3-11, 2000.
ROSA, P. S.; NEWTON, J. C.; TRICHE, P. An ELISA test to detect Pythium
insidiosum infection in horses. In: CONGRESSO BRASILEIRO DE
MICROBIOLOGIA, 20., 1999, Salvador, BA. Anais... Salvador: Sociedade Brasileira
de Microbiologia, 1999. p. 151.
SAINT-PIERRE-CHAZALET, M. et al. Amphotericin B-sterol complex formation and
competition with egg phosphatidylcholine: a monolayer study. Biochimica et
Biophysica Acta, v. 944, p. 477-86, 1988.
SALLIS, E. S. V.; PEREIRA, D. I. B.; RAFFI, M. R. Pitiose cutânea em eqüinos: 14
casos. Ciência Rural, v. 33, p. 899-903, 2003.
SANDE, M. A.; MANDELL, G. L. Drogas antimicrobianas: drogas antimicóticas e
antivirais. In: GOODMAN, L.; GILMAN, A. G. As bases farmacológicas da
terapêutica. Rio de Janeiro: Guanabara, 1987. p.799-807.
SANTOS, C. et al. Does Immunotherapy Protect Equines from Reinfection by the
45
Oomycete Pythium insidiosum? Clinic Vacc Immunol., v. 18, n. 8, p. 1397-9, 2011c.
SANTOS, C. et al. Eficácia da imunoterapia no tratamento de pitiose facial em
equino. Act Sci Vet., v. 39, n. 1, p. 955-9, 2011d.
SANTOS, M. N. et al. Pitiose cutânea em eqüinos no Rio Grande do Sul. Pesquisa
Veterinária Brasileira, v. 7, p. 57-61, 1987.
SANTOS, M. N., LONDERO, A. T. Zigomicose subcutânea em cavalos. Pesquisa
Agropecuária Brasileira, v. 9, p. 7-8, 1974.
SANTSCHI, E. M.; ADAMS, S. D.; MURPHEY, E. D. How to perform equine
intravenous digital perfusion. In: ANNUAL CONVENTION OF AMERICAN
ASSOCIATION OF EQUINE PRACTITIONER, 44., Baltimore, Maryland, EUA.
Proceedings... Lexington: American Association of Equine Practitioners, 1998.
p.198-201.
SANTURIO, J. M. et al. Cutaneous Pythiosis insidiosi in calves from the Pantanal
region of Brazil. Mycopathologia, v. 141, p. 123-5, 1998.
SANTURIO, J. M. et al. Ferida da moda: epidemiologia, diagnóstico, tratamento e
experiência com equinos infectados no Pantanal. Comunicado Técnico Embrapa
Pantanal, v. 34, p. 1-8, 2004.
SANTURIO, J. M. et al. Pitiose: uma micose emergente. Acta Scientiae
Veterinariae, v. 34, p. 1-14, 2006a.
SANTURIO, J. M. et al. Teste de ELISA indireta para o diagnóstico sorológico de
pitiose. Pesquisa Veterinária Brasileira, v. 26, p. 47-50, 2006b.
SANTURIO, J. M.; FEREIRO, L. Pitiose: uma abordagem micológica e terapêutica.
Porto Alegre: UFRGS, 2008. 111 p.
SATHAPATAYAVONGS, B. et al. Human pythiosis associated with Thalassemia
Hemoglobinopathy Syndrome. Journal of Infectious Diseases, v. 159, p.274-80,
1989.
SCHÖFFSKI, P. et al. Safety and toxicity of amphotericin B in glucose 5% or intralipid
20% in neutropenic patients with pneumonia or fever of unknown origin: randomized
study. British Medical Journal, v. 317, p. 379-84, 1998.
SCHURKO, A. M. et al. Development of a Species-Specific Probe for Pythium
insidiosum and the Diagnosis of Pythiosis. Journal Clinical Microbiology, v. 42, p.
2411-8, 2004.
SEDRISH, S. A. et al. Adjunctive use of a neodymium:yttrium-aluminum garnet laser
for treatment of pythiosis granulomas in two horses. Journal of the American
Veterinary Medical Association, v. 211, p. 464-5, 1997.
SEKHON, A. S.; PADHYE, A. A.; GARG, A. K. In vitro sensitivity of Penicillium
marneffei and Pythium insidiosum to various antifungal agents. European Journal of
Epidemiology, v. 8, p. 427-32, 1992.
46
SHENEP, J. L et al. Successful medical therapy for deeply invasive facial infection
due to Pythium insidiosum in a child. Clinical Infectious Diseases, v. 27, p. 138893, 1998.
SILVA, J. S. V.; ABDON, M. M. Delimitação do Pantanal Brasileiro e suas subregiões. Pesquisa Agropecuária Brasileira, v. 33, p. 1703-11, 1998.
SILVA, R. A. et al. Outbreak of trypanosomosis due to Trypanosoma evansi in
horses of Pantanal Mato-Grossense, Brazil. Veterinary Parasitology, v. 60, p. 16771, 1995.
SOKOL-ANDERSON, M. L. et al. Role of cell defence against oxidative damage in
the resistance of Candida albicans to the killing effect of amphotericin B.
Antimicrobial Agents and Chemotherapy, v. 32, p. 702-5, 1988.
TABOSA, I. M. et al. Outbreaks of pythiosis in two flocks of sheep in northeastern.
Brazilian Veterinary Pathology, v. 41, p. 412-5, 2004.
TABOSA, I. M. et al. Pitiose cutânea em eqüinos no semi-árido da Paraíba. Arquivo
Brasileiro de Medicina Veterinária e Zootecnia, v. 51, p. 27-30, 1999.
TEERLINK, T.; DE KRUIJFF, B.; DEMEL, R. A. The action of pimaricin, etruscomycin
and amphotericin B on liposomes with varying sterol content. Biochimica et
Biophysica Acta, v. 599, p. 484-92, 1980.
THITITHANYANONT, A. et al. Use of an immunotherapeutic vaccine to treat a lifethreatening human arteritic infection caused by Pythium insidiosum. Clin Infect Dis.,
v. 27, n. 6, p. 1394-400, 1998.
THOMASSIAN, A. Afecções da pele. In: ______. Enfermidades dos cavalos. 4. ed.
São Paulo: Varela, 2005. p. 39-41.
TRISCOTT, J. A.; WEEDON, D.; CABANA, E. Human subcutaneous pythiosis.
Journal of Cutaneous Pathology, v. 20, p. 267-71, 1993.
TROST, M. et al. Aspectos clínicos, morfológicos e imunoistoquímicos da pitiose
gastrintestinal canina. Pesq Vet Bras., v. 29, n. 8, p. 673-9, 2009.
TÚRY, E.; CORÔA, A. C. Pitiose cutânea em eqüinos no estado do Pará. In:
CONGRESSO BRASILEIRO DE MEDICINA VETERINÁRIA, 25., 1997, Gramado,
RS. Anais... Porto Alegre: Sociedade de Medicina Veterinária do Rio Grande do Sul,
1997. p. 150.
VANDEPUTTE, J.; WACHTEL, J. L.; STILLER, E. T. Amphotericin A and B antifungal
antibiotics produced by a Streptomycete. II. The isolation and properties of the
crystalline amphotericins. Antibiotics Annual, v. 1955-6, p. 587-91, 1956.
VANITTANAKOM, N. et al. Identification of emerging human-pathogenic Pithium
insidiosum by serological and molecular assay-based methods. Journal of Clinical
Microbiology, v. 42, p. 3970-4, 2004.
VARLAM, D. E. et al. Apoptosis contributes to amphotericin B-induced
47
nephrotoxicity. Antimicrobial Agents and Chemotherapy, v. 45, p. 679-85, 2001.
VERTUT-CROQUIN, A. et al. Differences in the interaction of the polyene antibiotic
amphotericin B with cholesterol- or ergosterolcontaining phospholipid vesicles. A
circular dichroism and permeability study. Biochemistry, v. 22, p. 2939-44, 1983.
WALSH, T. et al. Liposomal amphotericin B por empirical therapy in patients with
persistent fever and neutropenia. New England Journal of Medicine, v. 340, p. 764771, 1999.
WERNER, L. A.; HARDY, J.; BERTONE, A. L. Bone gentamicin concentration after
intraarticular injection or regional intravenous perfusion in the horse. Veterinary
Surgery, v. 32, p. 559-65, 2003.
WHITE, B. S.; PETERSON, R. P.; HARTSEL, S. C. Amphotericin B and nystatin
show different activities on sterol free vesicles. Biochemical and Biophysical
Research Communications, v. 164, p. 609-14, 1989.
WHITEHAIR, K. J. et al. Regional limb perfusion for antibiotic treatment of
experimentally induced septic arthritis. Veterinary Surgery, v. 5, p. 367-73, 1992c.
WHITEHAIR, K. J. et al. Regional limb perfusion with antibiotics in three horses.
Veterinary Surgery, v. 21, p. 286-92, 1992a.
WHITEHAIR, K. J. et al. Regional perfusion of the equine carpus for antibiotic
delivery. Veterinary Surgery, v. 21, p. 279-85, 1992b.
WHITEHAIR, K. L. Regional limb perfusion with antibiotics. In: ANNUAL
SYMPOSIUM OF THE AMERICAN COLLEGE OF VETERINARY SURGEONS
SYMPOSIUM, 5., 1995, Chicago, IL. Proceedings… Chicago: American College of
Veterinary Surgeons. p. 59.
WININGER, D. A.; FASS, R. J. Antibiotic-impregnated cement and beads for
orthopedic infections. Antimicrobial Agents and Chemotherapy, v. 40, p. 2675-9,
1996.
WU, T. C. On the development of antifungal agents: perspective of the U.S. Food
and Drug Administration. Clinical Infectious Diseases, v. 19, p. 54-8, 1994.
YOUNG, L. Y.; HULL, C. M.; HEITMAN, J. Disruption of ergosterol biosynthesis
confers resistance to amphotericin B in Candida lusitaniae. Antimicrobial Agents
and Chemotherapy, v. 47, p. 2717-24, 2003.
ZYGMUNT, W. A. Intracellular loss of potassium in Candida albicans after exposure
of polyene antifungal antibiotics. Applied Microbiology, v. 14, p. 953-6, 1966.
48
4 ARTIGO 2
49
TRATAMENTO DA PITIOSE EM MEMBROS DE EQUINOS POR MEIO DE
PERFUSÃO REGIONAL INTRAVENOSA COM ANFOTERICINA B ASSOCIADA
AO DIMETILSULFÓXIDO
RESUMO
A pitiose equina é uma doença endêmica no Pantanal Brasileiro e causa prejuízos
significativos a equinocultura. Neste trabalho são relatados 15 casos com infecção
por Pythium insidiosum como o aspecto distal dos membros pélvicos e torácica.Por
meio de excisão cirúrgica do tecido de granulação e termocautério, 50 mg de
anfotericina B (10 mL), diluída numa solução de DMSO a 10% ( 6 mL de DMSO em
44 mL de ringer lactato ), a infusão foi administrada por meio de um cateter colocado
na veia superficial do membro afetado sendo ao lado da lesão, após a colocação de
um garrote acima do local da injeção. Perfis bioquímicos, hematológicos e séricos
foram investigados e as lesões foram avaliados antes do tratamento e
semanalmente até a completa cicatrização de lesões. Vericou-se que cem por cento
(100 %) dos cavalos tratados com anfotericina B associada com DMSO teve
cicatrização completa num período entre 6-9 semanas após um tratamento,
dependendo do tamanho da lesão. A infusão não induziu efeitos colaterais locais.
Estudos hematológicos revelaram anemia inicial associada com baixa contagem de
hemácias e hematócrito, que foram resolvidos durante o período de tratamento. Um
aumento significativo na contagem total e diferencial leucocitários foi encontrado
antes do tratamento que diminui para valores fisiológicos durante as semanas após
o tratamento. A análise bioquímica de soros não apresentaram alterações
significativas nos parâmetros determinados utilizados para a avaliação das funções
hepática e renal. A infusão regional com administração de anfotericina B em uma
solução de DMSO a 10% por perfusão foi eficaz para o tratamento da pitiose em
membros equinas, sem efeitos colaterais.
Palavras chave: Análise bioquímica. Equinos. Infecção.
50
ABSTRACT
The equine pythiosis is endemic in the Brazilian Pantanal and cause significant
damage to equine . In this work are reported 15 cases of infection by Pythium
insidiosum as the distal aspect of the hind limbs and through surgical excision
torácica.Por granulation tissue thermocautery and 50 mg amphotericin B (10 mL) ,
diluted in a solution of DMSO at 10 % (6 mL DMSO in 44 ml of lactated Ringer ) , the
infusion was administered through a catheter placed in the vein of the affected
surface being adjacent to the lesion, after placing a tourniquet above the injection
site. Profiles biochemical , hematological and serum were investigated and the
lesions were evaluated before treatment and weekly until complete healing of injuries
. Vericou that one hundred percent (100%) horses treated with amphotericin B was
associated with DMSO in complete healing time between 6-9 weeks after treatment,
depending on the size of the lesion. The infusion did not induce local side effects.
Hematologic studies showed low initial anemia associated with red cell count and
hematocrit, which were resolved during the treatment period. A significant increase in
total and differential leukocyte count was found that before the treatment decreased
to physiological values during weeks after treatment. Biochemical analysis of serum
showed no significant changes in certain parameters used for the evaluation of
hepatic and renal function. The infusion regional administration of amphotericin B in a
DMSO solution at 10% by infusion was effective for the treatment of equine limb
Pythiosis without side effects.
Keyword: Biochemical analysis. Horses. Infection.
51
4.1 INTRODUÇÃO
Pitiose é uma doença infecciosa piogranulomatosa causada pelo oomyceto
parasita Pythium insidiosum. Este organismo filamentoso, inicialmente, afeta os
tecidos da pele e subcutâneo, mas pode afetar os tecidos adjacentes (tendões,
ligamentos e ossos), ou invadem o trato gastrointestinal e outros tecidos e órgãos,
resultando em doença multissistêmica (DE COCK; MENDONZA; PADHYE, 1987;
LEAL; LEAL; SANTURIO, 2001; LEAL; LEAL; FLORES, 2001; MENDOZA; AJELLO;
MCGINIS, 1996). A pitiose ocorre com frequência em regiões tropicais, subtropicais
e temperadas, provavelmente porque P. insidiosum requer um, o ambiente aquático
com temperatura elevada (30 a 40º C) e substrato orgânico vegetal para completar
seu ciclo de vida (CHAFFIN; SCHUMACHER; McMULLAN, 1992; CHAFFIN;
SCHUMACHER; McMULLAN, 1995). A pitiose cutânea em cavalos é caracterizada
por granulomas eosinofílicos com massas necróticas conhecidas como “kunkers”, e
que são caracterizadas macroscopicamente por massas irregulares amareloacinzentadas, em forma que lembra corais marinhos. Histologicamente este material
é composto por debris celulares de neutrófilos e eosinófilos e hifas do P. insidiosum
(CHAFFIN; SCHUMACHER; McMULLAN, 1995). O diagnóstico é geralmente
baseado
em
dados
clínicos,
epidemiológicos
e
confirmado
por
exames
histopatológico e de imuno-histoquímica (LEAL; LEAL; FLORES, 2001).
O tratamento da pitiose é um desafio, e a eficácia aparentemente depende
de fatores como o tamanho, duração e local da lesão; imunocompetência e tipo de
tratamento (LEAL; LEAL; SANTURIO, 2001; LEAL; LEAL; FLORES, 2001). Os
tratamentos conservadores são atualmente utilizados com ou sem excisão cirúrgica
da lesão para melhorar os resultados (LEAL; LEAL; FLORES, 2001). As drogas
antifúngicas mais comumente administrados sistemicamente utilizados para tratar
pitiose são iodeto de potássio e de sódio, cetoconazol, miconazol, fluconazol,
itraconazol, e anfotericina B (CHAFFIN; SCHUMACHER; McMULLAN, 1992; LEAL;
LEAL SANTURIO, 2001; SALLIS; PEREIRA; RAFFI, 2003; SANTURIO; ALVES;
PEREIRA, 2006), no entanto, P. insidiosum, por não ser um fungo verdadeiro, o
organismo possui uma maior resistência aos antifúngicos atualmente disponíveis
(FOIL, 2006).
A anfotericina B, um antibiótico macrólido polieno, produzido naturalmente
pelo Streptomyces nodosus actinomiceto (GOLD; STOUT; PAGANO, 1956;
52
DISMUQUES, 2000; VANDEPUTTE; WACHTEL; STILLER, 1956). O mecanismo de
ação do fármaco é caracterizado a partir da ligação direta aos esteróis presentes na
membrana celular do parasita, alterando a integridade e resultando em reações
osmóticas de eletrólitos (potássio, sódio, magnésio, cloreto) para o meio intracelular,
e também alterando metabolitos essenciais ao fungo (nucleótidos e proteínas),
provocando assim a morte do parasita (CHAPMAN; SULLIVAN; CLEARY, 2008;
RICHARDSON; WARNOCK, 2003). Dória, Freitas e Linardi (2012) descreveram que
92% dos cavalos afetados por P. insidiosum e apresentando tecido de granulação
exuberante nos membros torácicos ou pélvicos, tratados com perfusão regional
intravenosa com anfotericina B mostrou resolução completa da lesão 35 ou 60 dias
depois de um ou dois tratamentos, respectivamente e considerou a perfusão
regional intravenosa de anfotericina B uma terapia adjuvante eficaz para excisão
cirúrgica e termocauterismo, no tratamento de pitiose cutânea em membro de
equinos.
Perfusão regional intravenosa é uma técnica indireta que consiste na infusão
de fármaco num vaso periférico isolado, a partir da circulação sistêmica, através da
utilização de um torniquete (garroteamento) (MARTINEZ, 2004; SANTSCHI;
ADAMS; MURPHEY, 1998). Com isso, espera-se que as drogas administradas
mediante esta técnica, irão atingir os tecidos alvos, por difusão através de leitos nas
proximidades dos capilares devido ao grande volume de perfusão. A concentração
elevada da droga, e a alta pressão transitória intravascular estabelecida pelo
torniquete, gera um aumento do gradiente de concentração entre os tecidos e
espaço intravascular. Esta técnica maximiza a difusão da droga para o fluido
sinovial, ossos e tecidos moles, bem como tecidos pouco vascularizado, onde os
agentes são geralmente protegidos (ERRICO; TRUMBLE; BUENO, 2008; GILLIAM;
STREETER; PAPICH, 2008; MARTINEZ, 2004; WERNER; HARDY; BERTONE,
2003).
Diante dos resultados obtidos por Dória et. al 2012, hipoteticamente
melhores resultados poderiam ser evidenciados com a administração perfusão
intravenosa membro regional (IRLP) fazendo a associação de anfotericina B e
dimetilsulfóxido (DMSO), para alcançar maiores concentrações anfotericina B dentro
de tecidos infectados por P. insidiosum, e reduzir os efeitos colaterais inflamatórias
locais. Já foi demonstrado que o DMSO é um eficaz antiinflamatório e analgésico
(ALSUP; DEBOWES, 1984; BRAYTON, 1986; WELCH; DEBOWES; LIEPOLD,
53
1989, WELCH; WATKINS; DEBOWES, 1991). Pode também possuir algum efeito
inibitório sobre o crescimento de uma variedade microrganismos, inclusive fungos,
como resultado do seu efeito sobre a resposta imune e a redução de endotoxina
induzidas por danos nos tecidos (ALSUP; DEBOWES, 1984; BRAYTON, 1986;
WELCH; DEBOWES; LIEPOLD, 1989). Outros estudos têm demonstrado aumento
do fluxo sanguíneo por dilatação vascular com aplicação de DMSO (ALSUP;
DEBOWES, 1984). Tais propriedades associadas com a sua capacidade para
penetrar as membranas biológicas fornecem base para a sua utilização em conjunto
com um fármaco anti-fúngico para perfusão regional de membro afetados por
dermatites fúngicas (CIMETTI; MERRIAM; D'OENCH, 2004).
Diante deste contexto, objetivo do presente estudo foi avaliar a eficácia e
viabilidade de uso da técnica de perfusão intravenosa membro regional no
tratamento adjuvante de pitiose cutânea em membros de equinos, utilizando uma
associação de anfotericina B e DMSO diluídos em solução de Ringer com lactato,
administrados após a excisão cirúrgica e termocauterização de feridas causadas por
granulação exuberante na pitiose. Avaliar também, os efeitos adversos, locais e
sistêmicos, da administração dos fármacos e a evolução da reparação cicatricial das
lesões cutâneas.
O presente estudo compreende uma atividade complementar, qualitativa,
aos estudos realizados por Dória, Freitas e Linardi (2012).
54
5 MATERIAL E MÉTODOS
Foram utilizados 19 equinos, destes 15 que tinham entre 4 meses a 15 anos
de idade, de ambos os sexos, sendo eles de diferentes raças, entre elas, raça
Pantaneira, Quarto de Milha e alguns sem raça definida, com escore corporal entre 2
e 3 (HENNEKE et al., 1983). Estes 15 animais apresentavam ferida granulomatosa
devido à infecção por pitiose, em membro torácico ou pélvico, distalmente às
articulações úmero-radial e úmero-ulnar ou femoro-tibial e femoro-patelar. Os 19
equinos foram distribuídos em dois grupos experimentais. Um grupo constituído de
15 equinos, machos (n=10) e fêmeas (n=5), tratados mediante a excisão cirúrgica da
ferida, termocauterização e a IRLP com anfotericina B e Dimetilsufóxido (DMSO), e
com peso médio variando entre 100 e 400 kg e outro grupo constituído de quatro
animais controles, não tratados porém contém a doença administrando o ringer
lactato, machos (n=2) e fêmeas (n=2), com idades entre 4 meses a 15 anos e peso
entre 200 e 450 kg. Os animais foram encaminhados para o Hospital Veterinário da
Universidade de Cuiabá (HOVET), por meio de contatos com proprietários de
fazendas na região do Pantanal Mato-Grossense e adjacências do município de
Cuiabá, MT. Estes animais foram mantidos em baias, livres de áreas alagadiças, em
regime de alimentação à base de alfafa, concentrado (ração comercial),
suplementação mineral e água ad libitum, durante todo o período experimental.
5.1 AVALIAÇÃO CLÍNICA
No 1º dia do experimento, os equinos foram contidos em tronco individual e
submetidos ao exame clínico (FEITOSA, 2004). Avaliou-se a frequência cardíaca
(FC; batimentos/minuto) por auscultação torácica, a frequência respiratória (FR;
movimentos respiratórios/minuto) pela observação da movimentação do gradil
costal, o tempo de preenchimento capilar (TPC; segundos) por compressão digital
da gengiva, a motilidade intestinal (classificada como normal, hipomotilidade ou
hipermotilidade) por auscultação abdominal e a temperatura retal (T) por meio de
termômetro clínico convencional.
5.2 AVALIAÇÃO HISTOPATOLÓGICA
A avaliação histopatológica foi realizada no Laboratório de Patologia
55
Veterinária da Universidade de Cuiabá (LPV-UNIC).
Foi realizada biópsia para confirmação do diagnóstico em cada uma das
feridas, nos membros dos equinos. As biópsias contendo “kunkers” (1x1x1 cm),
destinados à avaliação histopatológica, foram fixados em solução de formol neutro a
10% e, posteriormente, clivados, processados rotineiramente e incluídos em
parafina. Dessa forma, após fixação e clivagem, o material foi desidratado em
concentrações crescentes de álcool etílico. Em seguida, foram submetidos à
diafanização pelo xilol e embebição em parafina líquida a 59 ºC. Dos fragmentos
incluídos em blocos de parafina, foram realizados cortes de 5 µm de espessura, com
auxílio de micrótomo rotativo16. Os cortes foram corados pela hematoxilina-eosina
(HE) e Prata Metenamina de Grocott (GMS - Grocott´s methenamine silver) (LEAL;
LEAL; SANTURIO, 2001; SALLIS; PEREIRA; RAFFI, 2003; PEDROSO et al., 2009).
As lâminas coradas foram analisadas em microscopia de luz e fotografadas com
câmera fotográfica digital acoplada ao microscópio.
5.3 TÉCNICA DE IMUNO-HISTOQUÍMICA
O método imuno-histoquímico foi realizado no Laboratório de Patologia
Veterinária da Universidade Federal de Mato Grosso (LPV-UFMT).
Os materiais de biópsia contendo “kunkers” (1x1x1 cm), destinados à
imunohistoquímica, foram imersos em solução de formol neutro a 10%, por um a
dois dias, clivados, processados rotineiramente e incluídos em parafina. Cortes
histológicos de 5 µm de espessura foram obtidos com auxílio de micrótomo rotativo.
Os cortes histológicos foram montados nas lâminas, previamente tratadas com
solução de gelatina 0,3% e aderidos a estas por meio do calor (60 ºC), durante 24
horas, após o que as lâminas foram submetidas à imuno-histoquímica. Utilizou-se o
método streptavidina-biotina marcada19 (LSAB), de acordo com Brown et al. (1988)
e Gimeno, Massone e Portiansky (1999).
A desparafinização dos cortes foi realizada em estufa à 60º C, durante 30
minutos. Na sequência, os cortes foram hidratados em soluções de xilol I e II,
permanecendo dez minutos em cada solução e com passagens sucessivas, a cada
dois minutos, em álcool 100%, 90%, 80% e 70% e, posteriormente, foram lavados
em água destilada por dez vezes. Foi realizado o bloqueio da peroxidase endógena
pela incubação das lâminas com peróxido de hidrogênio a 3%, em água destilada,
56
durante 15 minutos, à temperatura ambiente e, as amostras foram, novamente,
lavadas em água destilada. O bloqueio de proteínas inespecíficas foi realizado
incubando-se os cortes com leite em pó desnatado a 5%, diluído em solução tampão
de fosfato (PBS), durante 15 minutos. A recuperação antigênica foi realizada com
solução tampão de citrato de sódio a 10 mM, com pH 6,0, mediante calor (microondas, potência máxima), por dois minutos, adicionando, conforme necessário,
solução tampão (citrato de sódio ou PBS) para evitar a evaporação. Após cinco
minutos, destinados à resfriação da amostra, nova lavagem em água destilada foi
realizada. A incubação com o anticorpo primário policlonal anti-Pythium insidiosum
produzido em coelho (cedido à Universidade Federal do Mato Grosso – UFMT,
produzido pelo Laboratório de Pesquisas Micológicas – LAPEMI da Universidade
Federal de Santa Maria – UFSM) foi realizada na diluição de 1:100, em solução
tampão (PBS), mantida por 1 hora, a 37 ºC, em estufa e, nova lavagem com água
destilada
foi
realizada.
Após
este
procedimento,
incubou-se
o
complexo
streptavidina-biotina (LSAB) com o anticorpo secundário biotinilado universal durante
20 minutos, em temperatura ambiente, seguido pela lavagem com tampão TBS
(solução TRIS salina tamponada) e incubação pela streptavidina, também, por 20
minutos, em temperatura ambiente e lavagem com água destilada. A revelação da
reação foi feita com o cromógeno diaminobenzidina20 (DAB), durante 5 a 10
minutos, seguido de lavagem em água destilada. A contra-coloração dos cortes foi
realizada com hematoxilina de Harris, com permanência de um minuto. As lâminas
foram lavadas em água corrente e passaram por desidratações sucessivas, a cada
um minuto, em banhos de álcool 70%, 80%, 90% e 100% e soluções de xilol III e IV.
A montagem das lâminas foi realizada com bálsamo do Canadá21. O protocolo para
a imuno-histoquímica utilizada neste trabalho foi adaptado de Gimeno, Massone e
Portiansky (1999).
As lâminas coradas foram analisadas em microscopia de luz e fotografadas
em câmera fotográfica digital acoplada ao microscópio.
O anticorpo primário foi produzido em coelho por meio de uma única
inoculação de 20.000 zoósporos de Pythium insidiosum, via subcutânea, sem a
utilização de adjuvantes. Coletas de sangue a cada 14 dias foram realizadas e a
quantificação dos anticorpos foi feita pela técnica de Elisa. O soro utilizado
corresponde à coleta no 45º dia, o qual apresentou uma densidade ótica (DO) de
0,281. A DO considerada positiva para coelhos é de 0,105 (PEDROSO et al., 2009).
57
5.4 PROCEDIMENTO EXPERIMENTAL
Os animais foram submetidos a jejum alimentar, doze horas antes do início
do experimento. Após avaliação clínica, em ambos os grupos, colocou-se um cateter
intravenoso, 14G, na veia jugular dos equinos e foi realizada anestesia geral
intravenosa, mediante tranquilização com acepromazina 1%, na dose de 0,1 mg/kg,
via intravenosa e após 5 minutos, a administração intravenosa de éter-glicerilguaiacol, na dose de 100 mg/kg e indução/manutenção anestésica com cetamina
10% (2 mg/kg), associada na mesma seringa, com midazolam (0,1 mg/kg), via
intravenosa. Doses complementares de cetamina 10% (2 mg/kg) associada ao
midazolam (0,1 mg/kg) foram realizadas, conforme necessário, para eliminar dor e
movimentação durante o procedimento experimental.
Após a anestesia, os animais foram posicionados em decúbito lateral,
esquerdo ou direito, de acordo com a localização da ferida. Os membros sadios
foram contidos com auxílio de cordas e/ou travões e o membro com a ferida de
pitiose mantido em posição elevada em relação ao solo, para realização do
procedimento experimental.
Procedeu-se a limpeza da ferida e regiões adjacentes com água e sabão e
antissepsia com povidona-iodo e álcool 70%. Na sequência, foi realizada hemostasia
preventiva, por meio de garroteamento do membro, com torniquete de borracha, na
região proximal à ferida (em relação ao tronco) e excisão cirúrgica, com lâmina de
bisturi número 23, do tecido de granulação exuberante e dos “kunkers”, evitando
exposição óssea ou penetração articular.
Fragmentos cúbicos de 2 cm² foram colhidos, acondicionados em solução
de formol tamponado a 10% e enviados para avaliação histopatológica e imunohistoquímica (BROWN et al., 1988, GIMENO; MASSONE; PORTIANSKY, 1999). Os
testes de imuno-histoquímica foram realizados, mediante o encaminhamento de
blocos de parafina contendo fragmentos de tecido, pelo Laboratório de Patologia
Veterinária da Universidade Federal de Mato Grosso, Cuiabá, MT. O protocolo
utilizado foi semelhante ao realizado por Ubiali et al. (2013) em animais com rinite
micótica causada por P. insidiosum.
Na sequência, o torniquete foi lentamente afrouxado para que se realizasse
a hemostasia por termocauterização. Após cinco minutos, destinados à reperfusão
sanguínea do membro, o garrote de borracha foi reposicionado, padronizando-se
58
duas voltas (360º) em torno do membro, de maneira tensa. Após tricotomia e
antissepsia com povidona-iodo, uma veia superficial engurgitada, localizada proximal
à ferida e distal ao torniquete, foi canulada, conforme o diâmetro, com cateter
intravenoso números 20, 22 ou 24 G para a administração da droga. De acordo com
a localização das feridas, as veias ou seus ramos cateterizados foram, no membro
torácico, cefálica e digital palmar comum e, no membro pélvico, safena, digital
plantar comum e digital dorsal comum. Após implantação do cateter, administrou-se,
no Grupo Anfotericina B mais DMSO, 10 mL da solução de anfotericina B (0,83
mg/mL), composta por 50 mg de anfotericina B (10 mL de diluente), diluída em 44
mL de solução de Ringer Lactato com 6 ml de DMSO e no grupo controle, 60 mL de
solução de Ringer lactato. O volume total foi administrado manualmente,
padronizando-se o tempo de infusão em cinco minutos, com auxílio de seringa de 60
mL e extensor de cateter o escalpe número 21. O garroteamento, em ambos os
grupos, foi mantido por 40 minutos após a administração das soluções, perfazendo
um total de tempo de garroteamento de 45 minutos.
O cateter foi retirado 10 minutos após a remoção do torniquete e exerceu-se
pressão manual sobre a veia canulada, durante 10 minutos, para hemostasia. Após
este procedimento, foi realizada bandagem com algodão e ataduras na ferida, as
quais eram substituídas a cada 3 ou 4 dias, sendo o curativo tópico realizado apenas
com povidona-iodo. Após recuperação anestésica, todos os animais receberam dose
única de antiinflamatório (fenilbutazona 4 mg/kg, via intravenosa).
A aplicação do protocolo foi realizada pelo mesmo pesquisador, em todos os
animais deste estudo, para minimizar variações.
5.5 AVALIAÇÃO DAS FERIDAS
As feridas foram fotografadas e avaliadas antes do início do procedimento
experimental, quanto à localização anatômica, dimensões (cm²) sendo o tamanho da
lesão (comprimento e largura) utilizando uma régua, tempo de evolução e
macroscopia da lesão. As feridas foram consideradas como pequenas, quando sua
área atingia até 25 cm2 como feridas grandes quando sua área ultrapassava 25 cm².
Durante o período de avaliação, foi realizado o exame da locomoção, observando-se
presença de ferida no local de infusão das soluções, aumento de volume,
sensibilidade à palpação do membro afetado e claudicação ao passo, a qual foi
59
classificada em: severa (++), discreta (+) e ausente (-).
Além disso, as feridas foram classificadas conforme o seguinte critério:
Ferida tipo 1: a lesão constitui-se de tecido de granulação exuberante, com
ulcerações cutâneas extensas, com superfície de aspecto nodular, que drena
exsudato serossanguinolento viscoso, geralmente acompanhada por grande
aumento de volume local. Ao corte, a coloração das superfícies é esbranquiçada, a
consistência firme, com presença de fístulas que se comunicam com cavidades, as
quais contém concreções branco-amareladas, de consistência firme, com aspecto
de coral (“kunkers”), quase sempre envoltas por exsudato purulento. Ferida tipo 2: a
lesão constitui-se de tecido de granulação não exuberante, de coloração róseaamarelada,
com
presença
de
tecido
necrótico
e
ausência
de
secreção
serossanguinolenta ou “kunkers”. Ferida tipo 3: evidencia-se linha de epitelização
nas margens da lesão, a qual constitui-se de tecido de granulação rosado, plano,
com ausência de secreções ou “kunkers”. Ferida tipo 4: evidencia-se epitelização
parcial da lesão, a qual constitui-se de tecido de granulação rosado, plano, com
ausência de secreções ou “kunkers”. Ferida tipo 5: Ferida cicatrizada. Evidencia-se
epitelização completa, com pelos na região da lesão. As feridas foram fotografadas e
avaliadas imediatamente antes do início do procedimento experimental (D0) e aos
sete (D7), catorze (D14), vinte e um (D21), vinte e oito (D28), trinta e cinco (D35) e
sessenta (D60) dias após o procedimento experimental inicial (D0).
Os dados obtidos na fase experimental foram avaliados nos diferentes
tempos e apresentados de maneira descritiva, por meio de texto, tabelas e figuras,
descrevendo - se as variáveis qualitativas e quantitativas, em forma de frequências
(absolutas e relativas) e percentuais de animais que apresentavam determinada
característica, em determinado tempo, para cada item avaliado nos grupos
tratamento e controle.
60
6 RESULTADOS
Em ambos os grupos, os equinos com pitiose, no dia 0 (D0), evidenciavam
condições corporais de animais muito magros e magros (escore corporal entre 2 e
3). No grupo tratado por perfusão regional intravenosa com anfotericina B e
dimetilsulfóxido, todos os animais, no D60, apresentavam condições corporais
classificadas como moderadas (escore corporal 5), enquanto no grupo controle o
escore corporal dos animais foi mantido entre 2 e 3 (FIGURA 1).
Todos os animais possuíam históricos de insucesso nos tratamentos
adotados, seja por excisão do tecido de granulação exuberante e cauterização com
ferro incandescente ou por aplicação de produtos cáusticos, como o ácido sulfúrico
(solução de bateria) ou mesmo com outros produtos como grafite, zinco e óxido de
manganês (pilha seca).
Figura 1. Ilustração do progresso da condição corporal de equinos do grupo tratado com anfotericina
B e DMSO, aplicada pela técnica de perfusão regional intravenosa do membro, entre a
primeira (D0) e a terceira semana (D21) avaliação.
Os animais de ambos os grupos apresentaram frequências cardíaca (FC
61
entre 28 a 40 batimentos/minuto) e respiratória (FR entre 8 e 16 movimentos
respiratórios/minuto), tempo de preenchimento capilar (TPC entre 1 e 2 segundos),
motilidade intestinal (normal) e temperatura entre 37,2 e 38,9 C º) dentro dos valores
considerados fisiológicos para a espécie equina (FEITOSA, 2004), o que permitiu
que fossem submetidos aos procedimentos anestésico e cirúrgico.
No exame clínico inicial (D0), constatou-se, em todos os animais tinham
inchaço nos membros afetados e as lesões foram clinicamente descrita como tecido
de granulação exuberante com extensa ulceração, superfície nodular e exsudato
viscoso, geralmente associado a edema local. Cortes de tecido tinha uma superfície
branca, consistência firme, e fístulas contendo Kunkers, geralmente rodeado por
exsudato purulento com sinais intensos de prurido, caracterizado pela automutilação. Os animais, em ambos os grupos, no D0, apresentavam feridas tipo 1.
Em todos os casos, a evolução da ferida, descrita pelos proprietários, foi rápida,
sendo que, em torno de 15 a 20 dias, as lesões atingiam grande tamanho. Todas as
feridas, embora fossem granulomatosas e com secreção abundante, não
apresentavam miíase.
A análise das alterações por meio da técnica histoquímica de H&E revelou,
em todos os animais, áreas necróticas eosinofílicas extensas (“kunkers”) e
multifocais, na derme superficial e profunda, contendo imagens negativas de
estruturas tubuliformes, irregulares, septadas e com ramificações em ângulo reto
(“pseudo-hifas”). Associado as lesões anteriormente descritas havia também
infiltrado inflamatório difuso e intenso, principalmente na periferia dos “kunkers”,
predominando eosinófilos e, também, neutrofílos e células mononucleares
(macrófagos, linfócitos, plasmócitos e raras células gigantes de Langerhans). Havia
tecido de granulação exuberante, com proliferação de fibroblastos, fibras colágenas
e neovascularização acentuada (FIGURA 2). As ulcerações na epiderme
apresentavam infiltrado neutrofílico moderado a intenso e, por vezes, colônias
bacterianas basofílicas superficiais. Por meio da técnica histoquímica de coloração
pela prata (GMS), nas áreas de necrose, visualizou-se grande quantidade de
“pseudo-hifas” longas, septadas, irregulares e bem delimitados, seccionadas
longitudinal e transversalmente, coradas em preto ou marrom-escuro e localizadas
principalmente na periferia dos “kunkers”, características de P. insidiosum (FIGURA
2). O diagnóstico histopatológico foi de dermatite piogranulomatosa, focal extensa,
acentuada, associada a “pseudo-hifas” características de P. insidiosum (pitiose
62
cutânea), nos 18 animais desta pesquisa.
O diagnóstico etiológico de pitiose, nos 18 casos, foi elucidado pela
aplicação da técnica de imuno-hístoquimica, obtendo-se imunomarcação positiva
com uso do kit (LSAB - DAKO) anti-Pythium insidiosum, e caracterizada pela
visualização de estruturas ramificadas e septadas.
Neste estudo observou-se que o tempo de evolução apresentado pelas
feridas pequenas foi de seis semanas enquanto para as feridas grandes o tempo de
evolução foi de oito semanas.
No dia 0, todos os cavalos (15) do grupo tratamento possuíam lesões, em
torno de 90º (4 cavalos, 26,7%), 180 º (7 cavalos, 46,6%) e 360º (4 cavalos, 26,7%)
da área afetada em relação a circunferência do membro. Dos Quinze animais que
foram submetidos ao tratamento com anfotericina B e DMSO, 11 possuíam feridas
grandes (73,3%) e, outras quatro feridas pequenas (26,7%). (TABELA 2).
Figura 2. A - Derme, área focal de necrose (Kunkers) e dermatite eosinofilica, neutrofílica e tecido de
granulação H&E 10x. B - área de central de necrose com imagens (negativas) não coradas,
tubulares, ramificadas e irregulares (hifas) H&E 40x. C - Hifas irregulares e ramificadas no centro ou
na periferia dos “kunkers”, Gömori (GMS) 40x. D - imunomarcação positiva com uso do kit (LSAB DAKO) para Pythium insidiosum 40x.
63
Quadro 1. Valores referentes ao número e porcentagem (%) de equinos que apresentavam feridas
2
2
grandes (> 25 cm ) e feridas pequenas (< 25 cm ), submetidos à técnica de perfusão regional
intravenosa do membro com anfotericina B e DMSO e de equinos do grupo controle.
Grupos
Ferida Grande (> 25 cm)
Potro
Ferida Pequena (< 25 cm)
Adulto
Total
Potro
Total
Anfotericina e 3 (20%)
DMSO
(73%)
8 ( 53%)
11
1(7%)
27%)
Controle
4 (80%)
5
0
1 (20%)
(100%)
Adulto
3 (20%)
0
4(
0
Os três equinos adultos e um potro do grupo controle apresentavam feridas
grandes (100%), perfazendo um total de cinco feridas, pois um animal apresentava
feridas em ambos os membros torácicos.
Dois animais (13,4%) do grupo tratamento apresentavam feridas no
metacarpo ou metatarso (canela), sendo que em quatro animais (26,6%) a lesão
estava localizada, também, na articulação metacarpo-/metatarso-falangiana (boleto);
em um animal (6,6%) a ferida estava sobre as falanges proximal e média (quartela),
em dois animais (13,4%) a localização da lesão era sobre o tarso (jarrete) e em dois
animais (13,4%) a ferida localizava-se no rádio (braço). Em outros casos, teve
envolvimento de mais de uma região, três animais (20%) a ferida se estendia da
articulação metacarpo-/metatarso-falangiana (boleto) até as falanges proximal e
média (quartela), e um animal (6,6%)l a ferida inicia no rádio até as falanges
proximal e média (quartela). Dentre essas feridas, seis (40%) estavam distribuídas
nos membros torácicos e 9 (60%) nos membros pélvicos.
No grupo controle, três animais (75%) apresentavam as feridas sobre o
metacarpo (canela), sendo que um desses apresentava feridas em ambos os
membros torácicos e, outro animal (25%), apresentava ferida sobre as falanges
proximal e média (quartela). Dentre essas feridas, quatro se desenvolveram nos
membros torácicos (80%) e uma abrangia o membro pélvico (20%).
64
Quadro 2. Discriminação da localização anatômica, tempo de evolução e dimensões da ferida (cm2)
na primeira avaliação (D0) dos equinos submetidos à técnica de perfusão regional intravenosa do
membro com anfotericina B e DMSO e nos equinos do grupo controle.
ANIMAL
LOCALIZAÇÃO
DIMENSÃO CICATRIZAÇÃO Reaplicação
(SEMANAS)
01
Região cranial, medial e caudal distal do
180º
9
Não
rádio até casco; MAD
02
Região cranial, lateral e caudal do boleto
180º
8
Não
e quartela; MPE
03
Região cranial, lateral e caudal do
180º
9
Não
boleto; MPE
04
Região boleto; MPD
180º
8
Não
05
Região cranial, medial e caudal da
180º
6
Não
porção média e distal tíbia e do tarso;
MPD
06
Região cranial, lateral e caudal da
180º
9
Não
porção média e distal do rádio; MAE
07
Região lateral do terço proximal da
90º
6
Não
canela; MAD
08
Região palmar do carpo; MAD
180º
6
Não
09
Região cranial e lateral da porção
90º
6
Não
proximal, média e distal da tíbia; MPD
10
11
12
13
14
15
Região lateral, cranial e medial do boleto
e quartela; MPE
Região lateral, cranial e caudal da
porção média e distal da canela; MPE
180º
8
Não
180º
9
Não
Região cranial, lateral e caudal da
porção média e distal do rádio; MAE
Região cranial, lateral e caudal da
quartela; MPD
Região cranial, lateral e caudal do
boleto; MAE
Região lateral, cranial e medial do boleto
e quartela; MPE
90º
6
Não
90º
6
Não
90º
6
Não
180º
9
Não
Foi verificado que todas as quinze lesões regrediram após uma única
administração de anfotericina B, em uma solução de DMSO a 10%.
Nestes casos, no sétimo dia (D7), as feridas foram classificadas como tipo 2,
sendo que, em uma pequena área ou em alguns pontos havia tecido de granulação
de coloração vermelha-escura ou preta, com secreção serossanguinolenta e
“kunkers” (FIGURA 3).
No 14º dia (D14), as lesões iniciais regrediram para tecido de granulação
rosa – amarelo com ausência de exsudato, fístulas e Kunkers, caracterizando ferida
tipo 2. Com ausência de Kunkers, não houve necessidade da reaplicação.
Nas semanas subsequentes, até reepitelização completa, já se observava
crescimento de pelos na sexta semana (cinco cavalos 33,33 %), em 8 semanas
(cinco cavalos 33,33%), e 9 semanas (cinco cavalos 33,33%) após a perfusão
65
regional com anfotericina B e DMSO. No D60 (de 8 a 9 semanas), as feridas foram
classificadas como tipo 5.
Figura 3. Ilustração da evolução da cicatrização de feridas de pitiose de eqüinos tratados com
aplicação única de anfotericina B e DMSO, pela técnica de perfusão regional intravenosa do
membro, no primeiro dia (D0) e nos dias 7.
Todos os animais (100%), em ambos os grupos, apresentavam, antes do
tratamento (D0), aumento de volume dos membros afetados, mais acentuado nas
áreas adjacentes às feridas granulomatosas com exsudato serossanguinolento, os
quais foram reduzidos, após o tratamento, para lesão mínima ou imperceptível, no
60º dia do período pós-operatório (D60).
A administração de anfotericina B e DMSO pela técnica de perfusão regional
intravenosa não induziu efeitos colaterais locais. No grupo controle não foram
evidenciadas alterações no aparelho locomotor decorrentes da perfusão regional
intravenosa com ringer lactato.
Cem por cento (100%) dos cavalos tratados com anfotericina B associado
com DMSO tiveram evolução completa de cicatrização da lesão em um período que
variou entre 6 -9 semanas após o tratamento, dependendo do tamanho da lesão.
O tempo de garroteamento de 45 minutos foi considerado adequado para
tratar feridas de pitiose, por meio da técnica de perfusão regional intravenosa do
membro, independente do tamanho ou peso do animal ou localização da ferida. Não
foram observadas alterações locais, regionais ou sistêmicas devido ao tempo de
garroteamento e ao material usado no garroteamento (compressão) do membro.
66
6.1 AVALIAÇÃO DA DOSE DE ANFOTERICINA B
A dose e o volume total de anfotericina B (0,83 mg/mL/60 mL) e DMSO (6
mL/60 mL) foi adequada para tratar feridas de pitiose, por meio da técnica de
perfusão regional intravenosa do membro, independente do tamanho ou peso do
animal ou localização da ferida.
Figura 4. Ilustração da evolução da cicatrização de feridas de pitiose de equinos tratados com
anfotericina B e DMSO, aplicada pela técnica de perfusão regional intravenosa do membro,
na primeira avaliação (D0) e no último dia (D60) do período pós-operatório.
67
7 DISCUSSÃO
Foram empregados animais adultos e jovens, machos e fêmeas, com feridas
de localização em membro torácico ou pélvico, esquerdo ou direito, em posição
distal às articulações do cotovelo e joelho, de forma que houvesse espaço suficiente
para posicionamento do torniquete e que favorecesse a canulação de uma veia
distal a este, o mais próximo possível da ferida a ser perfundida. Com a perfusão
regional intravenosa do membro, buscou-se obter uma concentração elevada do
fármaco antimicótico (anfotericina B) e no local e nos tecidos circunvizinhos às
lesões, conforme descrito por Pille, Baere e Ceelen (2005). Deve-se destacar que,
além da exérese cirúrgica, outro fármaco foi administrado concomitantemente, o
dimetilsufóxido para aumentar a absorção dérmica.
Todos os animais desse estudo possuíam histórico de habitarem pastos com
áreas alagadiças, ambiente considerado como predisponente para que ocorra a
infecção pelo P. insidiosum. Sabe-se que a enfermidade causada por este “pseudofungo” quase que invariavelmente está localizada nos apêndices locomotores ou nas
partes baixas do corpo que entram em contato com o material vegetal submerso,
contaminado pelo “pseudo-fungo”, sendo os membros de equinos, a região
anatômica mais frequentemente acometida, pois ao adentrar os alagados para beber
água ou se alimentar de capim, na época chuvosa, como no Pantanal MatoGrossense, os animais adquirem a doença (MENDOZA; AJELLO; McGINIS, 1993;
SANTURIO; ALVES; PEREIRA, 2006).
Descrevemos o tratamento bem sucedido de pitiose em membros de cavalos
usando IRLP, ambos com anfotericina B e solução de DMSO em associação com a
excisão cirúrgica e termocautério. Nossos resultados estão em contraste com os
relatórios (CHAFFIN; SCHUMACHER; McMULLAN, 1992. ; FOIL, 1996; LEAL;
LEAL; SANTURIO, 2001; LEAL; LEAL; FLORES, 2001; SALLIS; PEREIRA; RAFFI,
2003; SANTURIO; ALVES; PEREIRA, 2006) anteriores e oferece um tratamento
eficaz para pitiose, da mesma forma como mostrado por Dória, Freitas e Linardi
(2012) , tecnicamente economicamente viável.
Infecção por P. insidiosum em membros equinos ainda representa um
desafio. A excisão cirúrgica tem sido combinada com a imunoterapia, e/ou terapia
sistêmica, intralesional, que estão ligadas a administração tópica de drogas
antifúngicas para melhorar a eficácia terapêutica (LEAL; LEAL; SANTURIO, 2001;
68
LEAL; LEAL; FREITAS, 2001; SANTURIO; ALVES; PEREIRA, 2006). Características
típicas de lesões pitiose tais como trombose local, isquemia, necrose do tecido e
formação de abscessos, diminuição fornecimento de sangue local, fornecem uma
concentração baixa do fármaco terapêutico o que diminui a eficácia para atingir o
organismo alvo (MARTINEZ, 2004; POOLE; BRASHIER, 2003; WHITEHAIR;
ADAMS; PARKER, 1992). Com isso, a administração sistêmica de anfotericina B
não resultar em concentrações terapeuticamente eficazes no local da infecção por P.
insidiosum, e ainda promove efeitos colaterais como nefrotoxicidade e anemia
(CHAPMAN; SULLIVAN; CLEARY, 2008; WORSTER; LILLICH; COX, 2000). No
entanto, IRLP demonstrou ser uma técnica eficaz para a obtenção de alta
concentração de fármaco nos tecidos (HARISS; GALUPO; VAN HOOMGMOED,
2002; MARTINEZ; CRUZ, 2006; MURPHEY; SANTICHI; PAPICH, 1999; PARRASANCHEZ; LUGO; BOOTHE, 2006; PILLE; BAERE; CEELEN, 2005; SCHEUCH;
VAN HOOMGMOED; WILSON, 2002; WHITEHAIR; ADAMS; PARKER, 1992,
WHITEHAIR, 1995), certamente, aumentando a eficácia terapêutica da anfotericina
B contra o agente. A morte se dá por inibição de processos metabólicos essenciais
do P. insidiosum (DÓRIA; FREITAS; LINARDI, 2012).
Tratamento sistêmico de pitiose tem sido relatada a ser marginalmente
eficaz quando as lesões estavam localizadas nos membros (FREY; VELHO; LINS,
2007). A incapacidade de reduzir completamente uma lesão, por causa de sua
proximidade com articulações ou ossos aumenta o desafio de tratar pitiose e
favorece a persistência da infecção. Segundo alguns autores, apenas pequenas
lesões e superficial pitiose podem ser tratadas com mais sucesso (FOIL, 1996;
FREY; VELHO; LINS, 2007; LEAL; LEAL; SANTURIO, 2001; LEAL; LEAL; FLORES,
2001). No entanto, Doria, Freitas e Linardi (2012) foram capazes de tratar com êxito
lesões pitiose independentemente do tamanho, por uma combinação de um
protocolo semelhante ao do nosso estudo, porém sem uso do DMSO. Do mesmo
modo, este estudo demonstra que a associação da anfotericina B e DMSO
proporciona melhores resultados uma vez que 100% de cavalos (15 cavalos)
mostraram resolução completa da lesão após uma única aplicação da técnica de
perfusão regional intravenosa, enfatizando que todos eles eram grandes lesões
circunvizinhas até 360 º da área afetada.
A excisão do tecido de granulação é importante para proporcionar uma
superfície apropriada para a cicatrização, porque a presença de tecido de
69
granulação exuberante é considerada um inibidor da mitose epitelial (FOSSUM et
al., 2002). No entanto, a excisão cirúrgica e termocautério não são suficientes para o
tratamento de infecções locais, com membros de P. insidiosum (DÓRIA; FREITAS;
LINARDI, 2012). Em situações excessivamente crônicas, há mais fibrose e tecido de
granulação, o que isola o oomiceto de mecanismos de defesa do organismo, bem
como de drogas antifúngicas administradas sistemicamente, mas uma concentração
elevada concentração ocorre na IRPL (WHITEHAIR; ADAMS; PARKER, 1992), tal
como demonstrado no presente estudo. Nos 15 cavalos tratados, com resolução
completa da lesão, não houve recorrência por até 1 ano, após o uso do presente
protocolo de tratamento, mesmo quando a excisão dos tecidos de granulação e
kunkers estava incompleta.
Em alguns casos podemos observar a resolução completa da infecção
pitiose, uma semana após o tratamento, observa-se tecido de granulação com
ausência de exsudato, fístulas ou kunkers e a tendência para epitelização nas
semanas subsequentes. O membro com infecção teve o período de cura relacionado
com o tamanho da lesão. Como podemos observar, quanto maior a lesão era, mais
tempo demora para cicatrizar completamente. Verificou-se que 27% das lesões
levaram 6 semanas para cicatrizar, sendo quatro lesões com dimensões de 90 º C.
Já 46% das lesões cicatrizaram com oito semanas, representados por sete lesões
que cercavam 180 º da área afetada e 27 % das lesões demoraram nove semanas
para cicatrizar, representado por quatro lesões que cercavam 360 º da área afetada.
Dória, Freitas e Linardi (2012) reportaram que a administração de anfotericina B por
perfusão regional intravenoso foi eficaz para tratar pitiose nos membros de equinos,
porém com efeitos colaterais manejáveis. A associação de anfotericina B e DMSO
proporcionou melhores resultados uma vez que um único IRLP foi eficaz para tratar
a infecção e não houve observação dos efeitos colaterais locais ou sistêmicos,
demonstrado no presente estudo, com a ajuda de perfis hematológicos e da
bioquímica do soro.
A presença de anemia em animais com pitiose cutânea esta associada à
redução de glóbulos vermelhos e o valor de PCV, como foram registrados nos
equinos antes do tratamento, entre outros fatores atribui-se a anemia a presença de
feridas exsudativa e prurido que levam à auto- mutilação, sangramento e ambiente
propício à infecção secundária (CHAFFIN; SCHUMACHER; McMULLAN, 1995;
FOIL, 1996; MEIRELES; RIET-CORREA; FISCHMAN, 1993; MENDOZA; AJELLO;
70
MCGINIS, 1996; POOLE; BRASHIER, 2003). O leucograma revelou uma leucocitose
marcado com neutrofilia e eosinofilia antes do tratamento. As maiores contagens de
neutrófilos no sangue foram para a remoção fagocítica dos produtos de degradação
do tecido ou P. insidiosum. Da mesma forma, Worster, Lillich e Cox (2000) e Sallis,
Pereira e Raffi (2003) mostraram leucocitose neutrofílica em cavalos com pitiose. A
eosinofilia observada foi devido à sensibilidade à proteína estranha de um parasita
que pode ser uma parte de um fenómeno imunológico (FELDMAN; ZINKL; JAIN,
2000). Os resultados do leucograma estavam de acordo com as descobertas de
outros (CHAFFIN; SCHUMACHER; McMULLAN, 1995; FOIL, 1996; MEIRELES;
RIET-CORREA; FISCHMAN, 1993, MENDOZA; AJELLO; MCGINIS, 1996; POOLE;
BRASHIER, 2003). Podemos observar em nosso estudo que o quadro hematológico
(inflamação) foi reestabelecido nos animais do grupo tratamento uma ou duas
semanas após o procedimento, o que de certa forma pode ser atribuído ao efeito da
administração IRLP com DMSO. Concentrações de proteínas de fase aguda no
plasma confirmou estes resultados demonstrados pelo decréscimo nos valores de
fibrinogênio após o tratamento. Quanto aos resultados bioquímicos, não foram
observadas alterações nas atividades das enzimas séricas (AST, GGT, ALP, uréia e
creatinina). Certificando a ausência dos efeitos colaterais sistêmicos, como as
alterações descritas para fígado e rins. Com isso, os resultados obtidos estiveram de
harmonia com descobertas anteriores que indicam que o aumento da concentração
de droga em perfusão regional, mantém a concentração plasmática abaixo do limite
de toxicidade. Estes avanços permitem um uso mais amplo de certos medicamentos
que
são
considerados
perigosos
e
dispendiosos,
quando
administrada
sistemicamente em cavalos, como é o caso da anfotericina B e DMSO (CHAPMAN;
SULLIVAN; CLEARY, 2008; DISMUKES, 2000; ERRICO; TRUMBLE; BUENO, 2008;
FILIPPIN; SOUZA, 2006; GILLIAM; STREETER; PAPICH, 2008; GOLD; STOUT;
PAGANO, 1956; MARTINEZ, 2004; VANDEPUTTE; WACHTEL; STILLER, 1956;
WERNER; HARDY; BERTONE, 2003).
Esta técnica foi considerada apropriada para o tratamento de pitiose sem
efeito local (espessamento da pele, celulitico, inflamação, edema, dor) ou (disfunção
hepática ou renal) colaterais sistêmicos. Embora seja esperado que a anfotericina B
poderia induzir a inflamação vascular no sítio da administração (DÓRIA; FREITAS;
LINARDI, 2012), DMSO por ser um potente antinflamatório que atua por limitação da
produção de radicais livres e por suprimir a produção de prostaglandina
71
(MCILWRHAITH, 2002; WELCH; WATKINS; DEBOWES, 1991). DMSO também
reduz a agregação de plaquetas e, portanto, reduz a incidência da formação de
trombos nos locais de anastomose dos pequenos vasos (BRAYTON, 1986). Essa
atividade ajuda a normalizar a perfusão tecidual em face dos insultos vasculares que
muitas vezes acompanham as condições sépticas da extremidade equina
(BRAYTON, 1986). DMSO também parece possuir atividade analgésica (ALSUP;
DEBOWES, 1984; WELCH; DEBOWES; LIEPOLD, 1989). Especula-se que os
efeitos bacteriostático e bactericida de DMSO pode ser provocada pela sua
capacidade para penetrar as membranas biológicas (ALSUP; DEBOWES, 1984;
BRAYTON, 1986).
Partimos do pressuposto de que, usando uma taxa de infusão apropriado, o
aumento da pressão intravascular favorece a difusão da droga através dos tecidos e
aumenta a concentração do fármaco nos tecidos-alvo (WHITEHAIR, 1995; HARRIS;
GALUPO; VAN HOOMGMOED, 2002; SCHEUCH; VAN HOOMGMOED; WILSON,
2002) e a associação DMSO aumentou a difusão da droga através dos tecidos
afetados proporcionando melhores resultados no que diz respeito do controle de
infecção pitiose. Em contraste com Dória, Freitas e Linardi (2012) o estudo, foi
possível observar que as características iniciais de feridas pitiose complicados não
foram associados com o sucesso do tratamento. Demonstramos que as lesões
maiores e mais invasivas em que a excisão cirúrgica completa não foi alcançada,
devido ao risco de expor o osso ou estruturas sinoviais, foram completamente
curada após uma única administração. Assim, os nossos resultados sugerem que
mesmo quando uma dose baixa de anfotericina B é administrada em associação
com DMSO por perfusão intravenosa do membro regional, o sucesso no tratamento
da pitiose em membros de equino é promissor.
72
8 CONCLUSÕES
Com base nos resultados obtidos, conclui-se que a administração de
anfotericina B e dimetilsufóxido por perfusão regional intravenosa nos membros de
eqüinos, em uma aplicação, associada à remoção cirúrgica, promove a remissão da
infecção por Pythium insidiosum, com nenhuma alteração sobre os tecidos
diretamente expostos ao fármaco, constituindo-se uma alternativa terapêutica, viável
e eficaz, para o tratamento de pitiose em membros de eqüinos, promovendo
cicatrização completa das feridas.Visto que é uma técnica vantajosa, principalmente
em questão de custo e também no caso do DMSO que diminui o tempo de
cicatrização sendo assim a associação do DMSO com anfotericina B se torna uma
técnica melhor que a já testada sem o uso do DMSO.
73
REFERÊNCIAS
ALSUP, E. M., DEBOWES, R. M. Dimethylsulfoxide. J Am Vet Med Assoc., n. 9,
p.1011-4, 1984.
BRAYTON, C. F. Dimethylsulfoxide (DMSO): a review. Cornell Vet., n. 76, p. 61-90,
1986.
BROWN, C. C. et al. Use of imunohistochemical methods for diagnosis equine
pytiosis. Am J Vet Res., n. 49, p. 1866-8, 1988.
CHAFFIN, M. K.; SCHUMACHER, J.; HOOPER, N. Multicentric cutaneous pythiosis
in a foal. J Am Vet Med Assoc., n. 201, p. 310-2, 1992.
CHAFFIN, M. K.; SCHUMACHER, J.; MCMULLAN, W. C. Cutaneous pythiosis in the
horse. Vet Clin North Am Equine Pract., n. 11, p. 91-103, 1995.
CHAPMAN, S. W.; SULLIVAN, D. C.; CLEARY, J. D. In search of the holy grail of
antifungal therapy. Trans Am Clin Climatol Assoc., n. 119, p. 197-216, 2008.
CIMETTI, L. J.; MERRIAM, J. G.; D’OENCH, S. N. How to perform intravenous
regional limb perfusion using amikacin and DMSO. In: ANNUAL CONVENTION OF
THE AMERICAN ASSOCIATION OF EQUINE PRACTITIONERS, 50., Denver
Colorado, 2004. Proccedings... Colorado, 2004. p. 1429-1204.
DE COCK, A. W. A. M.; MENDONZA, L.; PADHYE, A. A. Pythium insidiosum sp. The
etiologic agent of pythiosis. J Clin Microbiol., n. 25, p. 344-9, 1987.
DISMUKES, W. E. Introduction to antifungical drugs. Clin Infect Dis., n. 30, p. 653-7,
2000.
DÓRIA, R. G. S.; FREITAS, S. H.; LINARDI, R. L. Treatment of pythiosis in equine
limbs using intravenous regional perfusion of amphotericin B. Vet Surg., n. 41, p.
759-65, 2012.
ERRICO, J. A.; TRUMBLE, T. N.; BUENO, A. C. D. Comparison of two indirect
techniques for local delivery of a high dose of an antimicrobial in the distal portion of
forelimbs of horses. Am J Vet Res., n. 69, p. 334-42, 2008.
FEITOSA, F. L. F. Exame clínico geral ou de rotina. In:___. Semiologia veterinária:
a arte do diagnóstico. São Paulo: Roca, 2004. p. 29-45.
FELDMAN, B. F.; ZINKL, J. G.; JAIN, N. C. Schalm’s veterinary hematology. 5. th.
Philadelphia: Lippincott Williams and Wilkins, 2000. p. 1344.
FOIL, C. S. Update on pythiosis (Oomycosis). Orlando: Proc North American
Veterinary Conference, 2006. p. 57-63.
FOSSUM, T. W.; HEDLUND, C. S.; HULSE, D. A. Cirurgia do Sistema Tegumentar.
in: ______. Cirurgia de pequenos animais. São Paulo: Roca, 2002. p. 101-71.
FREY, J. R. F; VELHO, J. R.; LINS, L. A. Pitiose eqüina na região sul do Brasil.
74
Revista Portuguesa de Ciências Veterinárias, n. 102, p. 561-2, 2007.
GILLIAM, J. N.; STREETER, R. N.; PAPICH, M. G. Pharmacokinetics of florfenicol in
serum and synovial fluid after regional intravenous perfusion in the distal portion of
the hind limb of adult cows. Am J Vet Res., n. 69, p. 997-1004, 2008.
GIMENO, E. J.; MASSONE, A. R.; PORTIANSKY, E. L. Introducción a las técnicas
de inmunohistoquímica y aplicaciones en patología veterinaria. In: CURSO
INTERNACIONAL DE POSGRADO EN TECNICAS DE INMUNOHISTOQUIMICA,
Lectinhistoquimica y Microscopia Eletrônica, 10., La Plata, Argentina, 1999.
Proccedings... La Plata, 1999. p. 61-111.
GOLD, N.; STOUT, H. A.; PAGANO, J. F. Amphotericin A and B, antifungal
antibiotics produced by a streptomycete I. In vivo studies. Antibiot Annu., 1956, p.
579-86.
HARRIS, F. K.; GALUPO, L. D.; VAN HOOMGMOED, L. M. Antibiotic delivery to the
forelimb digital flexor tendon sheath and metacarpophalangeal joint of horses by
three regional limb perfusion techniques. In: ANNUAL CONFERENCE OF THE
VETERINARY ORTHOPEDIC SOCIETY, 29., Canyons, UT, 2002. Proccedings...
Canyons, 2002. p 63.
HENNEKE, D. R. et al. Relationship between condition score, physical
measurements and body fat percentage in mares. Equine Vet J., v. 15, n. 4, p. 371–
2, Oct. 2013.
LEAL, A. B. M.; LEAL, A. T.; SANTURIO, J. M. Pitiose eqüina no pantanal brasileiro:
aspectos clínicos patológicos de casos típicos e atípicos. Braz J Vet Res., n. 21, p.
151-6, 2001a.
LEAL, A. T.; LEAL, A. B. M.; FLORES, E. F. Pitiose. Ciência Rural, n. 31, p. 735-43,
2001b.
MARTINEZ, L. R. Valoración de la perfusion regional de la porción distal de la
extremidade anterior del caballo con vancomicina: estudio experimental. 2004.
Tesis (Doctoral) - Universidad Complutense de Madrid, 2004. Disponível em
<http://eprints.ucm.es/tesis/vet/ucm-t27455.pdf>. Acesso em: 10 jan. 2010.
MARTINEZ, L. R.; CRUZ, A. M. Antimicrobial regional limb perfusion in horses. J Am
Vet Med Assoc., n. 228, p. 706-712, 2006.
MCLLWRAITH, C. W. Diseases of joints, tendons, ligaments, and related
structures, in Stashak TS (ed): Adam’s lameness in horses. 5. ed. Philadelphia:
Lippincott Williams & Wilkins, 2002. p. 459-644.
MEIRELES, M. C. A.; RIET-CORREA, F.; FISCHMAN, O. Cutaneous pytiosis in
horses from Brazil. Mycoses, n. 36, p. 139-42, 1993.
MENDOZA, L.; AJELLO, L.; MCGINIS, M. R. Infections caused by the oomycetus
pathogen Pythium insidiosum. J Med Microbiol., n. 6, p. 151-64, 1996.
MURPHEY, E. D.; SANTICHI, E. M.; PAPICH, M. G. Regional intravenous perfusion
75
of the distal limb of horses with amikacin sulfate. J Vet Pharmacol Ther., n. 22, p.6877, 1999.
PARRA-SANCHEZ, A.; LUGO, J; BOOTHE, D. M. Pharmacokinetics and
pharmacodynamics of enrofloxacin and low dose of amikacin administered via
regional intravenous limb perfusion in standing horses. Am J Vet Res., n. 67, p.
1687-95, 2006.
PEDROSO, P. et al. Diagnóstico imunoistoquímico de pitiose cutânea em equinos.
Act Sci Vet., v. 37, n. 1, p. 49-52, 2009.
PILLE, F.; BAERE, S.; CEELEN, L. Synovial fluid and plasma concentrations of
ceftiofur after regional intravenous perfusion in the horse. Vet Surg., n. 34, p. 610-7,
2005.
POOLE, H. M.; BRASHIER, M. K. Equine cutaneous pythiosis. Compendium on
Continuing Education for the Practicing Veterinarian, n. 25, p. 229-36, 2003.
RICHARDSON, M. D.; WARNOCK, D. W. Antifungal Drugs. In: ______. Fungal
Infection: diagnosis and management. 3. ed. Oxford, UK: Blackwell, 2003. p. 29-79.
SALLIS, E. S. V.; PEREIRA, D. I. B.; RAFFI, M. R. Pitiose cutânea em eqüinos: 14
casos. Ciência Rural, n. 33, p. 899-903, 2003.
SANTISCHI, E. M.; ADAMS, S. D.; MURPHEY, E. D. How to perform equine
intravenous digital perfusion. In: ANNUAL CONVENTION OF THE AMERICAN
ASSOCIATION OF EQUINE PRACTITIONERS, 44., Baltimore MD, 1998.
Proccedings... 1998. p. 198-201.
SANTURIO, J. M.; ALVES, S. H.; PEREIRA, D. B. Pitiose: uma micose emergente.
Acta Scient Vet., n. 34, p. 1-14, 2006.
SCHEUCH, B. C.; VAN HOOMGMOED, L. M; WILSON, W. D. Comparison of
intraosseous or intravenous infusion for delivery of amikacin sulfate to the tibiotarsal
joint of horses. Am J Vet Res., n. 63, p. 374-80, 2002.
THOMASSIAN, A. Afecções da pele. In: ____. Enfermidades dos cavalos. 4. ed.
São Paulo: Varela, 2005. p. 39-41.
UBIALI, D. G. et al. Pathology of nasal infection caused by Conidiobolus lamprauges
and Pythium insidiosum in sheep. J Comp Pathol., v. 149, n. 2-3, p. 137-45, 2013.
VANDEPUTTE, J.; WACHTEL, J. L.; STILLER, E. T. Amphotericin A and B antifungal
antibiotics produced by a Streptomycete. II. The isolation and properties of the
crystalline amphotericins. Antibiot Annu., n. 1955-1956, p. 587-591, 1956.
WELCH, R. D.; DEBOWES, R. M.; LIEPOLD, H. W. Evaluation of the effects of intraarticular injection of dimethylsulfoxide on normal equine articular tissues. Am J Vet
Res., n. 50, p. 1180-2, 1989.
WELCH, R. D.; WATKINS, J. P.; DEBOWES, R. M. Effects of intra-articular
administration of dimethylsulfoxide on chemically induced synovitits in immature
76
horses. Am J Vet Res., n. 52, p. 934-9, 1991.
WERNER, L. A.; HARDY, J.; BERTONE, A. L. Bone gentamicin concentration after
intra-articular injection or regional intravenous perfusion in the horse. Vet Surg., n.
32, p. 559-65, 2003.
WHITEHAIR, K. J.; ADAMS, S. B.; PARKER, J. E. Regional limb perfusion with
antibiotics in three horses. Vet Surg., n. 21, p. 286-92, 1992.
WHITEHAIR, K. J.; BOWERSOCK, T. L.; BLEVIS, W. E. Regional limb perfusion for
antibiotic treatment of experimentally induced septic arthritis. Vet Surg., n. 5, p. 36773, 1992.
WHITEHAIR, K. L: Regional limb perfusion with antibiotics. In: ANNUAL AMERICAN
COLLEGE VETERINARY SURGEONS SYMPOSIUM, 5., Chicago IL, 1995.
Proccedings... Chicago, 1995. p. 59.
WOSTER, A. A.; LILLICH, J. D.; COX, J. H. Pythiosis with bone lesions in a pregnant
mare. J Am Vet Med Assoc., n. 216, p. 1795-8, 2000.
77
APÊNDICE
78
APÊNDIA A - Discriminação das cidades de origem, raça, sexo, idade e peso (kg)
dos equinos que foram tratados com anfotericina b e dmso,
aplicada pela técnica de perfusão regional intravenosa do membro
e dos equinos do grupo controle
Animal
01
02
03
04
05
06
07
08
Município
Poconé
Poconé
Cuiabá
Cuiabá
Poconé
Poconé
Poconé
Cuiabá
Raça
Pantaneira
Pantaneira
SRD
SRD
Pantaneira
Pantaneira
Pantaneira
Quarto de
Milha
Quarto de
Milha
SRD
Sexo
Fêmea
Fêmea
Macho
Macho
Fêmea
Fêmea
Fêmea
Macho
Idade
4 meses
4 meses
12 anos
3 anos
7 meses
3 anos
2 anos
3 anos
Peso
140 Kg
140 Kg
330 Kg
300 Kg
156 Kg
325 Kg
230 Kg
320 kg
Macho
3 anos
320 Kg
Macho
4 anos
300Kg
Macho
7 anos
320 Kg
Macho
4 anos
300 Kg
09
Cuiabá
10
Cuiabá
11
Poconé
12
Poconé
Quarto de
Milha
Pantaneira
13
Poconé
Pantaneira
Macho
5 anos
320 Kg
14
Poconé
Pantaneira
Macho
3 anos
280 Kg
15
Cuiabá
Poconé
Pantaneira
Macho
Macho
2 anos
2 anos
200
Varzea
Grande
Cuiabá
Pantaneira
Fêmea
8 anos
250
Pantaneira
Macho
11 anos
300
Poconé
Pantaneira
Fêmea
14 anos
450
16
(controle)
17
(controle)
18
(controle)
19
(controle)
Legenda: SRD sem raça definida.