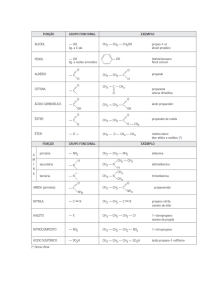
ISOMERIA - I
OH
CH2
O estudo de isomeria é dividido em duas
partes:
Isomeria Plana: onde a visualização dos
isômeros ocorre na forma plana das
moléculas.
Isomeria espacial: onde a visualização dos
isômeros ocorre na forma espacial da
molécula, por tanto sendo mais difícil para
o aluno e por isso veremos alguns casos
restritos.
Isomeria: É quando conpostos diferentes
apresentam a mesma fórmula molecular:
Exemplo:
A fórmula molecular do 2-penteno é de C5
H10 e a fórmula molecular do ciclo-pentano
C5 H10 .
H3C – CH = CH – CH2 – CH3
CH2
/ \
H 2C
CH2
|
|
H2C – CH2
C5 H10
C5 H10
CH3
Álcool benzílico
metil-benzeno
C7 H8 O
1-hidróxi-2C7 H8 O
Isomeria de Cadeia: Os compostos
pertencem
a
mesma
função
mas
apresentam cadeias diferentes.
Exemplo:
H2C – CH – CH2 – CH3 e H3C – CH2 – CH2 –
CH2 – CH3
|
CH3
C5 H12
C5
H12
2-metil-butano
pentano
cadeia
aberta,
ramificada,
cadeia aberta,
saturada
e
homogênea
normal,
saturada e
homogênea
Isomeria plana:
Ocorre de quatro formas:
H2C = CH – CH2 – CH3
Isomeria de Função: Os compostos diferem
pela função orgânica. Os principais
isômeros de função são:
Álcool e éter
Álcool aromático e fenol
Aldeido e cetona
Ácidos carboxílicos e éster
Exemplo:
H3C – CH2 – OH
etanol
C2 H6 O
OH
e H3C – O – CH3
metóximetano
C2 H6 O
H3C – CH2 – C = O
|
H
propanal
C3 H6 O
H3C – CH2 – C = O
|
OH
Ácido propanóico
metila
C3 H6 O2
e H3C – C – CH3
||
O
propanona
C3 H6 O
H3C – C – O – CH3
||
O
etanoato de
C3 H6 O2
2-buteno C4 H8
C4 H8
cadeia aberta, normal,
fechada,
insaturada
e
normal,
ciclo-butano
cadeia
homogênea
saturada
e
homogênea
Isomeria de Posição: Os compostos
pertencem a mesma função, apresentam a
mesma cadeia mas se diferenciam pela
posição de um radical, grupo funcional ou
insaturação.
Exemplo:
H3C – CH – CH2 – CH2 – CH3 e
CH2 – CH3
|
CH3
2-metil-pentano C6 H14
C6 H14
H3C – CH2 – CH – CH2
CH2
|
|
H3C – CH2 – CH –
|
CH3
3-metil-pentano
e H3C – CH2 – CH2 –
OH
OH
2-butanol
H10 O
cetona
enol
cetoenólica
C4 H10 O
1-butanol
C4
ISOMERIA - II
H2C = CH – CH2 – CH3
CH3
C4 H8
1- buteno
e H3C – CH = CH –
C4 H8
2-buteno
Isomeria de Compensação ou Metameria:
ocorre em compostos que apresentam a
mesmo função, a mesma cadeia e se
caracteriza pelo deslocamento de um
heteroátomo.
Obs: a isomeria de compensação só ocorre
em cadeias heterogêneas, ou seja, ocorre
entre os compostos das funções éter, éster
e aminas secundárias e terciárias.
Exemplo:
H3C – CH2 – O – CH2 – CH3 e H3C – O – CH2 – CH2
– CH3
C4 H10 O
etóxietano
metóxipropano
H3C – NH – CH2 – CH2 – CH3 e H3C – CH2 – NH –
CH2 – CH3
C4 H11 N
dietilamina
Tautomeria:
É um caso particular de isomeria de função
onde os compostos coexistem. Existem dois
tipos de tautomeria:
Aldoenólica ocorre entre aldeido e enol.
Cetoenólica ocorre entre cetona e enol.
Exemplo:
H3C – C = O
H2C = CH
|
|
H
OH
etanal
etenol
aldeido
enol
aldoenólica
H3C – C – CH3
CH2
||
O
propanona
Ou
Em cadeias fechadas.
C4 H10 O
H3C – C – O – CH3 e HC – O – CH2 – CH3
||
||
O C3 H6 O2
O C3 H6 O2
etanoato de metila
metanoato de
etila
C4 H11 N
metil-n-propilamina
Isomeria Espacial:
Somente vista no espaço, ocorre de dois
tipos:
Isomeria Geométrica:
Ocorre
em
compostos
de
cadeia
insaturada por uma dupla ligação e que
apresente ligantes diferentes no carbono
da dupla ligação.
H3C – C =
|
OH
propenol
ISOMERIA - III
Isomeria Ótica:
Ocorre quando o composto apresenta
carbono assimétrico.
A isomeria ótica ocorre pelo desvio do
plano da luz polarizada.
Dextrógero desvia o plano da luz
polarizada para a direita. Isômero ativo.
Levógero desvia o plano da luz
polarizada para a esquerda. Isômero ativo
O
dextrógero
e
o
levógero
são
enantiomorfos ou enantiômeros, ou seja, um
é a imagem especular do outro.
Racêmico É a soma de um dextrógero
com um levógero, o racêmico não
apresenta desvio no plano da luz
polarizada e é o isômero inativo.
Carbono Assimétrico apresenta quatro
ligantes diferentes.
R1
|
R2 – C – R4
|
R3
R1
R1
C*
C*
R4
R2
R4
R2
R3
dextrógiro
R3
levógiro
Número de Isômeros Ativos:
N1a = 2n onde n é o número de carbonos
assimétricos.
Número de Isômeros Inativos ( Racêmicos ):
NR = 2n - 1 onde n é o número de carbonos
assimétricos.
Obs: O número de racêmicos é sempre a
metade do número de isômeros ativos.
Exemplo:
Para o composto a seguir:
H CH3 OH
|
|
|
H3C – C* -- C* -- C* -- CH3
|
|
|
OH H
F
I.
Existem 3 carbonos assimétricos, assim n = 3.
Logo: Nia = 2n :. Nia = 23 :. Nia = 8
Existindo 8 isômeros ativos é porque 4 são
dextrógeros e 4 são levógeros.
O número de isômeros ativos?
II. O número de racêmicos ?
NR = 2n-1 :. NR = 23-1 :. NR = 22 :. NR = 4
Existem 4 isômeros racêmicos, o que já era
previsto se existem 8 isômeros ativos, dos
quais 4 são dextrógeros e 4 são levógeros só
são possíveis 4 misturas de pares dextrógero
e levógero o que resulta em 4 misturas
racêmicas. O que nos faz concluir que o
número de isômeros inativos é sempre a
metade do número de isômeros ativos.
III. O número de isômeros óticos?
É a soma dos isômeros ativos com os
isômeros inativos.
Logo: NO = 12
Isômero Meso:
Ocorre quando existem
assimétricos iguais.
dois
carbonos
Exemplo:
A molécula do ácido tatárico.
Apresenta um dextrógiro, um levógiro, um
meso e um racêrmico.