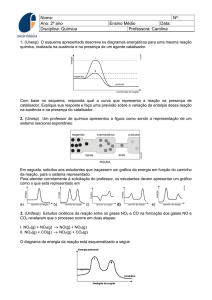
1) Alguns medicamentos de natureza ácida, como vitamina C (ácido ascórbico) e aspirina
(ácido acetilsalicílico), são consumidos na forma de comprimidos efervescentes. Um
professor partiu desse acontecimento cotidiano para demonstrar a influência de certos
fatores na velocidade de reação (ver figura abaixo). Primeiramente (I), pediu que os alunos
medissem o tempo de dissolução de um comprimido efervescente inteiro num copo de água
natural (25°C). Em seguida (II), sugeriu que repetissem a experiência, usando um
comprimido inteiro, num copo de água gelada (5°C). Finalmente (III), recomendou que
utilizassem um comprimido partido em vários pedaços, num copo de água natural (25°C).
Os estudantes observaram que, em relação ao resultado do primeiro experimento, os tempos
de reação do segundo e do terceiro foram, respectivamente:
a) menor e maior;
b) menor e igual;
c) maior e igual;
d) maior e menor;
e) NDA.
2) O estudo cinético, em fase gasosa, da reação representada por:
NO2 + CO → CO2 + NO
Mostrou que a velocidade da reação não depende da concentração de CO, mas depende da
concentração de NO2 elevada ao quadrado. Esse resultado permite afirmar que:
a) o CO atua como catalisador.
b) o CO é desnecessário para a conversão de NO2 em NO.
c) o NO2 atua como catalisador.
d) a reação deve ocorrer em mais de uma etapa.
e) a velocidade da reação dobra se a concentração inicial de NO2 for duplicada.
3) O gráfico a seguir refere-se ao diagrama energético de uma reação química
(reagentes→produtos), onde se vêem destacados dois caminhos de reação:
Após uma analise das entalpias dos reagentes, dos produtos e dos valores a, b, c e d,
podemos afirmar que:
a) reação é endotérmica e a presença do catalisador diminuiu o ΔH de a para b;
b) reação é endotérmica e a representa o ΔH com a presença do catalisador;
c) reação é exotérmica e a energia de ativação, sem a presença do catalisador, é
representada por c;
d) presença do catalisador diminuiu o ΔH da reação representada por c;
e) presença do catalisador diminuiu a energia de ativação de a para b e mantém constante o
ΔH da reação representada por d.
Cinética 2
4) No início do século XX, a expectativa da Primeira Guerra Mundial gerou uma grande
necessidade de compostos nitrogenados. Haber foi o pioneiro na produção de amônia, a
partir do nitrogênio do ar. Se a amônia for colocada num recipiente fechado, sua
decomposição ocorre de acordo com a seguinte equação química não balanceada:
2NH3(g) → N2(g) + 3H2(g).
As variações das concentrações com o tempo estão ilustradas na figura a seguir:
A partir da análise da figura acima, podemos afirmar que as curvas A, B e C representam a
variação temporal das concentrações dos seguintes componentes da reação,
respectivamente:
a) H2, N2 e NH3
b) NH3, H2 e N2
c) NH3, N2 e H2
d) N2, H2 e NH3
e) H2, NH3 e N2
6) (FUVEST/SP) Foram realizados quatro experimentos. Cada um deles consistiu na adição
de solução aquosa de ácido sulfúrico de concentração 1mol/L a certa massa de ferro. A
25°C e 1 atm, mediram-se os volumes de hidrogênio desprendido em função do tempo. No
final de cada experimento, sempre sobrou ferro que não reagiu. A tabela mostra o tipo de
ferro usado em cada experimento, a temperatura e o volume da solução de ácido sulfúrico
usado. O gráfico mostra os resultados.
As curvas 1 a 4 correspondem, respectivamente, aos experimentos:
a)
b)
c)
d)
e)
1
D
D
B
C
C
2
C
C
A
D
D
3
A
B
C
A
B
4
B
A
D
B
A
7) (UFRN/RN) O peróxido de hidrogênio em solução é conhecido como água oxigenada e é
utilizado como antisséptico. Essa substância se decompõe, como mostra a equação:
H2O2(aq) → H2O(l) + 1/2 O2(g)
Num laboratório, a tabela foi obtida a partir de concentração de peróxido reagente versus
tempo de reação.
a) Calcule as velocidades médias de reação nos intervalos 1-2 e 2-3 e explique por que os
valores são diferentes.
b) Explique por que, adicionando-se pequena quantidade de dióxido de manganês (MnO2)
sólido à solução aquosa de peróxido de hidrogênio, o tempo de reação diminui.
8) (UFSC/SC) A combustão do dióxido de enxofre é uma etapa intermediária na fabricação
de ácido sulfúrico. Essa reação se processa de acordo com a equação I:
2 SO2 (g) + 1 O2 (g) → 2 SO3 (g) + 198 kJ (I)
À temperatura ambiente, o dióxido de enxofre é oxidado muito lentamente pelo oxigênio.
Porém, na presença de monóxido de nitrogênio, a reação se processa rapidamente, de
acordo com as equações II e III:
2 NO (g) + 1 O2 (g) → 2 NO2 (g) (II)
2 SO2 (g) + 2 NO2 (g) → 2 SO3 (g) + 2 NO(g) (III)
Com relação às informações do enunciado, é CORRETO afirmar que:
(01) A concentração de monóxido de nitrogênio durante a formação do SO3 é constante.
(02) O monóxido de nitrogênio atua como inibidor.
(04) A adição de catalisador altera a entalpia da reação.
(08) A formação do SO3, à temperatura ambiente e na ausência de monóxido de nitrogênio,
é um processo cineticamente desfavorável.
(16) A formação do SO3 é um processo endotérmico.
(32) O monóxido de nitrogênio atua como catalisador diminuindo a energia de ativação da
reação.