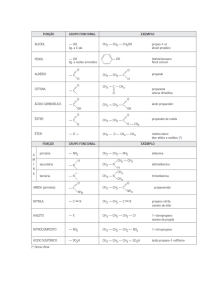
01) Um isômero do éter CH3OCH3 é o:
a) ácido acético.
Fórmula molecular do éter
b) éter dietílico.
C2H6O
c) propanol.
d) etanol.
e) etano.
éter
dietílico
propanol
etanol
ácido
acético
O
H3CH–3CCH
2–
2––OH
CH3
H–H
3C
CH
2O
CH
–C–CH
2CH
– 2OH
3C– –
OH
Fórmula molecular
Fórmula
Fórmula molecular
molecular
C4H10O
C232H486O2
02) Indique, dentre as alternativas a seguir, a que apresenta um
hidrocarboneto isômero do 2, 2, 4 – trimetil – pentano.
a) octano.
b) pentano.
2, 2, 4 – trimetil – pentano
c) propano.
CH3
d) butano.
e) nonano.
H3C – C – CH2 – CH – CH3
CH3
Pág. 558
Ex. 05
CH3
Fórmula molecular
C8H18
octano
H3C – CH2 – CH2 – CH2 – CH2 – CH2 – CH2 – CH3
Fórmula molecular
C8H18
03) Os compostos etanol e éter dimetílico demonstram
que caso de isomeria?
a) Cadeia.
b) Posição.
c) Compensação.
d) Função.
e) Tautomeria.
Por pertencerem à funções
químicas diferentes
são
ISÔMEROS DE FUNÇÃO
04) Os compostos etóxi – propano e metóxi – butano
apresentam:
a) isomeria de cadeia.
b) isomeria de posição.
c) isomeria de compensação.
diferem na posição do
d) isomeria funcional.
HETEROÁTOMO
e) tautomeria.
etóxi – propano
H3C
CH2
O
CH2
CH2
CH3
CH2
CH3
metóxi – butano
H3C
O
CH2
CH2
05) A, B e C têm a mesma fórmula molecular: C3H8O.
“A” tem um hidrogênio em carbono secundário e é
isômero de posição de “B”. Tanto “A” como “B” são
isômeros de função de “C”. Escreva as fórmulas
estruturais e os nomes de A, B e C.
Os compostos “A” e “B” são álcoois
H3C
CH
CH3
H3C
CH2
1 – propanol
OH
2 – propanol
O isômero de função do álcool é um ÉTER
H3C
O
CH2
metoxi – etano
CH3
CH2
OH
06) (PUC-RS) O propeno e o ciclopropano são representados,
respectivamente, pelas fórmulas:
CH2
CH2
CH
CH3
H2C
CH2
Pela análise dessas substâncias, pode-se afirmar que:
a) são polares.
b) são isômeros de cadeia.
c) apresentam diferentes massas moleculares.
d) apresentam mesma classificação de átomos de carbono.
e) apresentam diferentes tipos de ligação entre os átomos.
Pág. 558
Ex. 02
07) (PUC-MG)“A 4-metil-2-pentanona é usada como solvente
na produção de tintas, ataca o sistema nervoso central,
irrita os olhos e provoca dor de cabeça”.
O composto citado é isômero funcional de:
a) 1 – hexanol.
b) hexanal
c) 4 – metil – butanal.
Pág. 558
Ex. 04
4 – metil – 2 – pentanona
H3C – CH – CH2 – C – CH3
d) 4 – metil – 1 – pentanol
CH3
e) pentanona.
O
Fórmula molecular
C6H12O
hexanal
H3C – CH2 – CH2 – CH
2 – CH2 – CH2
1 2– –hexanol
H3C – CH2 – CH
CH2 – CH2 – C
O
OH
H
Fórmula
Fórmulamolecular
molecular
CC6H
1412
OO
6H
08) Entre os compostos abaixo ocorre isomeria:
H3C – C – CH3
O
a) de posição.
b) de cadeia.
c) cis-trans.
d) tautomeria.
e) óptica
e
H2C = C – CH3
OH
09) (UPE-2007–Q1) Analise o equilíbrio representado pela equação
química abaixo:
HH
3C3C
O
C CHO
H
H2C
H2C
Em relação ao conceito de isomeria, é verdadeiro afirmar que o
equilíbrio:
a) não exemplifica caso de isomeria.
b) exemplifica um caso de isomeria de cadeia entre alcenos.
c) apenas evidencia a mudança da fórmula estrutural do etanal
para a cetona.
d) evidencia um caso particular de isomeria funcional conhecido
com o nome de tautomeria.
e) evidencia tão somente o efeito ressonante entre álcoois
insaturados.
OH
CH2O
CH
É quando os isômeros apresentam
as ligações entre seus átomos
dispostas de maneira diferente no espaço
Existem dois tipos de isomeria espacial
Isomeria geométrica ou cis-trans.
Isomeria óptica.
Pode ocorrer em dois casos principais:
Em compostos com duplas ligações.
Em compostos cíclicos.
Nos compostos com duplas ligações
deveremos ter a seguinte estrutura:
R1
R3
C=C
R2
R1
R4
R2
e
R3
R4
CH3
CH3
CH3
C=C
H
CIS
C=C
H
A estrutura que apresentar
os átomos de hidrogênio no
mesmo lado do plano é a
forma
CIS
H
H
TRANS
CH3
A estrutura que apresentar os
átomos de hidrogênio em
lados opostos do plano é a
forma TRANS
Nos compostos cíclicos a isomeria cis-trans é observada quando
aparecerem
grupos ligantes diferentes em dois carbonos do ciclo
H
H3C
CH3
H
TRANS
H3C
CH3
H
H
CIS
No caso de não existirem dois
átomos de hidrogênio nos carbonos da dupla ligação
A IUPAC recomenda a utilização dos
prefixos Z e E
Z: zusammen (juntos)
E: entgegen (opostos)
O composto que apresentar, do mesmo lado
do plano imaginário, os ligantes
do carbono com os maiores números atômicos (Z),
será denominado “Z”
o outro será o “E”
Cl
Z=6
H3C
Z=6
C
C
Cl
H
Z = 17
H3C
CH3
CH3
C
C
H
Z-2-clorobut-2-eno
H3C
CH3
C
Z=1
C
Cl
H
E-2-clorobut-2-eno
01) Dados os seguintes compostos orgânicos:
I. (CH3)2C = CCl2
III. CH3ClC = CClCH3
II. (CH3)2C = CClCH3
IV. CH3FC = CClCH3
Assinale a opção correta:
a) Os compostos I e III são isômeros geométricos.
b) Os compostos II e III são isômeros geométricos.
c) O composto II é o único que apresenta isomeria
geométrica.
d) Os compostos III e IV são os únicos que apresentam
isomeria geométrica.
e) Todos os compostos apresentam isomeria geométrica.
02) (UESC) Admite isomeria geométrica, o alceno:
a) 2, 3 – dimetil – 2 – penteno
b) 1 – penteno
c) 3 – metil – 3 – hexeno
d) eteno.
e) 4 – etil – 3 – metil – 3 – hexeno
2, 3 3– –dimetil
1metil
– penteno
penteno
– 32 – hexeno
HH3H
C3C C CH2C
C
H
CH2CH
2 2
C CH
C 2 C CH
H 3 CHCH
3 3 H
CH
CH3CH
3 3
CH
03) Apresenta isomeria cis-trans:
a) 1 – buteno.
b) 2 – metil – 2 – buteno.
c) 2 , 3 – dimetil – 2 – buteno.
d) 1 , 1 – dimetil – ciclobutano.
e) 1 , 2 – dimetil – ciclobutano.
2,132––dimetil
dimetil
metil
1 –––buteno
–2ciclobutano
2– –buteno
buteno
1, 2 – dimetil – 1,
ciclobutano
H2 C
H2 2C
C H2
H
C
C
CH
CH
3
H3H
C33CC
H
H
H
CC
CC
CH
CH33
C C H2
C
C
H
H CH
CH33 CH
H3
CH3
CH3 CH3
C H2
04)(UESC) Admite isomeria geométrica, o alceno:
a) 2, 3 – dimetil – 2 – penteno.
b) 1 – penteno.
c) 3 – metil – 3 – hexeno.
d) eteno.
e) 4 – etil – 3 – metil – 3 – hexeno.
2, 3 –3 dimetil
– metil
1 –– penteno
23 – penteno
hexeno
H3H
C H3CCCH2 C
C
H
C CH
2 2 CH
CH
3 3
C 2 C CHCH
2 CH
3CH
H
CH3CH3CH3H
05) (U.DE UBERABA-MG) As balas e as gomas de mascar com sabor
de canela contêm o composto cinamaldeído (ou aldeído cinâmico)
que apresenta a fórmula estrutural abaixo.
O
H
2
1
3
H
H
O nome oficial deste composto orgânico é:
a) trans – 3 – fenil propenal.
b) trans – 1 – fenil propenal.
c) trans – 3 – fenil propanal.
d) trans – 3 – benzil propenal.
e) cis – 3 – fenil propenal.
trans
- 3 - fenil
propenal
06) (Covest-2006) O óleo de soja, comumente utilizado na cozinha, contém
diversos triglicerídeos (gorduras), provenientes de diversos ácidos graxos,
dentre os quais temos os mostrados abaixo. Sobre esses compostos,
podemos afirmar que:
a) o composto 4 é um ácido carboxílico
de cadeia aberta contendo duas duplas
ligações conjugadas entre si.
FALSO
b) os compostos 2 e 3 são isômeros cis-trans.
VERDADEIRO
c) o composto 1 é um ácido carboxílico de
cadeia insaturada.
CH 3 ( CH 2 ) 16 COOH
(1)
CH 3 ( CH 2 ) 7
H
e) o composto 3 é um ácido graxo de cadeia
fechada contendo uma insaturação (cis).
( CH 2 ) 7 COOH
(2)
CH 3 ( CH 2 ) 7
H
CH 3 ( CH 2 ) 4
H
d) o composto 2 é um ácido graxo de cadeia
aberta contendo uma dupla ligação (cis).
H
( CH 2 ) 7 COOH
H
(3)
CH 2
H
H
( CH 2 ) 7 COOH
H
(4)
É um ácido carboxílico de
cadeia aberta com duas
duplas ligações
ALTERNADAS
Luz natural é um conjunto de ondas
eletromagnéticas que vibram em vários planos,
perpendiculares à direção de propagação do feixe
luminoso
Luz polarizada é um conjunto de ondas
eletromagnéticas que vibram ao longo de um
único plano
É possível obter uma luz polarizada fazendo a luz
natural atravessar uma substância polarizadora,
como o prisma de Nicol
(dois cristais de CaCO3 cortados em forma de prisma e
colados com
bálsamo-do-canadá para não interferir no caminho da
luz) ou ainda uma lente polaróide
Chamamos de dextrógira
Algumas substâncias são capazes de provocar um
a substância que desvia o plano de vibração da luz
desvio no plano da luz polarizada
polarizada para a direita
e a representamos por “d” ou (+).
Será levógira a substância que desvia
Estas substâncias
o plano de vibração da
possuem atividade óptica
luz polarizada para a esquerda
(opticamente ativas)
e a representamos por “l” ou ( – ).
A mistura em partes iguais
As formas dextrógira e levógira, que correspondem
dos antípodas ópticos fornece por compensação
uma a imagem da outra, foram chamadas
dos efeitos contrários um conjunto opticamente
antípodas ópticos ou enantiomorfos
inativo, que foi chamado mistura racêmica
As substâncias assimétricas
possuem
atividade óptica
A estrutura orgânica que tem carbono
assimétrico
possuirá atividade óptica (opticamente
ativa)
É o átomo de carbono que
possui quatro ligantes diferentes entre si
Oscomo
quatroo grupos
ligados
composto
temao
H
OH
carbono
destaque são
carbonoemassimétrico,
diferentes entre si
H
C
C
H
Cl
H
ele apresenta
ATIVIDADE ÓPTICA
Este carbono é
ASSIMÉTRICO
Para uma substância orgânica, com carbono assimétrico,
o número de isômeros ativos e inativos
é dado pelas expressões:
número de isômeros ativos
número de isômeros inativos
2
2
n
n–1
“n” é o número de carbonos assimétricos
H
H
OH
C
C
H
Cl
H
tem um carbono assimétricos n = 1.
2
2
n–1
= 2
1n
= 2 isômeros ativos
1–1
= 2
0
= 1 isômero inativo
01) Na estrutura abaixo, quando se substitui “ R ” por
alguns radicais, o composto adquire atividade óptica.
Qual dos itens indica corretamente esses radicais?
R 2
CH
H3C
C
CH
R 2
a) metil e etil.
b) metil e propil.
c) etil e propil.
d) dois radicais metil.
e) dois radicais etil.
CH3
COOH
CH2
CH3
02) (FAFI – MG) Em relação ao ácido lático, cujas fórmulas espaciais estão
representadas abaixo, estão corretas as opções, exceto:
COOH
H
COOH
COOH
OH HO
CH3
H
H
COOH
OH
H
HO
CH3
(I)
espelho
CH3
ácido lático – ácido – 2 – hidroxipropanóico
a) Possui átomo de carbono assimétrico.
b) Possui atividade óptica.
c) Apresenta carboxila e oxidrila (hidroxila).
d) Possui isomeria cis-trans.
e) As suas estruturas não são superponíveis.
( II )
espelho
CH3
03) (UPE-2007 – Q2) Analise as estruturas I, II, III e IV, abaixo.
CH2OH
H
OH
CH2OH
OH
H
CH3
CH3
(I)
(II)
CH2OH
H
OH
CH2OH
(III)
É correto afirmar que
a) somente as estruturas I e II apresentam isomeria ótica.
b) somente as estruturas I e III apresentam atividade ótica.
c) somente as estruturas III e IV apresentam atividade ótica.
d) somente as estruturas I e IV apresentam isomeria ótica.
e) todas apresentam atividade ótica.
CH2OH
OH
H
CH2OH
(IV)
04) (Covest – 2005) Diversos compostos orgânicos são responsáveis pelo
odor de vários alimentos. Dentre eles, podemos citar:
A partir das estruturas acima pode-se afirmar que:
0 0 A nomenclatura do composto orgânico responsável pelo aroma da
canela, é 3 – fenilpropanal.
1 1 A cicloexilamina possui um centro estereogênico (quiral).
2
3
2 O acetato de octila, responsável pelo aroma da laranja, apresenta
uma função éter.
3 O composto responsável pelo aroma da baunilha, apresenta as
funções fenol, aldeído e éter.
4 4 O composto responsável pelo aroma da canela, pode apresentar
isomeria cis-trans.
05) (UPE-2006-Q2) Analise as afirmativas acerca dos diversos compostos
orgânicos e suas propriedades e assinale-as devidamente.
F 0 0 Os compostos butanal e metilpropanal exemplificam um caso de
isomeria espacial
O
O
F 1 1 Os isômeros de posição pertencem à mesma função orgânica e
H3Cpossuem
3C
C
C
CH2a mesma
CH2 cadeia,
mas diferem Hentre
si CH
apenas quanto
à
H
H
posição do heteroátomo
V 22
3
ISÔMEROS DE POSIÇÃO PERTENCEM À MESMA FUNÇÃOCH
ORGÂNICA
SÃO ISÔMEROS
DE isômero
CADEIA
Um hidrocarboneto
cíclico
pode
ser
dePELA
umPOSIÇÃO
hidrocarboneto
E TÊM A MESMA CADEIA,
MAS
DIFEREM
ENTRE SI
DE UM RADICAL OU UMA INSATURAÇÃO
alifático insaturado
V 3 3 Os cresóis, C7H8O, são conhecidos quimicamente como
hidroximetilbenzenos
podem
apresentar
isomeria
plana,
tanto de
SÃO
ISÔMEROS
2C
e eH
CH
CH
3
função como de posição
C3H6 OH
C 3 H6
OH
F 4 4 A atividade ótica de uma substância está relacionada com a simetria
cristalina ou molecular das substâncias
É UM CRESOL
É ISÔMERO
DE
É ISÔMERO DE
ESTÁ
RELACIONADA
COM A ASSIMETRIA
FUNÇÃO DO
POSIÇÃO DO
CH2
CH3
OH
CH3
06) (Covest-2007) A partir das estruturas
moleculares ao lado podemos afirmar
que:
H H 3C
H 3C
C
H 3C
(I)
H
H
C
H H 3C
H 3C
C
C
H
heral
H
C
H
H
H
C
C
CH
H C
3
OH
HO
3
HOOC
Está(ão) correta(s):
COOH
ácido lático
( III )
COOH
H
H H
H
H
C
CH 3
C
C
H
H
ácido 2-metilbutanóico
COOH
C
H 3C
H
H 3C
C
H
a) 1 apenas
b) 2 e 3 apenas
c) 1 e 3 apenas
d) 1, 2 e 3
e) 3 apenas
O
C
C
H
C
H 3C
( II )
H
H
2) Os compostos representados em (II)
são exatamente iguais; portanto não
apresentam nenhum tipo de isomeria.
C
geranial
H
C
3) Os ácidos representados em (III) são
diferentes; portanto, não apresentam
nenhum tipo de isomeria.
C
C
H
C
O
C
H
1) Os compostos representados em (I),
geranial e heral, apresentam isomeria
cis/trans.
H
ácido pentanóico
07) O número total de isômeros (ativos e inativos) da molécula
abaixo é:
a) 2.
H
I
H3C – C –
I
Cl
b) 4.
c) 6.
d) 8.
H
I
C – NH2
I
Cl
e) 10.
Este composto possui dois átomos de carbono assimétricos diferentes,
portanto n = 2
n
2
= 2
2
n–1
2
= 4 isômeros ativos
2–1
= 2
total de isômeros:
1
=
2
= 2 isômero inativo
4 ativos + 2 inativos = 6 isômeros
08) (FESP-PE) Considere o composto:
ácido 2,3-dicloro-3-fenilpropanóico
Ele apresenta:
a) 4 isômeros sem atividade óptica.
b) um total de 6 isômeros, sendo 2 sem atividade
óptica.
c) um total de 4 isômeros, sendo 2 sem atividade
óptica.
d) não apresenta isomeria óptica.
e) só 2 isômeros ativos e um meso composto.
09) O ácido cloromático
Cl
OH
O
C – COOH
HOOC –CCHCl C
– CHOH
C
HO
O
OH
H
H
apresenta:
a) 4 isômeros ativos e 2 racêmicos.
b) 2 isômeros ativos e 1 racêmico.
c) 8 isômeros ativos e 4 racêmicos.
d) 6 isômeros ativos e 3 racêmicos.
e) 16 isômeros ativos e 8 racêmicos.
Tem dois carbonos assimétricos diferentes, portanto n = 2
2n
12n – 1
2
2 = 4 isômeros ativos
= 2 isômeros racêmicos