2
CAPITULO 2
Estrutura atômica e ligação interatômica
DEM
FUNDAMENTOS CIÊNCIA DOS MATERIAIS
UDESC
“Porque estudar Estrutura Atômica e Ligação interatômica? ....... porque o tipo de ligação nos
permite explicar as propriedades de um material......”
2
2
2
ESTRUTURA ATÔMICA
JOHN DALTON
o átomo é
a partícula elementar
a menor partícula que constituía a matéria
todos os átomos de um mesmo elemento
químico são iguais, até mesmo as massas
1.808 - o átomo é uma minúscula
esfera maciça,
indivisível,
Impenetrável
indestrutível.
"modelo da bola de bilhar".
J.J. THOMSOM
A matéria é formada por partículas
extremamente pequenas chamadas átomos;
O átomo é
Uma esfera maciça
Indestrutível e intransformável
Elementos químicos são atomos que
apresentam mesmas propriedades (tamanho,
massa e forma)
os átomos podem se unir entre si formando
"átomos compostos"; - reações químicas
"modelo de pudim com passas"
2
ESTRUTURA ATÔMICA
ERNEST RUTHERFORD
O átomo é:
Formado por elétrons que orbitam em torno
de um núcleo
o raio de um átomo poderia ser em torno de
10.000 vezes maior que o raio de seu
núcleo. (nucleo 10-15m – elétron espaço de
10-10m)
Modelo da átomo nucleado
FISICA QUANTICA
NIELS BOHR
Os elétrons:
Só podem ocupar níveis de energia bem
definidos
Giram em torno do núcleo em órbitas com
energias diferentes.
Tendem a ter a menor energia possível
As órbitas interiores apresentam energia
mais baixa e à medida que se encontram
mais afastadas do núcleo o valor da sua
energia é maior..
2
ESTRUTURA ATÔMICA
Particulas carregadas exercem força umas sobre as outras
•
•
•
Proporcional ao produto das cargas
para cargas com mesmo sinal – força repulsiva
Inversamente proporcional à distancia entre elas
Porque os protons não
se afastam no nucleo?
O ATOMO
Possui um núcleo que concentra quase toda a massa e retém a carga positiva
O diâmetro do átomo é 100000 vezes o diâmetro do núcleo
O núcleo é circundado por por elétrons que são portadores de cargas negativas
A massa do elétron é de 9,10939 x 10-31 kg
O núcleo é composto por dois tipos de partículas, prótons e nêutrons
O nêutron não possui carga e não interage com os prótons
O nêutron possui massa de 1,67482 x 10-27 Kg
Os protons possuem carga de 1,602 x 10-19C
Os protons tem massa de 1,67262 x 10-27
O numero de prótons é o numero atômico (Z)
O numero de neutrons é (N)
O numero de prótons + neutrons é o numero de massa (A)
2
ESTRUTURA ATÔMICA
Partículas pequenas devem ser tratadas pela Mecânica Quantica
O estados eletrônicos em um átomo são descritos por orbitais quânticos
Define-se a função de energia
Define-se a função de onda
Números que representam estados quânticos de partículas são chamados
de números quânticos
Numero quântico principal ( n )
•
•
•
•
•
•
n só pode assumir valores naturais n=1,2,3,4,5
A cada valor de n corresponde a um valor de energia
Quanto maior n menor o valor de energia
Se n for muito grande a energia tende a zero
Os níveis de energia mais baixo são mais afastados
Os níveis de energia mais elevados são mais próximos, tendendo ao contínuo
Função de onda ( n, l e ml)
Função de probabilidade
2
ESTRUTURA ATÔMICA
O átomo é composto por um núcleo que concentra praticamente toda sua
massa. Essa massa é a soma das massas dos nêutrons e dos prótons.
Como o núcleo é positivamente carregado, ele exerce uma força atrativa
sobre os elétrons que orbitam a sua volta. Como resultado dessa atração
entre o núcleo e os elétrons, surgem os orbitais quanticos. Cada orbital é
caracterizado por uma energia En e uma função de onda. Os números
quanticos n, l e m especificam os estados de um elétron no átomo. O
numero quantico ms , spin que tem relação com o efeito magnético
2
ESTRUTURA ATÔMICA
O átomo
Elétron
núcleo
Núcleo = Prótons + Nêutrons
Elétron 9,11x10-31 Kg
Proton 1,67x10-27 Kg
Neutron 1,67x10-27 Kg
-1,60 x10-19 C
+1,60x10-19 C
-----
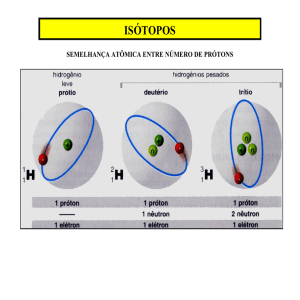
ISOTOPOS
O elemento químico
Número de protons – Número atômico (Z)
Massa atômica (A) – Massa de protons + Massa de neutrons
Unidade de massa atômica (uma)
uma/átomos = g/mol
1/12 da massa atômica do isótopo mais comum do carbono
2
Modelo Atômico
Conceito Quântico
Niveis
Estados energéticos
Aos elétrons só são permitidos
valores específicos de energia
Elétron
núcleo
Átomo de Bohr
Energia eV
Energia J
2
Modelo Atômico
Conceito Mecânico Ondulatório
Não existe um orbital discreto mas sim
uma probabilidade de encontrar o
elétron estar em vários locais ao redor
do núcleo
Energia eV
Energia J
Elétron possui características tanto
de onda como de partícula
2
Números Quânticos
Número quântico principal (n) – numero inteiro a partir da unidade, ou K,L,M,N
Número quântico (L) – nível da subcamada – s, p, d, f
Número quântico (ml) – numero de estado energético de cada subcamada - v
Momento de spin (m) - +1/2 -1/2
Número
quântico
principal
Designação
Subcamadas
Número de
estados
Número de elétrons
Por subcamada
Por camada
Estado Fundamental
Princípio de exclusão de Pauli
2
Elétron de valência
Elemento
Número Atômico
Configuração Eletrônica
2
Átomos nos sólidos
Energia
Superposição de estados S
Sólidos
Separação
Níveis de energia e separação atômica
2
Átomos nos sólidos
Camada de
valência
Parcialmente
Preenchidas
Níveis
atômicos
Níveis
atômicos
Isolante
Metal
Banda
Condução
Elétrons
Vazios
Banda de
valência
Semi condutores
Bandas de energia para condutores, semicondutores e isolantes
A tabela Periódica
2
•
•
•
Da criação do universo ???
Existem 92 elementos químicos estáveis
O mais simples é o Hidrogênio e o mais complexo o urânio
Hidrogênio
Urânio
Z=1
1s1
Z = 92
A = 238
1s22s22p63s23p64s23d104p65s24f105p66s24f145d106p67s25f4
Litio
3 protons
Sódio
11 protons
Potássio
Rubidio
Cesio
Frâncio
4 neutrons
23 neutrons
1s2 2s1
1s2 2s22p63s1
Mesma configuração
A tabela Periódica
2
•
•
•
•
Surge a ideia de classificar os elementos por suas semelhanças químicas
Primeiros dados seculo XVIII – Lavoisier
Dimitry Ivanovitch Mendeleiev – Tabela de PERIODICIDADE de propriedades
A tabela tinha lacunas
Escândio (Sc)
Germânio (Ge)
A tabela períodica ultrapassou a ideia de ser um mero sistema de
classificação de elementos e se tornou um instrumento de pesquisa científica
• Argonio (Ar) – descoberto em 1894 – William Ramsay e John William
Strutt
• Helio (He), Neônio (Ne), Criptônio (Kr) e Xenônio (Xe) – foram
descobertos depois
• Enrico fermo – Propos a possibilidade de criar novos elementos - 1934
Bombardeamento de núcleos por nêutrons
Efeito de decaimento ( um neutron decai
emitindo um elétron e tornando-se um
proton
2
A tabela Periódica
•
•
•
•
•
•
•
•
1940 – netúnio (Np) Z= 93
Plutônio (Pu)
Z=94
Amerício (Am) Z=95
Cúrio (Cm)
Z=96
Berquélio (Bk) Z=97
Califórnio (Cf)
Z=98
Einstênio (Es)
Z=99
Fermio (Fm)
Z=100
Fusão – dois nucleos colidem a altas energias e fundem-se formando um
núcleo de maior peso atômico
•
•
•
•
•
•
Mendelévio (Md) Z= 101
Helio + Einstênio
Nobélio (No)
Z= 102
Laurêncio (Lr)
Z= 103
Candidato a se chamar Rutherfordio (Rf)
Candidato a se chamar Dúbnio (Db)
Candidato a se chamar Seabórgio (Sg)
Fusão fria –
• Geram-se elementos de baixo tempo de decaimento
2
A tabela Periódica
2
A tabela Periódica
Numero atômico
Elétrons em seus
niveis de energia
Simbolo
Nome
Massa atômica
média
2
A tabela Periódica
Período
Não apresentam propriedades similares
O primeiro elemento da linha é reativo
O ultimo elemento da linha é inerge
Grupo ou Família
Propriedades Similares
Mesmo número de elétrons de valência
2
Os Metais na Tabela Periódica
2
As Cerâmicas na Tabela Periódica
2
Os Polimeros na Tabela Periódica
2
Os Semicondutores na Tabela Periódica
Quando combinados entre si (coluna III-V e II-VI) os metais (quadrados
claros) assumem propriedades semicondutoras.
2
E os seres vivos ????
Somente seis elementos químicos forma as moléculas de organismos vivos:
•
•
•
•
•
•
Carbono
Hidrogênio
Oxigênio
Nitrogênio
Fosforo
Enxofre
Carboidratos
Proteinas
Lipídios
Ácidos nucleicos
2
Ligações químicas
2
Ligações químicas – Espaçamento Interatômico
Força de atração possui origem eletrostática,
interação Coulombiana, interações dipolares,
interações entre elétrons na última camada.
r
r
Força de repulsão possui origem
quântica. Princípio de Exclusão de Pauli:
duas partículas não podem ocupar o
mesmo estado quântico.
Na distância de equilíbrio, a força de atração
entre os íons é compensada pela força de
repulsão entre as nuvens eletrônicas
2
Ligações químicas –Energia de ligação
Força de atração e de repulsão em
função da distância interatômica r
para dois átomos isolados
Energia potencial em função da
distância interatômica r para dois
átomos isolados
Energia de ligação é a energia associada com a formação da ligação partindo
da condição inicial que os átomos (íons) estão inicialmente separados de uma
distância infinita.
Sempre que uma ligação é formada, o sistema apresenta uma redução de energia.
A energia é mínima na condição interatômica de equilíbrio (poço de potencial).
Quanto mais fundo o poço, mais estável é a ligação, maior é o ponto de fusão/ebulição
2
Ligações químicas –Propriedades
Valores típicos para a0 são da ordem de
0.3nm (0.3x10-9m)
Valores típicos para a energia de ligação
são entre 600 e 1500 kJ/mol
A energia de ligação está diretamente
relacionada com o ponto de fusão do
material
Tipo de Ligação
Energia de Ligação
Kcal/mol
Iônico
Covalente
Metálica
Van der Waals
150-370
125-300
25-200
< 10
Modulo de elasticidade
2
Ligações químicas –Propriedades
Coeficiente de expansão térmica
Os átomos estão constantemente vibrando ao redor da posição de equilíbrio.
• A distância interatômica de equilíbrio, ao, só é bem definida quando a temperatura é 0
K.
• Normalmente o poço de potencial não é simétrico e a distância interatômica média
aumenta gerando a EXPANSÃO TÉRMICA.
•curva encontra-se na forma de um
poço de energia potencial, e o
espaçamento interatômico em
condições de equilíbrio a uma
temperatura de 0 K, ro, corresponde
ao ponto mínimo no poço de energia
potencial.
• um incremento na temperatura,
aumenta a energia vibracional
fazendo com que a distância
interatômica média aumente.
2
Ligações químicas –Propriedades
Coeficiente de expansão térmica
Curva Assimétrica
A expansão térmica se deve à curva do
poço de energia potencial ser assimétrica, e
não às maiores amplitudes vibracionais dos
átomos em função da elevação da
temperatura.
Curva Simétrica
• Se a curva da energia potencial fosse
simétrica não existiria qualquer variação
liquida ou global na separação interatômica
e, consequentemente, não existiria
qualquer expansão térmica.
2
Ligações Iônicas
2
Ligações Iônicas
2
Ligações Covalentes
2
Ligações Covalentes
2
Iônica – covalente = fração covalente
2
Ligações Metálicas
2
Ligações Metálicas
2
Ligações Secundárias
As propriedades macroscópicas dos
materiais dependem essencialmente
do tipo de ligação entre os átomos.
2
Covalente
Semicondutores
Polimeros
Secundária
Metálica
Metais
Iônica
Cerâmicas e vidros
2
Transição contínua entre forças de ligação
Polimeros
Diamante
Polímeros
Grafita
Cristal líquido
Covalente
Vidros Iônicos
Semicondutores dopados
Metais de transição
Sais
Ligas
Cerâmicas Iônicas
Iônico
Metálico
Metais alcalinos
2
Resumo – Ligações químicas
http://www.cimm.com.br/portal/
http://www.acobrasil.org.br/