Capacitação para a realização do teste rápido
Alere para diagnóstico sorológico da
leishmaniose visceral canina (LVC)
Leishmaniose Visceral
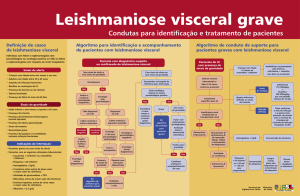
Epidemiologia
Cerca de 400 mil novos casos por ano no mundo.
Cerca de 97% dos casos de LV nas Américas
ocorrem no Brasil.
Se não for tratada a tempo pode ser fatal.
Leishmaniose Visceral
Agente etiológico
Protozoários do gênero Leishmania
Principal espécie nas Américas:
Leishmania (Leishmania) infantum chagasi
Leishmaniose Visceral
Vetor
Flebotomíneo
No Brasil, Lutzomyia longipalpis e Lutzomyia cruzi
Principal reservatório
Cão
Leishmaniose Visceral
Foco e transmissores da leishmaniose.
Leishmaniose Visceral
Diagnóstico da LVC
Clínicoepidemiológico
Parasitológico
Pesquisa
direta
Cultura e
isolamento
Imunológico
Molecular
PCR
Teste
rápido
ELISA
Leishmaniose Visceral
Diagnóstico Clínico
Leishmaniose Visceral
Diagnóstico clínico
Leishmaniose Visceral
Diagnóstico Parasitológico-Exame direto
Visualização do parasito em exame direto
através de microscopia ótica-punção de
medula óssea
Elevada especificidade (100%)
Baixa sensibilidade (52 a 89%)
Leishmaniose Visceral
Diagnóstico parasitológico-cultura e isolamento
Meio clássico NNN (Neal, Novy,
Nicolle) + meio líquido Schneider ou
LIT (Liver Infusion Triptose
Leishmaniose Visceral
Caracterização da espécie Leishmania
Anticorpos monoclonais
Análise eletroforética por isoenzimas, também chamada
de Multi Locus Enzyme Electrophoresis (MLEE)
Biologia molecular/PCR
Leishmaniose Visceral
Caracterização da espécie Leishmania
Anticorpos monoclonais
Análise eletroforética por isoenzimas, também chamada
de Multi Locus Enzyme Electrophoresis (MLEE)
Biologia molecular/PCR
Leishmaniose Visceral
Biologia molecular/ PCR
Muitos protocolos disponíveis e ausência de um kit padrão
Para ser usado em saúde pública faz-se necessário padronização de
um protocolo
Pontos importantes que podem influenciar a sensibilidade e
especificidade das técnicas moleculares:
Tipo de amostra/ Protocolo de extração de DNA
Iniciadores/ Revelação/ Termocicladores/ Fase de infecção
Leishmaniose Visceral
Sorologia
Diagnóstico de eleição para controle do reservatório canino
Protocolo validado em ensaio multicêntrico, 2011:
Triagem
Teste rápido
imunocromatográfico
TR DPP Bio-Manguinhos
Confirmação
Ensaio Imunoenzimático
ELISA Bio-Manguinhos
Leishmaniose Visceral
Sorologia
Superação da estimativa de demanda de kits TR DPP realizada pelo
Ministério da Saúde-Desabastecimento de kits em 2014 e atendimento de
cota por estado em 2014/2015
Necessidade de traçar alternativas para complementar estoque de testes
rápidos imunocromatográficos
Possui complexo antigênico similar ao TR DPP Bio-Manguinhos
Teste rápido imunocromatográfico Alere como alternativa para
complementar demanda de testes rápidos utilizados na triagem dos cães
Leishmaniose Visceral
Critérios para escolha do teste rápido Alere:
Único teste rápido imunocromatográfico disponível comercialmente
com registro no Ministério da Agricultura, Pecuária e Abastecimento
Avaliação prévia do
Referência Nacional
Capacidade de atendimento à demanda apresentada pelo
Ministério da Saúde
seu
desempenho
pelo
Laboratório de
Leishmaniose Visceral
Pontos importantes!!!
A distribuição do teste rápido imunocromatográfico TR DPP BioManguinhos será mantida
Portanto, o teste rápido
complementação do TR DPP
Alere
é
uma
alternativa
para
Alere Leishmaniose Ac Test Kit
Teste rápido imunocromatográfico (TRI)
Detecção: anticorpos Leishmania infantum
Antígeno: proteína recombinante rK28 (rK9, rK39 e rK26)
Amostras: soro, plasma ou sangue total canino.
Alere Leishmaniose Ac Test Kit
Avaliação de desempenho do kit pelo Serviço de Doenças
Parasitárias
170 amostras :79 amostras positivas e 91 negativas
Duplicata
Ensaio 1: Sensibilidade de 91,1%; Especificidade de 100%
Ensaio 2: Sensibilidade de 89,9%; Especificidade de 98,8%
Apresentação do kit TRI Alere
1
1
5 ou 10 Cartões de
resultados
2
5 ou 10 Tubos de
amostra descartáveis
com EDTA
3 1 Frasco com solução
tampão de teste
3
2
4
5
Nota: as lancetas serão fornecidas junto com o kit, como um anexo
4
5 ou 10 Dispositivos de
teste
5
5 ou 10 Tubos
capilares de 10μL
Coleta e preparação da amostra
1
Coleta de amostra de sangue capilar para exame no campo
Imobilize o cão
2
Perfure a orelha
com a lanceta
3
Colete 10µl de
sangue
Coleta e preparação da amostra
Coleta de amostra de sangue capilar para exame no campo
Materiais necessários para coleta de
sangue venoso
1
3
7
5
6
Descarte de
2
Álcool
3
Algodão
4
Caneta
5
Seringa
6
Tubos de coleta
7
Agulha
2
4
1
perfuro-cortante
Coleta e preparação da amostra
1
Coleta de amostra de sangue para exame no laboratório
Após fazer a contenção,
limpe a área de coleta
com álcool e algodão
2
Colete o sangue
com a seringa
3
Descarte a agulha e
dispense o sangue no tubo
com a identificação do cão
Procedimentos para a realização do TRI Alere
Nota: Não interpretar após 30 minutos.
Atenção
Os tubos capilares possuem uma marcação de 10μL.
< 10μL pode resultar em testes falso-negativos;
> 10μL pode invalidar o teste.
Teste inválido devido ao excesso de amostra
Leitura e interpretação dos resultados
RESULTADO NEGATIVO
A presença de somente uma linha na janela C
Leitura e interpretação dos resultados
RESULTADO POSITIVO
A presença de duas linhas coloridas (C e T)
Leitura e interpretação dos resultados
INVÁLIDO
Ausência da linha controle C após execução do teste.
Leitura e interpretação dos resultados
Escala visual para interpretação dos resultados
Precauções
1) O kit é sensível ao calor e deve ser
armazenado à temperatura de 2 a 30°C.
2) Não congelar o kit
3) Realizar o teste imediatamente após a
abertura do envelope.
4) Não reutilizar a plataforma de teste.
5) Não utilizar o kit após o vencimento.
Precauções
6) Se a amostra não for testada imediatamente, manter
sob refrigeração:
sangue total > 2 a 8º C por 24 horas
soro ou plasma > até 5 dias
prazo maior, conservar a -20ºC.
7) Manusear todas as amostras do sangue como sendo
capazes de transmitir doenças infecciosas.
8) Fazer o descarte correto:
resíduo com risco biológico
perfuro-cortante para agulhas e lancetas.
Educação em saúde
Utilizar o tempo de espera durante a realização do teste para
passar informações ao proprietário sobre a leishmaniose
visceral e as medidas de controle
Considerações Finais
Algoritmo para o diagnóstico da leishmaniose visceral canina
Teste Rápido
Não Reagente
Cão Negativo
Nota técnica conjunta Nº 01/2011 CGDT- CGLAB/DEVIT/SUS/MS.
Considerações Finais
Algoritmo para o diagnóstico da leishmaniose visceral canina
Teste Rápido
Reagente
ELISA Não
Reagente ou
indeterminado
Cão
Negativo
Nota técnica conjunta Nº 01/2011 CGDT- CGLAB/DEVIT/SUS/MS.
Considerações Finais
Algoritmo para o diagnóstico da leishmaniose visceral canina
Teste
Rápido
Reagente
ELISA
Reagente
Eutanásia
Nota técnica conjunta Nº 01/2011 CGDT- CGLAB/DEVIT/SUS/MS.
Obrigado pela atenção!
Dúvidas, entrar em contato com:
Serviço de Doenças Parasitárias
Instituto Octávio Magalhães
Fundação Ezequiel Dias
Tel.: 31-3314 4663/4661
[email protected]
OU
Departamento de Assessoria Técnica
Para esclarecimentos de dúvidas quanto ao produto e
assessoria técnica:
Tel: 0800 11 3262
[email protected]
Responsável técnico: Marcelo Santos Genelhu
[email protected]