LEISHMANIOSE VISCERAL
A Leishmaniose Visceral, também conhecida popularmente como calazar ou barriga
d’água, trata-se da infecção por protozoário do complexo Leishmania donovani, que
compreende a L. chagasi (América), a L. donovani (Índia, China, Iraque e Leste da África) e a
L. infantum (Norte da África e Europa Mediterrânea). Historicamente era uma doença restrita a
animais, porém com o avanço da urbanização, o homem passou a assumir a condição de
hospedeiro da Leishmania, tornando o calazar uma antropozoonose.
Segundo a OMS, constitui uma das seis endemias de maior destaque em nível
mundial. Dos doze países atingidos na América Latina, 90% da casuística provém do Brasil,
sobretudo da região Nordeste. O primeiro registro da doença no país data de 1913, quando da
realização da necropsia no Paraguai de um paciente com esplenomegalia febril proveniente de
Minas Gerais.
WikiPETia Médica
1
De 1984-2002, aproximam-se de 50 mil os casos da doença notificados no Brasil,
sendo 66% deles proveniente de estados como Bahia, Ceará, Maranhão e Piauí. A doença
acomete principalmente crianças menores de 10 anos (54,4% dos casos), deste total 41,0% se
concentram na população pediátrica menor que 5 anos, em decorrência de fatores como a
imaturidade imunológica celular e a forte associação com a desnutrição nessa faixa etária.
Estudos demonstram também que pertencem ao sexo masculino a maioria dos casos (60%),
muito embora não se encontrem justificativas para esse acometimento preferencial. Não existe
diferença em casuística entre raças.
De modo geral, ambientes de aspectos geográficos, climáticos e sociais diferenciados
tem sido palco do adoecer pelo calazar. Com o tempo, tem-se visto uma transição
epidemiológica da doença: anteriormente restrita a regiões rurais (pouco urbanizadas); porém
agora em avanço a ambientes peri-urbanos e urbanos de grandes metrópoles.
A etiologia da doença compreende, conforme dito, protozoários do gênero Leishmania,
parasita intracelular obrigatório do sistema fagocítico mononuclear, também chamado retículoendotelial. O agente apresenta duas formas morfológicas distintas: a flagelada (promastigota),
encontrada no tubo digestivo dos insetos vetores e a aflagelada (amastigota), presente no
tecido dos vertebrados infectados.
WikiPETia Médica
2
Há tanto reservatório urbanos (cão) quanto silvestres (raposas, gambás), podendo-se
dizer que existe uma enzootia, isto é, uma endemia entre animais. Os vetores envolvidos com
a transmissão da doença são o Lutzomya longipalpis e o Lutzomya cruzy. Esses insetos
possuem hábito herbívoro, no entanto a fêmea apresenta também atividade hematófaga,
utilizando o sangue para a postura dos ovos e perpetuação da espécie. No período de chuvas,
há um boom populacional de vetores, aumentando a freqüência do ataque a humanos
principalmente ao anoitecer e, conseqüentemente, fazendo crescer o número de indivíduos
doentes.
Diagnóstico no cão: Nos animais susceptíveis, a apresentação clínica é
caracteristicamente insidiosa, envolvendo onicogrifose, esplenomegalia,
linfadenopatia, coriza, cerato-conjutivite, alopecia/dermatites, apatia, edema
de patas, diarréia e/ou hemorragia intestinal. A confirmação laboratorial
sorológica se dá através do Elisa ou da Imunofluorescência indireta.
Ciclo de Transmissão
Ao picar o animal infectado, o vetor adquire formas amastigotas do protozoário, as quais se
chegam ao interior do seu tubo digestivo com a eclosão dos monócitos adquiridos a partir do
repasto sanguíneo. Nessa topografia, a leishmania aflagelada torna-se flagelada e migra para
as glândulas salivares do inseto. Com isso, ela se deposita na derme do homem, sendo
englobada por macrófagos. Incapazes de fagocitar o parasito por completo, os macrófagos
rompem com a divisão binária repetitiva da leishmania, já transformada novamente em
aflagelada. Com isso ocorre parasitemia, entrada em monócitos no sangeu e disseminação
para órgãos do sistema fagocítico mononuclear: linfonodos, fígado, baço e medula óssea.
No que diz respeito à susceptibilidade diferencial entre as pessoas, sabe-se que os
extremos de idade são mais vulneráveis à infecção-doença. Nele, o braço celular de resposta
imune pouco se expressa; enquanto que o humoral revela-se ineficaz para conter o avanço da
parasitemia.
O espectro clínico da apresentação da infecção pelo complexo leishmania é bem
amplo, podendo ser oligo-assintomático (maioria), moderado e grave. A infecção, quando
inaparente, não requer tratamento ou notificação; o seu diagnóstico se dá por sorologia
(Imunofluorescência indireta/Elisa) ou mesmo por reação de Montenegro ( + ). A infecçãodoença, em contrapartida, é marcada por uma esplenomegalia febril com ou sem
hepatomegalia, podendo sua evolução ser didaticamente dividida em período inicial, de estado
e final.
WikiPETia Médica
3
• PERÍODO INICIAL
o
o
o
o
forma AGUDA, variável;
febre < 3 semanas, palidez, hepatoespleno, baço 5cm abaixo RCE,
estado geral do paciente é preservado;
Anemia com Hb> 9, leucócitos e plaquetas nl, VHS elevado (>50mm) e
as proteínas totais e frações podem estar discretamente alteradas;
IFI e ELISA (+) e Montenegro (-). O aspirado de MOV/baço: formas
amastigotas do parasita.
• PERÍODO DE ESTADO
o
o
o
o
Quadro clínico arrastado > 2 meses;
Febre irregular, emagrecimento, palidez e aumento das VMGs, estado
geral do paciente já mostra certo nível de comprometimento;
Pancito, inversão alb/glob, aumento TGO/TGP (2-3X nl), bilirrubinas,
aumento discreto de Ur e Cr;
Anticorpos anti-Leishmania, Montenegro (-). Parasita em aspirado de
medula óssea, baço, fígado e linfonodos;
• PERÍODO FINAL
o
o
o
Sem DX e tto, doença evolui, febre contínua e EGC; desnutrição
(cabelos quebradiços, cílios alongados e pele seca), edema dos
membros inferiores - anasarca.
Outras manifestações: hemorragias
petéquias), icterícia e ascite.
(epistaxe,
gengivorragia
e
ÓBITO: infecções bacterianas e/ou sangramentos
O diagnóstico diferencial é feito basicamente com as seguintes condições clínicas:
Febre tifóide (Anemia menos proeminente, esplonomeg. mais discreta); Malária (Acessos
febris, calafrios, sudorese noturna); Endocardite infecciosa (Anemia menos proeminente,
esplonomeg. mais discreta); Enterobacteriose sep. Prolongada (Lobo hepático esq >dir,
leucocitose); Neoplasias hematológicas – mieloproliferativas (MMA, PV, LMC) e Outras
(doenças de depósito).
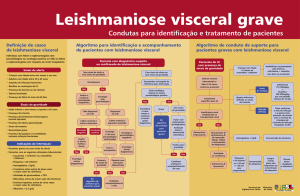
No atendimento de pacientes com suspeita/confirmação de Leishmaniose visceral,
devem ser observados alguns fatores que falam a favor de um pior progóctico – maior
morbimortalidade, complicações mais freqüentes, maior tempo de internação hospitalar, etc.
São eles:
•
Idade < a 6 meses ou > a 65 anos
•
Desnutrição grave
WikiPETia Médica
4
•
Co-morbidades, infecção bacteriana secundária inclusive (ex. PAC, ITU, etc)
•
Uma das seguintes manifestações clínicas:
o
icterícia
o
fenômenos hemorrágicos (exceto epistaxe)
o
edema generalizado
o
sinais de toxemia (letargia, má perfusão, cianose, taquicardia ou
bradicardia, hipoventilação ou hiperventilação e instabilidade
hemodinâmica).
Mesmo não preenchendo fatores de gravidade, pacientes que apresentem sinais de
alerta também são merecedores de atenção especial por parte dos profissionais de saúde.
Compreendem esse grupo indícios, sugestivos de gravidade potencial, alguns como:
•
Crianças: idade entre 6 meses e 1 ano
•
Adultos com idade entre 50 e 65 anos
•
Recidiva
•
Diarréia, vômitos
•
Infecção bacteriana suspeita
•
Febre há mais de 60 dias
Como métodos complementares de diagnóstico específico, conta-se com os
imunológico e o parasitológico. Em associação com clínica e outros dados laboratoriais, o teste
sorológico reagente reforça o diagnóstico de Leishmaniose visceral. Os mais utilizados são o
IFI (a partir de 1:80) e os ensaios imunoenzimáticos (K-39). Sensibilidade da sorologia: 90100% nos imunocompetentes e 50-60% nos imunodeprimidos.
Mesmo na presença de sorologia reagente, convém fazer uso de métodos de
diagnóstico parasitológicos para evitar os falsos-positivos da imunologia, bem como para se
contar com um parâmetro de controle pré e pós tratamento, muito embora não se indique mais
a repetição de métodos invasivos enquanto critério de cura.
A punção aspirativa esplênica constitui o método de maior sensibilidade (90-95%), não
sendo realizada rotineiramente em decorrência de restrições ao procedimento, como o risco
maior de sangramentos, rotura esplênica, etc. O aspirado de MOV, biópsia hepática e a
aspiração de linfonodos apresentam menor sensibilidade. O material coletado pode ser
submetido ao exame direto – imprint, Giemsa ou Wright, Leishman, Panóptico – ou cultura,
meio NNN. Historicamente, relata-se um método de análise que consistia na inoculação em
hamsters, hoje em dia sem utilidade. O PCR, identificação do DNA da leishmania no material
colhido, representa o método de maior acurácia disponível, possui sensibilidade e
especificidade próximas de 100%. A limitação ao seu emprego rotineiro encontra-se no alto
custo.
Além dos exames complementares específicos para auxílio no diagnóstico, convém a
solicitação de outros, a exemplo de hemograma completo, VHS, TAP/TTPA, creatinina sérica,
transaminases, eletrólitos, albumina, globulina, hemocultura, urocultura, sumário de urina e
Raio X de tórax.
WikiPETia Médica
5
A hospitalização está indicada para pacientes que apresentem pelo menos um sinal de
gravidade ou alarme; bem como para aqueles que exibam alguma das alterações laboratoriais
a seguir:
•
leucócitos < 1.000/mL ou neutróflos < 500/mm3
•
plaquetas < 50.000/mL
•
HB < 7g/dL
•
Cr 2x> VR
•
TAP < 70%
•
Bil> VR
•
TGO/TGP 5x> VR
•
Albumina < 2,5mg/mL
•
RX de tórax: infecção ou edema pulmonar
A estratégia terapêutica perpassa tanto tratamento de suporte (dieta
hiperprotéica/hipercalórica, hidratação, hemodiálise*, antibioticoterapia, antibioticoprofilaxia,
hemotransfusões, uso de fatores estimuladores de colônia de granulócitos/monócitos,
ventilação mecânica*, sedação/analgesia*, drogas vasoativas*, reposição eletrolítica), quanto o
tratamento específico com drogas anti-leishmania.
A droga de primeira escolha na maioria dos casos para o tratamento específico são os
antimoniais pentavalentes, como o Stibogluconato de sódio e o Antimoniato-N-metil glucamina.
Recomenda-se dose de 20mg de Sb+5 kg/dia, EV ou IM por 20-40 dias. Como paraefeitos,
podem desencadear distúrbios de repolarização (inversão e achatamento da onda T e aumento
do intervalo QTC). Após o 20º dia de tratamento, ECG semanal/ausculta cardíaca cuidadosa.
Se arritmia, suspender e usar droga alternativa. Constituem contra-indicações formais ao uso
do antimoniais as seguintes situações:
•
uso de beta-bloqueadores e antiarrítmicos
•
insuficiência renal ou hepática
•
grávidas nos dois primeiros trimestres
•
ECG com intervalo QTC superior a 400ms (homens) e 450 ms (mulheres)
Diante de gestação, contra-indicação, toxicidade ou refratariedade aos antimoniais,
recomenda-se o uso de Anfotericin B, dose 1mg/kg/dia, máximo de 50mg/dia, diluídos na
proporção 1mg/10mL de SG 5%, correndo de 4-6h. Pode haver efeitos colaterais dosedependentes: alterações pumonares / renais; flebite, cefaléia, febre, calafrios, astenia, dores
musculares e articulares, vômitos e hipotensão, sobrecarga hídrica, hipocalemia.
São admitidos basicamente critérios clínicos para a cura da Leishmaniose visceral, a
saber:
•
Desaparecimento da febre: geralmente a partir do 5º dia de medicação
•
Melhora do hemograma: a partir da 2ª semana
WikiPETia Médica
6
•
Redução da hepatoespleno: primeiras semanas
•
Eletroforese de proteínas: se normaliza depois de meses
•
OBS1.: Recomenda-se acompanhamento ambulatorial com 3/6/12 meses após a alta;
a sorologia se negativa tardiamente.
•
OBS2.: Se melhora persistente, o controle através de novo parasitológico se torna
dispensável.
Bibliografia
Guia de Vigilância Epidemiológica; Ministério da Saúde, 2005.
Leishmaniose visceral grave – normas e condutas; Ministério da Saúde, 2006.
Manual de vigilância e controle da Leishmaniose visceral; Ministério da Saúde, 2003.
Manual de Recomendações para Diagnóstico, Tratamento e Acompanhamento da coinfecção Leishmania-HIV.
Guia de Bolso de Doenças Infecciosas e Parasitárias- 7ª edição; Ministério da Saúde,
2008.
WikiPETia Médica
7