Avaliação dos efeitos biológicos adversos dos fármacos anti-hipertensivos
Losartan e Valsartan em ouriço-do-mar Lytechinus variegatus
(ECHINODERMATA, ECHINOIDEA).
Nathália Sayuri Yamamoto1, Camilo Dias Seabra Pereira1,2 , Fernando Sanzi Cortez1, Fabio
Hermes Pusceddu1, Aldo Ramos Santos1 , Walber Toma1 , Luciana Lopes Guimarães1.
1
2
Laboratório de Ecotoxicologia, Universidade Santa Cecília, 11045-907, Santos, SP, Brasil.
Instituto do Mar, Universidade Federal de São Paulo, 11030-400, Santos, SP, Brasil.
Os fármacos anti-hipertensivos são amplamente utilizados no mundo todo, tendo evidências
da ocorrência destes compostos como o Losartan e o Valsartan em baixas concentrações em
matrizes ambientais e nos efluentes domésticos. Devido a esses fatos, este estudo avaliou os
efeitos dos fármacos Losartan e Valsartan por meio de ensaios de toxicidade para avaliar os
efeitos crônicos em ouriço-do-mar Lytechinus variegatus. Os ensaios crônicos foram
realizados de acordo com a norma NBR 15350/2012, para os fármacos Losartan e Valsartan,
onde revelaram os valores de CENO (Concentração de Efeito Não Observado – 50 mg.L-1) e
CEO (Concentração de Efeito Observado – 70 mg.L-1) para o Losartan e de (CENO – 12,5
mg.L-1 e CEO – 25 mg.L-1) para o Valsartan, diferenças que poderiam ser justificadas pelos
valores de Kow destas moléculas. Estes resultados demonstram a improvável ocorrência de
risco ecológico destes fármacos no ambiente, por se tratar, de concentrações de efeito
superiores aos já relatados no ambiente aquático.
Palavras-chave: Ecotoxicologia; Losartan; Valsartan; Lytechinus variegatus.
___________________________________________________________________________
Assessment of adverse biological effects of antihypertensive drugs Losartan
and Valsartan on urchin Lytechinus variegatus (ECHINODERMATA,
ECHINOIDEA).
The antihypertensive drugs are widely used worldwide, with evidence of the occurrence of
these compounds as Losartan and Valsartan in low concentrations in environmental matrices
and domestic effluents. Due to these facts, this study evaluated the effects of drugs Losartan
and Valsartan through toxicity tests to assess the chronic effects on sea -urchin Lytechinus
variegatus. Chronic assays were performed according to NBR 15350/2012, for
pharmaceuticals Losartan and Valsartan, which showed values NOEC (No Observed Effect
Concentration - 50 mg.L-1) and (CEO Concentration Effect observed - 70 mg L-1) for Losartan
and (NOEC - 12.5 mg. L-1 and CEO - 25 mg L-1) for Valsartan, differences that could be
justified by the values of Kow these two molecules. These results demonstrate the unlikely
occurrence of ecological risk of these drugs in the environment, because it is, in effect
concentrations higher than those already reported in the aquatic environment.
Keywords: Ecotoxicology, Losartan, Valsartan and Lytechinus variegatus.
Original received on December, 2013
UNISANTA BioScience – p. 27 - 32; Vol. 3 nº 1, (2014)
Página 27
Introdução
Os fármacos e produtos de higiene pessoal são produzidos e consumidos em grandes
quantidades no mundo todo. Estes compostos são utilizados na cura e no tratamento de
doenças e, dessa forma, são produzidos para serem persistentes e manterem suas propriedades
químicas tempo suficiente para atender um propósito terapêutico. Após o consumo, cerca de
50 a 90 % de uma dosagem de um fármaco é excretada inalterada (MULROY, 2001) e a outra
parte dessas substâncias são metabolizadas e excretadas pelas fezes e urina. Assim, esses
resíduos de fármacos alcançam o ambiente natural através de lançamentos de esgotos in
natura, ou então por meio de lançamentos de efluentes após tratamento convencional nas
estações de tratamento de esgoto (ETEs), os quais não removem completamente essas
substâncias (BELISÁRIO et al., 2009).
Em diversas partes do mundo, estudos recentes sobre a identificação de compostos
farmacêuticos em matrizes ambientais (água de abastecimentos, águas superficiais e em
sedimentos) têm demonstrado a ocorrência de muitas classes de fármacos encontrados em
concentrações que variam de pg.L -1 até mg.L -1 (BILA & DEZOTTI, 2003).
Os anti-hipertensivos representam uma das principais classes de fármacos com
potencial risco de causar efeitos biológicos em organismos aquáticos, seja pelo uso difundido
em todo mundo, ou ainda pela atuação em seus respectivos alvos moleculares. O fármaco
Losartan, um anti-hipertensivo pertencente à classe dos antagonistas dos receptores (tipo
AT1) da angiotensina II (OPARIL et al., 2001), foi identificado por Larsson et al. (2007) em
efluentes na Índia em concentrações de até 2,5 µg.L -1. Guimarães et al. (2012), identificaram
alguns fármacos em água superficial marinha na área adjacente ao descarte do efluente do
emissário submarino de Santos (São Paulo, Brasil), dentre eles o Losartan e o Valsartan.
A presença destes compostos farmacêuticos no ambiente leva a necessidade de conhecer os
efeitos adversos que podem causar à biota aquática. Assim, torna-se importante realizar
estudos com o emprego de ensaios ecotoxicológicos, sendo possível observar os efeitos que
os efluentes industriais e domésticos, substâncias químicas, fármacos, entre outros
contaminantes, podem causar nos sistemas biológicos.
Alguns animais marinhos têm sido utilizados como organismos-teste em ensaios de
toxicidade, como o ouriço-do-mar Lytechinus variegatus, esta espécie é normalmente
encontrada desde a Carolina do Norte (Estados Unidos) até a costa sudeste do Brasil (ABNT
NBR 15350, 2012). Os ouriços-do-mar são considerados bons bioindicadores ambientais por
terem alta sensibilidade às mudanças que ocorrem no ambiente, além disso, estes
invertebrados marinhos são animais com forma de vida sedentária, o que permite investigar a
contaminação de um determinado local ao longo do tempo (VENTURA et al., 2007). Os
estágios, embrionário e larval, de invertebrados marinhos são menos tolerantes ao tóxico do
que o estágio adulto, por isso tem sido utilizado para avaliar a qualidade da água marinha e
dos sedimentos (BELLAS et al., 2005).
Diante destes fatos, este estudo tem como objetivo analisar os efeitos biológicos dos
fármacos Losartan e Valsartan por meio de ensaios de toxicidade para avaliação dos efeitos
crônicos em ouriço-do-mar Lytechinus variegatus.
Materiais e Métodos
Substâncias – teste
UNISANTA BioScience – p. 27 - 32; Vol. 3 nº 1, (2014)
Página 28
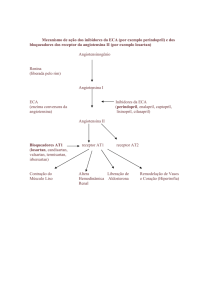
As estruturas químicas do Losartan (CAS 124750-99-8) (2-butil-4cloro-1-[[2’-(1Htetrazol-5-il)[1,1’-bifenil]-4-il]metil]1H-imidazol-5-metanol) de valor de log Kow
(Coeficiente de Partição octanol/água) igual 1,19 (ao pH 7,0), e do Valsartan (CAS 13786253-4) (n-(1-oxopentil)-n-[[2’-(1H-tetrazol-5-il)[1,1’-bifenil]-4-il]metil]-L-valine) de log Kow
igual a 3,65 estão apresentadas na figura 1 (FDA, 2002).
Losartan
Valsartan
Figura 1. Estrutura química do Losartan e Valsartan.
Fonte: Hazardous Substances Data Bank (2013).
Ensaio de toxicidade para avaliar o efeito crônico (Embriolarval) de curta duração com
Lytechinus variegatus (ECHINODERMATA, ECHINOIDEA).
Os ensaios crônicos foram realizados de acordo com a ABNT/NBR 15350/2012 e
consiste na exposição de embriões de ouriço-do-mar (Lytechinus variegatus) por um período
de 24 a 28 horas, a várias diluições da substância que será analisada durante o período de
desenvolvimento embriolarval.
Inicialmente, gametas de L. variegatus foram obtidos através de uma injeção de KCl
0,5 M. Após induzir a liberação dos gametas, as fêmeas foram acondicionadas em recipiente
menor que o seu diâmetro com a superfície aboral voltada para baixo, onde os ovócitos, de
coloração amarelo-alanajados, foram mantidos até o momento da fertilização. Os machos
foram estimulados e os espermatozoides (de coloração branca) foram coletados com uma
pipeta Pasteur e colocados em béqueres de 30 mL. Em seguida, foi preparada uma solução de
0,5 mL de espermatozoide avolumada para 25 mL com água de diluição. Essa solução foi
agitada para evitar a formação de grumos. Após este procedimento, foi adicionado de 1,2 mL
a 2 mL da solução de espermatozoides no recipiente com os ovócitos, com leve agitação
durante 10 minutos para fertilização. Após este período, foram retiradas três alíquotas de 10
µL desta solução para observação em câmara de Sedgwick-Rafter para verificar a taxa de
fertilização dos ovócitos, a qual, pelos critérios de aceitabilidade do ensaio, deve ser de no
mínimo 80%.
Foram realizados três ensaios crônicos com o Losartan e dois ensaios crônicos com o
Valsartan. Cada ensaio foi conduzido com quatro réplicas para cada diluição, em tubos de
ensaios de 10 mL. Os compostos foram diluídos em água marinha natural filtrada em uma
membrana de celulose (0,45 µm de porosidade), com valores de pH, oxigênio dissolvido e
salinidade dentro dos padrões de aceitabilidade do método. Para o Losartan foram
estabelecidas as concentrações de 3, 125; 6,25; 12,5; 25; 50; 100; 200 mg.L-1 e um controle
para os ensaios preliminares. E as concentrações definitivas (denominadas soluções-teste)
para o Losartan foram de 50; 70; 98; 137,2; 192,08 mg.L -1 e um controle. Para as diluições do
fármaco Valsartan, foi necessário a utilização do solvente dimetilsufóxido (DMSO) para a
solubilização inicial deste fármaco. As concentrações estabelecidas para os ensaios definitivos
UNISANTA BioScience – p. 27 - 32; Vol. 3 nº 1, (2014)
Página 29
com Valsartan foram de 1,562; 3,125; 6,25; 12,5; 25; 50; 100 mg.L-1 e um controle com água
do mar e um controle com DMSO (nas concentrações finais dos ensaios com Valsartan).
Após colocar os embriões em cada frasco-teste (300 embriões), os ensaios foram
mantidos em uma câmara de germinação por 24 a 28 horas, com temperatura de 25 ± 2 °C e
fotoperíodo de 12 a 16 horas de luz. A partir do controle foi retirada uma alíquota para
verificar se pelo menos 80 % das larvas atingiram o estágio de pluteus. Após a verificação
desse estágio, o ensaio foi encerrado com 0,5 mL de formol tamponado com bórax. A leitura
dos resultados foi realizada com auxílio de uma câmara de Sedgwick -Rafter, onde os 100
primeiros organismos foram analisados e o grau de desenvolvimento foi estabelecido como
normal ou retardado. Ao término dos ensaios, os dados foram analisados com o uso do
software TOXTAT 3.5 (WEST & GULLEY, 1996) para determinação da Concentração de
Efeito Não Observado (CENO) e Concentração de Efeito Observado (CEO).
Resultados e Discussão
Os resultados obtidos nos ensaio de toxicidade para avaliação dos efeitos crônicos dos
fármacos Losartan e Valsartan são apresentados na tabela 1. Os valores foram expressos como
a média de três ensaios para o Losartan e dois ensaios para o Valsartan.
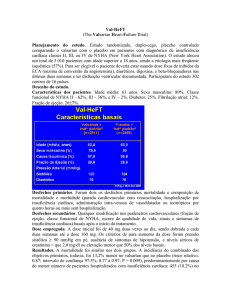
Tabela 1 – Toxicidade crônica (Embriolarval) dos fármacos Losartan e Valsartan para
Lytechinus variegatus.
CENO
CEO
Losartan
50 mg.L-1
70 mg.L-1
Valsartan
12,5 mg.L-1
25 mg.L-1
CENO – Concentração de Efeito Não Observado; CEO – Concentração de Efeito Observado.
Apesar de ambos os fármacos terem sido projetados para atuação no mesmo alvo
molecular (receptor AT1 para Ang II) as diferenças observadas para os valores de CENO e
CEO poderiam ser justificadas pelas diferenças nos valores de Kow para as duas moléculas,
aonde se observam efeitos para o Valsartan, cujo valor de log Kow é de 3,65, em
concentrações inferiores deste fármaco, enquanto os valores superiores observados para
CENO e CEO nos ensaios com o Losartan poderiam ser um reflexo do seu baixo valor de
log Kow, que é de 1,19.
Dados relacionados à farmacocinética são de fundamental importância para a
avaliação do risco ambiental dos fármacos. Dentre os conceitos associados a esta linha
farmacológica encontram-se os valores de Kow. Sabe-se que, a partir destes valores, é possível
correlacionar os parâmetros farmacocinéticos de uma molécula, tais como absorção,
distribuição, metabolização e excreção no organismo humano, bem como a propriedade de
bioacumulação em organismos aquáticos, contribuindo deste modo para análises
ecotoxicológicas. De acordo com esta visão, fármacos que apresentam maiores valores de Kow
possuem maior efeito bioacumulativo, aumentando deste modo, a possibilidade da geração de
danos ecotoxicológicos. Estas informações podem ser visualizadas nos ensaios realizados
(Tabela 1), onde o fármaco Valsartan, que possui maior valor de Kow quando comparado ao
Losartan, demonstra menores valores de CENO e CEO. Tais dados podem confirmar a
hipótese de que Valsartan apresentaria maior risco de danos ambientais quando comparado
com a Losartan.
UNISANTA BioScience – p. 27 - 32; Vol. 3 nº 1, (2014)
Página 30
No entanto, é improvável a ocorrência de efeitos adversos crônicos destes fármacos
em ambiente aquático marinho, pois as concentrações de efeitos para estes dois fármacos são
superiores às concentrações já relatadas na literatura científica para o ambiente aquático.
Conclusões
O efeito crônico do fármaco Losartan nos ouriços-do-mar Lytechinus variegatus foi
observado na concentração de 70 mg.L-1 , já para o fármaco Valsartan observou-se efeitos a
partir da concentração de 25 mg.L-1, diferenças que podem ser justificadas pelos valores de
Kow destes fármacos. É improvável a ocorrência de efeitos adversos crônicos destes fármacos
no ambiente aquático marinho, pois as concentrações de efeitos são superiores às
concentrações já relatadas em ambiente aquático.
Referências Bibliográficas
ABNT – ASSOCIAÇÃO BRASILEIRA DE NORMAS TÉCNICAS. Ecotoxicologia
Aquática. – Toxicidade crônica de curta duração – Método de ensaio com Ouriço-do-mar
(Echinodermata: Echinoidea). Rio de Janeiro. NBR 15350, 2012.
BELLAS, J.; BEIRAS, R.; MARIÑO-BALSA, J. C.; FERNÁNDEZ, N. Toxicity of organic
compounds to marine invertebrate embryos and larvae: a comparison between the sea urchin
embryogenesis bioassay and alternative test species. Ecotoxicology, 14 (3). p. 337-353, 2005.
BELISÁRIO, M.; BORGES, P. S.; GALAZZI, R. M.; PIERO, B. D.; ZORZAL, P. B.;
RIBEIRO, A. V. F. N.; RIBEIRO, J. N. Emprego de resíduos naturais no tratamento de
efluentes contaminantes com fármacos poluentes. Revista Científica Internacional 2 (10).
2009.
BILA, D. M & DEZOTTI, M. Fármacos no ambiente. Química Nova. 26 (4): p. 523-530,
2003.
FDA – U.S. Food and Drugs Administration. Center for drug evalution and research.
Approach Package for: Aplication number 20-386/S-019 and 029. Environment
Assesment/Fonsi. p.8. 2002. Disponível em: <http://www.accessdata. fda.gov/
drugsatfda_docs /nda/2004/20-86S019_Cozaar_EAFONSI. pdf>. Acesso em: 02 de out. 2013.
GUIMARÃES, L. L.; PEREIRA, C. D.S.; CORTEZ, F. S.; TOMA, W.; CHOUERI, R. B.;
PUSCEDDU, F. H.; SANTOS, A. R.; CÉSAR, A. Determinação de fármacos na área de
influência do emissário submarino de Santos, SP. [Apresentado ao 12º Congresso Brasileiro
de Ecotoxicologia, ECOTOX; 12, 2012, Pernambuco; Brasil]. (Pôster).
HSDB – Hazardous Substances Data Bank. Toxnet. Toxicology Data Network. 2012.
Disponível em: <http://toxnet.nlm.nih.gov/>. Acessado em: 02 de out. 2013.
LARSSON, D. G.; PEDRO, C.; PAXAEUS, N. Effluent from drug manufactures contains
extremely high levels of pharmaceuticals. Journal of Hazardous Materials. 148. p. 751-755.
2007.
MULROY, A. When the cure is the probleam. Water Environment Technology. 13 (2): p. 3236, 2001.
OPARIL, S.; WILLIAMS, D.; CHRYSANT, S. G.; MARBURY, T. C.; NEUTEL, J.
Comparative efficacy of the Olmesartan, Losartan, Valsartan and Irbesartan in the control of
essential hypertension. The journal of Clinical Hypertension. 3 (5): p. 283-318. 2001.
VENTURA, C. R. R.; VERÍSSIMO, I.; LIMA, R. N. P.; BARCELLOS, C. F.; OIGMANPSZCZOL, S. S. Echinodermata. In: Biodiversidade marinha da Baía da Ilha Grande. Org.
UNISANTA BioScience – p. 27 - 32; Vol. 3 nº 1, (2014)
Página 31
Joel C. Creed Débora O. Pires e Marcia A. de O. Figueiredo. Ministério do Meio Ambiente.
Brasília, 416 p. 2007.
WEST, Inc. & GULLEY, D. Western Ecossistems Technology. TOXTAT 3.5 Computer
Program., 1996.
UNISANTA BioScience – p. 27 - 32; Vol. 3 nº 1, (2014)
Página 32