Avaliação dos efeitos biológicos do fármaco Losartan em microcrustáceos
Daphnia similis e Ceriodaphnia dubia (CRUSTACEA, CLADOCERA).
Nathália Sayuri Yamamoto 1, Camilo Dias Seabra Pereira1,2, Fernando Sanzi Cortez1, Fabio
Hermes Pusceddu1, Aldo Ramos Santos1, Luciana Lopes Guimarães1.
1
2
Laboratório de Ecotoxicologia, Universidade Santa Cecília, 11045-907 Santos, SP, Brasil.
Institutos do Mar, Universidade Federal de São Paulo, 11030-400 Santos, SP, Brasil.
O Losartan é um antihipertensivo amplamente utilizado que possui evidências de ocorrência
em efluentes domésticos e matrizes ambientais (água superficial, sedimento). Diante disso, o
presente estudo avaliou a toxicidade aguda e crônica deste composto, por meio de ensaios de
toxicidade com os microcrustáceos D. similis e C. dubia, respectivamente. Os ensaios de
toxicidade aguda, realizados de acordo com a norma NBR 12713/2009, demonstraram uma
concentração efetiva média (n=3) de 175,26 mg.L -1 . Já o ensaio preliminar para avaliação de
efeito crônico, realizado de acordo com a NBR 13373/2010, revelou uma a concentração de
efeito observado (CEO) de 100 mg.L -1. Estes resultados evidenciam a improvável ocorrência
de risco ecológico do Losartan, em função das concentrações de efeito serem superiores às
concentrações já relatadas em ambiente aquático. Além disso, estes dados poderão gerar
subsídios para o estabelecimento de concentrações seguras deste composto na legislação
ambiental.
Palavras-chave
Ecotoxicologia, fármaco, Losartan, Daphnia similis e Ceriodaphnia dubia.
__________________________________________________________________________
Assessment of the biological effects of the pharmaceutical Losartan on
microcrustaceans Daphnia similis and Ceriodaphnia dubia
(CRUSTACEA, CLADOCERA).
The Losartan is a widely used antihypertensive that has evidence of occurrence in effluents
and environmental matrices (surface water, sediment). Therefore, the present study assessed
the acute and chronic toxicity of this compound by means of toxicity tests with the
microcrustaceans D. similis and C. dubia, respectively. The acute toxicity tests, conducted in
accordance with the NBR 12713/2009, demonstrated a median effective concentration (n=3)
of 175.26 mg.L-1. The preliminary test for chronic effect assessment, conducted in accordance
with the NBR 133732010, revealed a observed effect concentration (CEO) of 100 mg.L-1.
These results demonstrate the unlikely occurrence of ecological risk for Losartan, considering
that effect concentrations were greater than those recognized as environmentally relevant. In
addition, these data may generate support for the establishment of safe concentrations for this
compound in the environmental legislation.
Keywords
Ecotoxicology, pharmaceutical, Losartan, Daphnia similis and Ceriodaphnia dubia.
___________________________________________________________________________
UNISANTA BioScience – p. 49 - 53; Vol. 1, nº 2 (2012)
Página 49
INTRODUÇÃO
O avanço de novas tecnologias e o crescimento populacional permitiu o
desenvolvimento na área da indústria farmacêutica, assim como na descoberta e produção de
novos medicamentos em larga escala. Muitos deles vêm sendo utilizados no mundo todo, em
grandes quantidades (Daughton & Ternes, 1999), tanto na medicina humana como na
medicina veterinária (Khetan & Collins, 2007). Dessa forma, em diversas partes do mundo,
estudos atuais têm abordado a presença de resíduos de fármacos encontrados em matrizes
ambientais (como em água de abastecimentos, águas superficiais e em sedimentos), em
concentrações que variam de pg.L-1 até mg.L-1 (Bila & Dezotti, 2003). Embora as
concentrações de resíduos farmacêuticos sejam baixas no ambiente, a mistura deles pode
provocar efeitos sinérgicos (Reis Filho et al., 2007). As principais classes de fármacos
encontrados no ambiente aquático, com potencial risco de causar efeitos biológicos nos
organismos aquáticos, são os antibióticos, antiinflamatórios, analgésicos, antidepressivos,
antihipertensivos, entre outros (Melo et al., 2009; Daughton & Ternes, 1999; Narvaez &
Jímenez, 2012; Fent et al, 2006). Entre as diversas classes de medicamentos citados
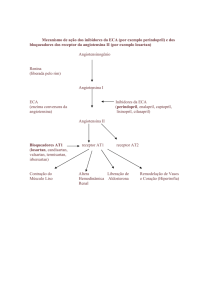
anteriormente, o fármaco Losartan, pertencente a uma classe de antihipertensivos mais
recentes, age de forma a bloquear seletivamente os receptores da angiotensina II,
interrompendo o sistema renina angiotensina (Oparil et al., 2001). No estudo feito por Larsson
et al. (2007) foi constatado a presença deste fármaco em amostras de efluentes na Índia em
concentrações de até 2,5 g.L-1. No estudo realizado por Guimarães et al., (2012) relata a
presença deste composto em água superficial marinha da área adjacente ao descarte do
efluente do emissário submarino de Santos, S.P., destacando a importância deste estudo.
A ocorrência de substâncias farmacêuticas no ambiente aquático leva à necessidade de
se conhecer os possíveis efeitos adversos destas sobre a biota. O emprego de ensaios
ecotoxicológicos é de suma importância para avaliar os efeitos biológicos causados por
efluentes industriais e domésticos, por amostras ambientais e substâncias químicas, dentre
elas os fármacos. Os métodos ecotoxicológicos permitem conhecer os efeitos e os
mecanismos de ação dos contaminantes nos sistemas biológicos (Zagatto, 2006).
Neste contexto, o presente estudo tem como objetivo avaliar a toxicidade do fármaco
Losartan por meio de ensaios de toxicidade para avaliação de efeitos agudos e crônicos em
Daphnia similis e Ceriodaphnia dubia, respectivamente.
MATERIAIS e MÉTODOS
Substância teste
O Losartan (CAS 124750-99-8) (2-butil-4-cloro-1-[[2’-(1H-tetrazol-5-il)[1,1’-bifenil]4-il]metil]1H-imidazol-5-metanol) (Figura 1), pertence a uma classe recente de medicamentos
antihipertensivos bloqueadores dos receptores (tipo AT1) da angiotensina II (Bonfilio, 2010).
UNISANTA BioScience – p. 49 - 53; Vol. 1, nº 2 (2012)
Página 50
Figura 1. Estrutura química do Losartan. Fonte: Hazardous Substances Data Bank.
Ensaio de toxicidade para avaliação de efeito agudo
Este ensaio foi realizado de acordo com a ABNT/NBR 12713/2009. Para realização do
mesmo, neonatas de D. similis (6 a 24 horas de idade) foram expostas a diferentes
concentrações do Losartan, em quatro réplicas, por um período de 48 horas em câmara de
germinação com fotoperíodo (16 horas de luz difusa) e temperatura, controlados (20±2 ºC).
Após o período de exposição foi analisado a imobilidade e mortalidade dos organismos nas
diferentes concentrações. Em seguida foi empregado o método estatístico Trimmed
Spearman-Karber para determinação da concentração efetiva inicial mediana (CE(I)50).
Ensaio de toxicidade para avaliação de efeito crônico
Este ensaio preliminar foi realizado de acordo com a ABNT/NBR 13373/2010. O
efeito na reprodução de C. dubia foi avaliado por meio da exposição de neonatas (até 24 horas
de idade) a diferentes concentrações do Losartan por um período de sete dias em câmara de
germinação com fotoperíodo (16 horas de luz difusa) e temperatura (25±2 ºC) controlados.
Durante o ensaio, a água do controle e as soluções-teste foram renovadas a cada dois dias e as
neonatas geradas foram retiradas e contadas. Ao término do ensaio os dados foram analisados
com o uso do software TOXSTAT 3.5 (West & Gulley, 1996) para determinação da
concentração de efeito observado (CEO) e concentração de efeito não observado (CENO).
RESULTADOS e DISCUSSÃO
Os resultados dos ensaios para avaliação de efeito agudo (n=3) expressos em CE50 48h
e a respectiva média, desvio padrão (DP) e coeficiente de variação (CV) estão apresentados na
Tabela 1.
Tabela 1 – Toxicidade aguda do Losartan para D. similis.
Ensaios
CE5048h (mg.L-1)
(IC)
1
138.70
(117,46 – 163,78)
2
187.97
(174,81 – 202,13)
3
199.12
(181,91 – 217,97)
Média
175,26
--DP
32,15
--CV
18,34
--DP = Desvio Padrão, CV = Coeficiente de Variação, IC = Intervalo de Confiança.
A concentração efetiva média obtida no presente estudo demonstra uma maior
sensibilidade de D. similis quando comparado com os resultados do estudo realizado pela U.S.
UNISANTA BioScience – p. 49 - 53; Vol. 1, nº 2 (2012)
Página 51
Food and Drug Administration (FDA, 2002) com diferentes organismos-teste, como por
exemplo, D. magna (CL5048h – 331 mg.L-1) Pimephales promelas (CL5048h – > 1000 mg.L-1),
Oncorhynchus mykiss (CL5096h – > 929 mg.L-1).
No ensaio de toxicidade preliminar para avaliação de efeito crônico, foram obtidos
valores de CENO e CEO de 10 mg.L -1 e 100 mg.L-1, respectivamente. Estes resultados
também demonstraram uma maior sensibilidade de C. dubia quando comparado aos dados
publicados no estudo acima citado com a microalga Pseudokirchneriella subcaptata (CENO –
143 mg.L-1).
No sentido de garantir um nível elevado de proteção à saúde humana e ao meio
ambiente, a União Europeia colocou em prática o sistema REACH, um sistema integrado
único de registro, avaliação, autorização e restrição de substâncias químicas. No âmbito desta
política, que está em vigor desde 2006, a diretiva 93/67/EEC classifica as substâncias
químicas de acordo com os resultados pontuais de toxicidade (CEC, 1996). Com isso, baseado
nos resultados preliminares obtidos no presente estudo, o Losartan poderia ser classificado
como uma substância “Não tóxica” (CE50 > 100 mg.L -1).
CONCLUSÃO
O Losartan causou efeito agudo em D. similis na concentração média de
175,26 mg.L-1. Já o efeito crônico na reprodução de C. dubia foi observado na concentração
de 100 mg.L-1. Sendo assim, é improvável a ocorrência de efeitos biológicos adversos deste
fármaco no ambiente aquático, pois as concentrações de efeitos são superiores às
concentrações ambientalmente relevantes.
REFERÊNCIAS BIBLIOGRÁFICAS
ABNT – ASSOCIAÇÃO BRASILEIRA DE NORMAS TÉCNICAS. Ecotoxicologia
Aquática. - Toxicidade agudo - Método de ensaio com Daphnia spp. (Crustacea, Cladocera).
Rio de Janeiro. NBR 12713, 2009.
ABNT – ASSOCIAÇÃO BRASILEIRA DE NORMAS TÉCNICAS – Ecotoxicologia
Aquática – Toxicidade crônica – Método de ensaio com Ceriodaphnia spp. (Crustacea,
Cladocera). Rio de Janeiro. NBR 13373, 2010.
BILA, D. M.& DEZOTTI, M. Fármacos no ambiente. Química Nova. 26 (4): p. 523-530,
2003.
BONFILIO, R.; MENDONÇA, T.F.; PEREIRA, G. R.; ARAÚJO, M. B. Losartan potassium
dissolution test for drug release evalution in pharmaceutical capsules using HPLC and UV
spectrophotometry. Química Nova. 33 (2): p. 377-383, 2010.
CEC (COMMISION OF THE EUROPEAN COMMUNITIES). Technical guidance
document in support of commission directive 93/67/EEC on risk assessment for new notified
substances. Part II, environmental risk assessment. Luxemburg: Office for official publication
of the European Communities, 1996.
UNISANTA BioScience – p. 49 - 53; Vol. 1, nº 2 (2012)
Página 52
DAUGHTON, C. G. & TERNES, A. T. Pharmaceutical and personal care products in the
environment: Agent of subtle change? Environment Health Perspectives. 107 (6): p. 907944, 1999.
FDA – U.S. Food and Drug Administration. Center for drug evaluation and research.
Approach Package for: Aplication number 20-386/S-019 and 029. Environment Assesment/
Fonsi. p.8. 2002. Disponível em: <http://www.accessdata. fda.gov/ drugsatfda_docs /nda/
2004/20-86S019_Cozaar_EAFONSI. pdf>. Acesso em: 24 de nov 2012.
FENT, K.; WESTON, A. A.; CAMINADA, D. Ecotoxicology of human pharmaceuticals.
Aquatic Toxicology. 76. p. 122-159. 2006.
GUIMARÃES, L. L.; PEREIRA, C. D. S.; CORTEZ, F. S.; TOMA, W.; CHOUERI, R. B.;
PUSCEDDU, F. H.; SANTOS, A. R.; CÉSAR, A. Determinação de fármacos na área de
influência do emissário submarino de Santos, SP. [Apresentado ao 12º Congresso Brasileiro
de Ecotoxicologia, ECOTOX; 12, 2012, Pernambuco; Brasil]. (Pôster).
HSDB – Hazardous Substances Data Bank. Toxnet. Toxicology Data Network. 2012.
Disponível em: <http://toxnet.nlm.nih.gov/cgi-bin/sis/search/f?./temp/~TxzjK5:1>. Acesso
em: 14 de nov. 2012.
KHETAN, S. K. & COLLINS, T. J. Human pharmaceuticals in the aquatic environment: A
challenge to green chemistry. Chemical Reviews. 107. p. 2319-2364, 2007.
LARSSON, D. G.; PEDRO, C.; PAXAEUS, N. Effluent from drug manufactures contains
extremely high levels of pharmaceuticals. Journal of Hazardous Materials. 148. p. 751-755.
2007.
MELO, S. A. S.; TROVÓ, A. G.; BAUTITZ, I. R.; NOGUEIRA, R. F. P. Degradação de
fármacos residuais por processos oxidativos avançados. Química Nova. 32 (1): p. 188-197,
2009.
NARVAEZ, J. F. V. & JÍMENEZ, C. C. Pharmaceutical products in the environment:
Sources, effects and risks. Vitae. Revista de la Facultad de Química Farmacéutica. 19 (1):
p. 93-108. 2012.
OPARIL, S.; WILLIAMS, D.; CHRYSANT, S.G.; MARBURY, T.C.; NEUTEL, J.
Comparative efficacy of olmesartan, losartan, valsartan, and irbesartan in the control of
essential hypertension. The Journal of Clinical Hypertension. 3(5): p. 283-318. 2001.
REIS FILHO, R. W.; BARREIRO, J. C.; VIEIRA, E. M.; CASS, Q. B. Fármacos, ETEs e
corpos hídricos. Revista Ambi-Água, 2 (3): p. 54-61. 2007.
ZAGATTO, P. A. Ecotoxicologia. In: Zagatto, P. A. & Bertoletti, E. (Eds.). Ecotoxicologia
Aquática: Princípios e Aplicações. São Carlos, S.P. Rima, p. 1-13, 2006.
WEST, Inc. & GULLEY, D. Western Ecossistems Technology. TOXTAT 3.5 Computer
Program., 1996.
UNISANTA BioScience – p. 49 - 53; Vol. 1, nº 2 (2012)
Página 53