Anais do 45º Congresso Brasileiro de Cerâmica
0104101
30 de maio a 2 de junho de 2001 - Florianópolis – SC
INFLUÊNCIA DAS CARACTERÍSTICAS ÁCIDO-BÁSICAS DA SUPERFÍCIE DOS
ÓXIDOS NA ESTABILIDADE DE DISPERSÕES CERÂMICAS DE AL2O3 OU SNO2
COM DISPERSANTES COMERCIAIS
Douglas Gouvêa e Bruno B.S. Murad
Departamento de Engenharia Metalúrgica e de Materiais
Escola Politécnica da USP – Av. Prof. Mello Moraes, 2463 – Cidade
Universitária – São Paulo – SP e-mail [email protected].
Resumo
Uma dispersão cerâmica estável pode ser obtida através da combinação de
um pó cerâmico, um solvente e um dispersante. Polímeros adsorvidos às partículas
de óxidos podem estabilizar uma dispersão através da formação de um potencial de
repulsão entre as partículas que pode ser de origem eletrostática, estérica ou da
combinação das duas. A característica ácida da superfície do SnO 2 faz com que
ocorra uma competição entre a adsorção dos polímeros derivados de ácidos
poliacrílicos e das hidroxilas. O aumento do potencial zeta ocorre devido à mudança
do pH e não devido à adsorção dos polímeros. No caso da alumina, a superfície
básica permite a adsorção dos polímeros e o aumento do potencial zeta sem que
haja competição com os grupos OH-. Este estudo foi realizado através da medida
simultânea de potencial zeta e pH das suspensões através da técnica ESA
(Electrokinetic Sonic Amplitude) com um equipamento ESA 8000 da Matec.
Palavras chave: dispersões cerâmicas, dispersantes, dióxido de estanho, alumina.
Influence of Acid-Basic Characteristic of Al2O3 or SnO2 Surfaces on the
Stability of Ceramic Dispersions with Commercial Dispersants
Abstract
A stable ceramic dispersion can be obtained by mixing a ceramic powder, a
solvent and a dispersant. Polymers adsorbed to ceramic particles may stabilize the
dispersions by creating a repulsion charge among then. The stabilization has an
electrostatic or steric origin, or even the sum of both processes. The adsorption
Anais do 45º Congresso Brasileiro de Cerâmica
0104102
30 de maio a 2 de junho de 2001 - Florianópolis – SC
depends on the characteristics of the powder surface. The basic/acid characteristic of
the surface originates a competition between the adsorption of polymers derived from
polyacrilic acids and hidroxiles due to acidic characteristics of the SnO2 surface. On
the other hand, alumina’s basic surface allows polymers to adsorb and to increase
the zeta potential without any competition between them and OH - ions. This study
was carried out by simultaneously measuring the pH, zeta potential temperature and
conductivity of the system. ESA (Eletrokinetic Sonic Amplitude) technique was used,
with a Matec ESA 8000 equipment.
Key words: ceramic dispersions, commercial dispersants, tin dioxide, alumina.
1 - INTRODUÇÃO
A escolha do tipo de dispersante durante a formulação de uma dispersão
cerâmica depende do solvente utilizado, do método de conformação para a
preparação do corpo cerâmico e das características físico-químicas do pó e de sua
superfície.
As principais características de um pó cerâmico que influenciam a preparação
de uma dispersão são a distribuição granulométrica e as propriedades físicoquímicas da superfície do material. A distribuição granulométrica, principalmente a
fração inferior a 0,5 m, influencia de forma determinante a reologia das suspensões
[1]. O estado da superfície é modificado, por exemplo, pela alteração no número de
hidroxilas formadas devido à hidratação e, em conseqüência, da modificação no
ponto isoelétrico (IEP) e nas isotermas de adsorção dos dispersantes. A utilização
de solventes é necessária para se fornecer fluidez ao sistema e ao mesmo tempo
para possibilitar a homogeneização dos aditivos.
Os solventes podem ser
classificados como polares e não-polares, onde a água é o solvente polar mais
utilizado. Os solventes polares apresentam uma forte interação com a superfície
dos óxidos devido à característica iônica da interface óxido/solvente.
O tipo de conformação utilizado é que determina, na maioria das vezes, o tipo
de solvente.
A pressão de vapor é um outro critério muito importante na sua
seleção. A eliminação do solvente é facilitada pela alta pressão de vapor e de
preferência a temperaturas inferiores às da queima dos ligantes. Paredes ou partes
Anais do 45º Congresso Brasileiro de Cerâmica
0104103
30 de maio a 2 de junho de 2001 - Florianópolis – SC
finas do produto influenciam também a seleção do solvente apropriado. Em peças
com paredes muito finas, a alta volatilidade pode levar a formação de uma tensão
excessiva no interior da peça cerâmica, se os poros forem muito pequenos e
tortuosos. Um alto ponto de ebulição pode ser desejável para evitar-se a formação
de bolhas durante o estágio de eliminação do solvente [1].
Dispersantes são necessários para evitar a sedimentação rápida das partículas
cerâmicas no solvente e para possibilitar a preparação de dispersões com uma alta
concentração de sólido. A natureza e a quantidade otimizada de dispersante pode
ser determinada em função da viscosidade e do comportamento com relação a
sedimentação. Dois mecanismos principais podem agir para gerar forças para a
repulsão entre as partículas: eletrostático e/ou estérico [1].
eletrostático,
as
forças
de
repulsão
são
originadas
No mecanismo
basicamente
pelo
desenvolvimento de cargas elétricas na partícula, em decorrência da interação entre
sua superfície e o meio líquido, formando a dupla camada elétrica. Já no mecanismo
estérico, ocorre a adsorção superficial de polímeros que dificultam a aproximação
das partículas por impedimento mecânico.
Uma dispersão é considerada estável quando não ocorre aglomeração,
coagulação ou floculação das partículas. De fato, o problema é de origem cinética e
consiste em que partículas submetidas ao movimento térmico podem se aproximar
umas das outras a uma distância suficientemente pequena para formar associações,
permanentes ou não. O problema pode ser tratado pela teoria DLVO [1,2]. A
estabilização é controlada pelo potencial elétrico da superfície das partículas e pela
espessura da dupla camada elétrica formada pelos contra-íons (íons que
apresentam cargas opostas àquela da superfície).
O estudo do potencial de
superfície é feito através da determinação do potencial zeta, , que representa o
potencial elétrico no plano de cisalhamento quando a partícula esta em movimento
sob ação de um campo elétrico. Os valores de potencial zeta são relacionados a
estabilidade das dispersões. Um potencial de aproximadamente 20 mV, em valor
absoluto e à temperatura ambiente, é necessário para assegurar a estabilização
eletrostática de suspensões pouco concentradas.
Durante a conformação por deposição eletroforética (EPD) as partículas devem
apresentar um alto potencial zeta, pois o material é conformado através da ação de
um campo elétrico [3], e o solvente deve ser estável a esta solicitação elétrica.
Anais do 45º Congresso Brasileiro de Cerâmica
0104104
30 de maio a 2 de junho de 2001 - Florianópolis – SC
Os dispersantes derivados de polímeros de ácidos acrílicos são os mais
comuns para a preparação de dispersões estáveis de óxidos cerâmicos em água. A
estabilização dessas dispersões é conseguida através do aumento do potencial de
repulsão entre as partículas.
Esta repulsão ocorre porque as moléculas do
dispersante se adsorvem sobre a superfície do pó cerâmico.
Por efeito elétrico
(aumento do potencial zeta) e/ou efeito estérico (aumento da entropia), impede que
as partículas entrem em contato e coagulem [4]. A adsorção deste tipo de polímero
na superfície das partículas de óxidos ocorre, geralmente, devido à formação de
ligações tipo ponte de hidrogênio ou por atração eletrostática.
Em estudos anteriores mostrou-se que a adição de poli (acrilato de amônio)
durante a conformação por EPD de dispersões de SnO 2 diminuem a taxa de
deposição [5].
Ao mesmo tempo verificou-se que a viscosidade da dispersão
aumenta e os valores de potencial zeta, calculados a partir das curvas de cinética de
deposição, diminuíram com o aumento da concentração de dispersante. Todos os
resultados mostraram que a ação do dispersante era pouco efetiva para esse
sistema.
O presente trabalho teve como objetivo verificar a influência de diferentes
dispersantes comerciais nos valores de potencial zeta durante a preparação de
dispersões de SnO2 e Al2O3. Estes dois óxidos são insolúveis em meios ácidos e
básicos ao mesmo tempo em que apresentam pontos isoelétricos (IEP) bastante
diferentes (ácido para o SnO2 e básico para o Al2O3) . Foram realizadas medidas de
potencial zeta em função do pH, tipo e concentração de dispersantes em meios
aquosos.
2 - MATERIAIS E MÉTODOS
Foi utilizado o dióxido de estanho (Minasolo - 99,9% mín. - área de superfície
específica
=
7
m2/g),
alumina
específica = 10 m2/g) , como
(ALCOA
A1000SG
-
área
de
superfície
solvente água destilada e como dispersantes:
Duramax D - 3005 (sal de amônio de um poli eletrólito), Duramax D - 3007 (sal de
amônio de um copolímero acrílico), Duramax - 3021 (sal de amônio de um poli
eletrólito), todos da Rohm and Haas.
Anais do 45º Congresso Brasileiro de Cerâmica
0104105
30 de maio a 2 de junho de 2001 - Florianópolis – SC
As principais características dos dispersantes utilizados são apresentados na
Tabela 1.
Tabela 1 – Principais características dos dispersantes utilizados.
nome
% em massa de sólido
Mw
Contra-íon
pH
D-3005
35
2400
NH4+
7,2
D-3007
45
5000
NH4+
3,2
D-3021
40
2500
NH4+
7,2
Para a análise da influência do pH sobre o potencial zeta da dispersão, utilizouse uma dispersão em água contendo 2% em volume de SnO2 sem a presença de
nenhum dispersante.
Partindo-se do pH inicial, variou-se o pH até 13 através da titulação com uma
solução 2N de hidróxido de potássio. A titulação ácida foi realizada através da
adição com uma solução 2N de ácido nítrico. Tratamento idêntico foi realizado para
uma suspensão aquosa de alumina, contendo 5% em volume de material cerâmico,
partindo-se do pH de equilíbrio da dispersão pH = 9.
Para a análise da influência de cada um dos dispersantes separadamente,
partiu-se de uma suspensão inicial idêntica à descrita no parágrafo anterior,
variando-se a concentração de dispersantes através da adição de uma solução
aquosa de dispersante com concentração 1:5 em volume. O aparelho mediu, então,
a variação do potencial zeta e do pH induzida pela ação das soluções dos diferentes
dispersantes.
Para as medidas de potencial zeta das suspensões, foi usada a técnica ESA
(Electrokinetics Sonic Amplitude), que permite a determinação do potencial zeta para
dispersões com até 10% em volume de sólidos ou a mobilidade eletroforética para
dispersões com até 50% em volume de sólido, ou seja, em condições reais de
preparação de dispersões cerâmicas. A técnica é baseada no efeito eletro-acústico
que se produz quando um campo elétrico alternado de alta freqüência é aplicado
sobre dois eletrodos imersos em uma suspensão de partículas carregadas. O
equipamento utilizado foi o ESA-8000 da MATEC que permitiu a medida simultânea
de potencial zeta, pH, condutividade elétrica e temperatura.
Anais do 45º Congresso Brasileiro de Cerâmica
0104106
30 de maio a 2 de junho de 2001 - Florianópolis – SC
3 - RESULTADOS E DISCUSSÃO
3.1
Variação do potencial zeta em função do pH
As curvas de variação do potencial zeta em função do pH comparativas entre o
SnO2 e Al2O3 são mostradas na Figura 1.
50
SnO2
Al2O3
40
30
(mV)
20
10
0
-10
-20
-30
-40
-50
0
1
2
3
4
5
6
7
8
9
10
11
12
13
14
pH
Figura 1 - Curvas de potencial zeta em função do pH para a alumina e o óxido de
estanho. Dispersões a 2% em volume de SnO2 e 5% em volume de Al2O3.
Os valores de pH ponto isoelétrico (IEP) medidos para a Al2O3 e para o SnO2
foram, respectivamente, 8,0 e 3,5, e estão de acordo com os valores apresentados
na literatura [ 6 ]. Estes valores mostram que a superfície da alumina apresenta
caráter básico e a superfície do SnO2 caráter ácido com relação à água.
Este
comportamento é evidenciado quando os pós dos dois materiais são introduzidos
em água deionizada. O pH da dispersão de SnO2 é cerca de 4 e da alumina em
torno de 9. Isto pode ser interpretado considerando que a superfície do SnO 2 em
água apresenta a tendência a adsorver preferencialmente grupos hidroxilas (OH -),
ou seja, apresentar um comportamento de um ácido fraco. Já o comportamento
para a superfície da alumina é de uma base fraca. Estas características ácidobásicas da superfície devem determinar também o mecanismo de adsorção de
polímeros na superfície dos diferentes óxidos.
Anais do 45º Congresso Brasileiro de Cerâmica
0104107
30 de maio a 2 de junho de 2001 - Florianópolis – SC
As curvas apresentadas na Figura 1 mostram dois valores máximos (em
módulo) de potencial zeta: um a pH ácido e outro a pH básico. É interessante
observar que o maior valor de potencial zeta (em módulo) para cada óxido ocorre
sempre para pH oposto ao pH do ponto isoelétrico, ou seja, para o SnO 2 que
apresenta pHIEP = 3,5 (ácido) o máximo valor de potencial zeta ( = - 39 mV) é obtido
em pH = 11,5 (básico). A alumina o pHIEP = 8,0 e o máximo valor de potencial zeta
( = + 34 mV) é obtido para pH = 2,4. O fenômeno observado evidencia que a
afinidade da superfície com comportamento de um base fraca é maior para íons H + e
aquela que apresenta comportamento de uma ácido fraco é maior para os íons OH -.
Deve-se levar em consideração que, no caso da adsorção de um polímero à
superfície do óxido, a característica de doação ou recepção de pares eletrônicos
(conceito de ácido e bases de Lewis) pode ter uma influência determinante na
energia de adsorsão.
Outro fator que deve ser levado em consideração é a
capacidade da adsorsão dos polímeros ocorrer através da formação de pontes de
hidrogênio com as hidroxilas formadas na superfície dos óxidos imersos em água.
A curva de potencial zeta em função do pH para a alumina apresenta apenas
uma inflexão (pH 8), correspondente à estabilização de um tipo e ligação entre a
superfície do óxido e um grupo de íons OH- da água. Para o dióxido de estanho,
além dessa inflexão (pH 9), vê-se uma inflexão (em pH 3,5), semelhante a um
patamar. Provavelmente, essa segunda inflexão corresponde a um outro tipo de
interação superfície/íon OH-, que será estudada em posterior etapa do trabalho
através de análise por espectroscopia no infravermelho.
3.2
Influência da concentração de dispersantes no potencial zeta e pH de
dispersões de SnO2 e Al2O3
3.2.1 O caso do SnO2
A análise da influência da concentração de cada um dos dispersantes no pH e
no potencial zeta da dispersão de SnO2 é mostrada na seqüência de curvas da
Figura 2.
A adição dos dispersantes torna mais negativo o potencial zeta em todos os
casos. O máximo valor de potencial zeta obtido foi de = -23 mV e ocorreu para o
Anais do 45º Congresso Brasileiro de Cerâmica
0104108
30 de maio a 2 de junho de 2001 - Florianópolis – SC
dispersante D-3021. Os dispersantes D-3005 e D-3021 levaram a uma variação
bastante sensível no pH da dispersão obtendo-se um pH final de 7,5. No caso do
3007 o pH final se mantém ácido em torno de 3,5.
zeta
-5
pH
D-3005
(A)
(mV)
-10
-15
-20
-25
-30
0,00
0,02
0,04
0,06
12
11
10
9
8
7 pH
6
5
4
3
2
0,08
0
zeta
-15
-20
-25
-30
0,00
0,02
0,04
12
11
(B)
10
9
8
7 pH
6
5
4
3
2
0,06
0,08
volume de dispersante/massa de SnO2 (ml/g)
0
zeta
pH
D-3021
-5
(C)
-10
(mV)
D-3007
-10
volume de dispersante/massa de SnO2 (ml/g)
-15
-20
-25
-30
0,00
pH
-5
(mV)
0
0,02
0,04
0,06
12
11
10
9
8
7 pH
6
5
4
3
2
0,08
volume de dispersante/massa de SnO2 (ml/g)
Figura 2 - Comparação do comportamento do pH e do potencial zeta para
dispersões de SnO2 2% em volume com diferentes dispersantes: (A) D3005, (B)
D3007 e (C) D3021.
Os dispersantes D-3005 e D-3021 são mantidos em pH básico (com relação
ao pKa de ionização do polímero) para que a dissociação de seus grupos acrilatos
leve a formação de cargas elétricas. Quando o polímero se adsorve a superfície do
óxido as cargas geradas pela ionização do mesmo podem contribuir para o aumento
do potencial zeta e, em conseqüência, da formação de uma dispersão mais estável.
Os dispersantes derivados de poliácidos acrílicos devem permanecer
ionizados em solução aquosa. Para isso, o pH básico é mantido através da adição
de NH4(OH) ou NaOH. Esse é o caso dos dispersantes D-3005 e D-3021. Desta
forma, o pH da solução será sempre básico.
A variação observada no pH é devida ao pH final da solução de dispersantes.
O pH final das soluções dos dispersantes D-3005 e D-3021 é 7,2. No caso do
dispersante D3007, o pH final da solução é 3,2. Como o pH da dispersão de SnO 2 é
Anais do 45º Congresso Brasileiro de Cerâmica
0104109
30 de maio a 2 de junho de 2001 - Florianópolis – SC
igual a 4, era esperado que no caso dos dispersantes D-3005 e D-3021 o pH
aumentasse e no caso do D-3007, diminuísse. O mais interessante é observar que,
na Figura 3, o potencial zeta pára de aumentar em módulo justamente para valores
de pH igual ao pH final das soluções dos dispersantes D-3005 e D-3021. Isto pode
significar que a variação do potencial zeta observado para tais tipos de dispersantes
está diretamente ligada à variação do pH, e não especificamente à adsorção das
moléculas dos dispersantes. Este comportamento explicaria o fenômeno observado
durante a deposição por eletroforese do SnO2 com dispersantes à base de
poli(acrilatos de amônio) [5]. A diminuição da massa depositada ocorreria devido ao
aumento da viscosidade da solução. Desde que o dispersante não se adsorve à
superfície das partículas, todo material adicionado contribuiria para o aumento da
viscosidade do líquido, e assim, segundo o modelo proposto, diminuiria a taxa de
deposição do SnO2.
No caso do D-3007, em que a variação do pH não é significativa, observa-se
um aumento do valor em módulo do potencial zeta. Contudo, os valores máximos
obtidos não chegam a -19 mV, o que significa uma dispersão ainda pouco estável.
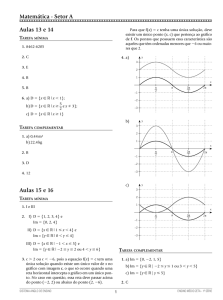
Figura 3 - Variação do potencial zeta em função do pH para o SnO2 com os
diferentes dispersantes, comparadas ao efeito sobre o pH da titulação com soluções
aquosas de HNO3 (2N) e KOH (2N) .
3.2.2 O caso do Al2O3
Para as dispersões de Al2O3, a variação de potencial zeta e pH com a adição
da solução de diferentes tipos de dispersantes pode ser observada na. Os
Anais do 45º Congresso Brasileiro de Cerâmica
0104110
30 de maio a 2 de junho de 2001 - Florianópolis – SC
dispersantes D-3005 e D-3021 parecem ser muito efetivos na estabilização
deste material, já que a variação de pH é bastante pequena enquanto o potencial
zeta obtido é muito superior a –20mV. No caso do dispersante D-3007 ocorre uma
nítida variação para pH ácido, ao mesmo tempo que os valores de potencial zeta
são significativamente menores
0
10
zeta
pH
(mV)
6
-40
0,04
0,06
0,08
0,10
9
-20
4
0,12
6
5
-50
0,00
volume de dispersante/massa de alumina (ml/g)
0,02
0,06
0,08
0,10
4
0,12
10
9
-10
(mV)
0,04
volume de dispersante/massa de alumina (ml/g)
0
8
-20
zeta
pH
D-3021
(C)
-30
-40
-50
0,00
8
7 pH
-30
-40
5
0,02
D-3007
(B)
7 pH
-30
pH
-10
8
(A)
-20
-50
0,00
10
zeta
9
-10
(mV)
0
D-3005
7 pH
6
5
0,02
0,04
0,06
0,08
0,10
4
0,12
volume de dispersante/massa de alumina (ml/g)
Figura 4 - Variação do potencial zeta e do pH em função da adição de solução de
dispersantes D-3005 (A), D-3007(B) e D-3021(C) a uma dispersão de alumina em
água (5 % em volume de sólido).
No caso da alumina, os dispersantes parecem adsorver à superfície das
partículas e modificam a dupla camada elétrica elevando sua carga superficial
negativa e possibilitando a estabilização das dispersões. Contudo, a diminuição do
pH faz com que o potencial zeta final seja inferior ao obtido com os dispersantes D3005 e D-3021.
A variação do potencial zeta em função do pH para as dispersões de alumina
com a adição de diferentes dispersantes pode ser observada na Figura 5. Para o
dispersante D-3007 fica nítida a variação do pH ao mesmo tempo em que ocorre a
estabilização dos valores de potencial zeta.
Anais do 45º Congresso Brasileiro de Cerâmica
0104111
30 de maio a 2 de junho de 2001 - Florianópolis – SC
0
D-3021
-10
D-3007
(mV)
D-3005
-20
-30
-40
-50
5
6
7
8
9
10
pH
Figura 5 - Variação do potencial zeta em função do pH para a alumina com os
diferentes dispersantes.
3.3. Comparação entre as dispersões de SnO2 e Al2O3
A adição de solução dos dispersantes D-3005 e D-3021 ao SnO2 parece gerar
uma modificação do potencial zeta devido ao aumento do pH. No caso da alumina, o
efeito parece estar ligado à adsorsão destes polímeros à superfície dos grãos de
Al2O3, que ocorre, no caso de óxidos, por pontes de hidrogênio[1]. A superfície do
SnO2, por apresentar um IEP ácido, tem uma grande afinidade por grupos OH enquanto o Al2O3 apresenta um IEP básico e, por conseqüência, grande afinidade
por íons H+. A adição de uma solução de polímero em meio básico a uma dispersão
de SnO2 deve gerar uma competição entre a adsorção de OH - e do polímero à
superfície. A ligação do OH- deve ser muito mais forte, uma vez que tal espécie é um
íon determinante de potencial e, por conseqüência,
preferencial
sua adsorção deve ser
à ligação dos polímeros por pontes de hidrogênio à superfície dos
SnO2.
Ao mesmo tempo, a geração de cargas elétricas negativas na superfície do
SnO2 devido à adsorção dos grupos OH- pode, por repulsão eletrostática, impedir a
adsorção do polímero que se encontra carregado negativamente. No caso da
alumina, ocorre justamente o inverso. Em primeiro lugar, a dispersão já se encontra
em um pH mais básico que a solução e não existe geração de cargas negativas. As
moléculas de polímero podem se adsorver a superfície da alumina por pontes de
hidrogênio com as hidroxilas superficiais. Com a adição de um dispersante acrílico
em meio ácido (caso do D-3007) deve ocorrer uma competição entre a adsorção dos
íons H+ e o polímero carregado negativamente para a alumina.
Anais do 45º Congresso Brasileiro de Cerâmica
0104112
30 de maio a 2 de junho de 2001 - Florianópolis – SC
Desta forma, o potencial zeta total diminui e o valor máximo é bastante menor
que no caso dos outros dois dispersantes.
4 - CONCLUSÕES
A adsorção de polímeros na superfície de um pó cerâmico com a finalidade
de formação de uma dispersão estável é dependente das características ácidobásicas da superfície do óxido cerâmico utilizado e do tipo de polímero. Para óxidos
com IEP básico, como no caso da alumina, a adsorção de polímeros em meio básico
deve ocorrer por pontes de hidrogênio à superfície dos grãos e o aumento do
potencial zeta é devido à carga elétrica do dispersante que se encontra ionizado. No
caso de óxidos com IEP ácido, como no caso do SnO2, deve ocorrer uma
competição entre a adsorção de hidroxilas e a adsorção dos polímeros. Como o OH é um íon determinante de potencial para os óxidos sua adsorção deve ocorrer
preferencialmente àquela do polímero por pontes de hidrogênio. A geração de uma
carga superficial negativa pode por repulsão eletrostática impedir a adsorção do
polímero carregado negativamente.
Neste caso a mudança de potencial zeta
observada se deve unicamente à modificação do pH da solução. Caso semelhante
ocorre para a alumina com o dispersante D-3007, onde ocorre a competição entre a
adsorção do polímero e das espécies H+.
5 - AGRADECIMENTOS
À FAPESP pelo financiamento do projeto 97/06152-2 e à Rohm & Haas pelas
amostras dos dispersantes.
Anais do 45º Congresso Brasileiro de Cerâmica
0104113
30 de maio a 2 de junho de 2001 - Florianópolis – SC
6 - REFERÊNCIAS BIBLIOGRÁFICAS
[1]
J. P. Robert, L. Bergström and M. Dekker, Surface and Colloid Chemistry in
Advanced Ceramic Processing – Surfactant Science Series v. 51, Edited by, New
York, (1994), p. 136.
[2] F.S. Ortega, V.C. Pandolfelli e J.A. Rodrigues, Aspectos da Reologia e
Estabilidade de Suspensões Cerâmicas. Parte I: Fundamentos, Cerâmica, 43,
279 (1997), 5-10.
[3] P.Sarkar and P.S. Nicholson, Electrophoretic Deposition (EPD): Mechanisms,
Kinetics, and Applications to Ceramics, J. Am. Ceram. Soc., 79, 8, (1996), 1987 –
2002.
[4] F.S. Ortega, V.C. Pandolfelli e J.A. Rodrigues e D.P.F. de Souza, Aspectos da
Reologia e Estabilidade de Suspensões Cerâmicas. Parte II: Mecanismos de
Estabilidade Eletrostática e Estérica, Cerâmica 43, 280 (1997), 77-83.
[5] D.Gouvêa e B.S.S. Murad, Estudo Sobre a Influência das Concentrações de
Sólido e de um Dispersante sobre a Cinética de Deposição por Eletroforese do
SnO2, Cerâmica, 45, 292/293 (1999), 103-106.
[6] R.W. Cahn, P. Haasen and E.J.Kramer, Materials Science and Technology – A
Comprehensive Treatment, Processing of Ceramics – Part I, vol. 17A, New York,
editora VHC, (1996), p. 178.