Revisão – Química 2
Professor Jefferson Silva
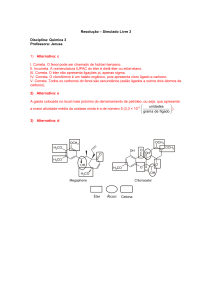
1. Reproduzir artificialmente todo o percurso químico de produção da morfina que acontece
nas papoulas é um grande desafio.
Em 2015, através da modificação genética do fermento, cientistas conseguiram transformar
açúcar em reticulina, cuja transformação em morfina, usando fermentos modificados, já era
conhecida.
Considere as afirmações abaixo, sobre a reticulina e a morfina.
I. Ambas apresentam as funções éter e hidroxila fenólica.
II. Ambas apresentam uma amina terciária.
III. Ambas apresentam dois anéis aromáticos.
Quais estão corretas?
a) Apenas I.
b) Apenas III.
c) Apenas I e II.
d) Apenas II e III.
e) I, II e III.
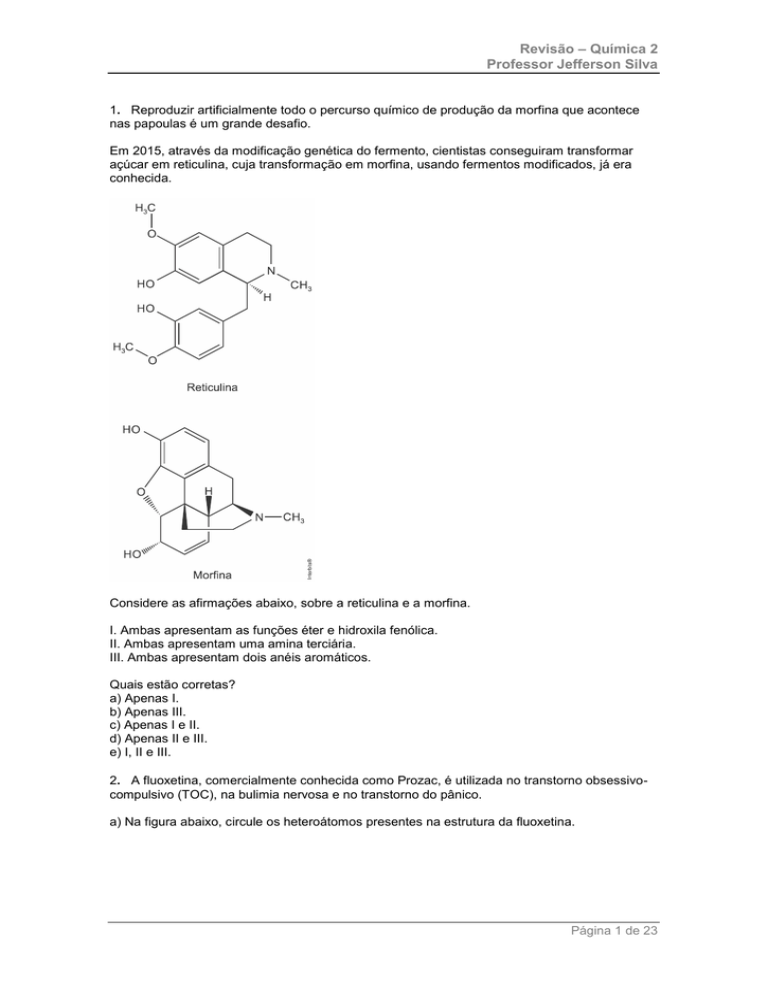
2. A fluoxetina, comercialmente conhecida como Prozac, é utilizada no transtorno obsessivocompulsivo (TOC), na bulimia nervosa e no transtorno do pânico.
a) Na figura abaixo, circule os heteroátomos presentes na estrutura da fluoxetina.
Página 1 de 23
Revisão – Química 2
Professor Jefferson Silva
b) Quais classes funcionais e qual tipo de isomeria espacial estão presentes na estrutura da
fluoxetina?
3. Sobre o composto abaixo, assinale o que for correto.
01) Seu nome IUPAC é 2-metil-1,4-pentadieno.
02) É um hidrocarboneto acíclico que apresenta duas ligações duplas.
04) É um isômero do 3-metil-1,4-hexadieno.
08) Todos os carbonos apresentam hibridação sp2 .
16) É um dieno.
4. Analise a fórmula que representa a estrutura do iso-octano, um derivado de petróleo
componente da gasolina.
De acordo com a fórmula analisada, é correto afirmar que o iso-ocatano
a) é solúvel em água.
b) é um composto insaturado.
c) conduz corrente elétrica.
d) apresenta carbono assimétrico.
e) tem fórmula molecular C8H18 .
5. Extrair um dente é um procedimento que não requer anestesia geral, sendo utilizados,
nesses casos, os anestésicos locais, substâncias que insensibilizam o tato de uma região e,
dessa forma, eliminam a sensação de dor. Você já pode ter entrado em contato com eles no
dentista ou se o médico lhe receitou pomada para aliviar a dor de queimaduras.
Exemplos de anestésicos locais são o eugenol e a benzocaína, cujas fórmulas estruturais
aparecem a seguir.
Página 2 de 23
Revisão – Química 2
Professor Jefferson Silva
Sobre as estruturas acima, é CORRETO afirmar que
a) o eugenol representa um hidrocarboneto insaturado.
b) a benzocaína possui uma estrutura saturada e homogênea.
c) as duas estruturas representam hidrocarbonetos insaturados e heterogêneos.
d) se verifica a presença de um grupo funcional ácido carboxílico no eugenol.
e) a benzocaína possui um grupo funcional amina e uma estrutura insaturada.
6. Analise as fórmulas que representam as estruturas do retinol (vitamina A), lipossolúvel, e
do ácido pantotênico (vitamina B5), hidrossolúvel.
Com base na análise das fórmulas, identifique as funções orgânicas presentes em cada
vitamina e justifique por que a vitamina B5 é hidrossolúvel e a vitamina A é lipossolúvel. Qual
dessas vitaminas apresenta isomeria óptica? Justifique sua resposta.
7. O uso de drogas tem gerado sérios problemas de saúde e sociais em muitos casos,
resultando na morte dos usuários. Esse é o caso do LSD-25, sigla alemã referente à
dietilamida do ácido lisérgico, uma das mais potentes substâncias alucinógenas de que se tem
conhecimento. A atividade dessa droga está relacionada a sua estrutura, na qual existem dois
carbonos esterogênicos, um grupo funcional amina, dois grupos amida. Essa molécula interfere
no mecanismo de ação da serotonina, um neurotransmissor do cérebro, causando os efeitos
alucinógenos e outras complicações.
Qual das estruturas representadas abaixo corresponde ao LSD25 ?
a)
Página 3 de 23
Revisão – Química 2
Professor Jefferson Silva
b)
c)
d)
e)
8. A síntese da substância 1 (óleo essencial de banana) é obtida através da reação clássica
conhecida com esterificação de Fischer.
Em relação à reação apresentada, podemos afirmar que
a) os reagentes empregados são aldeído e éter.
b) a reação não pode ser conduzida em meio ácido.
c) o produto orgânico obtido é denominado de etanoato de isoamila.
d) o álcool é denominado de acordo com a IUPAC, 2 metil butan 4 ol.
e) os reagentes empregados são cetona e éster.
9. Alimentos funcionais são alimentos que, além de suprir as necessidades diárias de
carboidratos, proteínas, vitaminas, lipídios e minerais, contêm substâncias que ajudam a
prevenir doenças e a melhorar o metabolismo e o sistema imunológico. O quadro a seguir
apresenta dois compostos funcionais investigados pela ciência.
Página 4 de 23
Revisão – Química 2
Professor Jefferson Silva
alimentos
componentes ativos
propriedades
sálvia, uva,
soja, maçã
ação antioxidante,
antisséptica e vaso
constritora
sardinha,
salmão, atum,
truta
redução do
colesterol e ação
anti-inflamatória
(http://ainfo.cnptia.embrapa.br. Adaptado.)
a) Em relação à molécula de tanino, qual é o grupo funcional que une os anéis aromáticos ao
anel não aromático e qual é o grupo funcional que confere características ácidas a esse
composto?
b) Escreva a equação química da reação entre o ácido alfa-linolênico e o metanol.
10. A curcumina é um composto natural abundante no rizoma da erva perene cúrcuma
(Curcuma longa Linnaeus). Na índia, essa erva é utilizada na culinária como corante e também
na medicina por ter ação anti-inflamatória, anticarcinogênica e anti-infecciosa.
(Quím. Nova, vol. 37, 2014. Adaptado.)
a) Circule e identifique, na estrutura da curcumina a seguir, os grupos característicos das três
funções orgânicas presentes nesse composto.
b) Escreva a fórmula molecular da curcumina.
11. Quando há falta de insulina e o corpo não consegue usar a glicose como fonte de energia,
as células utilizam outras vias para manter seu funcionamento. Uma das alternativas
encontradas é utilizar os estoques de gordura para obter a energia que lhes falta. Entretanto, o
resultado desse processo leva ao acúmulo dos chamados corpos cetônicos.
(www.drauziovarella.com.br. Adaptado.)
Página 5 de 23
Revisão – Química 2
Professor Jefferson Silva
a) Dê a nomenclatura IUPAC e a nomenclatura comercial do corpo cetônico representado.
b) Escreva a fórmula estrutural do isômero de função desse corpo cetônico com a sua
respectiva nomenclatura IUPAC.
12. As fórmulas estruturais de alguns componentes do aroma do azeite de oliva estão
representadas as seguir.
a) Classifique as substâncias 1, 2 e 3 segundo os radicais funcionais que possuem.
b) Indique qual das fórmulas estruturais corresponde a um isômero geométrico do tipo cis.
Escreva a estrutura completa desse isômero, com todos os átomos representados, com a
sua indicação cis.
13. As substâncias cujas fórmulas estruturais estão apresentadas a seguir são alguns dos
constituintes químicos encontrados no pequi, um fruto muito apreciado na culinária goiana.
a) Entre as estruturas representadas, indique aquelas que possuem radicais funcionais
característicos de ésteres e de alcoóis.
b) Entre as fórmulas estruturais apresentadas, indique aquelas que correspondem a
substâncias alifáticas e escreva a fórmula molecular para a substância 5.
14. Duas das moléculas presentes no gengibre são benéficas à saúde: shogaol e gingerol.
Observe suas fórmulas estruturais:
Aponte o tipo de isomeria espacial presente, respectivamente, em cada uma das estruturas.
Página 6 de 23
Revisão – Química 2
Professor Jefferson Silva
Nomeie, ainda, as funções orgânicas correspondentes aos grupos oxigenados ligados
diretamente aos núcleos aromáticos de ambas as moléculas.
15. Os monômeros buta-1,3-dieno e 2-cloro-buta-1,3-dieno são muito utilizados na
fabricação de borrachas sintéticas, sendo, este último, também conhecido como cloropreno,
uma substância resistente a mudanças de temperatura, à ação do ozônio e ao clima adverso.
a) Escreva as fórmulas estruturais dos monômeros mencionados.
b) A partir do monômero 2-cloro-buta-1,3-dieno é obtido o poli2-cloro-but-2-eno conhecido
comercialmente como neopreno, um elastômero sintético. Escreva a reação de obtenção do
neopreno a partir do cloropreno e indique o tipo de isomeria espacial que ocorre nesse
elastômero.
16. A gasolina é constituída por uma mistura de compostos de carbono, predominantemente
por alcanos. O ponto de ebulição desses compostos aumenta, proporcionalmente, com o
aumento do número de átomos de carbono presentes nas respectivas estruturas. Entretanto, a
presença de ramificações em estruturas de alcanos contendo o mesmo número de átomos de
carbono promove diminuição do ponto de ebulição.
De acordo com essas considerações, responda aos itens a seguir.
a) Disponha os alcanos, a seguir em ordem crescente de ponto de ebulição, usando os
números de I a V.
(I) 2-metil-hexano
(II) heptano
(III) 3,3-dimetilpentano
(IV) hexano
(V) 2-metilpentano
b) Quantos isômeros estruturais possui o hexano?
Represente a fórmula estrutural completa para cada isômero estrutural.
17. O etanol, CH3CH2OH, é o biocombustível mais utilizado no Brasil. O seu uso em
substituição aos derivados do petróleo contribui na redução de gases poluentes e na mitigação
do efeito estufa. O éter dimetílico, isômero do etanol, é um combustível que pode ser obtido a
partir do gás natural ou a partir da biomassa.
a) Escreva a equação balanceada da reação da combustão completa do etanol.
b) Apresente a fórmula estrutural do éter dimetílico. Qual tipo de isomeria ocorre entre o etanol
e o éter dimetílico?
TEXTO PARA A PRÓXIMA QUESTÃO:
Leia o texto para responder à(s) questão(ões).
A torta do algodão, subproduto da extração do óleo das sementes, contém proteínas e energia,
e pode ser usada para alimentação de animais. Entretanto, o uso é limitado devido à presença
de gossipol entre os componentes da torta.
(“Uso de subprodutos de algodão na nutrição de ruminantes”, 2010.
www.RCVT.org.br.Adaptado).
18. Analise a fórmula estrutural do gossipol apresentada.
Página 7 de 23
Revisão – Química 2
Professor Jefferson Silva
a) Determine a fórmula molecular do gossipol.
b) Identifique as funções orgânicas presentes na estrutura apresentada para o gossipol.
TEXTO PARA A PRÓXIMA QUESTÃO:
Analise a tabela a seguir para responder à(s) questão(ões).
Substância
Fórmula estrutural
Exemplo de aplicação
1
Solvente para gomas, corantes, gorduras,
ceras e borrachas.
2
Solvente orgânico, usado por muito tempo
como anestésico por inalação.
3
Germicida para uso externo.
4
Intermediário em síntese de fármacos.
5
Síntese de polímeros condutores.
19. a) Dentre as substâncias relacionadas na tabela, indique aquelas que possuem átomo de
carbono quiral.
b) Informe qual a característica de substâncias que apresentam átomo de carbono quiral.
20. O composto a seguir, representado por sua estrutura química, é um metabólito importante
de espécies de Leishmania.
Página 8 de 23
Revisão – Química 2
Professor Jefferson Silva
As seguintes afirmações são feitas a respeito desse composto:
I. sua massa molar é igual a 291 g mol1.
II. o carbono diretamente ligado à função orgânica amina é classificado como secundário.
III. todos os átomos de carbonos externos aos dois ciclos possuem hibridização sp3 .
IV. sua estrutura química apresenta apenas um átomo de carbono quaternário.
Assinale a alternativa CORRETA.
a) Apenas as afirmações I e II são verdadeiras.
b) Apenas as afirmações II e IV são verdadeiras.
c) Apenas as afirmações I, III e IV são verdadeiras.
d) Apenas as afirmações II, III e IV são verdadeiras.
e) Apenas as afirmações II e III são verdadeiras.
21. O confrei (Symphytum officinale L.) é uma planta utilizada na medicina tradicional como
cicatrizante, devido à presença da alantoína (estrutura 1), mas também possui alcaloides
pirrolizidínicos, tais como o da estrutura 2, os quais são comprovadamente hepatotóxicos e
carcinogênicos. O núcleo destacado na estrutura 2 recebe o nome de necina ou núcleo
pirrolizidina.
a) Nas estruturas 1 e 2, os grupos funcionais que contêm átomos de oxigênio caracterizam
duas funções orgânicas. Relacione cada função com o respectivo composto.
b) A estrutura 1 apresenta isomeria óptica? Qual é o caráter ácido-básico do grupo necina?
Justifique suas respostas.
22. Deu no noticiário do Bom Dia Brasil:
“A polícia civil de São Paulo está à procura de seis mulheres suspeitas de aplicar um golpe
conhecido como boa noite, Cinderela”.
Boa noite, Cinderela refere-se a um crime que consiste em drogar uma vítima para roubá-la ou
estuprá-la. As drogas que costumam ser usadas nessa prática são GHB (ácido 4hidroxibutanoico), Ketamina, rohypnol e clorofórmio (triclorometano). Em comum essas
drogas apresentam um efeito depressor sobre o sistema nervoso central.
Página 9 de 23
Revisão – Química 2
Professor Jefferson Silva
Fonte: Telejornal Bom dia Brasil. São Paulo. TV Globo, 15 set. 2014
Para as duas substâncias destacadas em negrito, demonstre se ambas apresentam carbonos
quirais. Justifique sua resposta.
23. Em uma das etapas do ciclo de Krebs, a enzima aconitase catalisa a isomerização de
citrato em isocitrato, de acordo com a seguinte equação química:
A isomeria plana que ocorre entre o citrato e o isocitrato é denominada de:
a) cadeia
b) função
c) posição
d) compensação
24. O Mal de Parkinson, doença degenerativa cuja incidência vem crescendo com o aumento
da duração da vida humana, está associado à diminuição da produção do neurotransmissor
dopamina no cérebro. Para suprir a deficiência de dopamina, administra-se por via oral um
medicamento contendo a substância dopa. A dopa é absorvida e transportada nessa forma
para todo o organismo, através da circulação, penetrando no cérebro, onde é convertida em
dopamina, através de reação catalisada por enzima adequada, representada pela equação:
a) Identifique as funções orgânicas presentes em cada uma das duas substâncias, dopa e
dopamina.
b) Analise as fórmulas da dopa e da dopamina e decida se as substâncias apresentam
atividade óptica. Em caso positivo, copie a fórmula estrutural correspondente para o espaço
de resolução e resposta, de uma ou de ambas as substâncias, assinalando na fórmula o
átomo responsável pela atividade óptica.
25. Óleos vegetais contêm ésteres triglicerídeos. Ao reagir com etanol, esses triglicerídeos se
transformam num tipo de biodiesel, isto é, numa mistura de ésteres etílicos.
O esquema representa o processo químico envolvido na produção desse biodiesel a partir do
éster triglicerídeo mais abundante do óleo de soja.
Página 10 de 23
Revisão – Química 2
Professor Jefferson Silva
a) Considerando as proporções estequiométricas, CALCULE a massa de etanol, CH3CH2OH,
necessária para reagir com 1 mol de triglicerídeo.
b) ESCREVA a fórmula estrutural da glicerina, um subproduto da produção do biodiesel.
c) INDIQUE se a cadeia carbônica ligada à carbonila dos ésteres etílicos dos ácidos oleico e
linoleico é saturada ou insaturada. No caso de ser insaturada, INDIQUE também o número
de ligações duplas existentes na cadeia carbônica.
Página 11 de 23
Revisão – Química 2
Professor Jefferson Silva
Gabarito:
Resposta da questão 1:
[C]
A reticulina e a morfina apresentam as funções éter e hidroxila fenólica e, também, amina
terciária (átomo de nitrogênio ligado a três átomos de carbono):
A reticulina apresenta dois núcleos aromáticos e a morfina apresenta um núcleo aromático:
Resposta da questão 2:
a) Heteroátomos presentes na estrutura da fluoxetina:
Página 12 de 23
Revisão – Química 2
Professor Jefferson Silva
b) Classes funcionais: haleto, éter e amina.
Tipo de isomeria espacial: isomeria óptica (pois a molécula apresenta carbono assimétrico ou
quiral).
Resposta da questão 3:
01 + 02 + 16 = 19.
[01] Correta. O nome oficial do composto, de acordo com as regras da IUPAC será:
Ramificação: grupo metil (ligado ao 2 carbono da cadeia principal)
Cadeia principal: 5 carbonos (pent) com duas ligações duplas (dien), nos carbonos 1 e 4
da cadeia.
Assim teremos: 2-metil-1,4-pentadieno.
[02] Correta. O composto apresenta uma cadeia aberta (acíclica) com duas ligações duplas em
sua cadeia principal.
[04] Incorreta. A quantidade de átomos de carbono e hidrogênio das duas moléculas são
diferentes, condição para que ocorra isomeria.
[08] Incorreta. Os carbonos que apresentam hibridação sp2 irão apresentar nessa molécula
ligação dupla, e os carbonos assinalados abaixo apresentam apenas ligações simples:
[16] Correta. O composto é um dieno, ou seja, apresenta duas duplas.
Resposta da questão 4:
[E]
Página 13 de 23
Revisão – Química 2
Professor Jefferson Silva
O iso-octano é insolúvel em água, pois é apolar, é um composto saturado, pois apresenta
apenas ligações simples entre os átomos de carbono.
Não conduz eletricidade, pois não sofre ionização.
Não apresenta carbono quiral ou assimétrico.
O iso-octano tem fórmula molecular C8H18 .
Resposta da questão 5:
[E]
[A] Incorreta. Um hidrocarboneto possui apenas átomos de carbono e hidrogênio.
[B] Incorreta. A benzocaína possui uma estrutura insaturada, pois apresenta ligações duplas
entre carbonos.
[C] Incorreta. Em ambas as estruturas a cadeia principal é o anel benzênico, sendo portanto,
classificadas como cadeia homogênea.
[D] Incorreta. O eugenol apresenta as funções: fenol e éter.
[E] Correta. A benzocaína apresenta o grupo amina (NH2 ) ligada ao anel benzênico que
apresenta duplas ligações, ou seja, é insaturada.
Resposta da questão 6:
Funções orgânicas presentes em cada vitamina:
A vitamina B5 é hidrossolúvel, pois apresenta grupos que fazem ligações de hidrogênio com a
água, ou seja, as funções álcool, amida e ácido carboxílico.
A vitamina A é lipossolúvel, pois é predominantemente apolar, fazendo dipolo-induzido com as
cadeias de moléculas de gordura.
A vitamina B5 ou ácido pantotênico apresenta isomeria óptica, pois possui carbono quiral ou
assimétrico.
Página 14 de 23
Revisão – Química 2
Professor Jefferson Silva
Resposta da questão 7:
[D]
A atividade da dietilamida do ácido lisérgico está relacionada a sua estrutura, na qual existem
dois carbonos esterogênicos (* carbonos quirais ou assimétricos), um grupo funcional amina,
dois grupos amida.
Resposta da questão 8:
[C]
[A] Incorreta. Os reagentes empregados possuem as funções: ácido carboxílico e álcool.
[B] Incorreta. A reação se processa em meio ácido.
[C] Correta. O éster formado recebe o nome de acetato de isopentila ou etanoato de isoamila.
[D] Incorreta. O álcool é denominado de 3-metil butan-1-ol.
[E] Incorreta. Os reagentes empregados são: ácido carboxílico e álcool.
Resposta da questão 9:
a) O grupo funcional carboxilato (função éster) une os anéis aromáticos ao anel não
aromático no tanino.
O grupo funcional que confere características ácidas a esse composto é o fenol.
Página 15 de 23
Revisão – Química 2
Professor Jefferson Silva
b) Equação química da reação entre o ácido alfa-linolênico e o metanol:
Resposta da questão 10:
a) Grupos característicos das três funções orgânicas presentes nesse composto (éter, fenol
e cetona):
b) Fórmula molecular da curcumina: C21H20O6 .
Resposta da questão 11:
a) Nomenclatura IUPAC: propanona.
Nomenclatura comercial: acetona.
b) Fórmula estrutural do isômero de função da propanona, o propanal (nomenclatura IUPAC):
Página 16 de 23
Revisão – Química 2
Professor Jefferson Silva
Resposta da questão 12:
a) Teremos:
b) A fórmula estrutural que corresponde a um isômero geométrico (substância 3) do tipo cis é:
Resposta da questão 13:
a) Estruturas que possuem radicais funcionais característicos de ésteres e de alcoóis: 3, 5 e
1, respectivamente.
b) Fórmulas estruturais que correspondem a substâncias alifáticas (não aromáticas): 1, 3 e 4.
Página 17 de 23
Revisão – Química 2
Professor Jefferson Silva
Fórmula molecular para a substância 5: C14H6O8 .
Resposta da questão 14:
Tipo de isomeria espacial presente:
Funções orgânicas correspondentes aos grupos oxigenados ligados diretamente aos núcleos
aromáticos:
Página 18 de 23
Revisão – Química 2
Professor Jefferson Silva
Resposta da questão 15:
a) Fórmulas estruturais:
b) A partir do monômero 2-cloro-buta-1,3-dieno é obtido o poli 2-cloro-but-2-eno conhecido
comercialmente como neopreno:
Tipo de isomeria espacial presente no neopreno: cis-trans.
Resposta da questão 16:
a) V IV III I II.
b) Total de 5 isômeros:
Página 19 de 23
Revisão – Química 2
Professor Jefferson Silva
Resposta da questão 17:
a) Equação balanceada da reação da combustão completa do etanol:
CH3CH2OH 3O2 2 CO2 3 H2O
b) Fórmula estrutural do éter dimetílico:
Resposta da questão 18:
a) C30H30O8
b) O composto apresenta as funções: aldeído e fenol.
Resposta da questão 19:
a) A substância 1 apresenta átomo de carbono quiral ou assimétrico (*):
b) Substâncias que apresentam átomo de carbono quiral ou assimétrico desviam o plano da luz
polarizada, ou seja, apresentam isomeria óptica.
Resposta da questão 20:
[A]
[I] Correta. A fórmula molecular desse composto é:
C15H17O5N
MM (15 12) (1 17) (16 5) (1 14) 291g / mol
Página 20 de 23
Revisão – Química 2
Professor Jefferson Silva
[II] Correta. Trata-se de um carbono secundário, por estar ligado a mais dois átomos de
carbono.
[III] Incorreta.
[IV] Incorreta. A referida estrutura não apresenta nenhum átomo de carbono quaternário.
Resposta da questão 21:
a) Composto 1: amida.
Composto 2: álcool.
b) A estrutura 1 apresenta isomeria óptica, pois possui carbono quiral ou assimétrico (*).
O caráter ácido-básico do grupo necina é básico devido a disponibilidade do par de elétrons
no átomo de nitrogênio.
Resposta da questão 22:
O ácido 4-hidroxibutanoico não apresenta carbono quiral ou assimétrico (carbono ligado a
quatro ligantes diferentes entre si):
Página 21 de 23
Revisão – Química 2
Professor Jefferson Silva
O Clorofórmio (triclorometano) não apresenta carbono quiral ou assimétrico (carbono ligado a
quatro ligantes diferentes entre si):
Resposta da questão 23:
[C]
A isomeria plana que ocorre entre o citrato e o isocitrato é denominada de posição, pois a
posição do grupo OH é diferente nos dois ânions.
Resposta da questão 24:
a) Dopa: Fenol, amina e ácido carboxílico.
Dopamina: Fenol e amina.
b) Dopa:
Resposta da questão 25:
a) De acordo com a equação mostrada, podemos notar que, para a reação de um
grupamento éster, do triglicerídeo é necessária a presença de uma molécula de álcool
etílico.
Portanto, para reagir com 1 mol de triglicerídeo serão necessários 3 mols de etanol.
Página 22 de 23
Revisão – Química 2
Professor Jefferson Silva
1mol de etanol _________ 46 g
3 mols de etanol ________ m
m 138g
b)
c) Para ésteres de cadeias saturadas vale a seguinte fórmula geral:
Assim:
Para n = 17, teremos um número de 35 hidrogênios caso a cadeia seja saturada.
Pela fórmula do triéster conclui-se que todas as cadeias carbônicas ligadas às carbonilas
são insaturadas, pois não obedecem a essa relação.
A cada insaturação, o número de hidrogênios diminuirá em 2 unidades.
Concluímos então, que em:
C17H33 há uma insaturação.
C17H31 há duas insaturações.
Página 23 de 23