1
Berílio - Be
Número atômico 4 | Massa atômica 9,01218 | Elétrons [He]2s2 |
História
Do grego ”beryllos” (berilo, um mineral). Em outras épocas foi chamado de glucínio (do
grego ”glykys”, doce) devido ao sabor dos seus sais (não se deve provar. É perigosamente
venenoso).
Como óxido no berilo e nas esmeraldas, foi descoberto pelo farmacêutico e químico francês
Louis Nicolas Vauquelin em 1798. O metal foi isolado pelo químico alemão Friedrich Wöhler
(também, de forma independente, pelo químico francês Antoine Bussy), ambos em 1828,
através da reação do potássio com o cloreto de berílio.
Disponibilidade
Existem cerca de 30 tipos de minerais. Os mais importantes são: bertrandita (hidrossilicato
de berílio), berilo (silicato de alumínio e berílio, 3BeO·Al2 O3 ·6SiO2 , pedra semipreciosa),
crisoberilo (aluminato de berílio, pedra semipreciosa) e fenacita (silicato de berílio).
Produção
O metal é produzido pela redução do fluoreto de berílio com magnésio metálico. Ele só se
tornou disponível comercialmente em 1957.
Propriedades
O metal apresenta uma cor cinza semelhante à do aço. É um dos metais mais leves e,
entre eles, é o que tem o mais alto ponto de fusão.
Módulo de elasticidade cerca de 1/3 maior que o do aço. Dispõe de elevada condutividade
térmica, é resistente ao ácido nítrico concentrado e não é magnético. Apresenta alta
permeabilidade aos raios-X.
Em temperatura ambiente, é resistente à oxidação pelo ar. Isso provavelmente se deve à
apassivação da superfície, ou seja, à formação de uma camada de óxido que bloqueia a
corrosão. Daí a capacidade de riscar vidro.
2
Grandeza
Calor de fusão
Calor de vaporização
Calor específico
Coeficiente de expansão térmica
Condutividade térmica
Eletronegatividade
Estados de oxidação
Estrutura cristalina
Massa específica do sólido
Módulo de elasticidade
Ponto de ebulição
Ponto de fusão
Resistividade elétrica
Velocidade do som
Valor
Unidade
7,95
297
1825
1,13
200
1,57
+2
hexagonal
1848
290
2469
1287
4
12870
kJ/mol
kJ/mol
J/(kg°C)
10−5 (1/°C)
W/(m°C)
Pauling
kg/m3
GPa
°C
°C
−8
10 Ω m
m/s
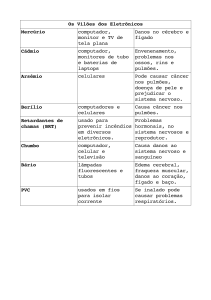
Berílio e seus sais são tóxicos e requerem cuidados especiais na manipulação. São potencialmente
cancerígenos e a exposição pode também provocar doenças pulmonares crônicas.
Compostos e/ou reações - alguns exemplos
Reação com oxigênio: 2Be + O2 →2BeO
Reação com nitrogênio: 3Be + N2 →Be3 N2
Reação com água: não reage, mesmo aquecido e água em forma de vapor.
Reação com halogênios: Be + Cl2 → BeCl2 | Be + Br2 → BeBr2
Reação com ácido: Be + H2 SO4 → Be++ + SO4 −− + H2
Aplicações - alguns exemplos
• Componente para ligas de cobre usadas em molas, contatos elétricos, eletrodos de solda
e ferramentas não produtoras de centelhas.
• Desde que apresenta transparência aos raios X, tem sido empregado em processos de
litografia por raios X na produção de circuitos integrados.
• Lâmpadas fluorescentes usavam, até certa época, compostos de berílio. A interrupção
ocorreu em função dos riscos para a saúde nos processos de fabricação.
• Material estrutural de várias partes de veículos espaciais e satélites.
• O óxido tem alto ponto de fusão e é usado em reatores nucleares e em cerâmicas
especiais (combina alto ponto de fusão com elevadas dureza, condutividade térmica e
rigidez dielétrica).
• Reatores nucleares (material de baixa absorção de nêutrons).
• Usado em dispositivos que exigem leveza, rigidez e estabilidade dimensional, como instrumentos.
Isótopos
A coluna % natural indica o teor encontrado no elemento natural. Valor nulo indica produção
artificial. Símbolos para tempos de meia-vida: s (segundo), m (minuto), h (hora), d (dia), a
3
(ano).
Símbolo
% natural
Massa
Meia-vida
Decaimento
6 Be
11 Be
0
0
0
100
0
0
6,0197
7,0169
8,0053
9,0122
10,0135
11,0217
5,9 10−21 s
53,28 d
7 10−17 s
Estável
2,6 106 a
13,8 s
12 Be
0
12,0269
0,024 s
13 Be
0
13,0428
0,004 s
2p p/ 4 He
CE p/ 7 Li
2α p/ n
β− p/ 10 B
β− p/ 11 B
β− + α p/ 7 Li
β− p/ 12 B
β− + n p/ 11 B
β− p/ 13 B
β− + n p/ 12 B
β− + 2n p/ 11 B
7 Be
8 Be
9 Be
10 Be
A tabela contém os principais isótopos do elemento. Não são necessariamente todos.
Mar/2005 | Página inicial do site