ANOTAÇÕES EM FARMACOLOGIA E FARMÁCIA CLÍNICA
19) TRATAMENTO FARMACOLÓGICO DA DISRITMIA CARDÍACA
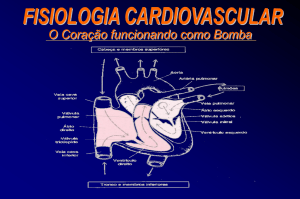
A contração e o relaxamento rítmicos do coração
baseiam-se no funcionamento das células especializadas do
sistema de condução do coração. As células especializadas
do nodo SA têm a mais rápida freqüência intrínseca de
geração de impulsos e atuam como marcadoras do ritmo
cardíaco. Os impulsos provenientes do nodo SA seguem
através dos átrios até o nodo AV e daí ao feixe AV e ao
sistema ventricular de Purkinje. O nodo AV constitui a única
conexão entre os sistemas de condução dos átrios e
ventrículos.
Fase 3 – ocorre a corrente de saída de K+ repolarizando a
célula; e
Fase 4 – ocorre a estabilidade elétrica dos miócitos atriais e
ventriculares, com potencial de membrana em repouso
sustentando em -90 mV e mantido pela corrente de fuga de
saída de K+ e pelos trocadores iônicos. Nessa fase os canais
de Na+ necessários para a despolarização dos miócitos
atriais e ventriculares se recuperam completamente.
As implicações clínicas da ativação cardíaca
desordenada variam de palpitações assintomáticas a arrtimia
fatal. O controle farmacológico das arritmias utiliza
medicamentos que exercem efeitos diretamente sobre as
células cardíacas inibindo a função de canais iônicos
específicos (canais de Na+ e de Ca+) ou alterando o aporte
autônomo do coração (bloqueio dos receptores betaadrenérgicos).
Os
átrios
e
os
ventrículos
funcionam
independentemente uns dos outros, ao ser bloqueada a
condução do nodo AV.
Fig. 01 – Sistema de condução cardíaco
Fig. 02 – Relação entre o eletrocardiograma e o potencial de
ação ventricular
O potencial de ação do músculo cardíaco é dividido em
cinco fases:
Fase 0 – representa a despolarização rápida do miócito
induzida pela abertura dos canais de sódio controlados por
voltagem. Esses canais se fecham após 1 a 2 milissegundos;
Fase 1 – é o período de repolarização curto e rápido que
ocorre no pico de subida do potencial de ação, devido à
inativação da corrente de entrada do Na+;
Fase 2 – ocorre o equilíbrio final entre as correntes iônicas
de entrada (despolarização) e de saída (repolarização)
mantendo o miócito em um estado despolarizado. Durante
essa fase, o Ca+ entra na célula causando a liberação de mais
Ca+ das reservas intracelulares e vinculando a
despolarização elétrica à contração mecânica do músculo,
em virtude da ação da actina e miosina;
O eletrocardiograma é utilizado para demonstrar
alterações nos impulsos cardíacos através do registro de
potenciais elétricos em vários locais na superfície do corpo.
O registro do ECG reflete alterações na excitação do
miocárdio. A compreensão básica do ECG é útil para
discutir as aplicações clínicas dos diversos agentes
antiarrítmicos.
1
Marcelo A. Cabral
ANOTAÇÕES EM FARMACOLOGIA E FARMÁCIA CLÍNICA
O eletrocardiograma normal contém três formas de
ondas elétricas: a onda P, o complexo QRS e a onda T. a
onda P representa a despolarização atrial; o complexo QRS
representa a despolarização ventricular; e a onda T
representa a repolarização ventricular. O ECG não mostra de
modo explícito a repolarização atrial, visto que a
repolarização atrial é “dominada” pelo complexo QRS. O
ECG também contém dois intervalos e um segmento: o
intervalo PR, o intervalo QT e o segmento ST. O intervalo
PR estende-se do início da onda P (despolarização inicial
dos átrios) até o início da onda Q (despolarização inicial dos
ventrículos). Por conseguinte, o comprimento do intervalo
PR varia de acordo com a velocidade de condução através
do nodo AV. por exemplo, se um paciente tiver um bloqueio
elétrico nodo AV, a velocidade de condução através do nodo
AV diminui, e o intervalo PR aumenta. O intervalo QT
começa no inicio da onda Q e termina no final da onda T,
representando toda a seqüência de despolarização e
repolarização ventriculares. O segmento ST começa no final
da onda S e termina no início da onda T. Esse segmento,
que representa o período durante o qual os ventrículos estão
despolarizados, corresponde à fase do platô do potencial de
ação ventricular.
Fisiopatologia da disfunção elétrica
Os distúrbios do ritmo cardíaco ocorrem em
conseqüência dos distúrbios na geração ou condução dos
impulsos do coração.
1) Defeitos na geração do impulso elétrico:
1.1 - automaticidade alterada em condições fisiológicas –
ocorre em função da estimulação provocada pelas
catecolaminas sobre os receptores beta-1, ocasionando o
aumento da freqüência cardíaca; ou pela estimulação do
nervo vago que libera acetilcolina, ativando os receptores
muscarínicos, com consequente diminuição da freqüência
cardíaca.
1.2 automaticidade alterada em condições patológicas –
nessa situação, as células marca-passo latentes assumem o
papel do nodo sinuatrial como marca-passo do coração.
Um batimento ectópico ocorre quando as células
marca-passo latentes desenvolvem uma freqüência de
disparo intrínseca, que é mais rápida do que a freqüência no
nodo sinuatrial.
A lesão tecidual direta (como o infarto) pode causar
desorganização estrutural na membrana celular. As
membranas acometidas são incapazes de manter gradientes
iônicos, que são de suma importância na manutenção dos
potenciais de membrana apropriados.
No ritmo sinusal normal, uma onda P precede cada
complexo QRS, e os intervalos RR permanecem
relativamente constantes ao longo do tempo.
Fig. 03 - Eletrocardiograma
A perda da conectividade da junção comunicante
constitui outro mecanismo pelo qual a lesão tecidual resulta
em alteração da automaticidade.
1.3 – atividade deflagrada – uma pós-despolarização ocorre
quando um potencial de ação normal deflagra
despolarizações anormais adicionais. Se uma pósdespolarização precoce for sustentada, pode resultar em um
tipo de arritmia ventricular, denominada “torsades de
pointes”, que representa emergência médica.
2) – Defeitos na condução do impulso
As disritmias cardíacas constituem distúrbios do ritmo
cardíaco relacionados a alterações na automaticidade,
excitabilidade, condutibilidade ou refratariedade das células
especializadas no sistema de condução do coração (células
do nodo Sinoatrial, nodo Atrioventricular e Fibra de
Purkinje).
A função cardíaca normal requer a propagação
desobstruída e tempestiva de um impulso Elétrico através
dos miócitos cardíacos. Em condições patológicas, a
alteração da condução do impulso pode resultar de uma
combinação de três mecanismos: reentrada, bloqueio da
condução e vias acessórias.
Automaticidade designa a capacidade de geração
espontânea de um potencial de ação por parte das células
marcadoras do ritmo cardíaco. Normalmente, o nodo
sinoatrial é o marcador do ritmo do coração devido à sua
automaticidade intrínseca. Excitabilidade é a capacidade do
tecido cardíaco de responder a um impulso e gerar um
potencial de ação. Condutividade e refratariedade
constituem a capacidade do tecido cardíaco de conduzir os
potenciais de ação. A condutividade relaciona-se à
capacidade de condução dos impulsos do tecido cardíaco e a
refratariedade indica as interrupções temporárias na
condutividade relacionadas à fase de repolarização do
potencial de ação.
Ocorre reentrada de um impulso elétrico quando um
circuito elétrico auto-sustentado estimula uma área do
miocárdio de modo repetitivo e rápido.
O bloqueio da condução é caracterizado quando um
impulso não consegue se propagar, devido à presença de
uma área de tecido cardíaco inexcitável. Essa área de tecido
inexcitável pode consistir em tecido normal que ainda está
refratário, ou pode apresentar um tecido lesado por
traumatismo, isquemia ou cicatrização.
As vias acessórias são constatadas pela presença do
Feixe de Kent, que é uma faixa do miocárdio que conduz
impulsos diretamente dos átrios para os ventrículos,
transpondo o nodo átrio-ventricular. O tecido ventricular
2
Marcelo A. Cabral
ANOTAÇÕES EM FARMACOLOGIA E FARMÁCIA CLÍNICA
desses pacientes recebe impulsos tanto da via de condução
normal quanto da via acessória.
bloqueio seletivo dos canais de sódio ou de cálcio das células
despolarizadas.
Devido ao seu potencial de interferir na ação de
bombeamento do coração, as disritmias que se originam dos
ventrículos são consideradas mais graves do que as que se
originam nos átrios.
Fármacos utilizados nas disritmias:
As drogas antidisrítmicas agem modificando a
formação e condução desordenadas dos impulsos que podem
induzir à contração do músculo cardíaco. Essas drogas são
classificadas em quatro grupos principais de acordo com o
efeito da droga sobre o potencial de ação das células
cardíacas. Embora tenham efeitos semelhantes sobre a
condução, drogas de uma categoria podem variar
significativamente quanto aos seus efeitos hemodinâmicos.
As disritmias sinusais originam-se do nodo SA,
consistindo na bradicardia sinusal (freqüência cardíaca < 60
batimentos por minuto), taquicardia sinusal (freqüência
cardíaca > 100 batimentos por minuto), parada sinusal
(assistolia) e síndrome da doença sinusal (alternância de
períodos de bradicardia e taquicardia).
As disritmias atriais originam-se de alterações na
geração de impulsos que ocorrem nas vias de condução ou
no músculo dos átrios. Consistem em contrações atriais
prematuras, flutter atrial (freqüência de despolarização atrial
de 240 a 450 batimentos por minuto) e fibrilação atrial.
As drogas da classe I agem bloqueando os canais
rápidos de Na+, da mesma maneira que fazem os anestésicos
locais. As drogas da classe I ligam-se aos canais mais
fortemente quando estes se encontram no estado aberto ou
refratário e menos fortemente aos canais no estado de
repouso. Por conseguinte, sua ação mostra a propriedade de
“dependência do uso”, isto é, quanto mais frequentemente os
canais são ativados, maior o grau de bloqueio produzido.
Elas afetam a condução dos impulsos, a excitabilidade e a
automaticidade em graus variáveis, sendo, por isso,
divididas, ainda, em três grupos: IA, IB e IC.
As alterações na condução dos impulsos através do
nodo AV acarretam distúrbios na transmissão dos impulsos
dos átrios aos ventrículos (bloqueio cardíaco de primeiro,
segundo e terceiro graus).
As alterações na condução dos impulsos do feixe de
HIS e do sistema de Purkinje causam alargamento e
alterações na configuração do complexo QRS do ECG.
As drogas da classe IA (quinidina, procainamida,
disopiramida, moricizina) diminuem a automaticidade,
deprimindo a fase 4 do potencial de ação, tornam menor a
condutividade, prolongando moderadamente a fase 0, e
prolongam a repolarização, estendendo a fase 3 do potencial
de ação. Por serem eficazes na supressão dos focos ectópicos
e no tratamento das disritmias reentrantes, as referidas
drogas são usadas nas disritmias supraventriculares e
ventriculares.
As disritmias ventriculares consistem em contração
ventricular prematura (CVP) que é causada por um marcador
do ritmo ventricular ectópico, a taquicardia ventricular
(frequência de 70 a 250 batimentos por minuto) e a
fibrilação ventricular (freqüência > 350 batimento por
minuto) que será fatal se não for tratada com êxito pela
desfibrilação.
Em geral as bradiarritmias não são controladas com a
terapia farmacológica de longo prazo e podem demandar
estimulação elétrica cardíaca permanente (implantação de
marca-passo). As taquiarritmias frequentemente podem ser
aliviadas com a terapia clínica de longo prazo.
As drogas da classe IB (lidocaína, fenitoína, tocainida,
mexiletina, aprindina) diminuem a automaticidade,
deprimindo a fase 4 do potencial de ação; têm pouco efeito
sobre a condutividade, diminuem a refratariedade, tornando
menor a fase 2, e abreviam a repolarização, diminuindo a
fase 3. As drogas desse grupo são usadas unicamente no
tratamento das disritmias ventriculares e têm pouco ou
nenhum efeito sobre a contratilidade miocárdica.
Mecanismos gerais dos agentes antiarrítmicos
Como as arritmias são causadas por uma atividade
marca-passo anormal ou por uma anormalidade na
propagação dos impulsos, a terapia das arritmias tem por
objetivo reduzir a atividade marca-passo ectópica e
modificar a condução ou a refratariedade em circuitos de reentrada para impedir movimento circular. Os principais
mecanismos disponíveis para atingir esses objetivos são:
As drogas da classe IC (flecainida, encainida,
propafenona, indecainida) diminuem a condutividade,
deprimindo acentuadamente a fase 0 do potencial de ação,
mas têm pouco efeito sobre a refratariedade ou a
repolarização. As drogas dessa classe são usadas nas
taquicardias supraventriculares e disritmias ventriculares
com risco de vida.
1 - o bloqueio dos canais de sódio;
2 - o bloqueio dos efeitos autônomos simpáticos no coração;
As drogas da classe II (propanolol, nadolol, atenolol,
timolol, acebutol, pindolol, esmolol) são drogas
bloqueadoras beta-adrenérgicas que agem amortecendo o
efeito sobre o coração da estimulação do sistema nervoso
simpático.
3 - o prolongamento do período refratário efetivo; e
4- o bloqueio dos canais de cálcio.
Os fármacos antiarrítmicos diminuem a automaticidade
dos marca-passos ectópicos em maior grau do que a do nodo
sinuatrial. Além disso, reduzem a condução e a
excitabilidade e aumentam o período refratário nos tecidos
despolarizados em maior grau do que no tecido normalmente
polarizado. Isso é efetuado principalmente através do
Embora o coração seja capaz de bater por si próprio
sem inervação do sistema nervoso, as fibras tanto simpáticas
quanto parassimpáticas inervam o nodo SA e o nodo AV e,
portanto, alteram a freqüência de automaticidade. A
estimulação simpa´tica libera noradrenalina, que se liga aos
3
Marcelo A. Cabral
ANOTAÇÕES EM FARMACOLOGIA E FARMÁCIA CLÍNICA
receptores beta1 adrenérgicos nos tecidos nodais. A ativação
desses receptores no nodo SA desencadeia um aumento na
corrente marcapasso, que aumenta a freqüência de
despolarização da fase 4 e, consequentemente, leva a um
disparo mais freqüente do nodo. A estimulação dos
receptores beta1 no nodo AV aumenta as correntes de Ca+ e
K+, aumentando, assim, a velocidade de condução e
diminuindo o período refratário do nodo.
potencial de ação diminui a reentrada. Como potente agente
da classe I, a amiodarona bloqueia os canais de Na+ e,
portanto, diminui a freqüência de disparo nas células
marcapasso; exibe bloqueio dos canais de Na+ dependente
de uso através de sua ligação preferencial aos canais que
estão na conformação inativada. A amiodarona exerce
atividade antiarrítmica de classe II através do antagonismo
não-competitivo dos receptores alfa-adrenérgicos e betaadrenérgicos. Como bloqueador dos canais de Ca+ (classe
IV), a amiodarona pode causar bloqueio significativo do
nodo atrioventricular e bradicardia, embora, felizmente, o
seu uso esteja associado a uma incidência relativamente
baixa de “torsade de pointes”.
Portanto, os antagonistas beta-1 afetam os potenciais
de ação dos nodos SA e AV através das seguintes ações:
a)
Diminuem a freqüência de despolarização da fase
4; e
b) Prolongam a repolarização.
O amplo espectro de ação da amiodarona é
acompanhado de um conjunto de efeitos adversos graves,
quando o fármaco é utilizado por longos períodos ou em
altas doses, tais como: hipotensão, diminuição da
contratilidade cardíaca, diminuição da função do nodo AV
ou SA, pneumonite, hiper ou hipotireoidismo, elevação das
enzimas hepáticas, neuropatia periférica, disfunção testicular
e pigmentação cutânea.
A diminuição da freqüência da despolarização da fase 4
resulta em automaticidade diminuída, o que, por sua vez,
reduz a demanda de oxigênio do miocárdio. A repolarização
prolongada do nodo AV aumenta o período refratário
efetivo, diminuindo ancidência de reentrada.
Essas drogas diminuem a automaticidade, deprimindo a
fase 4 do potencial de ação; tornam menor a freqüência e a
contratilidade cardíacas.
O sotalol antagoniza não-seletivamente os receptores
beta-adrenérgicos (ação de classe II) e também aumenta a
duração do potencial de ação ao bloquear os canais de K+
(ação da classe III). Esse fármaco é utilizado nas arritmias
ventriculares graves, particularmente em pacientes que não
conseguem tolerar os efeitos colaterais da amiodarona. A
exemplo de outros antagonistas beta, o sotalol pode causar
fadiga e bradicardia; e, à semelhança de outros agentes
antiarrítmicos da classe III, pode induzir torsades de pointes.
Tais medicações são eficazes no tratamento das
disritmias e taqui-disritmias supraventriculares secundárias à
atividade simpática excessiva, mas não muito eficazes no
tratamento das disritmias graves, como a taquicardia
ventricular recorrente.
As diferentes gerações de antagonistas betaadrenérgicos produzem graus variáveis de efeitos adversos.
Três mecanismos gerais são responsáveis pelos efeitos
adversos desses fármacos. Em primeiro lugar, o
antagonismo dos receptores beta-2 adrenérgicos provoca
espasmo do músculo liso, resultando em broncoespasmo,
extremidades frias e impotência. Esses efeitos são mais
comumente causados pelos antagonistas beta não seletivos
de primeira geração (propanolol). Em segundo lugar, a
exageração dos efeitos terapêuticos do antagonismo dos
receptores beta-1 pode levar a efeitos inotrópicos negativos
excessivos, bloqueio cardíaco e bradicardia. Em terceiro
lugar, a penetração do fármaco no SNC pode provocar
insônia e depressão.
O bretílio, à semelhança da guanetidina, concentra-se
nas terminações nervosas dos neurônios simpáticos,
causando a liberação inicial de noradrenalina; todavia, a
seguir, inibe a liberação adicional de noradrenalina. Esse
fármaco efetua uma simpatectomia química e, portanto,
exerce um efeito anti-hipertensivo. O bretílio também
aumenta a duração do potencial de ação nas células
cardíacas normais e isquêmicas. Os locais de atividade
antiarrítmicas consistem principalmente nas fibras de
Purkinje e, secundariamente, nos miócitos ventriculares.
Não exerce efeito sobre o tecido atrial.
As drogas da classe IV (verapamil, diltiazem,
nifedipina, bepridil, nitrendipina, isradipina, nicardipina)
agem bloqueando os canais de cálcio sensíveis à voltagem,
deprimindo, assim, a fase 4 e alongando as fases 1 e 2.
Cabe lembrar que, a acetilcolina diminui a freqüência
cardíaca, devido à ação agonista sobre os receptores
muscarínicos do nodo SA; por outro lado, a noradrenalina
aumenta a frequência ao ativar os receptores betaadrenérgicos no nodo SA.
Bloqueando a liberação intracelular dos íons cálcio,
essas drogas reduzem a força de contração do miocárdio e
diminuem, assim, a necessidade miocárdica de oxigênio. São
usadas para retardar a resposta ventricular nas taquicardias
atriais e fazer cessar as taquicardias supraventriculares
paroxísticas reentrantes, quando o nodo AV funciona como
via de reentrada.
As drogas da classe III (amiodarona, bretílio, sotalol,
n-acetilprocainamida – NAPA) agem ampliando o potencial
de ação cardíaco e a refratariedade. São usadas no
tratamento das disritmias ventriculares graves.
A amiodarona é principalmente um agente
antiarrítmico de classe III, mas também atua como agente
das classes I, II e IV. Seu mecanismo de ação se dá através
da alteração da membrana lipídica na qual se localizam os
canais iônicos e os receptores. Em todos os tecidos
cardíacos, a amiodarona aumenta o período refratário efetivo
através do bloqueio dos canais de K+ responsáveis pela
repolarização da célula. Esse prolongamento da duração do
Esses fármacos atuam preferencialmente nos tecidos
nodais SA e AV, visto que esses tecidos marcapasso
dependem das correntes de Ca+ para a fase de
despolarização do potencial de ação. Em contrapartida, os
bloqueadores dos canais de Ca+ exercem pouco efeito sobre
4
Marcelo A. Cabral
ANOTAÇÕES EM FARMACOLOGIA E FARMÁCIA CLÍNICA
os tecidos dependentes dos canais de Na+ rápidos, como as
fibras de Purkinje e o músculo atrial e ventricular.
usados no controle das disritmias, como a taquicardia atrial,
flutter atrial e fibrilação atrial.
Como diferentes tecidos expressam subtipos diferentes
de canais de Ca+, e diferentes subclasses de bloqueadores
dos canais de Ca+ interagem preferencialmente com
subtipos diferentes de canais de Ca+, os diversos
bloqueadores dos canais de Ca+ exercem efeitos diferenciais
em diferentes tecidos. A nifedipina exerce um efeito
relativamente maior sobre a corrente de Ca+ no músculo liso
vascular, enquanto o verapamil e o diltiazem são mais
efetivos nos tecidos cardíacos.
A adenosina, um nucleosídeo endógeno presente em
todas as células, é usada para o tratamento endovenoso
emergencial da taquicardia supra-ventricular paroxística que
envolve o nodo AV. Ela hiperpolariza o tecido de condução
cardíaco interrompendo a condução nodal AV e torna mais
lenta a descarga do nodo SA.
Os agentes da classe IV podem provocar bloqueio
nodal AV ao reduzir excessivamente a velocidade de
condução. A administração de verapamil intravenoso a
pacientes em uso de beta-bloqueadores pode precipitar
insuficiência cardíaca grave e levar a uma dissociação
eletromecânica irreversível.
ЖЖЖЖЖЖ
Dois outros tipos de droga antidisrítmica, os
glicosídeos cardíacos e a adenosina, não são incluídos nesse
esquema de classificação.
Os glicosídeos cardíacos lentificam a freqüência
cardíaca (através do aumento da atividade vagal), sendo
Referências Bibliográficas
1. RANG, H. P. et al. Farmacologia. 4 edição. Rio de Janeiro: Guanabara Koogan, 2001;
2. KATZUNG, B. G. Farmacologia: Básica & Clinica. 9 edição. Rio de Janeiro: Guanabara Koogan, 2006;
3. CRAIG, C. R.; STITZEL, R. E. Farmacologia Moderna. 6 edição. Rio de Janeiro: Guanabara Koogan, 2005;
4. GOLAN, D. E. et al. Princípios de Farmacologia: A Base Fisiopatológica da Farmacoterapia. 2 edição. Rio de
Janeiro: Guanabara Koogan, 2009;
5. FUCHS, F. D.; WANNMACHER, L.; FERREIRA, M. B. C. Farmacologia Clínica. 3 edição. Rio de Janeiro: Guanabara
Koogan, 2004.
6. GILMAN, A. G. As Bases farmacológicas da Terapêutica. 10 edição. Rio de Janeiro: Mc-Graw Hill, 2005.
7. CONSTANZO, L. S. Fisiologia. 2 edição. Rio de Janeiro: Elsevier, 2004.
8. PORTH, C. M. Fisiopatologia. 6 edição. Rio de Janeiro: Ganabara Koogan, 2004
5
Marcelo A. Cabral