ISOMERIA
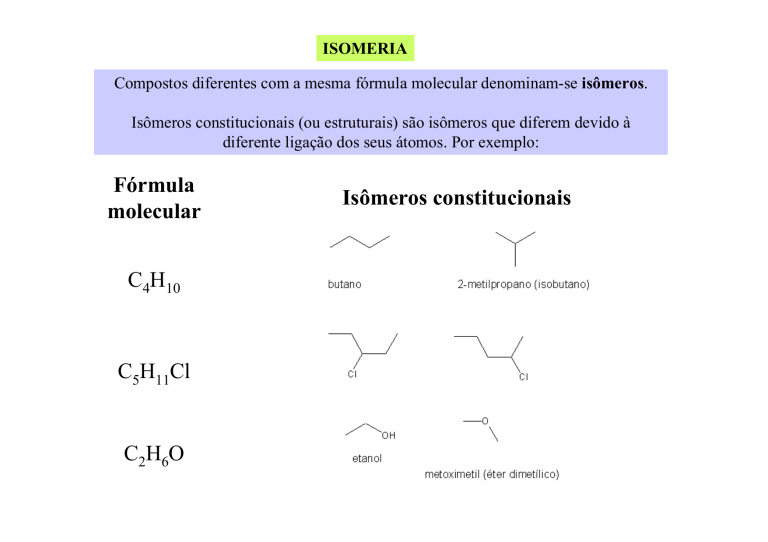
Compostos diferentes com a mesma fórmula molecular denominam-se isômeros.
Isômeros constitucionais (ou estruturais) são isômeros que diferem devido à
diferente ligação dos seus átomos. Por exemplo:
Fórmula
molecular
C4H10
C5H11Cl
C2H6O
Isômeros constitucionais
ISOMERIA
Os isômeros constitucionais podem ser subdivididos em:
a)
Isomeria de Função;
b) Isomeria de Cadeia;
c) Isomeria de posição;
d) Isomeria de Compensação ou Metameria;
e) Isomeria Dinâmica ou Tautomeria.
-Nem todos os grupos estão unidos ao mesmo centro
-São moléculas muito diferentes tanto em suas propriedades físicas como
químicas.
ISOMERIA
a) Isomeria de Função
A diferença entre os
isômeros está no
grupo funcional.
ISOMERIA
b) Isomeria de Cadeia
A diferença entre os
isômeros está no tipo
de cadeia carbônica.
ISOMERIA
c) Isomeria de
Posição
A diferença entre os
isômeros está na
posição de um grupo
funcional, de
uma insaturação ou
de um substituinte.
ISOMERIA
d) Isomeria de
Compensação ou
Metameria
A diferença entre os
isômeros está apenas
na posição de um
heteroátomo.
ISOMERIA
e) Tautomeria
Este tipo de isomeria ocorre quando dois compostos de mesma
fórmula molecular e grupos funcionais diferentes coexistem em
equilíbrio dinâmico no qual um deles está continuamente se
transformando no outro e vice-versa.
A tautomeria ocorre somente na fase líquida, em compostos cuja molécula possui um
elemento muito eletronegativo, como o oxigênio ou nitrogênio, ligado ao mesmo
tempo ao hidrogênio e a um carbono insaturado (que possui ligação π).
ESTEREOQUÍMICA
QUÍMICA NOVA, 20(6) (1997) OS FÁRMACOS E A QUIRALIDADE: UMA BREVE ABORDAGEM
ESTEREOQUÍMICA
TALIDOMIDA
ESTEREOQUÍMICA
E COM OS ALIMENTOS ?
DOCE
AMARGO
ESTEREOQUÍMICA
MOLÉCULA AQUIRAL
É aquela que é superponível com sua imagem no espelho
Têm elementos de simetria
ESTEREOQUÍMICA
MOLÉCULA QUIRAL
É aquela que não é superponível com sua imagem no espelho
ESTEREOQUÍMICA
Estuda as estruturas moleculares em três dimensões;
Estereoisômeros
Enantiômeros (enantion, grego oposto)
Diastereoisômeros
São produtos
diferentes?
ESTEREOQUÍMICA
ISÔMEROS
ESTEREOISÔMEROS
CONSTITUCIONAL
ENANTIÔMEROS
Imagem da molécula em um espelho
plano não é sobreponível a ela
mesmo
Todo enantiômero deve possuir um
centro quiral
Espelho
DIASTEREOISÔMEROS
Imagem da molécula, em um
espelho plano é sobreponível a ela
mesmo
ESTEREOQUÍMICA
CENTRO QUIRAL
Carbono com quatro grupos diferentes ligados a ele
Carbono QUIRAL Também chamado de centro quiral;
Características deste carbono:
Assimétrico;
Geometria tetraédrica;
Hibridação sp3;
ESTEREOQUÍMICA
COMO IDENTIFICAR UMA MOLÉCULA QUIRAL
1.
2.
Ao avaliar a sobreposição não devemos “romper ou formar” ligações;
Para ser uma molécula quiral basta uma única região do molécula não coincidir com a
outra imagem;
Espelho
III e IV Não são superponíveis ENANTIÔMEROS
ESTEREOQUÍMICA
COMO IDENTIFICAR UMA MOLÉCULA QUIRAL
3.
Moléculas quirais não possuem plano de simetria;
Plano de simetria
Esta molécula é AQUIRAL Possui plano de simetria
Esta molécula também possui plano de simetria AQUIRAL
ESTEREOQUÍMICA
COMO IDENTIFICAR UMA MOLÉCULA QUIRAL
2-cloropropano
2-clorobutano
ESTEREOQUÍMICA
CENTRO QUIRAL
1.
Outros átomos que também podem fazem quatro ligações pode ser um centro quiral;
Devido a geometria tetraédrica o centro quiral do carbono pode existir em ambos os
arranjos tridimensionais que não são imagens superponíveis;
Estereoisômeros as
imagens não são
superponíveis
2-butanol
ESTEREOQUÍMICA
Propriedades de moléculas quirais
•
Os ENANTIÔMEROS possuem as mesmas propriedades FÍSICAS (P.F; P.E; Espectro
IV; UV; RMN se medidos em solventes aquirais) EXCETO O SENTIDO DE
ROTAÇÃO DO PLANO DE POLARIZAÇÃO DA LUZ.
•
Os ENANTIÔMEROS possuem as mesmas propriedades QUÍMICAS EXCETO AS
REAÇÕES COM OUTROS COMPOSTOS OPTICAMENTE ATIVOS.
ATIVIDADE ÓTICA DE MOLÉCULAS QUIRAIS
DEXTROROTATÓRIAS (d, +) Gira a luz polarizada para a direita
LEVOROTATÓRIAS (l,-) Gira a luz polarizada para a esquerda
ESTEREOQUÍMICA
COMPOSTO OPTICAMENTE ATIVO
São capazes de modificar a rotação da luz polarizada;
COMPOSTOS QUIRAIS SÃO OPTICAMENTE ATIVOS
MISTURA RACÊMICA
Mistura de partes iguais dos enantiômeros (+) e (-).
IMPORTÂNCIA DA QUIRALIDADE
1.
A quiralidade está difundida em todo o universo;
2.
O corpo humano é estruturalmente QUIRAL;
3.
A maioria das moléculas dos seres vivos são quirais e, geralmente, somente um tipo
é encontrado;
4.
Quase todos os aminoácidos que formam as proteínas são quirais e todos desviam a
luz para a esquerda (levorotatórios);
ESTEREOQUÍMICA
ESTEREOQUÍMICA
ATIVIDADE ÓTICA
Descoberto pelo físico João-Baptista Biot – 1815;
1848 Luis Pasteur princípio da estereoquímica
Os enantiômeros giram o plano da luz polarizada em iguais quantidades mas em direções
opostas;
Onda eletromagnética
Ou seja, enantiômeros resolvidos (separados) apresentam atividade ótica;
As oscilações do campo elétrico e magnético podem ocorrer em todos os possíveis
planos perpendiculares a direção de propagação.
ESTEREOQUÍMICA
ATIVIDADE ÓTICA
Onda eletromagnética polarizada
Quando um feixe de luz comum passa através de um polarizador;
O polarizador interage com o campo elétrico da luz;
Após a interação a luz emerge do polarizador oscilando apenas em um plano;
POLARÍMETRO
Equipamento capaz de polarizar a luz;
A lente geralmente é constituída de CaCO3 em determinada forma cristalina Chamado de polaróide PRISMA DE NICOL;
ESTEREOQUÍMICA
ATIVIDADE ÓTICA
POLARÍMETRO
ESTEREOQUÍMICA
ATIVIDADE ÓTICA
POLARÍMETRO
A) Polarímetro sem amostra;
B)
Observação de uma amostra que não é opticamente ativa;
C)
Observação de uma amostra que é opticamente ativa;
Rotação da luz polarizada;
ESTEREOQUÍMICA
ATIVIDADE ÓTICA
MEDIÇÃO
Medições realizadas em graus;
A rotação pode ocorrer para duas direções:
DIREITA (SENTIDO DO RELÓGIO) Assume-se valor POSITIVO dextrorotatório (d, +)
ESQUERDA (SENTIDO CONTRÁRIO DO RELÓGIO) Assume-se valor
NEGATIVO Levorotatória (l, -);
FATORES QUE INFLUENCIAM:
Concentração da solução;
Comprimento de onda utilizado na fonte de luz;
Comprimento do tubo de amostra;
Temperatura;
Natureza do solvente.
ESTEREOQUÍMICA
ATIVIDADE ÓTICA
ROTAÇÃO ESPECÍFICA
D = raia D do sódio (589,6 nm);
T = temperatura, 0C;
α= rotação observada, graus
L = comprimento do tubo de amostra, cm
C = concentração da solução, g.mL-1
OBS: NO SI am = Poder rotatório ótico específico (rad m2 kg-1)
ESTEREOQUÍMICA
ATIVIDADE ÓTICA
ESTEREOQUÍMICA
NOMENCLATURA ENANTIÔMEROS: SISTEMA (R-S)
1.
Não existe correlação entre a configuração do enantiômero e a direção da rotação
ótica;
2.
Não existe correlação entre a designação R e S e a direção de rotação ótica;
R Do latin rectus (direito – a favor do relógio)
S Do latin sinister (esquerdo – contra o relógio)
COMO DETERMINAR A PRIORIDADE DOS GRUPOS?
ESTEREOQUÍMICA
NOMENCLATURA ENANTIÔMEROS: SISTEMA (R-S)
BASES (regras de precedência):
1.
Número atômico do elemento ligado ao centro quiral
•
Menor número atômico menor prioridade (4)
•
Maior número atômico maior prioridade (1)
OBS: No caso de isótopos o de maior massa atômica tem maior prioridade
2.
Quando os átomos ligados ao centro quiral forem iguais passa-se a determinar a
prioridade pelo próximo átomo;
3.
Deve-se posicionar o grupo de menor precedência (4) na posição contrária ao
observador (atrás do plano);
Visão da molécula com o grupo de menor prioridade apontando para fora do plano
ESTEREOQUÍMICA
NOMENCLATURA ENANTIÔMEROS: SISTEMA (R-S)
ESTEREOQUÍMICA
BASES:
3.
Quando houver ligações duplas ou triplas deve-se duplicar ou triplicar ambos os
átomos;
(S)-Alanina
[(S)-(+)-2-ácido
aminopropionico]
[α]D = +8.5°
(S)-Gliceraldeído
[(S)-(–)-2,3-dihidroxipropanal], [α]D = –8.7°
ESTEREOQUÍMICA
(R)-(+)-2-Metil-1-butanol
(R)-(–)-1-Cloro-2-metilbutano
(S)-(–)-2-Metil-1-butanol
S)-(+)-1-Cloro-2-metilbutano
ESTEREOQUÍMICA
NOMENCLATURA ENANTIÔMEROS: SISTEMA (R-S)
PROJEÇÕES DE FISCHER
1.
As linhas verticais representam ligações que se projetam para trás do plano do papel (ou
que estão no plano do papel);
2.
As linhas horizontais representam ligações que se projetam para fora do plano do papel;
3.
As intersecções das linhas horizontais e verticais representa um átomo de carbono,
normalmente um carbono quiral;
4.
Quando usamos as projeções de Fischer para testar a superponibilidade de duas
estruturas é permitido girá-las de 1800 no plano do papel;
5.
Não podemos girar as estruturas de nenhum outro ângulo;
6.
Deve-se manter as estruturas no plano do papel;
7.
Não é permitido virar as estruturas
Fischer
ESTEREOQUÍMICA
MISTURA RACÊMICA
Mistura de partes iguais de enantiômeros;
São opticamente inativos;
Podem ser separados:
Solventes quirais;
Cromatografia com coluna quiral;
Reações que envolvam substâncias também quirais;
Butanona
Aquiral
hidrogênio
Aquiral
(±)-2-butanol
quiral
ESTEREOQUÍMICA
DIASTEREOISÔMEROS
São estereoisômeros cujas moléculas não são imagens especulares superponíveis;
São moléculas que apresentam dois ou mais centros quirais (exceto para isômeros cis,
trans onde as moléculas não apresentam centros quirais);
Para compostos cujos centros quirais são tetraédricos (sp3) o número total de
estereoisômeros não excederá 2n, onde n é o número de centros quirais tetraédricos (regra
de van’t Hoff);
Os diasteroisômeros apresentam propriedades físicas diferentes (P.F; P.E; solubilidades,
etc.);
ESTEREOQUÍMICA
DIASTEREOISÔMEROS
Exemplos de diasteroisômeros sem carbono quiral
DIASTEROISÔMEROS
ESTEREOQUÍMICA
DIASTEREOISÔMEROS
Exemplos de diasteroisômeros com dois carbonos quirais
DIFERENTES PROPRIEDADES FÍSICAS
DISTEROISÔMEROS
ENANTIÔMEROS
ENANTIÔMEROS
MESMAS PROPRIEDADES FÍSICAS E QUÍMICAS
ESTEREOQUÍMICA
DIASTEREOISÔMEROS
Exemplos de diasteroisômeros com DOIS carbonos quirais
Diasteroisômeros
Exemplos de diasteroisômeros com UM carbono quiral
ESTEREOQUÍMICA
DIASTEREOISÔMEROS
Treonina
Enantiômeros
Enantiômeros
ESTEREOQUÍMICA
DIASTEREOISÔMEROS
MESOESTRUTURAS
Estruturas com dois carbonos quirais nem sempre possuem 4 estereoisômeros;
Ocorre com moléculas que mesmo contendo centros quirais elas são aquirais.
ESTEREOQUÍMICA
DIASTEREOISÔMEROS
MESOESTRUTURAS
CLASSIFICAÇÃO DAS RELAÇÕES ENTRE MOLÉCULAS
São superponíveis?
SIM
Tem a mesma fórmula molecular?
OU
São iguais em seus pesos moleculares e
suas composições elementares?
NÃO
Não são isômeros
NÃO
SIM
São a mesma
molécula
Diferem unicamente pelo
NÃO
arranjo de seus átomos no espaço?
São isômeros
São isômeros
estruturais
SIM
É um deles superponível
com a imagem no espelho do outro?
SIM
São enântiômeros
São quirais
NÃO
NÃO
São diasteroisômeros
NÃO
São intercambiáveis a
temperatura ambiente?
São estereoisômeros
São estereoisômeros
conformacionais
São superponíveis com suas
respectivas imagens no espelho?
SIM
SIM
São estereoisômeros
figuracionais
São aquirais










