UNIVERSIDADE FEDERAL DE PERNAMBUCO
DEPARTAMENTO DE BIOQUÍMICA
LABORATÓRIO DE IMUNOPATOLOGIA KEIZO-ASAMI
Nereide Stela Santos Magalhães
Recife, 2004
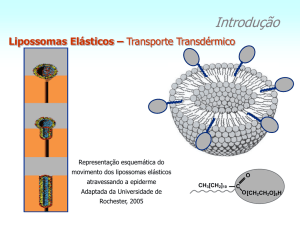
EVOLUÇÃO DA NANOTECNOLOGIA FARMACÊUTICA
CONVENCIONAL
LIPOSSOMAS
LIPOSSOMAS, NANOPARTÍCULAS NANOPARTÍCULAS
LIPOSSOMAS
NANOPARTÍCULAS
SÍTIO-ESPECÍFICOS
STEALTH®
- Metacrilatos
- Alquilcianoacrilatos
- Biodegradáveis
Polímeros pré-formados
•PLA
•PLGA
•PCL
Nanocápsulas
Nanoesferas
Polimerização in
situ
Nanopartículas
1970
1980
PLA-PEG
PLGA-PEG
PCL-PEG
Nanocápsulas
Nanoesferas
Lipossomas
Lipossomas-PEGLectina
Nanocápsulas
Nanoesferas
2000
Dex- PLA
1990
Dex- PCL
Groupo SLC/UFPE
Convencional
Nanocápsulas
Lipossomas
DextranaPCL-Lectina
?
Lipossomas
Descritos inicialmente em 1965
Alec D. Bangham
Vesículas esféricas formadas por bicamadas lipídicas com
capacidade de incorporar compostos hidrofílicos e hidrofóbicos.
LIPOSSOMAS
Estrutura das Membranas Biológicas
Figura 1. Arquitetura supramolecular das membranas
Leningher, 2000
Fosfolipídeos
Agregação
em água
Estruturas Lipídicas
Figura 2. Agregados de lipídeos anfipáticos dispersos em água
Leningher, 2000
Movimentos dos Lipídeos na Estrutura das
Membranas Biológicas
Leningher, 2000
Estruturas Lipídicas
• Monocamadas e micelas
Em meio aquoso, os lipídeos formam espontaneamente
estruturas.
– Monocamadas (baixas concentrações)
– Micelas (altas concentrações)
• CMC = concentração crítica micelar)
– Bicamadas lipídicas
– Vesículas
• Lipossomas
Lipossomas
Compartimento
interno aquoso
Micela
Bicamada
Lipossoma
www.cm.utexas.edu/.../overheads-2/ ch12_lipid-bilayer.jpg
Interações não covalentes nas
bicamadas lipídicas
• As bicamadas lipídicas possuem tendência
inerente a serem extensas
• As bicamadas lipídicas podem fecharem-se
sobre si mesmas e formar vesículas.
• As bicamadas lipídicas são auto-selantes,
pois um “orifício” na bicamada é
energeticamente desfavorável.
Interações não covalentes nas
bicamadas lipídicas
• Hidrofóbicas
• Forças atrativas de van der Waals
– Caudas hidrocarbonadas
• Atrações eletrostáticas
• Pontes de hidrogênio
– Cabeças polares – água
Moléculas de água são liberadas das caudas
hidrocarbonadas dos lipídeos quando essas caudas
ficam sequestradas no interior apolar da bicamada.
Transição de Fases em Bicamadas
• As transições de fases são sempres
endotérmicas; o calor é absorvido enquanto
a temperatura aumenta durante a transição.
• Fosfolipídeos apresentam temperaturas de
transição de fase específicas Tm: aumenta
com o comprimento da cadeia alifática,
diminui com a insaturação e depende da
natureza do grupo polar da cabeça.
Transição de Fases em Membranas
• T<Tm
– Bicamada organizada com cadeias alifáticas
relativamente imobilizadas (conformação extendida
máxima),
– Área superficial / lipídeo é mínima
– Espessura da bicamada é máxima
• T>Tm
– Fase cristalina líquida (mobilidade das cadeias
alifáticas é intermediária entre os estados sólido e
líquido de alcanos).
– Área superficial / lipídeo aumenta.
– Espessura da bicamada diminui de 10 a 15%.
Transição de Fases em Bicamadas
• Em bicamadas de fosfolipídeos puros, a
transição ocorre em faixa estreita de
temperatura. Ex:
– Tm dimiristoilfosfatidilcolina = 0,2oC.
• Membranas biológicas apresentam faixa
larga de transição de fase e dependem
fortemente da composição dos lipídeos e
proteínas.
Transição de Fases em Bicamadas
• Para certas bicamadas de lipídeos, uma modificação no
estado físico, chamada de pré-transição, ocorre de 5 a
15oC abaixo da Tm. Estas pré-transições envolvem
inclinação das cadeias hidrocarbonadas.
• Geralmente a fase de transição está relacionada com
uma modificação de volume.
• A transição de fase da bicamada é muito sensível à
presença de solutos que interagem com os lipídeos, tais
como cátions divalentes, substâncias lipossolúveis,
peptídeos e proteínas.
Lipossoma
Internalização de lipossomas por
células
LIPOSSOMAS
• DEFINIÇÃO
São vesículas aquosas, de diâmetro entre
0,1 e 0,5 µm, contituídas de uma ou mais
membranas fosfolipídicas de origem
natural. O princípio ativo pode estar
encapsulado na fase aquosa (hidrofílico) ou
ser retido pela membrana (lipofílico).
GLICEROFOSFOLIPÍDEOS
• FOSFOLIPÍDEOS
Principais constituintes das membranas biológicas
– Ácido fosfatídico
– Fosfatidilcolina (lecitina)
– Fosfatidiletanolamina
– Fosfatidilglicerol
– Difosfatidilglicerol (cardiolipina)
– Fosfatidilserina
– Fosfatidilinositol
COMPOSIÇÃO DOS LIPOSSOMAS
• Lipídeos
Características
Fosfatidilcolina de ovo
Diestearilfosfatidilcolina
Dipalmitoilfosfatidilcolina
constituinte principal e o mais utilizado
menos permeável à fase aquosa
fosfolipídeo sintético totalmente
saturado
utilizado em imunolipossomas
aumenta a permeabilidade lipossomal
pode aumentar a fusão lipossoma-célula
reduz a permeabilidade dos lipossomas
Incorporação máxima: 50 mol% com relação
aos fosfolipídeos totais
confere carga positiva aos lipossomas
confere carga negativa aos lipossomas
confere carga negativa aos lipossomas
utilizado em imunolipossomas
lipídeos antigênicos utilizados em
imunolipossomos
Fosfatidiletanolamina
Lisofosfatidilcolina
Colesterol
Estearilamina
Dicetilfosfato
Ácido fosfatídico
Esfinomielina
Cardiolipídeos
VANTAGENS
• São biodegradáveis
• Não possuem antigenicidade
• Protegem as drogas contra a ação enzimática
• Reduz a toxicidade das drogas
• Podem ser direcionados ao local de ação pela
adição de sinais moleculares, anticorpos
monoclonais, hormônios ou glicolipídeos
Classificação
SUV
LUV
20-100 nm
0,5 a 1,0
> 100 nm
5 a 15
MLV
> 0,5µm
35 a 65
Vesículas multilamelares:
MLV (Multilamellar Vesicles)
Vesículas pequenas unilamelares: SUV (Small Unilamellar Vesicles)
Vesículas grandes unilamelares: LUV (Large Unilamellar Vesicles)
LIPOSSOMAS
www.drugdeliveryparternships.com/html
MÉTODOS DE PREPARAÇÃO
DE LIPOSSOMAS
• Métodos mecânicos de Dispersão de fosfolipídeos
– Hidratação de filme lipídico
– Homogeneização por ultra-som
– Homogeneização por extrusão
– Microfluidificação
– Dispersão de lipossomas liofilizados
– Dispersão de lipossomas congelados
MÉTODOS DE PREPARAÇÃO
DE LIPOSSOMAS
• Métodos mecãnicos de Dispersão de solução
orgânica de fosfolipídeos
– Evaporação em fase reversa
– Injeção em solução etanólica
– Infusão em éter
• Dispersão de micelas mistas
– Eliminação de detergente
Metodologia
Preparação de Lipossomas
Filme lipídico
Lipids
Solvent
evaporation
Ultrasound
Liposomes
MLV’s
Aqueous phase
SUV’s
+ α-glu-SO4
Metodologia
Preparação de Lipossomas
CHCl3 : MeOH
Fosfatidilcolina de soja - Epikuron 200
Colesterol
Estearilamina
(Acido Úsnico)
Hidratação com
Tampão Fosfato pH 7,4
Filme lipídico
MLV’s
SUV’s
Sonicação
www.avantilipids.com/ PreparationOfLiposomes2B
Lipossomas
Branco
Lipossomas
Ác.Usnico
CONSERVAÇÃO DE
LIPOSSOMAS
• Métodos de Conservação
– Atmosfera de nitrogênio ou argônio
– Temperatura 4°C
– Abrigo da luz
– Liofilização
CONSERVAÇÃO DE
LIPOSSOMAS
• Alterações morfológicas e físicoquímicas
– Oxidação e hidrólise de fosfolipídeos
– Interações do tipo Van der Waals
• Agregação
• Presença de cargas negativas ou positivas
CARACTERIZAÇÃO DE
LIPOSSOMAS
• Obtenção de uma preparação homogênea
• Determinação do tamanho das vesículas
• Taxa de encapsulação
• Estabilidade físico-química
• Cinética de liberação in vitro
• Estabilidade em fluidos biológicos
• Interação com células
• Biodisponibilidade
CARACTERIZAÇÃO DE
LIPOSSOMAS
•
Estabilidade Físico-química
– Aspecto macroscópico
– Aspecto microscópico
– Diâmetro das partículas
– Viscosidade
– Condutividade
– pH
– Potencial de superfície (zeta)
– Temperatura de conservação
– Doseamento do fármaco
CARACTERIZAÇÃO DE
LIPOSSOMAS
• Estabilidade Físico-química
– Aspecto macroscópico
• Observação visual
– Cor
– Cremagem
– Exsudato
– Precipitado
– Separação de fase
CARACTERIZAÇÃO DE
LIPOSSOMAS
• Estabilidade Físico-química
– Aspecto microscópico
• Microscopia ótica (LUV, MLV)
• Microscopia Eletrônica
– Varredura (observação tridimensional da vesícula)
– Transmissão (observação de MLV)
– Força atômica (caracterização da superfície)
TITULO
Lipossomas
Lipossomas
Ácido Usnico
Aspecto microscópico de lipossomas contendo
ácido úsnico: Partículas uniformes bem
distribuídas com tamanho de aproximadamente
130 nm.
DETERMINAÇÃO DO TAMANHO DE
VESÍCULAS
MICROFOTOGRAFIA DE LIPOSSOMAS
TÉCNICA DE CRIOFRATURA
CARACTERIZAÇÃO DE
LIPOSSOMAS
• Determinação do tamanho das vesículas
– Contador de partículas Nanosizer
• Espectroscopia de auto-correlação de fótons
• Espalhamento da luz (light scattering)
• Determinação do potencial de superfície
Potencial zeta ξ (carga)
NANOSIZER (PCS)
NANOSIZER
CARACTERIZAÇÃO DE
LIPOSSOMAS
• Taxa de encapsulação
• Doseamento do fármaco
• Porcentagem de encapsulação
• Massa de substância encapsulada por
unidade de massa de lipídeo
Metodologia
Taxa de encapsulação de fármacos em lipossomas
• Determinação indireta
A percentagem de incorporação de fármacos em lipossomas
pode ser quantificada por HPLC, após separação do fármaco
encapsulado do não encapsulado, através de uma
ultrafiltração-centrifugação utilizando unidades filtrantes
ultrafree® (Millipore).
CARACTERIZAÇÃO DE
LIPOSSOMAS
• Influência de diferentes fatores sobre a
taxa de encapsulação
– Características do fármaco
– Métodos deficientes de separação e marcação
• Substâncias hidrossolúveis
• Substâncias lipossolúveis e anfifílicas
• Caso particular de proteínas
• DNA
ESTABILIDADE DE
LIPOSSOMAS
• Estabilidade Físico-química
– Acelerada
• Centrifugação
• Ciclos de congelamento-descongelamento (8
h a -18°C e 16 h a 25°C)
• Agitação mecânica (150 evoluções/min)
– Movimento horizontal
ESTABILIDADE DE
LIPOSSOMAS
• Estabilidade Físico-química
– A longo prazo
Medida de parâmetros físico-químicos em intervalos
de tempo regulares (1, 15, 30, 60, 180, 360, etc dias)
• Tamanho das vesículas
• Doseamento do fármaco
• Viscosidade
• Condutividade
• pH
• Avaliação dos aspectos macroscópico e microscópico
Metodologia
Avaliação da cinética de liberação in vitro
Direta
Indireta
Diálise
Diálise inversa
Meio receptor
Tampão
Meio doador
Lipossomas
Lipossomas
Avaliação da atividade em células
% ce ll viability
% cell viability
100
80
60
40
20
0
2.5
5
10
20
100
80
60
40
20
0
2.5
Lip Cont
Lipos AU
Teste de citotoxicidade
em células HEp-2
10
20
Conce ntration µg/ml
C once ntration µg/ml
UA Free
5
UA Free
Lip Cont
Lipos AU
Teste de citotoxicidade
em células NCIH-292
Citotoxicidade de lipossomas contendo ácido úsnico
LIPOSSOMAS COMO MARCADORES
ENDOCITOSE LIPOSSOMAL
VIAS DE ADMINISTRAÇÃO
VIAS de ADMINISTRAÇÃO DE
LIPOSSOMAS
• Parenteral (i.v.; i.m.; s.c.;i.c.)
• Cutânea
• Oftálmica
• Nasal
• Pulmonar
NANOTECNOLOGIA FARMACÊUTICA
• Lipossomas (Injetáveis)
– Terapia do Câncer
• resistência multi-droga
• Cardiotoxicidade
– Doenças Infecciosas
– Terapia Gênica
• Lipossomas (Tópicos)
– Farmacêuticos
– Cosméticos
APLICAÇÕES TERAPÊUTICAS
DE LIPOSSOMAS
• Antibioticoterapia
• Insuficiência respiratória neonatal (surfactante pulmonar)
• Enzimas
• Hormônioterapia
• Produtos de contraste
• Produtos radiofarmacêuticos
• DNA
• Vacinas
APLICAÇÕES TERAPÊUTICAS
DE LIPOSSOMAS
• Antiparasitários
• Agentes quelantes
• Antitumorais
• Insulina
LIPOSSOMAS ESTERICAMENTE
ESTABILIZADOS
PRODUTOS LIPOSSOMAIS
Produto
Fármaco
Companhia Status
Câncer
DaunoXome®
Doxil®
Daunorubicina
Doxorubicina
NeXstar
Aprovado Europa, US
Sequus (Alza)
Aprovado Europo, US
Evacet®
Doxorubicina
Liposome Co.
Fase III
Annamycin
Anamicin
Aronex
Fase I/II
Cisplatin
Cisplatin
Atragen®
Tretinoina
Edelfosine
Edelfosina
Aronex
Aronex
Liposome Co.
Fase II
Fase I/II
Fase I
Infecções
AmBisome®
Amphotericin B
NeXstar
Aprovado Europa, US
Nyotran®
Nistatina
Aronex
Fase III
MiKasome®
Amikacina
NeXstar
Fase II/III
Targeted
www.cwru.edu/menu/research/drugdelivery.htm
APLICAÇÕES DE LIPOSSOMAS
• Cosmetologia
– Vitaminas hidro e lipossolúveis
– Agentes hidratantes
– Elastina
– Colágeno
– Ácido hialurônico
APLICAÇÕES DE LIPOSSOMAS
• Cosmetologia
– Anti-radicais livres
– Antioxidantes
– Agentes rejuvenecedores
(remoção de colesterol)
APLICAÇÕES DE LIPOSSOMAS
• Farmácia de Manipulação
– Incorporação de lipossomas pré-fabricados em
• Cremes
• Protetores solares
• Gel
• Gel creme
• Xampu
CONTROLE DE QUALIDADE DE
PRODUTOS CONTENDO
LIPOSSOMAS
• Observação macroscópica
– observar a preservação das características iniciais do
produto e detectar sinais de instabilidade
• Observação microscópica
– detectar a presença dos lipossomas na preparação
• Determinação do ativo