2ª aula prática
Termodinâmica e estrutura da matéria
2ª aula prática
P2.1 - Calcule a altura de que deve cair a água duma cascata, para que a sua temperatura
aumente 1oC após atingir o solo.
(NOTA: admita que, ao atingir o solo, a energia potencial da água se converte integralmente
em energia interna)
P2.2 - Calcule a energia que é necessário fornecer a 200 g de gelo, que se encontra à
temperatura de -20 oC, para obter a mesma quantidade de vapor de água a 100 oC.
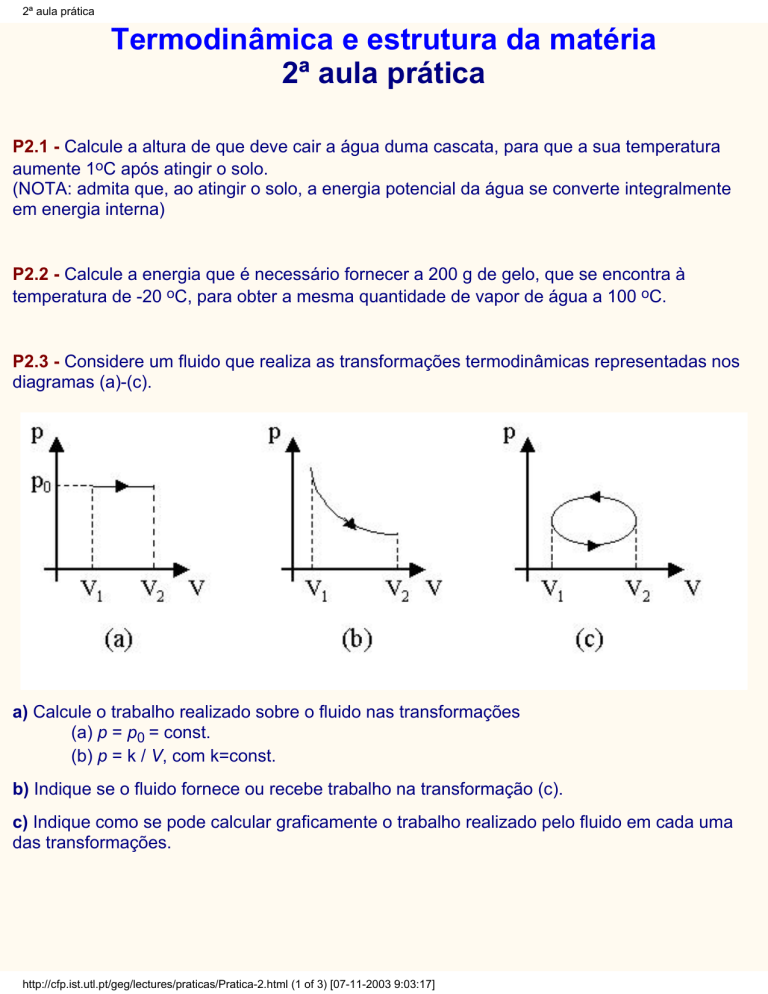
P2.3 - Considere um fluido que realiza as transformações termodinâmicas representadas nos
diagramas (a)-(c).
a) Calcule o trabalho realizado sobre o fluido nas transformações
(a) p = p0 = const.
(b) p = k / V, com k=const.
b) Indique se o fluido fornece ou recebe trabalho na transformação (c).
c) Indique como se pode calcular graficamente o trabalho realizado pelo fluido em cada uma
das transformações.
http://cfp.ist.utl.pt/geg/lectures/praticas/Pratica-2.html (1 of 3) [07-11-2003 9:03:17]
2ª aula prática
P2.4 - Considere os seguintes teoremas relativos à conservação da energia.
O Teorema da Energia Cinética
onde
εkM ... energia cinética (macroscópica)
Wex ... trabalho das forças exteriores
Win ... trabalho das forças interiores .
O Teorema da Energia Mecânica
onde
εm ... energia mecânica
εp = εp,in + εp,ex ... energia potencial total
εp,in ... energia potencial associada às forças interiores
εp,ex ... energia potencial associada às forças exteriores .
a) Utilize os Teoremas anteriores para mostrar que
onde
Wexnc ... trabalho das forças exteriores não conservativas
Winnc ... trabalho das forças interiores não conservativas
b) Combine o resultado de a) com o Primeiro Princípio da Termodinâmica, para mostrar que
em sistemas mecânicos se tem
onde
U ... energia interna
http://cfp.ist.utl.pt/geg/lectures/praticas/Pratica-2.html (2 of 3) [07-11-2003 9:03:17]
2ª aula prática
Q ... calor trocado entre o sistema e o exterior
Interprete o resultado obtido.
c) Aplique o resultado de b) ao estudo do contacto, com atrito, entre dois sólidos
indeformáveis. Considere os seguintes processos:
(i) isotérmico (T = const; sólidos em contacto com o ar)
[Admita que a energia interna dos sólidos é apenas função da temperatura]
(ii) adiabático (Q = 0; sólidos no vácuo)
DADOS:
Cm,p(água) = 1 cal g-1 oC-1 = 4,18 J g-1 oC-1
Cm,p(gelo) = 0,5 cal g-1 oC-1
λ vaporização(água) = 540 cal g-1
λ fusão(gelo) = 80 cal g-1
http://cfp.ist.utl.pt/geg/lectures/praticas/Pratica-2.html (3 of 3) [07-11-2003 9:03:17]












