LISTA CALORIMETRIA (CALOR LATENTE)
1. (Ufpel) Muitas pessoas gostam de café, mas
não o apreciam muito quente e têm o hábito de
adicionar um pequeno cubo de gelo para resfriá-lo
rapidamente. Deve-se considerar que a xícara
tem capacidade térmica igual a 30 cal/ºC e
contém inicialmente 120 g de café (cujo calor
específico é igual ao da água, 1 cal/g.ºC) a 100 ºC,
e que essa xícara encontra-se em equilíbrio
térmico com o líquido. Acrescentando-se uma
pedra de gelo de 10 g, inicialmente a 0 ºC, sendo
que o calor latente de fusão do gelo vale 80 cal/g,
após o gelo derreter e todo o sistema entrar em
equilíbrio térmico, desprezando-se as perdas de
calor para o ambiente, a temperatura do café
será igual a ?
88,75 ºC
2. (Ufrs) Uma amostra de uma substância encontra-se,
inicialmente, no estado sólido na temperatura T0 . Passa,
então, a receber calor até atingir a temperatura final Tf ,
quando toda a amostra já se transformou em vapor. O
gráfico abaixo representa a variação da temperatura T da
amostra em função da quantidade de calor Q por ela
recebida.
Considere as seguintes afirmações, referentes ao
gráfico.
I. T e T são, respectivamente, as temperaturas de
fusão e de vaporização da substância.
II. No intervalo X, coexistem os estados sólido e
líquido da substância.
III. No intervalo Y, coexistem os estados sólido,
líquido e gasoso da substância.
1
2
Quais estão corretas?
Apenas I e II.
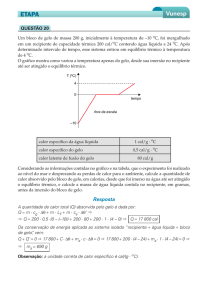
3. (Pucsp) Um cubo de gelo de massa 100 g e temperatura
inicial -10 ºC é colocado no interior de um micro-ondas. Após
5 minutos de funcionamento, restava apenas vapor d' água.
Considerando que toda a energia foi totalmente absorvida
pela massa de gelo (desconsidere qualquer tipo de perda) e
que o fornecimento de energia foi constante, determine a
potência utilizada, em W.
São dados:
Potência = calor(Q)/tempo.
Pressão local = 1 atm
Calor específico do gelo = 0,5 cal.g-1.0C-1
Calor específico da água líquida = 1,0 cal.g-1.0C-1
Calor latente de fusão da água = 80 cal. g-1
Calor de vaporização da água = 540 cal.g-1
1 cal = 4,2 J
1015
4. (Unifesp) 0,50 kg de uma substância a temperatura T0 =
40°C, na fase líquida, é colocado no interior de um
refrigerador, até que a sua temperatura atinja T1 = -10°C. A
quantidade de calor transferida em função da temperatura é
apresentada no gráfico da figura.
A parte do gráfico correspondente ao intervalo de -10°C a
2,0° foi ampliada e inserida na figura, à direita do gráfico
completo. Calcule:
a) O calor latente específico de solidificação.
L = -30.104 = -3,0.105 J/kg
b) O calor específico na fase sólida. Q = 2 kJ/(kgC)