AD. 2º COLEGIAL – 4º BIM
DEVERÁ SER EIMPRESSO, RESOLVIDO E ENTREGUE NA PRIMEIRA
AULA APÓS AS PROVAS DOS DIAS 07 e 08/11.
1. Qual a energia interna de 1,5 mols de um gás perfeito na temperatura de
20°C? Conisdere R=8,31 J/mol.K.
2. Quando são colocados 12 moles de um gás em um recipiente com êmbolo que
mantém a pressão igual a da atmosfera, inicialmente ocupando 2m³. Ao
empurrar-se o êmbolo, o volume ocupado passa a ser 1m³. Considerando a
pressão atmosférica igual a 100000N/m², qual é o trabalho realizado sob o
gás?
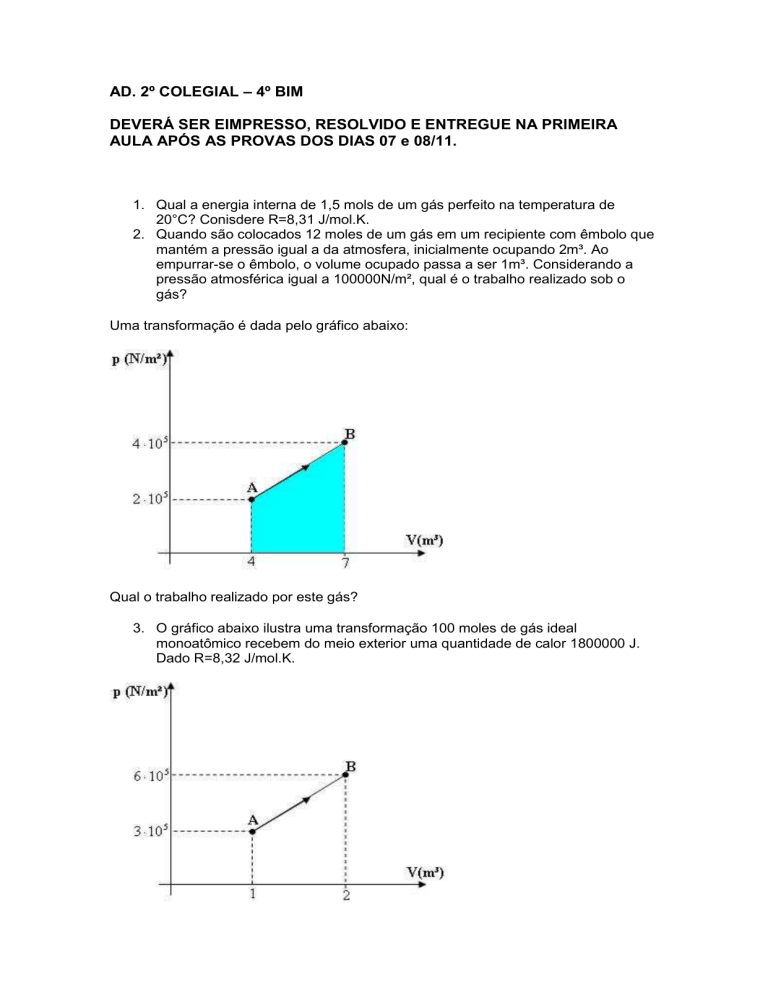
Uma transformação é dada pelo gráfico abaixo:
Qual o trabalho realizado por este gás?
3. O gráfico abaixo ilustra uma transformação 100 moles de gás ideal
monoatômico recebem do meio exterior uma quantidade de calor 1800000 J.
Dado R=8,32 J/mol.K.
Determine:
a) o trabalho realizado pelo gás;
b) a variação da energia interna do gás;
c) a temperatura do gás no estado A.
4. (UFRS-RS) Em uma transformação termodinâmica sofrida por uma amostra de gás
ideal, o volume e a temperatura absoluta variam como indica o gráfico a seguir,
enquanto a pressão se mantém igual a 20 N/m2. (veja o gráfico na resolução abaixo)
5. Sabendo-se que nessa transformação o gás absorve 250 J de calor, pode-se
afirmar que a variação de sua energia interna é de:
6. Um sistema gasoso recebe do meio externo 200 cal, em forma de calor.
Sabendo que 1 cal = 4,2 J, determinar a variação de energia interna numa
transformação isométrica.
7. Numa transformação isobárica, um gás realiza o trabalho de 400 J, quando
recebe do meio externo 500 J. Qual a variação de energia interna do gás nessa
transformação ?
8. Sobre um sistema realiza-se um trabalho de 3000 J e, em conseqüência ele
fornece 500 cal ao meio externo durante o mesmo intervalo de tempo. Se 1 cal
= 4,2 J, determine a variação de energia do sistema.
9. Numa transformação adiabática reversível, 20 g de um gás ideal evoluem de um
estado em que a temperatura vale 77 ºC para outro em que a temperatura vale 327
ºC. Qual o trabalho realizado nessa transformação, em joules?