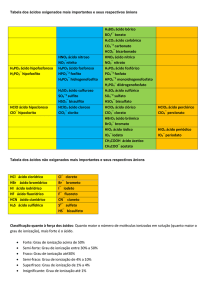
Ácidos
1.
(Unicamp-SP) Água pura é um mau
condutor de corrente elétrica. O ácido sulfúrico,
H2SO4 também é mau condutor. Explique o fato
de uma solução diluída de ác. Sulfúrico ser boa
condutora de corrente elétrica.
2.
Indique a equação de ionização total dos
compostos relacionados a seguir e dê o nome dos
ácidos:
a.
HNO3
b.
H2SO3
c.
H3PO4
d.
HCN
3.
Forneça
a
fórmula
dos
ácidos
relacionados a seguir:
a.
Ácido bromídrico
b.
Ácido sulfídrico
c.
Ácido periódico
d.
Ácido nitroso
4.
(Esal-MG) Uma solução aquosa de
H3PO4 é ácida devido a presença de:
a.
Água
b.
Hidrogênio
c.
Fósforo
d.
Fosfato
5.
(Unisinos-RS) Qual das substâncias a
seguir apresenta sabor azedo (ácido) quando em
solução aquosa?
a.
Na2S
b.
CaO
c.
NaOH
d.
NaCl
e.
HCl
6.
O HCN é um líquido branco e
transparente, com odor característico de
amêndoas amargas. Trata-se de um ácido fraco e
extremamente venenoso: na concentração de 0,3
mg/L no ar provoca morte imediata.
Comercialmente é conhecido como ácido
prússico. É usado na fabricação de plásticos,
corantes, fumigantes para orquídeas e poda de
árvores. Nos EUA, é usado nas câmaras de gás
para condenados à morte. Indique a alternativa
que contém o nome oficial do HCN.
a.
Ácido ciânico
b.
Ácido cianúrico
c.
Ácido cianídrico
d.
Ácido cianoso
e.
Ácido cianeto
7.
O H3PO2 puro é um sólido de baixo ponto
de fusão (26°C a 1 atm). Em solução aquosa
forma um líquido incolor que é um ácido fraco
utilizado como reagente em laboratório e na
obtenção de sais para uso médico. Seu nome
correto é:
a.
Ácido fosfórico
b.
Ácido fosforoso
c.
Ácido fosforídrico
d.
Ácido ortofosfórico
e.
Ácido hipofosforoso
8.
A glicose, C6H12O6, e o cloreto de
hidrogênio, HCl, são substâncias moleculares.
No entanto, a solução aquosa de glicose não é
condutora de corrente elétrica, ao contrário da
solução aquosa de cloreto de hidrogênio. Esse
fato pode ser explicado por:
a.
C6H12O6 possuir C e HCl não possuir C.
b.
C6H12O6 não sofrer ionização na água, ao
contrário do HCl.
c.
C6H12O6 ser substância facilmente
decomponível, ao contrário do HCl.
d.
C6H12O6 ser sólido e HCl, gás, nas
condições ambientais.
e.
C6H12O6 não ser solúvel em água.
9.
(Unicamp-SP) Indique, na afirmação a
seguir, o que é correto e incorreto, justificando
sua resposta em outras palavras: “Uma solução
aquosa de cloreto de hidrogênio, HCl, apresenta
o número de cátions H3O+ igual ao número de
ânions Cl. Portanto, é eletricamente neutra e não
conduz eletricidade”.
10.
Indique a equação de ionização total dos
compostos relacionados a seguir e dê o nome dos
ácidos.
a.
H3BO3
b.
H2CO3
c.
H4P2O7
d.
H3PO3
11.
Os nomes dos ácidos oxigenados HNO2,
HClO3, H2SO4 e H3PO4 são respectivamente:
a.
Nitroso, clórico, sulfúrico, fosfórico.
b.
Nítrico, clorídrico, sulfúrico, fosfórico.
c.
Nítrico, hipocloroso, sulfuroso, fosforoso.
d.
Nitroso, perclórico, sulfúrico, fosfórico.
e.
Nítrico, cloroso, sulfúrico, hipofosforoso.
12.
(Unisa-SP) O número de ligações
covalentes coordenadas (dativas) na molécula do
ácido perclórico é:
a.
Zero
b.
1
c.
2
d.
3
e.
4
13.
A Agência Nacional de Vigilância
Sanitária proibiu a comercialização de pomadas
e de talcos com ácido bórico na composição,
alegando que pesquisas feitas nos EUA
demonstraram que ele pode causar danos à
saúde, especialmente em crianças. Seu uso em
colírios, porém, continua livre. Indique a
alternativa que traz a fórmula correta do ácido
bórico.
a.
HBO
b.
HB2O
c.
H4B2O7
d.
H3BO3
e.
H3BO4
14.
(UFRS) Admitindo-se 100% de ionização
para o ácido clorídrico em solução diluída, podese afirmar que essa solução não contém a
espécie:
a.
HCl
b.
OHc.
H3Od.
H2O
e.
Cl
15.
Indique as equações parciais e a equação
global de ionização do ácido fosfórico. Forneça o
nome do ânion formado em cada etapa.
16.
(FEI-SP) A força de um ácido é medida
pelo(a):
a.
Poder de corrosão de metais
b.
Conteúdo de oxigênio
c.
Velocidade de ionização
d.
Grau de ionização
e.
Poder de volatilidade
17.
(UFPE) O ácido perclórico, HClO4, é um
ácido forte. Quais as espécies químicas
presentes, em maior concentração, em uma
solução aquosa deste ácido?
a.
H3O+ e ClO4b.
HClO4 e OHc.
OH-, Cl- e O2
d.
HClO4 e H3O+
e.
H3O+, Cl- e O2
18.
(UEPI) Sejam os seguintes ácidos, com
seus respectivos graus de ionização (α): HClO4
(α=97%); H2SO4 (α=61%), H3BO3 (α=0,025%);
H3PO4 (α=27%); HNO3 (α=92%). Assinale a
alternativa correta:
a.
H3PO4 é mais forte que H2SO4
b.
HNO3 é um ácido moderado (semiforte)
c.
HClO4 é mais fraco que HNO3
d.
H3PO4 é um ácido forte
e.
H3BO3 é um ácido fraco
19.
Calcule o grau de ionização α e indique a
força dos ácidos relacionados abaixo, com base
nas informações fornecidas em cada item
(verificadas experimentalmente a 25°C e 1 atm).
a.
A cada 3,01x1023 moléculas de fluoreto
de hidrogênio, HF, adicionados na água,
verifica-se que aproximadamente 2,56x1022
reagem sofrendo ionização e formando o ácido
fluorídrico, H3O+ + F-; as demais permanecem na
forma inicial.
b.
A cada 12,80 g de iodeto de hidrogênio,
HI, adicionado na água, verifica-se que 12,16 g
reagem sofrendo ionização e formando o ácido
iodídrico, H3O+ + I-; a massa restante permanece
na forma molecular.
c.
A cada 6,115 L de sulfeto de hidrogênio
gasoso, H2S, borbulhado na água, verifica-se que
4,647x10-3 L reagem sofrendo ionização e
formando o ácido sulfídrico, H3O+ + S-2; todo o
volume restante continua na forma molecular.
Dado: volume molar = 22,46 L/mol (25°C e 1
atm).
20.
(PUC-PR) Da série de ácidos abaixo
representada, qual apresenta a mesma
classificação, dentro do critério de número de
hidrogênios ionizáveis?
a.
HNO3, HNO2, H2S, H2SO3
b.
H3PO4, H3AsO3, H3BO3, H3PO3
c.
H2SO4, H2S2O8, H2CO3, HMnO4
d.
H2CrO4, H3AsO4, HIO3, HBr
e.
H3PO3, H2Cr2O7, H2SnO3, H2SO4