FRENTE III – QUÍMICA ORGÂNICA
AULA 4 – HALETOS, ALCOOIS, FENOIS
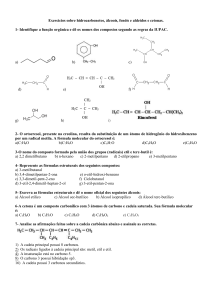
HALETOS ORGÂNICOS
São compostos que possuem um ou mais átomos de
halogênio (Flúor, Cloro, Bromo ou Iodo) ligados ao
carbono. O nome oficial é dado por:
citar ainda DDT e BHC, inseticidas organoclorados
muito utilizados na agricultura.
Nome do halogênio + nome do
hidrocarboneto correspondente
O nome usual é dado por:
“Brometo, cloreto, fluoreto
ou
iodeto”
de
“nome do radical”
Alguns haletos orgânicos são encontrados na
natureza naturalmente, mas em sua maioria, são
obtidos a partir de hidrocarbonetos por substituição
de um ou mais hidrogênios por halogênios. Existem:
•
haletos de alquila: o átomo de halogênio está
conectado a um carbono saturado.
•
haletos de arila: o átomo de halogênio está
conectado a um carbono aromático.
Principais características:
- compostos polares, em virtude da ligação polar
entre C e halogênio;
- pouco solúveis, pois não formam ligação de
hidrogênio com a água;
- aumento do ponto de ebulição está relacionado
com o aumento do número de C, com o aumento do
número de halogênios e/ou com o aumento da
massa atômica do halogênio.
- a temperatura de ebulição e a densidade dos
haletos são maiores que a dos alcanos de massa
molecular próxima:
Muitos haletos são usados na síntese de diversos
compostos orgânicos. Outros, como o clorofórmio e o
tetracloreto de carbono, são amplamente utilizados
como solventes.
O teflon e o PVC são polímeros halogenados muito
conhecidos e de vasta aplicação industrial. Podemos
Ainda, podemos citar os CFC (clorofluorcarbono),
vilões
nas
ultimas
décadas,
quando
foram
amplamente utilizados como gases propelentes em
aerossóis e líquidos refrigerantes em refrigeradores e
aparelhos de ar condicionado. Quando liberados na
atmosfera, reagem como o Ozônio, destruindo a
camada que protege a Terra dos raios UV. A seguir
estão as moléculas CFC e sua reação com o ozônio:
ALCOOIS
São compostos que apresentam o grupo hidroxila
( - OH ) ligado ao carbono saturado, independente
de existir ou não insaturações nos demais átomos de
carbono do composto.
A nomenclatura dos álcoois segue a mesma dos
hidrocarbonetos, a diferença está na terminação OL.
Existe ainda a nomenclatura usual, conforme pode
ser visto nos exemplos a seguir entre parênteses:
Em função do tipo de carbono ligado à hidroxila, os
álcoois podem ser classificados em:
- Primários: quando a hidroxila está presa a carbono
primário (propano-1-ol);
- Secundários: quando a hidroxila está presa a
carbono secundário (ciclopentanol);
- Terciários: quando a hidroxila está presa a carbono
terciário (2-metilpropan-2-ol);
Principais características:
Página 1
FRENTE III – QUÍMICA ORGÂNICA
AULA 4 – HALETOS, ALCOOIS, FENOIS
- álcoois de cadeia pequena são líquidos incolores
com cheiro característico e boa solubilidade em água,
este ultimo devido à formação de ligações de
hidrogênio;
- com o aumento da cadeia carbônica, temos a
diminuição da solubilidade em água e aumento da
temperatura de ebulição.
Comparando-se butano com propanol (massas
moleculares semelhantes) observamos diferenças
consideráveis na temperatura de ebulição:
A seguir, temos temperatura de ebulição dos 6
primeiros membros da série homóloga dos álcoois de
cadeia normal:
Um dos álcoois mais importantes é o etanol ou álcool
etílico.
H3C – CH2 - OH
Ele é obtido a partir da fermentação de
polissacarídeos (amido, celulose) ou dissacarídeos
(sacarose, maltose). Dentre as fontes principais
estão cana-de-açúcar, beterraba, batata, cevada,
arroz, etc.
No Brasil, o etanol é obtido a partir da cana-deaçúcar, representado pelas seguintes equações:
A maior parte do etanol no Brasil é utilizada como
combustível de veículos, e sua principal vantagem é
que sua queima não produz SO2, como produz a
gasolina. Está ainda presente em todas as bebidas
alcoólicas destiladas e não-destiladas.
O metanol é outro álcool de grande importância para
a indústria.
H3C –OH
Ele é obtido historicamente pela destilação da
madeira e hoje produzido sinteticamente. É matériaprima de partida da indústria de plástico, além de ser
utilizado como combustível de aviões a jato e carros
de corrida. Trata-se de um álcool altamente tóxico,
podendo levar a cegueira e até a morte, devido às
substancias formadas no fígado por sua ingestão
(metanal e ácido metanoico).
IMPORTANTE: Quando tivermos dois grupos hidroxila
em um mesmo carbono teremos DIÓIS GEMINAIS,
que são muito instáveis e decompõe-se rapidamente
por desidratação.
IMPORTANTE: Quando o grupo hidroxila estiver
ligado a um carbono insaturado, a função orgânica
não será álcool. Se o carbono for insaturado de um
alceno simples, a função será o ENOL e se o carbono
for insaturado de um anel aromático, a função será
FENOL.
FENOIS
São compostos que apresentam o grupo hidroxila
( - OH ) ligado ao carbono de um anel aromático.
Assim como os aromáticos, os fenóis possuem uma
nomenclatura a parte às regras IUPAC.
A principal aplicação dos fenóis é como agente
bactericida. Já foi amplamente utilizado como
desinfetante de materiais cirúrgicos, mas foi
substituído em razão de sua toxicidade.
Principais caraterísticas:
- Possuem elevadas temperaturas de ebulição por
apresentarem em sua composição o grupo hidroxila e
a presença de no mínimo 1 anel aromático (6
carbonos);
- São parcialmente solúveis em água.
Página 2