Evidências – mas não muito “evidentes” – da ocorrência de transformações
químicas
Filmes de detetive
Você já deve ter visto vários filmes de detetive. Logo no início, há um homicídio ou um roubo a ser
investigado. Em seguida, o protagonista é chamado e entra na “cena do crime” com um olhar “só
dele”, capaz de enxergar o que ninguém mais enxerga, percebendo detalhes importantes,
escondidos em objetos comuns.
No decorrer do filme, o detetive faz a análise das informações e das pessoas envolvidas,
classifica os suspeitos e as circunstâncias que os envolvem. Depois, ele procura conectar as
informações de forma lógica, criando hipóteses e escolhendo as mais prováveis, até descobrir o
modus operandi, a motivação e a identidade do criminoso.
Depois de algumas cenas de perseguição, com muitas
trocas de tiros e batidas de carros, acontece a prisão ou a
morte do criminoso. Com uma cena romântica no final, o
filme agrada a todos e já pode terminar. Sherlock Holmes
que o diga.
Uma das qualidades mais importantes para qualquer
investigador ou perito criminal é saber identificar e
diferenciar “pistas”, “evidências” e “provas”, diferenciandoas de outras informações sem importância. Afinal, muitas
coisas estão lá por acaso, sem nenhuma relação com o
crime.
Sabemos também que “pistas” são aquelas informações
importantes, mas insuficientes para uma conclusão
definitiva. Mas, as “evidências”, as “provas circunstanciais”
e as “provas cabais” são informações que têm um peso
muito maior, que oferecem um maior grau de certeza
sobre o ocorrido.
Ilustração de um livro de Conan Doyle, onde Sherlock Holmes investiga a cena de um crime.
Disponível em: http://commons.wikimedia.org/wiki/File:Abbe-03.jpg - Acesso: 22.11.2013.
Investigação científica
A investigação científica não é muito diferente. Há centenas de anos, os químicos, físicos e
biólogos estudam a natureza da matéria orgânica e inorgânica; e construíram um sistema de
interpretação e de linguagem que permite o estudo e a troca de informações sobre todos os tipos
de substâncias, misturas e fenômenos. As “ciências” são conhecimentos organizados e
sistematizados; por isso, as fórmulas e as equações químicas são as mesmas em todo o mundo.
O “olhar científico” permite classificar mais facilmente as coisas e os fatos, a partir de
generalizações conhecidas. É possível criar hipóteses, testá-las experimentalmente e fazer
descobertas.
Como um detetive, também precisamos identificar as “pistas”, e saber diferenciá-las das
“evidências” e das “provas” sobre os diversos mistérios que envolvem a matéria e a natureza.
Palavra-chave: substância
As expressões “transformação química”, “reação química” ou, ainda, “fenômeno químico”
significam exatamente a mesma coisa. São processos comuns que acontecem o tempo todo na
atmosfera, no solo, na água do mar e dos rios, no nosso sangue, nas células e organelas do
nosso corpo, nas plantas, nos motores dos carros, nas indústrias, nas cozinhas, nas padarias e
até no lixo...
Transformações como a respiração, digestão,
fermentação, corrosão de metais, combustão,
precipitação, decomposição e neutralização ácidobase são alguns exemplos de uma variedade imensa
de “fenômenos”, que são chamados “químicos”, por
uma única razão: há a “criação” de novas
substâncias. Nesse caso, os “produtos” do fenômeno
possuem outras fórmulas e outros nomes
químicos, diferentes das substâncias iniciais.
Ao contrário, o “fenômeno físico” é aquele em que
nenhuma nova substância é criada. São
transformações em que o mesmo material – uma ou
mais mistura de várias substâncias – sofre alguma
transformação, mas que não chega a alterar suas
características químicas microscópicas, no nível
atômico-molecular. Se essa natureza “íntima” não foi
modificada, não estamos obrigados a representá-la
por novas fórmulas e novos nomes químicos.
Amadurecimento de uvas, indicada por cores diferentes: uma transformação química
Disponível em: http://commons.wikimedia.org/wiki/File:Grapes_during_pigmentation.jpg - Acesso: 22.11.2013.
Mas, alguns problemas se apresentam:
– Como saber se uma transformação gerou novas substâncias, se não podemos “enxergar”
os átomos e as moléculas? Eles não podem ser vistos, nem mesmo com o auxílio do
microscópio ótico.
– Além disso, algumas transformações parecem transformar a natureza íntima da matéria e
são fenômenos físicos; enquanto outros fenômenos químicos podem acontecer sem serem
percebidos, mesmo por um observador atento.
– Muitos acreditam que fenômenos reversíveis são físicos; e que os irreversíveis são
químicos. Seria uma generalização muito útil e simples, se fosse verdadeira; mas não. Não
é verdade. Existem fenômenos físicos irreversíveis; e químicos reversíveis e viceversa.
“Então, como descobrir a verdade, Sherlock?”
“Bem, Watson, vamos por partes.”
Primeiro
Qualquer “transformação” implica em um estado inicial, diferente de um estado final.
Antes
ESTADO INICIAL
→
transformação
Depois
ESTADO FINAL
Gelo derretendo e água em ebulição
Mudanças de estado são fenômenos físicos, pois a substância é a mesma
Imagens disponíveis em: http://commons.wikimedia.org/wiki/File:Eis-3.jpg e
http://commons.wikimedia.org/wiki/File:Kochendes_wasser02.jpg Acesso: 20.11.2013.
Queima: um fenômeno químico, pois novas substâncias são formadas
Disponível em:http://commons.wikimedia.org/wiki/File:Coci%C3%B1a_de_le%C3%B1a._Forno.jpg Acesso: 20.11.2013
No fenômeno químico, chamamos o estado inicial de “reagentes”; e o final, de “produtos”.
Antes
REAGENTES
Depois
→
PRODUTOS
transformação química
Se o fenômeno é físico, há uma transformação, sim, mas das mesmas substâncias, que, por
isso, não são chamadas de reagentes, nem de produtos.
Por exemplo, a vaporização da água (H2O líquida), formando vapor de água (H2O vapor).
Antes
Depois
ESTADO INICIAL
ESTADO FINAL
H2O(l)
→
H2O(g)
transformação física
Segundo
O conceito de substância não é tão preciso, variando com o tipo de ligação química que o
material apresenta. Por isso, precisamos saber classificar as substâncias pelo tipo de ligações
químicas para, então, saber que tipo de unidade estrutural está presente no material a ser
classificado.
Ligação
química
Ligação
iônica
Ligação
metálica
Tipo de
substância
Sustância
iônica
Substância
metálica ou ligas
metálicas
Substância
molecular
Substância
covalente
Unidades
estruturais
Íons
Átomos
Moléculas
Átomos
(cátions e ânions se
atraindo “em rede”)
(ligeiramente
positivos, atraindo
elétrons livres)
(podem ser polares
ou apolares)
(neutros, formando
macromoléculas)
Exemplos
Ligação covalente
Sal de cozinha Cobre (Cu), ferro Gás oxigênio
Grafite (carbono
(NaCl),
(Fe), ouro (Au),
(O2), gás
puro), diamante
carbonato de
prata (Ag), zinco carbônico (CO2 ), (carbono puro),
cálcio (CaCO3),
(Zn), estanho
água (H2O),
areia ou sílica
sulfato de cobre (Sn), magnésio álcool (C2H6O),
(SiO2)
(CuSO4)
(Mg), lítio (Li).
glicose
(C6H12O6)
Condutividade
elétrica
Conduzem, se
derretidas ou
dissolvidas, mas
não no estado
sólido.
Conduzem.
Condutividade
térmica
Isolantes.
Condutores.
Isolantes.
Isolantes.
Sólidos, com
exceção do
mercúrio (Hg),
que é líquido.
Gases, líquidos
ou sólidos
Sólidos, com
altíssimos
pontos de fusão.
Insolúveis.
Depende da
polaridade.
Estado físico à Sólidos, com
temperatura
altos pontos de
ambiente
fusão e ebulição.
Solubilidade
em água
Geralmente
solúveis.
Não conduzem.
Não conduzem
(Apenas os ácidos, (exceto o grafite, por
se dissolvidos em
ter estruturas de
água, pois formam
ressonância,
íons.)
liberando elétrons)
(depende da
polaridade e do
tamanho das
moléculas)
Insolúveis.
Terceiro
Raramente as substâncias estão puras. Na maioria das vezes, os materiais, em geral, são
misturas de várias sustâncias, inclusive de tipos diferentes de substâncias.
Quarto
Se, após uma transformação, as unidades estruturais ou espécies químicas que formam as
substâncias do estado inicial permanecem inalteradas, o fenômeno é físico. Se as unidades
estruturais não são mais as mesmas, houve formação de uma ou mais substâncias novas no
sistema; então, o fenômeno é químico.
“Vamos investigar um mistério, Sherlock?”
Assim, em uma investigação científica, analisamos se uma transformação
qualquer produz mudanças nas características e propriedades
específicas das substâncias; em caso afirmativo, sabemos que uma nova
substância foi criada. Mas, além disso, talvez precisemos identificar qual
substância foi criada.
MISTÉRIO: O caso do gás não identificado
O contato entre um sólido e um líquido gerou bolhas, num experimento realizado
em um copo comum. O líquido usado foi água. O gás produzido não tem cheiro. O que se pode
deduzir? Consulte a tabela e perceba que o gás produzido é uma pista de que, provavelmente,
uma substância molecular foi criada, provavelmente de moléculas pequenas e apolares.
Hipótese 1: o gás já existia antes e o fenômeno é físico. Para aceitar isso, devemos procurar
saber se o sólido era, talvez, um tipo de balão solúvel em água, que, depois de dissolvido, liberou
o gás. Mas essa hipótese é pouco provável, pois o gás poderia estar visível, antes da
transformação, além de fazer o sólido flutuar, produzindo poucas bolhas.
Hipótese 2: o sólido é um comprimido efervescente que, em contato com a água, gera bolhas de
gás carbônico; fenômeno químico.
O comprimido contém bicarbonato de sódio (NaHCO3), que libera o ânion bicarbonato (HCO3-1) em
meio aquoso. O comprimido também contém um ácido que libera cátions “H+” na água. O
bicarbonato reage com ácido, liberando gás carbônico.
Bicarbonato de sódio:
uma substância iônica.
HCO3-1
+
ânion bicarbonato
H+
H2 O (l)
+
ácido qualquer
→ água
CO2 (g)
gás carbônico
Nesse processo, o ácido é neutralizado, já que o cátion H+ reage, formando água.
Hipótese 3: o sólido é um metal que, em contato com ácido dissolvido em água, gera gás
hidrogênio. Neste caso, o metal é corroído pelo ácido, que libera bolhas. O ácido também é
neutralizado nesse caso, já que os cátions H+ do ácido recebem elétrons e formam o gás
hidrogênio (H2) e vão para a atmosfera.
Fe
+
2 H+
ferro metálico
ácido qualquer
→
H2 (g)
+
gás hidrogênio
Fe2+(aq)
cátion dissolvido
“É elementar, meu caro Watson.”
Solução do mistério:
1) Se tivermos alguma pista de qual sólido foi usado e
como o metal é bem diferente do comprimido
efervescente, saberemos qual gás foi produzido.
2) Soluções ácidas encontradas não solucionam o
mistério, pois os “ácidos” estão em duas das hipóteses.
3) Se pudermos testar os gases formados em uma
chama, o mistério estará resolvido, pois o gás carbônico
apaga o fogo, enquanto o gás hidrogênio é combustível.
4) Outro caminho é verificar se há cátions de elementos
metálicos no líquido, para confirmar a hipótese três.
Estátua em bronze do personagem Sherlock Holmes, na Suíça.
O bronze é uma liga metálica de estanho (Sn) e cobre (Cu), muito
resistente à corrosão.
Disponível em: http://commons.wikimedia.org/wiki/File:Sherlock_Holmes_statue_at_Meiringen1.jpg Acesso: 22.11.2013
“Pistas” deixadas por um fenômeno químico
Se as substâncias e suas unidades estruturais mudam, podem mudar diversas características
macroscópicas da matéria; ou seja, ficam visíveis a olho nu.
Formação de bolhas, “espuma” ou efervescência
Aquecimento espontâneo ou resfriamento espontâneo
Mudança de cor
Emissão de luz
Mudança de consistência
Mudança de cheiro
Mudança de sabor
Formação de precipitado
Alterações dos pontos de fusão e de ebulição
Aumento ou diminuição na condutividade elétrica
Aumento ou diminuição da condutividade térmica
Aumento ou diminuição da solubilidade
“Mas, por que são apenas pistas e não provas, Holmes?”
Essas “pistas” vão se tornando “evidências” e “provas” de fenômeno químico, principalmente
quando acontecem várias simultaneamente. Se acontecem isoladas, podem ser decorrência de
algum fenômeno físico.
Exemplo 1:
O sal de cozinha, quando dissolvido em água, perde a consistência de sólido, mas não deixou de
ser cloreto de sódio (NaCl). Apenas uma mistura foi feita, não uma reação química. Misturar e
separar misturas são fenômenos físicos.
Exemplo 2:
Mudanças de consistência, que acontecem isoladamente, podem ser decorrência de simples
mudança de estado. O gelo é bem mais consistente que a água líquida, mas continua sendo
“água”.
A manteiga e a cera fria são bem duras, mas, quando
levemente aquecidas, derretem e perdem consistência.
Solidificação, fusão, ebulição e todas as outras
mudanças de estado são fenômenos físicos.
A cera fria é bem dura, mas perde consistência, quando
aquecida. Parece um fenômeno químico, mas é um fenômeno
físico.
Disponível em: http://commons.wikimedia.org/wiki/File:Cera_api_in_pani.jpg Acesso: 20.11.2013
Exemplo 3:
A queima do papel libera grande quantidade de calor e é
uma reação química; mas, quando dissolvemos soda
cáustica (hidróxido de sódio, NaOH) em água, também há
grande liberação de calor, podendo até ferver a água, se a
proporção de soda for grande. Apenas uma dissolução
exotérmica foi feita; portanto, uma mistura, e não uma
reação química.
Disponível em: http://commons.wikimedia.org/wiki/File:Reaccionprueba.png
Acesso: 20.11.2013
Exemplo 4:
A formação de um “precipitado” pode parecer uma “solidificação”, uma simples mudança de
estado. Mas não: um precipitado se forma, quando soluções aquosas se misturam, contendo sais
solúveis em água. Quando entram em contato, pode haver uma atração maior entre o cátion de
uma delas e o ânion de outra, que formam um novo sal insolúvel, que cristaliza e vai para o fundo.
Não se trata de um líquido que foi resfriado até abaixo de seu ponto de fusão e solidificou. Foi
uma reação química entre dois sais, formando um terceiro, que precipitou e, ainda, um quarto sal,
que permaneceu dissolvido.
Exemplo 5:
De forma semelhante, a dissolução do nitrato de potássio (KNO3) é endotérmica; ou seja,
quando dissolvemos esse sal em água, acontece resfriamento espontâneo e a mistura fica bem
gelada. Isto acontece porque o nitrato de potássio precisa absorver calor do ambiente para
dissolver, o que faz resfriar tudo em volta, até o recipiente onde foi feita a mistura. Como toda
dissolução, trata-se de um fenômeno físico.
Exemplo 6:
Uma barra de ferro, quando aquecida, fica incandescente,
emitindo uma luz avermelhada; ou seja, muda de cor e
emissão de luz. Mas o ferro aquecido
continua sendo a
substância simples “ferro”. O que acontece é que seus elétrons
ficam excitados com a energia fornecida do ambiente (calor),
saltam para as camadas mais externas da eletrosfera do átomo
e depois retornam aos níveis normais, emitindo a energia de
volta ao ambiente, na forma de luz. É um fenômeno físico.
Ferro incandescente, derretido, emitindo luz.
Fenômeno físico.
Disponível em: http://commons.wikimedia.org/wiki/File:Castingiron.jpg - Acesso: 20.11.2013
Generalizações ou “provas” de fenômenos físicos
Promover mudanças de estado por aquecimento ou resfriamento
Misturar
Separar misturas
Aquecer
Conduzir calor
Conduzir eletricidade
Produzir movimento
Funcionar de motor elétrico e funcionamento de dínamo
Produzir luz por aquecimento ou energia elétrica
Fazer funcionar lâmpadas elétricas
Mudanças de estado: fenômenos físicos
http://commons.wikimedia.org/wiki/File:Imagem_igor.jpg
“Podemos fazer generalizações de fenômenos químicos, Watson. São as provas que
procurávamos.”
Queima ou combustão
Toda queima ou combustão é uma reação química entre um combustível e um “comburente”,
geralmente o gás oxigênio (O2) do ar atmosférico, liberando grande quantidade de energia na
forma de luz e calor (fogo). Explosões são queimas muito rápidas, acompanhadas de grande
estrondo e produção de calor e luz; portanto, são fenômenos químicos. Não devemos confundir
explosão com “estouro”; um pneu ou um balão pode estourar, por causa da pressão do ar que o
arrebenta; mas não explode. Já um explosivo possui, em suas moléculas, átomos de oxigênio
para criar mais condições de contato e proximidade entre o oxigênio e os outros elementos, para
uma reação rápida.
Oxidação de metais e obtenção (redução) de metais a partir de minérios
Com exceção do ouro, que já é encontrado na natureza, na forma de metal amarelo, os outros
metais dificilmente são obtidos na forma “metálica” diretamente. Os minérios são substâncias
onde os elementos metálicos estão, na forma de cátions, sendo necessário algum processo
metalúrgico para sua conversão em metal.
No caso do ferro, os minérios contêm cátion
ferroso (Fe2+, amarelado), férrico (Fe3+,
avermelhado) ou ambos; e o processo
siderúrgico (metalurgia do ferro) usa carvão
em brasa para produção de monóxido de
carbono dentro do alto-forno. O monóxido de
carbono (CO) reage com o óxido de ferro III
(Fe2O3), formando ferro metálico (Feº) e
dióxido de carbono (CO2). No caso do
“enferrujamento”, a reação é oposta: o ferro
metálico reage com o oxigênio do ar, na
presença de água, formando hidróxido
ferroso (ferrugem amarela) ou hidróxido
férrico (ferrugem vermelha) ou a mistura de
ambos, misturados na superfície do ferro
metálico. Aos poucos, a ferrugem vai se “descascando” do objeto, expondo os átomos mais
internos, que, por sua vez, vão oxidando também, desgastando e corroendo o metal.
Nos fios e conexões elétricas de cobre, depois
de um tempo, também aparece uma espécie de
“ferrugem” do cobre: um sólido verde azulado,
chamado de “zinabre”. Como o cobre está
oxidado, ou seja, na forma iônica, a formação
do zinabre compromete a capacidade de
condução elétrica do cobre metálico (Cuº),
causando interrupções de funcionamento e
defeitos nas instalações elétricas.
Ferro e cobre oxidados.
Imagens disponíveis em:
http://commons.wikimedia.org/wiki/File:Rust.rost.JPG
e http://commons.wikimedia.org/wiki/File:Budapešť_0453.jpg
Acesso: 22.11.2013
Funcionamento de motor a combustão e a nossa biologia
Salvo os carros totalmente elétricos, os automóveis funcionam com motores a combustão, ou
seja, queimam algum combustível, seja álcool, gasolina, diesel etc. Os fenômenos de
“movimento” são considerados físicos, como é o caso do movimento de um carro por uma
estrada; mas são possíveis, devido a outros fenômenos de natureza química. A energia
armazenada no combustível é convertida em energia cinética, ou seja, em movimento circular nos
motores. De forma semelhante, quando uma pessoa anda, o fenômeno de deslocamento é
considerado físico; mas a energia produzida em seus músculos para que o movimento seja
possível, é fenômeno químico, pois há queima de glicose nas células para a produção de energia.
Cozinhar, fritar ou assar
Cozinhar ou fritar um ovo? Mas como, se o ovo
continua sendo “ovo”? Sim, mas o ovo cozido ou frito
já tem outra cor, outro sabor, outro cheiro, maior
consistência etc. São várias “pistas” juntas.
O que acontece é que suas proteínas sofrem
transformações por ação do calor, tendo sua cadeia
carbônica retorcida, modificando suas propriedades
físicas e químicas. Não é uma solidificação, pois ele
teria que ser resfriado e não aquecido, para
simplesmente “solidificar”. Todos os outros alimentos
preparados por ação do calor, que foram cozidos,
assados ou fritos, sofreram mudanças químicas.
Disponível em (acesso: 22.11.2013): http://commons.wikimedia.org/wiki/File:Telur.jpg
Produção de eletricidade por pilhas e baterias
Todas as pilhas e baterias produzem eletricidade a partir de reações químicas de oxirredução, em
que um elemento metálico perde elétrons para um outro elemento ionizado, cujos íons tenham
mais tendência de receber elétrons.
Os elétrons passam de um elemento a outro
através dos fios do circuito externo à pilha.
Na ilustração, uma “pilha de limão”, onde
um metal comum (ferro dos parafusos)
concorre mais para a perda de elétrons que
o cobre (metal nobre nas moedas), criando
uma “diferença de potencial” elétrico.
Os sumos dos limões são meios
eletrolíticos, ou seja, soluções aquosas
ricas em íons, para conduzir a corrente
elétrica.
Disponível em: http://commons.wikimedia.org/wiki/File:LED_Lighting_by_Lemon_Battery.jpg - Acesso: 22.11.2013
Quando a pilha ou bateria é recarregável, significa que o fenômeno químico é reversível. Ou
seja, usando uma corrente elétrica mais forte, de sentido oposto ao da pilha, os elétrons retornam
ao metal que os havia perdido.
Nos automóveis, há um “dínamo” ou
“alternador” para aproveitar a energia
cinética produzida pelo motor, convertendoa em energia elétrica, para manter a bateria
do carro carregada. Enquanto a bateria
descarrega pelo uso de faróis, rádio,
ignição etc., a reação química acontece em
um sentido; quando é recarregada pelo
dínamo ou alternador, a reação acontece
no sentido oposto.
Interior de um alternador. Fios enrolados de
cobre (bobina) e um conjunto de ímãs em
movimento transformam energia cinética em
energia elétrica.
Disponível em: http://commons.wikimedia.org/wiki/File:Dynamo.JPG - Acesso: 22.11.2013.
Carbonatos e bicarbonatos em reação com ácidos
Você já deve ter tomado bicarbonato de sódio dissolvido em água para aliviar a acidez estomacal.
Ou, talvez, já tenha adicionado a mesma substância em uma limonada ou suco de abacaxi para
“tirar o azedo”, e viu a produção de bolhas de um gás. Os carbonatos e bicarbonatos reagem com
ácido, neutralizando-os e liberando gás carbônico. A “espuma” formada sobre a limonada são
bolhas de gás carbônico.
Reações que emitem luz: vaga-lumes, pulseiras de neon e “luminol” para desvendar crimes
Existem reações químicas que liberam energia na forma de luz e de calor. A queima é um
exemplo. Mas existem outras reações que emitem mais luz do que calor, inclusive no mundo
vegetal e animal. Algumas algas e também peixes e crustáceos que vivem em grandes
profundidades no oceano são capazes de emitir luz. Os vaga-lumes também são capazes de
controlar a reação da substância “luciferina” com o oxigênio absorvido pela respiração, em
presença de ATP, íons magnésio (Mg2+) e a enzima luciferase, produzindo outra substância, a
“oxiluciferina” e luz.
Imagens disponíveis em: http://commons.wikimedia.org/wiki/File:Lampyris_noctiluca.jpg
e http://commons.wikimedia.org/wiki/File:Knicklichter_Party_1.JPG - Acesso: 22.11.2013.
As “pulseiras de neon”, na verdade, não são de neon. O “neon” ou “neônio” (Ne) é um gás que é
usado em lâmpadas fluorescentes para produzir luminosidade em letreiros de propaganda; mas,
há décadas, estão sendo substituídos por luminosos de LED. As pulserinhas ou lightsticks se
parecem com o neon dos letreiros e, por isso, são chamadas assim. Elas possuem duas
substâncias líquidas, o “luminol” (C8H7N3O2) e “peróxido de hidrogênio” (H2O2, água oxigenada),
que fica dentro de uma cápsula frágil de vidro bem fino. Quando dobramos a pulseira, a cápsula
de vidro se rompe, liberando o peróxido de hidrogênio e substâncias entram em contato. Então, a
reação acontece, com liberação de luz.
O luminol também é usado por peritos
criminas na localização do sangue que
foi lavado – mesmo que por várias
vezes - em cenas de homicídio, pois o
ferro do sangue é um catalisador para a
reação de luminescência do luminol. Em
presença de água oxigenada e de um
hidróxido, o ferro facilita a reação de
luminescência do luminol, produzindo
uma luz azul bem visível, quando se
apaga a luz do cômodo.
Luminol, em presença da hemoglobina do sangue
humano.
Disponível em:
http://commons.wikimedia.org/wiki/File:Luminol.jpg
Acesso: 22.11.2013
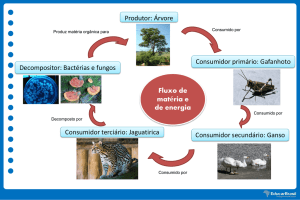
Fotossíntese, digestão e respiração: o maior equilíbrio ecológico da Terra
A reação de fotossíntese é a produção da substância orgânica glicose (C 6H12O6), a partir do gás
carbônico (CO2) e da água. As plantas conseguem fazer essa reação, absorvendo a luz solar com
o auxílio das moléculas de clorofila. A glicose armazena a energia solar nas ligações entre os
átomos. A “respiração” é o processo oposto ao da fotossíntese. Na respiração, a glicose é
queimada de forma enzimática, ou seja, com o auxílio de enzimas, que facilitam a queima sem
que haja produção de chamas. Os animais não conseguem fazer fotossíntese; ou seja, não
produzem suas próprias substâncias energéticas. Por isso, eles precisam comer as plantas, fazer
a digestão dos alimentos para absorver a glicose e outros nutrientes. A glicose é levada pela
corrente sanguínea até as células, onde é queimada e transformada em gás carbônico e água
novamente. Esse é o maior equilíbrio ecológico da Terra, traduzido de forma química, que
acontece entre plantas e animais.
6 CO2
+
Sentido da fotossíntese
6 H2O
C6H12O6
Sentido da respiração
Amadurecimento de frutas
Quando as frutas amadurecem, há mudanças significativas na sua cor, sabor e cheiro. Em geral,
ficam menos ácidas e mais adocicadas, acusando transformações de neutralização de seus
ácidos e aumento na quantidade e concentração de seus açúcares. Diversas reações químicas
acontecem neste processo. As mudanças de cor em suas cascas são devidas à presença de
substâncias indicadoras ácido-base que, com a diminuição ou aumento da acidez, formam
complexos de cores diferentes, ora com íons hidrônio (H3O+ ou H+, característicos do meio ácido),
ora com íons hidróxido (OH-, característicos do meio básico).
Fermentação
É a reação mais importante na fabricação de pães, bolos, bebidas alcoólicas e derivados do leite,
como iogurtes, queijos e coalhadas. Existem três tipos de fermentação:
Fermentação alcoólica: É realizada por alguns tipos de fungos ou leveduras, produzindo etanol
e dióxido de carbono. É importante na produção de vinho, cerveja, cachaça e todas as outras
bebidas alcoólicas e do pão. A cerveja e os vinhos espumantes são comercializados ainda em
processo de fermentação; e, por isso, produzem bolhas de gás carbônico o tempo todo.
A fermentação alcoólica produz gás carbônico, que
pode ser percebido na forma de bolhas.
Algumas bebidas são fermentadas e depois
armazenadas por longos períodos, em tonéis de
madeira, como o vinho.
Todas as bebidas são fermentadas. As bebidas de
maior teor alcoólico são também destiladas, como a
cachaça, a tequila, a vodca etc. O vinho e a cerveja
não são destilados.
Ao lado, alambiques para destilação de tequila. A
fermentação é uma reação química; a destilação é
apenas um método de separação de misturas;
portanto, fenômeno físico.
Imagens disponíveis em: http://commons.wikimedia.org/wiki/File:Fementação_alcoolica.jpg,
http://commons.wikimedia.org/wiki/File:Glass_widget_comparison.jpg,
http://commons.wikimedia.org/wiki/File:Sherry_cellar,_Solera_system_2,_2003.jpg e
http://commons.wikimedia.org/wiki/File:Copper_tequila_stills.jpg Acesso: 22.11.2013
Fermentação acética: é a continuação da fermentação alcoólica, que transforma o álcool em
ácido acético. Nesse processo, o vinho “estraga” ou “azeda”, se transformando em vinagre.
Fermentação láctica: Em geral, são as bactérias do gênero Lactobacillus que fazem a
fermentação. No caso do iogurte, as bactérias Lactobacillus bulgaricus e Streptococcus
thermophilus são adicionadas ao leite para produzir acidez, sabor e aroma desejados. Elas usam
a lactose (açúcar) do leite para produzir a energia de que precisam para viver e se multiplicar,
produzindo ácido láctico.
Disponível em: http://commons.wikimedia.org/wiki/File:Queijo_coalho.jpg Acesso: 22.11.2013
A acidez do ácido láctico provoca a coagulação das proteínas do leite e o “coalho”, que é usado
na fabricação de iogurtes e queijos. Alguns produtores e distribuidores de leite desonestos
costumam adicionar soda cáustica (hidróxido de sódio, NaOH) ao leite, para neutralizar o ácido
láctico produzido na fermentação, dando a impressão de que o leite ainda está na validade.
As evidências de uma reação de fermentação são:
1. A produção de bolhas, indicando a formação do gás carbônico (CO2).
2. O aumento de temperatura do sistema, pois a fermentação é exotérmica.
Conclusão
Reconhecer um fenômeno químico nem sempre é fácil. Mas, conhecendo os principais tipos de
reações e de fenômenos físicos, é possível diferenciá-los, com alto grau de acerto. Mantenha
sempre sua curiosidade e espírito científico e use sua habilidade de dedução!