
2ª Série do Ensino Médio
16. O gás cloro pode ser obtido pela eletrólise da água do mar ou pela
eletrólise ígnea do cloreto de sódio.
Assinale a afirmativa correta com relação a esses dois processos:
(A)
(B)
(C)
(D)
(E)
Ambos liberam CA2 gasoso no cátodo.
Ambos envolvem transferências de dois elétrons por mol de sódio.
Ambos liberam H2 no cátodo.
Ambos liberam Na metálico no cátodo.
Um libera H2 e outro, Na metálico no cátodo.
17. Alumínio metálico é produzido industrialmente pela eletrólise de
alumina fundida, utilizando-se grafite como eletrodo positivo. O processo
pode ser representado pela equação:
2 AA2O3 + 3 C → 4 AA + 3 CO2
As reações que podem ocorrer espontaneamente são:
(A) I e II;
(B) I e IV;
(C) I, III e IV;
(D) III e IV;
(E) II e III.
20.
A quantidade de carga elétrica necessária para depositar, por
eletrólise, 63,5 g de cobre a partir de íons Cu2+ é:
(A)
(B)
(C)
(D)
(E)
1 C;
2 C;
1 F;
2 F;
3 F.
A respeito dessa reação, é correto afirmar que:
21. A massa de metal depositada quando uma corrente de 10 A atravessa
uma solução de AgNO3, durante 16 minutos e 5 segundos, é:
(A)
(B)
(C)
(D)
(E)
(A)
(B)
(C)
(D)
(E)
o
o
o
o
o
alumínio se reduz espontaneamente em presença de grafite;
alumínio sofre oxidação no pólo negativo da célula;
carbono atua como oxidante no pólo positivo;
número de oxidação do alumínio passa de +2 a zero;
número de oxidação do carbono passa de zero a +4.
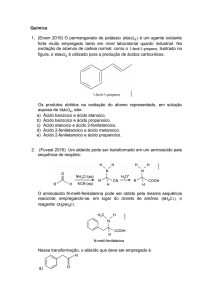
18. Adicionam-se iodo e bromo a uma solução contendo I– e Br–. A
partir das semi-reações apresentadas e considerando as concentrações
1,0 mol/L, assinale a voltagem da reação espontânea:
9,8 g;
14,16 g;
18,5 g;
4,9 g;
10,8 g.
22. Para a deposição eletrolítica de 11,2 g de um metal cujo peso
atômico é 112, foram necessários 19300 C. Portanto, o número de
oxidação do metal é:
(A)
(B)
(C)
(D)
(E)
+1
+2
+3
+4
+5
23. Os aldeídos reagem com o ácido cianídrico dando:
(A)
(B)
(C)
(D)
(E)
+0,531 V
+1,601 V
– 1,601 V
– 0,531 V
+1,07 V
19.
Considere as reações incompletas e os dados da tabela a seguir:
IIIIIIIV-
Pb + Mg2+ →
Br- + Fe2+ →
Pb2+ + Ni →
Zn + Ag+ →
(A)
(B)
(C)
(D)
(E)
oximas;
hidrazina;
nitrila;
ácido barbitúrico;
cianidrinas;
24. Um composto de fórmula C6H12O apresenta isomeria óptica. Quando
reduzido por hidrogênio, este composto transforma-se em álcool
secundário. Qual dos nomes abaixo representa o composto?
(A)
(B)
(C)
(D)
(E)
2-hexanona;
3-metil-pentanona-2;
dimetil-butanona;
hexanal;
2-metil-3-pentanona.
25. A oxidação do metil propeno na presença de solução de KMnO 4
em meio H2SO4 produz:
(A) propanona, gás carbônico e água;
(B) propanona e o aldeído fórmico;
(C) ácido propanóico e o aldeído fórmico;
(D) ácido propanóico e o ácido fórmico;
(E) somente gás carbônico e vapor d’água.
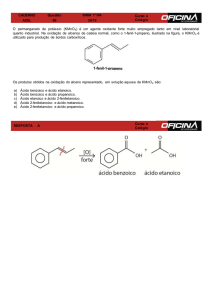
26. Os produtos da oxidação de um dado alceno são: ácido metil
propanóico e acetona.
O alceno em questão é:
(A)
(B)
(C)
(D)
(E)
2-metil-3-hexeno;
3-metil-3-hexeno;
2,3-dimetil-2-penteno;
2,4-dimetil-2-penteno;
2,3,3-trimetil-1-buteno.
27. Um alceno, por ozonólise seguida de hidrólise, produziu metanal e
etil-metil-cetona. O alceno utilizado foi:
(A)
(B)
(C)
(D)
(E)
2-metil buteno-2;
metil propeno;
penteno-2;
2-metil buteno-1;
3,3-dimetil buteno-1.
28.
A oxidação exaustiva do buteno-2 produz:
(A)
(B)
(C)
(D)
(E)
propanona;
ácido etanóico;
ácido butanóico;
ácido metanóico;
butanona.
29.
Um dos componentes da cera de abelha é a substância:
O
//
H3C – (CH2)24 – C
\
O – (CH2)27 – CH3
Ela pode ser formada pela reação entre:
(A)
(B)
(C)
(D)
(E)
30.
dois ácidos carboxílicos;
um aldeído e um álcool;
uma cetona e um álcool;
um aldeído e um ácido carboxílico;
um ácido carboxílico e um álcool.
Na reação de saponificação:
CH3COOCH2CH2CH3 + NaOH → X + Y
Os nomes dos compostos X e Y são :
(A)
(B)
(C)
(D)
(E)
álcool etílico e propionato de sódio;
ácido acético e propóxido de sódio;
acetato de sódio e álcool propílico;
etóxido de sódio e ácido propanóico;
ácido acético e álcool propílico.








![A B ÁCIDO HEXANÓICO [O] [O] X [O] PENTAN-2-ONA Y 3](http://s1.studylibpt.com/store/data/005175326_1-e3b7b0d195d078a9e664a5fbbc00c029-300x300.png)

