Apostila de Química 08 – Funções
Oxigenadas
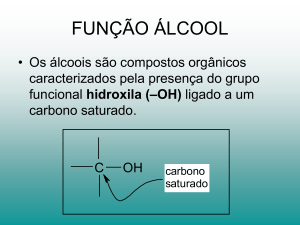
1.0 Álcool
Compostos que apresentam grupo hidroxila ligado ao carbono saturado.
Apresentam pelo menos 1 grupo OH pro carbono.
Grupo Funcional
C – OH
Sufixo
Prefixo
OL
---
1.1 Classificação
Quantidade de grupos hidroxila:
Monoálcool – 1 hidroxila.
Diálcool – 2 hidroxilas.
Poliálcool – 3 ou mais hidroxilas.
Os monoálcoois podem ser classificados em função do tipo de carbono que
contém a hidroxila:
Carbono primário – Primário.
Carbono secundário – Secundário.
Carbono terciário – Terciário.
1.2 Nomenclatura
1.2.1 Nomenclatura Oficial
As mesmas regras dos hidrocarbonetos.
A diferença é o sufixo „-ol‟.
1.2.1.1 Alcoóis Saturados
Monoálcool – Ao apresentar mais que 2 átomos de carbono, indica-se a posição
do OH numerando a cadeia a partir da extremidade mais próxima do carbono
que contém a hidroxila.
Poliálcoois:
As posições do OH são fornecidas pelos menores números possíveis.
As quantidades são indicadas adicionando-se ao sufixo os prefixos que
indicam quantidade.
1.2.1.2 Alcoóis Insaturados
Contém pelo menos uma dupla ou tripla ligação entre carbonos que não
apresentam o grupo OH.
Ordem de prioridade – Grupo funcional, insaturações e ramificações.
1.2.2 Nomenclatura Usual – Monoálcoois
Usa-se o nome do radical ao qual está liga ao grupo OH, usando o esquema –
Álcool radical-ico.
Exemplo:
H3C – OH: Álcool metílico
H3C – CH2 – OH: Álcool etílico
H3C – CH – CH3: Álcool isopropílico.
|
OH
1.3 Principais Alcoóis
1.3.1 Metanol ou Álcool Metílico
Fórmula condensada – CH3 – OH.
Solubilidade em água – Infinita.
Antigamente – obtinha-se o metanol destilando madeira, ganhando o nome de
“álcool da madeira”.
Atualmente – Produzido a partir de carvão e água.
Utilizado como solvente.
Matéria-prima para polímeros.
Era utilizado no Brasil como aditivo da gasolina, sendo substituído pelo etanol –
Grande capacidade de corrosão de aços e toxicidade.
1.3.2 Etanol ou Álcool etílico
Fórmula condensada – CH3 – CH2 – OH.
Solubilidade em água – Infinita.
Obtido a partir da fermentação de polissacarídeos ou dissacarídeos – Cana-deaçúcar, beterraba, batata, cevada e arroz.
No Brasil, a maior parte é utilizado como combustível de veículos – Não produz
dióxido de enxofre (SO2).
2.0 Fenol
Compostos que apresentam grupo hidroxila ligado diretamente ao carbono do
anel aromático.
Apresentam propriedades antibacterianas e fungicidas.
Reage com bases.
Grupo Funcional
C6H5 – OH
Sufixo
---
Prefixo
HIDRÓXI
2.1 Nomenclatura Oficial
As mesmas regras dos hidrocarbonetos.
A diferença é o prefixo „hidróxi-‟.
Se houver ramificações, deve indicar suas posições, obtendo os menores valores
possíveis.
Não há regras usuais para fenóis - Os compostos metilfenol são conhecidos
como cresóis.
2.2 Principal Fenol
2.2.1 Hidroxibenzeno, Fenol ou Ácido Fênico
Fórmula condensada – C6H5 – OH.
Primeiro anti-séptico – Queda muito grande na mortalidade por infecção pósoperatória.
Corrosivo e tóxico.
3.0 Aldeído
Compostos que apresentam grupo carbonila na extremidade da cadeia.
Grupo Funcional
– CHO
Sufixo
Prefixo
AL
---
3.1 Nomenclatura
3.1.1 Nomenclatura Oficial
As mesmas regras dos hidrocarbonetos.
A diferença é o sufixo „-al‟.
O grupo funcional está sempre na extremidade – Ele sempre será o numero 1,
não precisando indicá-lo.
Se existirem 2 grupos funcionais – Usa-se o sufixo „-dial‟.
3.1.2 Nomenclatura Usual
Os 4 aldeídos simples possuem nomes usuais formados pelos prefixos – Form-,
acet-, proprion-, e butir-, seguidos da palavra aldeído.
Exemplos:
Metanal – Formaldeído.
Etanal – Acetaldeído.
Propanal – Proprionaldeído.
Butanal – Butiraldeído.
3.2 Principal Aldeído
3.2.1 Metanal, Formaldeído ou Aldeído Fórmico
Fórmula condensada – COH2.
Gás incolor extremamente irritante para as mucosas.
Quando dissolvido em água – Forma uma solução chamada formol ou formalina.
Desnatura proteínas tornando-as resistentes à decomposição por bactérias –
Usado como fluído de embalsamento, na conservação de espécies biológicas e
como anti-séptico.
4.0 Cetona
Compostos que apresentam grupo carbonila, sendo este carbono secundário.
Grupo Funcional
– CO –
Sufixo
Prefixo
ONA
4.1 Nomenclatura
4.1.1 Nomenclatura Oficial
As mesmas regras dos hidrocarbonetos.
A diferença é o sufixo „-ona‟.
O grupo funcional deve possuir o menor número da cadeia.
---
4.1.2 Nomenclatura Usual
O grupo CO é denominado cetona e seus ligantes são considerados radicais.
Exemplo:
O
||
H3C – C – CH2 – CH3: Etil-metil-cetona.
4.2 Principal Cetona
4.2.1 Propanona, Dimetil-Cetona ou Acetona
Fórmula condensada – CH3 – CO – CH3.
Líquido a temperatura ambiente.
Apresenta odor irritante.
Dissolve-se em água e em solventes orgânicos – Utilizado como solvente de
tintas, vernizes e esmaltes.
Utilizada na extração da cocaína – Controlada pelo Departamento de
Entorpecentes da Polícia Federal.
São encontradas em pequenas quantidades no sangue, chamados de corpos
cetônicos – Formada pela degradação incompleta de gorduras.
5.0 Ácido Carboxílico
Compostos que apresentam grupo carboxila.
Resultado da união dos grupos carbonila e hidroxila.
Todo ácido monocarboxílico de até 15 carbonos apresenta odor desagradável.
Ácidos carboxílicos de cadeia longa são chamados de ácidos graxos.
Grupo Funcional
– COOH –
Sufixo
Prefixo
ÓICO
ÁCIDO
5.1 Nomenclatura Oficial
As mesmas regras dos hidrocarbonetos.
A diferença é o sufixo „-óico‟ e do prefixo „ácido‟.
O grupo funcional está sempre na extremidade – Ele sempre será o numero 1,
não precisando indicá-lo.
Se existirem 2 grupos funcionais – Usa-se o sufixo „-dióico‟.
5.2 Derivados Diretos de Ácidos Carboxílicos
Sais – Os ácidos carboxílicos, ago reagirem com uma base, originam sal e água.
Anidridos – Substâncias obtidas pela desidratação de ácidos carboxílicos.
5.3 Principais Ácidos Carboxílicos
5.3.1 Ácido Metanóico ou Ácido Fórmico
Fórmula condensada – HCOOH.
Líquido incolor de cheiro irritante.
Usado como fixador de pigmentos e corantes em tecidos.
5.3.2 Ácido Etanóico ou Ácido Acético
Fórmula condensada – H3C – COOH.
Líquido incolor de cheiro irritante e sabor azedo.
Utilizado em vinagres.
5.3.3 Ácido Benzóico
Fórmula condensada – C6H5 – COOH.
Sólido branco, cristalino, solúvel em água.
Utilizado como fungicida.
6.0 Éster Orgânico
Compostos que apresentam grupo –COO–.
Origina-se a partir da substituição do hidrogênio do grupo OH de um ácido
carboxílico por um radical orgânico.
Grupo Funcional
– COO –
Sufixo
ATO
Prefixo
NOME DO RADICAL
6.1 Nomenclatura Oficial
As mesmas regras dos hidrocarbonetos.
A diferença é o sufixo „-ato‟ e na adição do nome do radical que substitui o
hidrogênio.
Exemplo:
H3C – COO – COH3: Etanoato de metila.
H3C – CH2 – COO – CH2 – CH3: Propanoato de etila.
7.0 Éter
Compostos que apresentam um átomo de oxigênio entre 2 radicais orgânicos.
Grupo Funcional
–O–
Sufixo
VER ABAIXO
Prefixo
VER ABAIXO
7.1 Nomenclatura
7.1.1 Nomenclatura Oficial
Há 2 formas de se classificar um éster:
Primeira maneira – Prefixo que indica os números de carbonos do menor
radical + oxi + Nome do hidrocarboneto correspondente ao maior radical.
Segunda maneira – Radical + Radical + éter, sendo os radicais em ordem
alfabética.
Exemplos:
H3C – O – CH2 – CH3: Metoxietano ou etil-metil-éter.
H3C – CH2 – O – CH2 – CH3: Etoxietano ou dietil-éter.
7.1.2 Nomenclatura Usual
Utiliza-se o esquema – Éter + Nome do menor radical + Nome do maior radical
+ ico.
Se os 2 radicais forem iguais, o prefixo „di‟ é dispensado.
Exemplos:
H3C – O – CH2 – CH3: Éter metil-etílico.
H3C – CH2 – O – CH2 – CH3 – Éter etílico.
7.2 Principal Éter
7.2.1 Etoxietano, Éter Dietílico, Éter Sulfúrico ou Éter
Fórmula condensada – H3C – CH2 – O – CH2 – CH3.
Líquido incolor.
Inflamável e extremamente volátil.
Utilizada como anestésico, relaxando os músculos, afetando ligeiramente a
pressão arterial, a pulsação e a respiração.
Causa irritação no trato respiratório e pode provocar incêndios nas salas de
cirurgia.
Utilizada na extração da cocaína – Controlada pelo Departamento de
Entorpecentes da Polícia Federal.