UNIVERSIDADE FEDERAL DO PARÁ
CAMPUS UNIVERSITÁRIO DE BRAGANÇA
PROGRAMA DE PÓS-GRADUAÇÃO EM BIOLOGIA AMBIENTAL
CURSO DE MESTRADO E DOUTORADO EM RECURSOS BIOLÓGICOS DA
ZONA COSTEIRA AMAZÔNICA
COMPOSIÇÃO DA QUIROPTEROFAUNA E SUA
SOROPREVALÊNCIA DE ANTICORPOS CONTRA O VÍRUS DA
RAIVA NO NORDESTE DO PARÁ
LANNA JAMILE CORRÊA DA COSTA
BRAGANÇA -PA
2011
Lanna Jamile Corrêa da Costa
COMPOSIÇÃO DA QUIROPTEROFAUNA E SUA
SOROPREVALÊNCIA DE ANTICORPOS CONTRA O VÍRUS DA
RAIVA NO NORDESTE DO PARÁ
Dissertação de Mestrado apresentada ao Programa de
Pós-graduação em Biologia Ambiental (Mestrado e
Doutorado em Recursos Biológicos da Zona Costeira
Amazônica), da Universidade Federal do Pará, Campus
de Bragança, como parte dos requisitos necessários à
obtenção do grau de Mestre em Biologia Ambiental.
.
Prof. Dr. Marcus Emanuel Barroncas Fernandes
(Orientador)
BRAGANÇA -PA
2011
Lanna Jamile Corrêa da Costa
COMPOSIÇÃO DA QUIROPTEROFAUNA E SUA
SOROPREVALENCIA DE ANTICORPOS CONTRA O VÍRUS DA
RAIVA NO NORDESTE DO PARÁ
Banca Examinadora:
______________________________________ - Orientador
Prof. Dr. Marcus Emanuel Barroncas Fernandes
Universidade Federal do Pará - Campus de Bragança
__________________________________________- Titular
Dr. Wilson Uieda
Universidade Estadual de Paulista - Campus de Botucatu
__________________________________________- Titular
Dra. Ana Cristina Mendes de Oliveira
Universidade Federal do Pará
__________________________________________- Titular
Dra. Daniele Barbosa de Almeida Medeiros
Instituto Evandro Chagas
__________________________________________- Suplente
Dra. Elizabeth Salbé Travassos da Rosa
Instituto Evandro Chagas
__________________________________________- Suplente
Profa. Dra. Cláudia Nunes-Santos
Universidade Federal do Pará – Campus de Bragança
BRAGANÇA-PA
2011
i
Always look on the bright of life.
(Monty Python)
ii
Dedico a meus pais: Maria José e José Nicolau, os
principais responsáveis pela criação deste trabalho.
iii
AGRADECIMENTOS
À Universidade Federal do Pará, ao Programa de Pós-Graduação em Biologia
Ambiental (Mestrado e Doutorado em Recursos Biológicos da Zona Costeira
Amazônica), e ao Instituto de Escossistemas Costeiros pela formação e oportunidade de
desenvolver esta pesquisa.
À Fundação de Amparo a Pesquisa do Estado do Pará (FAPESPA) pelo auxílio
financeiro através do projeto do edital número 003/2008 entitulado: “Diversidade e
abundância de morcegos e diagnóstico sócio-ambiental em localidades com registro de
raiva, em humanos e herbívoros, no Nordeste do Pará”, e também pela bolsa de
mestrado referente ao edital número 021/2008.
À Dr. Luzia Martorelle e Ana Paula Cataoka do Laboratório de Zoonoses e
Doenças Transmitidas por Vetores no Centro de Controle de Zoonoses (CCZ/SP), pelos
exames sorológicos realizados nos morcegos capturados no presente trabalho.
Ao Laboratório de Ecologia de Manguezal pelo suporte e apoio para realização
deste trabalho.
Ao Prof. Dr. Marcus pela orientação e oportunidade de realizar este trabalho.
À Fernanda Atanaena por me ensinar muitas coisas referentes ao
desenvolvimento deste trabalho e pela sua amizade.
Ao Tacio por sua ajuda fundamental e indispensável, além de sua alegria que
tornaram muitos momentos difíceis em momentos de descontração.
À Lenilda por estar em praticamente todas coletas, sem ela o trabalho teria se
tornado muito mais difícil e muito menos divertido.
Ao Edson, que sem frescura alguma, teve coragem de me levar
a muitas de minhas coletas em seu carro à qualquer horário e aos lugares quase
inacessíveis.
iv
Aos moradores das vilas visitadas, por me respeitarem e me acolherem com
muita dignidade, principalmente àqueles que me cederam lugares em suas casas, pela
paciência, pela alimentação e por ainda me ajudarem em parte do trabalho.
Ao Rubens e Suzane que em algum momento também me auxiliaram.
Aos meus amigos da turma de mestrado 2009 e aos meus amigos e
companheiros do Laboratório de Ecologia do Manguezel pela amizade e
companheirismo.
Aos meus pais, Maria José e José Nicolau, grandes responsáveis pela minha
educação e caráter, sempre apoiadores e compreensivos, obrigada pelos conselhos,
exemplo, amor e finalmente, por sonharem comigo os meus sonhos...
E a todos que, em momentos não menos importantes dos citados acima,
ajudaram de forma muito importante, os meus sinceros agradecimentos.
v
RESUMO
Nos anos de 2004 e 2005 foram notificados surtos de Raiva humana transmitida
por morcegos hematófagos no Estado do Pará. Este evento despertou o interesse no
estudo das diferentes espécies de morcegos da fauna regional, enfocando,
principalmente, a soroprevalência de anticorpos contra o Vírus da Raiva (RABV) nessas
espécies. As coletas foram realizadas nos municípios de Bragança, Augusto Corrêa e
Viseu, no nordeste do Estado do Pará. Para a captura dos morcegos foram utilizadas dez
redes de espera (12 x 3 m), expostas por duas noites em cada localidade durante os
períodos seco e chuvoso. Os indivíduos capturados foram identificados em nível de
espécie e deles foram obtidas amostras de soro para determinar o nível de produção de
anticorpos contra a Raiva. O estudo resultou na coleta de 949 indivíduos pertencentes a
quatro guildas, 36 espécies, 23 gêneros e quatro famílias. A família Phyllostomidae
apresentou maior percentual de capturas (98%), sendo a espécie Carollia perspicillata a
melhor representada no presente trabalho (n=307; 40%). Em relação à densidade, os três
municípios diferiram significativamente (ANOSIM, R=0,31; p<0,05), ao contrário a
diversidade não apresentou diferença significativa (Kruskal Wallis, H=1,40; gl=2;
p>0,05). Contudo, o município de Bragança destacou-se por apresentar o maior número
de espécies (n=27) e de indivíduos (n=406), o que pode ser resultado da não ocorrência
de surtos em Bragança, sendo assim sua densidade e riqueza de espécies não foi afetada
devido à aderência de algumas medidas de vigilância e controle da Raiva adotadas
durante esse período. A soroprevalência para os municípios combinados foi elevada
(49%) e a diferença entre eles variou significativamente (χ2=10,32; gl= 2; p<0,05),
sendo o município de Viseu o que apresentou maior percentual de indivíduos
soropositivos (62%). Entre as espécies analisadas, Artibeus planirostris foi a que
apresentou maior percentual de indivíduos soropositivos (52%). Os resultados baseados
no número de indivíduos soropositivos e soronegativos nos diferentes períodos do ano
vi
(seco e chuvoso) mostraram diferença bastante significativa (χ2=28,61; gl=1 p<0,001),
sendo o período chuvoso o que apresentou percentual mais elevado (67%; n=95). O
grande de número de indivíduos apresentando produção de anticorpos indica que o
circula muito ativamente na região dos três municípios, sugerindo que tais espécies
tiveram contato com esse vírus. Os resultados do presente estudo mostram que a região
estudada apresenta circulação do RABV entre morcegos de diferentes espécies, sendo
necessário
um
constante
monitoramento
através
epidemiológicas para a vigilância e controle da raiva.
de
medidas
sanitárias
e
vii
ABSTRACT
In 2004 and 2005 outbreaks were reported of human Rabies transmitted by
vampire bats in the State of Para. These events led to the study of different bat species
of the regional fauna, focusing mainly on the seroprevalence of Rabies Virus (RABV)
antibodies in these species. Samples were collected in the municipalities of Bragança,
Viseu, and Augusto Corrêa in the northeastern of the State of Para. For the capture of
ten bats were used mist nets (12 x 3 m), exposed for two nights in each location during
the dry and rainy season. The individuals captured were identified to the species level
and their serum samples were obtained to determine the level of antibody production
against rabies. The study resulted in the collection of 949 individuals belonging to four
guilds, 36 species, 23 genera, and four families. The family Phyllostomidae had a higher
percentage of catches (98%), and the species Carollia perspicillata showed higher
percentage in the present study (n=307, 40%). In relation to the density, the three
municipalities differ significantly (ANOSIM, R=0,31, p<0,05), unlike diversity showed
no significant difference (Kruskal Wallis, H=1,40, df=2, p>0,05). However, the
municipality of Bragança presented the highest number of species (n=27) and
individuals (n=406). These results certainly express the non-occurrence of outbreaks in
Bragança and they did not affect the density and richness of species by the rabies
surveillance and control. The seroprevalence for the municipalities combined was high
(49%) and the difference among them varied significantly (χ2=10,32; df=2; p<0,05), the
municipality of Viseu presented the highest percentage of seropositive individuals
(62%). Among the species analyzed, Artibeus planirostris showed the highest
percentage of seropositive individuals (52%). Results based on the number of
seropositive and seronegative individuals in different seasons of the year (dry and rainy)
showed high significant difference (χ2=28,61; df=1; p<0,001), and the rainy season
presented the highest percentage (67%; n=95).The high levels of antibodies found in
viii
specimens analyzed may indicate that the RABV circulates very actively in the region
of the three municipalities, suggesting that these species were in contact with the
RABV. Finally, the results showed that the studied region presents circulation of the
viral flow among bats of different species, requiring constant monitoring through
sanitary and epidemiological measures for the surveillance and control of the rabies.
ix
LISTA DE TABELAS
Tabela 1:
Proporção de capturas realizadas com redes de espera nos
municípios de Bragança, Augusto Corrêa e Viseu..............................
Tabela 2:
Índice de Shannon (H’) estimado para a área de trabalho e para os
municípios de Bragança, Augusto Corrêa e Viseu..............................
Tabela 3:
20
21
Morcegos capturados nos municípios de Bragança (B), Augusto
Corrêa (AG) e Viseu (V), Nordeste do Pará. Guildas: Frugívora (F),
Insetívora (I), Nectarívora (N), Sanguívora (S)................................... 22
Tabela 4:
Número de indivíduos positivos e negativos para produção de
anticorpos em Bragança, Augusto Corrêa e Viseu, no Estado do
Pará......................................................................................................
Tabela 5
28
Soroprevalência relacionada ao sexo e faixa etária dos morcegos
registrados nos municípios de Bragança, Augusto Corrêa e Viseu,
no Estado do Pará................................................................................
Tabela 6:
31
Número de indivíduos das quatro espécies mais abundantes com
maior número de amostras positivas e negativas para produção de
anticorpos nos municípios de Bragança, Augusto Corrêa e Viseu, no
Estado do Pará.....................................................................................
32
x
LISTA DE FIGURAS
Figura 1:
Mapa ilustrando os municípios e suas respectivas localidades-alvo
na mesorregião Nordeste do Pará........................................................
Figura 2:
13
Abundância relativa das subfamílias de Phyllostomidae capturadas
nos municípios de Bragança, Augusto Corrêa e Viseu........................ 21
Figura 3:
Abundância relativa das guildas de morcegos capturadas nos
municípios de Bragança, Augusto Corrêa e Viseu..............................
Figura 4:
23
Percentual de indivíduos por categoria reprodutiva nos períodos
seco e chuvoso. MSDR (machos sem descida testicular), MDT
(machos com descida testicular), FNR (fêmeas não reprodutivas).....
Figura 5:
25
Comparação entre os valores absolutos de espécimes de morcegos
registrados para os períodos seco e chuvoso nos municípios
inventariados, de forma separada e combinada, no Estado do Pará....
Figura 6:
26
Comparação entre os valores absolutos das espécies de morcegos
registradas nos períodos seco e chuvoso nos municípios
inventariados, de forma separada e combinada no Estado do Pará.....
Figura 7:
27
Comparação dos valores percentuais de morcegos soropositivos e
soronegativos para a produção de anticorpos capturados em
Bragança, Augusto Corrêa e Viseu, entre os três municípios
combinados no Estado do Pará............................................................
Figura 8:
Comparação
entre
os
valores
percentuais
de
indivíduos
soropositivos e soronegativos nos períodos seco e chuvoso nos
municípios inventariados de forma separada e combinada no Estado
29
xi
do Pará.................................................................................................
Figura 9:
30
Comparação dos valores percentuais de espécimes de morcegos
soropositivos e soronegativos para a produção de anticorpos da
raiva nos municípios de Bragança, Augusto Corrêa e Viseu, e para
os três municípios combinados no Estado do Pará.............................. 33
Figura 10:
Comparação dos valores percentuais de indivíduos das quatro
espécies
mais
abundantes
de
morcegos
soropositivos
e
soronegativos para a produção de anticorpos da raiva nos
municípios de Bragança, Augusto Corrêa e Viseu, no Estado do
Pará......................................................................................................
33
xii
LISTA DE ABREVIATURAS
ABLV – Australian bat lyssavirus
ARAV – Aravan vírus
BHK 21 – Baby Hamster Kidney (linhagem de fibrolasto de hamster)
CCZ-SP – Centro de Controle de Zoonoses em São Paulo
CZB – Coleção de Zoologia de Bragança
DE – Densidade por espécie
DI – Densidade por indivíduo
DUVV – Duvenhage vírus
E – Equitabilidade
EBLV-1 – European bat lussavirus tipo 1
EBLV-2 – European bat lyssavirus tipo 2
FNR – Fêmeas não reprodutivas
gl – Graus de liberdade
H’ – Índice de Shannon
H.R. – Hora.rede
IBAMA – Instituto Brasileiro de Meio Ambiente e Recursos Naturais Renováveis
ICTV – Comitê Internacional de Taxonomia de Vírus
INPPAZ – Instituto Panamericano de Proteccion de Alimentos y Zoonosis
IRKV – Irkut virus
KHUV – Khujand vírus
LBV – Lagos bat vírus
ln – log neperiano
MDT – Machos com descida testicular
MOKV – Mokola virus
xiii
MSDT – Machos sem descida testicular
n – Número de indivíduos
NE – Número de espécies capturadas
NI – Número de indivíduos capturados
OPAS – Organização Panamericana de Saúde
RABV – Rabies vírus
REC – Razão espécie/capturas
RFFIT – Rapid Fluorescent Focus Inibition Test (Teste Rápido de Inidição do Foco de
Florescência
SHIBV – Shimoni bat virus
SNC – Sistema Nervoso Central
UI/mL – Unidades Internacionais por mililitro
VAg 2 – Variante dois do vírus da raiva
VAg 3 – Variante três do vírus da raiva
VAg 4 – Variante quatro do vírus da raiva
VAg 5 – Variante cinco do vírus da raiva
VAg 6 – Variante seis do vírus da raiva
WHO – World Health Organization
WCBV – West Caicasian bat virus
χ2 – Teste do Qui-quadrado
xiv
SUMÁRIO
1. INTRODUÇÃO ........................................................................................................... 1
1.1. A BIOLOGIA E ECOLOGIA DOS MORCEGOS................................................1
1.2. A RAIVA................................................................................................................3
1.3. A PRODUÇÃO DE ANTICORPOS NEUTRALIZANTES CONTRA O VÍRUS
DA RAIVA....................................................................................................................7
1.4. A RAIVA NO ESTADO DO PARÁ......................................................................9
2. OBJETIVOS..............................................................................................................11
2.1. OBJETIVO GERAL.............................................................................................11
2.2. OBJETIVOS ESPECÍFICOS...............................................................................11
3. METODOLOGIA...................................................................................................... 12
3.1. ÁREA DE ESTUDO ..........................................................................................12
3.2. CAPTURA DE MORCEGOS..............................................................................14
3.3. IDENTIFICAÇÃO DOS ESPÉCIMES................................................................14
3.4. DETERMINAÇÃO DO ESTADO REPRODUTIVO.........................................15
3.5. DENSIDADE, DIVERSIDADE E ESFORÇO DE CAPTURA..........................15
3.6. COLETA DE SANGUE.......................................................................................16
3.7. TÉCNICA DE SORONEUTRALIZAÇÃO EM CULTIVO CELULAR............16
3.8. ANÁLISE DE DADOS........................................................................................18
3.8.1. DENSIDADE E DIVERSIDADE E SIMILARIDADE................................18
3.8.2.RAZÃO
SEXUAL,
CLASSES
DE
IDADE
E
VARIAÇÃO
ESTACIONAL........................................................................................................18
3.8.3. SOROLOGIA................................................................................................19
4. RESULTADOS .......................................................................................................... 20
4.1. ESFORÇO DE CAPTURA, ABUNDÂNCIA E DIVERSIDADE......................20
xv
4.2. RAZÃO SEXUAL E PROPORÇÃO ENTRE CLASSES ETÁRIAS.................23
4.3. CATEGORIAS REPRODUTIVAS E SUA VARIAÇÃO ESTACIONAL.........24
4.4. VARIAÇÃO ESTACIONAL ENTRE OS MUNICÍPIOS...................................25
4.5. PREVALÊNCIA SOROLÓGICA........................................................................27
5. DISCUSSÃO ........................................................................................................... ...34
5.1. COMPOSIÇÃO DA QUIROPTEROFAUNA.....................................................34
5.2. PREVALÊNCIA SOROLÓGICA........................................................................37
6. REFERÊNCIAS BIBLIOGRÁFICAS ..................................................................40
1
1. INTRODUÇÃO
1.1. A BIOLOGIA E ECOLOGIA DOS MORCEGOS
Os morcegos são os únicos mamíferos com capacidade real de vôo devido à
transformação de suas mãos em asas. Pertencem à ordem Chiroptera, palavra derivada
do grego cheir (=mão) e pteron (=asa) (REIS et al., 2007). Estão entre os mamíferos de
maior distribuição geográfica ao redor do mundo, sendo superados apenas pelos
roedores (Mammalia, Rodentia) em se tratando de diversidade ecológica (HILL &
SMITH, 1984) e de acordo com Huston et al. (2001), representam um quarto das
espécies de mamíferos atualmente conhecidos.
As espécies de morcegos registradas encontram-se distribuídas em duas
subordens: Megachiroptera, com apenas uma família (Pteropodidae) restrita ao Velho
Mundo e Microchiroptera com 16 famílias de distribuição mundial (SIMMONS et al.,
2005). No total são conhecidas 17 famílias, 202 gêneros e 1120 espécies distribuídas
pelo mundo (SIMMONS, 2005), sendo que nove famílias, 64 gêneros e 167 espécies
são registradas para o Brasil (REIS et al., 2007). Contudo, de acordo com Tavares et al.
(2008), a diversidade real dos morcegos do Brasil é indeterminada, porque as grandes
áreas permanecem sem amostragem e os inventários sistemáticos ainda são
incompletos.
Apesar de ser o segundo grupo de mamífero em diversidade de espécies no
país, perfazendo quase um terço das espécies terrestres (REIS et al., 2007), os morcegos
ainda são biológica e ecologicamente pouco conhecidos, mesmo aquelas espécies
consideradas comuns (MIRETZKI, 2003).
Sabe-se que mundialmente esse grupo de mamíferos ocupa os mais diversos
biomas em todos os continentes, com exceção de regiões muito frias como os pólos ou
regiões muito elevadas, além de algumas ilhas no oceano Pacífico (FINDLEY, 1988).
2
Sua ampla distribuição geográfica foi bastante favorecida pela sua capacidade
de vôo, sendo esta, inevitavelmente, associada à grande diversidade de hábitos
alimentares, que os permitiu o uso de uma gama de recursos. Dessa maneira, a Ordem
Chiroptera destaca-se pela presença em praticamente todos os grupos tróficos, com
exceção dos saprófagos, podendo ingerir desde partes florais, pólen, néctar, frutos,
pequenos vertebrados como anfíbios, répteis, peixes, mamíferos e até invertebrados e
sangue (PERACCHI et al., 2006).
Devido à grande variedade de hábitos alimentares os morcegos influenciam
diretamente na formação da estrutura da vegetação e manutenção dos ecossistemas,
onde possuem um importante papel ecológico, especificamente em florestas das regiões
tropicais e subtropicais (WHITTAKER & JONES, 1994; WALKER, 2001).
De fato, a presença maciça dos quirópteros nos diversos ecossistemas ao redor
do mundo ressalta a relevância desses animais na manutenção dos ambientes. Morcegos
frugívoros, por exemplo, dão suporte à dispersão de sementes e recolonização de
espécies nativas em áreas degradadas (LANGONI et al., 2008) e ainda são potenciais
indicadores de perturbação ambiental, especialmente os filostomídeos (MEDELLIN et
al., 2000).
Sabe-se que os insetívoros são responsáveis, em grande parte, pelo controle da
população de insetos, abrangendo inclusive os sistemas agrícolas e orgânicos (ZAHAN
et al., 2005). Muitas espécies de nectarívoros são responsáveis pela polinização de uma
enorme variedade de plantas (VONHF et al., 2004, THIELE & WINTER, 2005). Não
menos importantes são as espécies carnívoras, as quais participam no controle
populacional de pequenos vertebrados, alimentando-se de peixes, rãs, camundongos,
aves, e até de outros morcegos, podendo ainda complementar sua dieta consumindo,
eventualmente, insetos e frutos (BORDINONG, 2005).
3
Os morcegos hematófagos, por sua vez, estão restritos a América Latina e
compreendem apenas três espécies: Desmodus rotundus (E. Geoffroy, 1810), Diaemus
youngi (Jentink, 1893) e Diphylla ecaudata Spix, 1823, explorando basicamente o
sangue de vertebrados endotérmicos como aves e mamíferos (REIS et al., 2007). Sabese que nos ecossistemas naturais, os morcegos hematófagos auxiliam no controle das
populações de vertebrados herbívoros, evitando que surperpopulações dessas presas
destruam a vegetação e, consequentemente, o ecossistema, sendo que esse controle
populacional é feito não somente por sangrias dos animais, mas também por
transmissão de doenças letais (BREDT et al., 1998).
É importante salientar que muitas espécies de morcegos estão associadas à
incidência e/ou distribuição geográfica de determinadas epidemiologias causadas por
agentes patogênicos, tais como: bactérias, fungos e vírus (GREENHALL et al., 1983;
HILL & SMITH, 1984; CALISHER et al., 2006). Algumas dessas patologias, as quais
teriam uma importância específica no controle populacional de outros grupos da fauna
silvestre, como citado anteriormente, incluíram os humanos como hospedeiros no seu
ciclo. Algumas espécies de morcegos, principalmente, os de hábito alimentar
sanguívoro, passaram a ser considerados os principais transmissores de doenças
humanas graves como, por exemplo, a Raiva, uma zoonose bastante conhecida não só
por acometer determinadas espécies de animais silvestres e domésticos, mas também o
homem.
1.2. A RAIVA
A Raiva é uma das doenças mais antigas conhecidas pelo homem e, ainda nos
dias atuais, representa um sério problema de saúde pública além de um empecilho ao
desenvolvimento pecuário (INPPAZ, 1996). Trata-se de uma antropozoonose que atinge
o sistema nervoso central (SNC) causando um quadro de encefalomielite infecciosa
4
aguda e, na maioria dos casos, fatal, cujo agente etiológico pertence à ordem
Mononegavirales, família Rhabdoviridae e gênero Lyssavirus (ICTV, 2005).
Este gênero possui sete principais genótipos caracterizados (BOURHY et al.,
1993; GOULD et al., 1998), sendo que outros quatro estão em processo de
classificação. Entre os sete genótipos estão: Rabies virus ou vírus clássico da raiva
(RABV/genótipo 1); Lagos bat vírus (LBV/genótipo 2); Mokola virus (MOKV/genótipo
3); Duvenhage virus (DUVV/genótipo 4); European bat lyssavirus tipo 1 (EBLV1/genótipo 5); European bat lyssavirus tipo 2 (EBLV-2/genótipo 6); e Australian bat
lyssavirus (ABLV/genótipo 7).
O genótipo 1 (RABV) trata-se do mais importante genótipo, por apresentar
distribuição mundial infectando mamíferos terrestres, morcegos hematófagos e não
hematófagos das Américas; o genótipo 2 (LBV) é um vírus isolado de morcegos
frugívoros da região de Lagos, na Nigéria; o MOKV (genótipo 3) foi isolado de
humanos, também na Nigéria, e de felinos no Zimbabwe e na Etiópia; o DUVV
(genótipo 4) inclui os vírus isolados de morcegos insetívoros e de humanos na África do
Sul (KOTAIT & CARRIERE, 2005). Os genótipos 5 (EBLV-1) e 6 (EBLV-2) ocorrem
na Europa, e o 7 (ABLV) é encontrado na Austrália. Até o momento, apenas o genótipo
3 não foi isolado de quirópteros (TORDO et al., 2000; WHO, 2005).
Alem desses sete genótipos, a partir de 2003 outros quatro foram isolados de
morcegos insetívoros, no centro e sudeste da Ásia, são eles: Aravan virus (ARAV)
(ARAI et al., 2003); Khujand virus (KHUV) (KUZMIN et al., 2003); Irkut virus
(IRKV) e West Caucasian bat virus (WCBV) (BOTVINKIN et al., 2003). Mais
recentemente, foi submetido à apreciação o 12° genótipo, denominado Shimoni bat virus
(SHIBV), encontrado em morcegos insetívoros na África Oriental (KUZMIN et al.,
2010).
5
Badrane et al. (2001) dividiram os genótipos a partir das diferenças na sequência
da glicoproteína e de suas propriedades biológicas, como patogenicidade e
imunogenicidade, em dois filogrupos: genótipos 1, 4, 5, 6 e 7, integrantes do filogrupo
I, e genótipos 2 e 3, do filogrupo II. O Comitê Internacional de Taxonomia de Vírus
(ICTV) ratificou os genótipos propostos, classificando o ARAV, KHUV e IRKV como
integrantes do filogrupo I; o WCBV não apresentou afinidade com nenhum dos dois
filogrupos até agora conhecidos (ICTV, 2009), contudo o 12° genótipo proposto
(SHIBV), pelas evidências trata-se de um terceiro membro do filogrupo II (KUZMIN et
al., 2010).
Dentro de um mesmo genótipo, as diferenças genéticas e antigênicas classificam
o RABV em variantes que podem ser mantidas em uma ou mais espécies atuando como
reservatório regional (SCHNEIDER et al., 1973; RUPPRECHT et al., 2002). Texeira et
al. (2005) apontam para o fato de que a existência de muitas variantes parece ser uma
iniciativa de adaptação do vírus às diferentes espécies hospedeiras, incluindo morcegos
hematófagos e não-hematófagos.
No Brasil foram identificadas seis variantes antigênicas compatíveis com perfis
preestabelecidos para estudos de amostras isoladas nas Américas: variantes 2 (cão –
VAg 2), 3 (Desmodus rotundus – VAg 3), 4 (Tadarida brasiliensis – VAg 4), 5 (D.
rotundus da Venezuela – VAg 5), 6 (Lasiurus cinereus – Vag 6) e “Lab” (reagente a
todos os anticorpos utilizados) (FAVORETTO et al., 2002).
O RABV é mantido em quatro ciclos: i) urbano - incluindo os animais
domésticos; ii) silvestre terrestre – envolvendo os vertebrados terrestres; iii) silvestre
aéreo – que inclui os morcegos; iv) rural – relacionado aos herbívoros de criação
(BRASIL, 2004). De acordo com a OPAS (2007), a Raiva urbana, caracterizada pela
presença do vírus em animais domésticos de estimação (cães e gatos), é ocasionada,
geralmente, pela VAg 2 encontrada apenas nestas espécies. Contudo a VAg 3 apresenta
6
maior importância epidemiológica, haja vista ser encontrada em todos os mamíferos
domésticos e no homem.
Apesar desses ciclos tornarem-se importantes problemas econômicos e de saúde
pública na América Latina, a Raiva em ambientes urbanos tem sido controlada através
da vacinação de animais de estimação, gerando bons resultados na redução do número
de casos em humanos e não-humanos em certos países latino-americanos. Por outro
lado, a Raiva em animais silvestres ainda é um problema emergente. Mesmo com a
vacinação do gado, ainda existem certas desvantagens em função dos bovinos serem
fontes fartas de alimento e de fácil acesso para os morcegos vampiros (SCHINEIDER et
al., 2009), mantendo a epizootiologia da Raiva nas populações desses morcegos
(FORNES et al., 1974), assim, para Souza et al. (2005) a forma mais eficaz de mitigar a
Raiva rural ainda é o controle dos morcegos vampiros.
Mayen (2003) menciona que o controle das populações de morcegos não
diferencia áreas de grandes criações pecuaristas daquelas de subsistência. Como
conseqüência, as campanhas de controle resultariam na morte indiscriminada de muitos
morcegos de outras espécies, as quais são de extrema relevância para o balanço
ecológico das florestas nativas e para a diversidade desse grupo de mamíferos.
Contudo, é importante enfatizar que diversas espécies de morcegos apresentam
hábito colonial formando grandes grupos em locais como cavernas, edificações ou
ambientes similares. Neste caso, a facilidade da transmissão intra e interespecífica do
vírus nas colônias deve ser considerada. Por outro lado, deve-se também observar que i)
a falta de registros de surtos periódicos de Raiva entre as colônias e ii) a incidência
relativamente baixa de ocorrência natural da doença são notórias (BRASS, 1994).
Na região Neotropical, a esta doença está intimamente associada à guilda de
morcegos hematófagos, sendo D. rotundus a única diretamente envolvida no ciclo da
Raiva em herbívoros, e o mais comum morcego vampiro das Américas (UIEDA et al.,
7
1998). Devido à expansão da doença, a espécie tem interferido em seu ciclo aéreo, o que
faz com que casos de Raiva também em morcegos não-hematófagos venham se
tornando mais comuns (LANGONI et al., 2008).
Constantine (1988) relata que nos registros de espécies não-hematófagas
contaminadas estariam incluídas seis das nove famílias de morcegos que habitam as
Américas:
Emballonuridae,
Noctilionidae,
Mormoopidae,
Phyllostomidae,
Vespertilionidae e Molossidae. O mesmo autor afirma que a família Vespertilionidae já
apresentou diagnóstico confirmado também na Europa. Para a África e Ásia, apenas a
família Pteropodidae teria destaque na transmissão da Raiva.
De acordo com Sodré et al. (2010), no Brasil um número significativo de
espécies de morcegos pertencentes às famílias Phyllostomidae, Vespertilionidae e
Molossidae já foi diagnosticado como positivo para a Raiva entre os anos de 1996 a
2009, sendo o índice de positividade mais elevado para as espécies pertencentes às duas
últimas famílias. Contudo, o contato entre um morcego não-hematófago contaminado
com o RABV com um hospedeiro potencial de outra ordem é ocasional. Além do mais,
segundo Constantine (1988), quando mordidas são empreendidas pelos morcegos, estas
seriam apenas do tipo “defensivas”.
1.3. A PRODUÇÃO DE ANTICORPOS NEUTRALIZANTES CONTRA O VÍRUS DA
RAIVA
A explicação para a aparente ausência da doença generalizada nas colônias de
morcegos pode ser devido ao desenvolvimento de anticorpos neutralizantes no soro
após a exposição não letal ao vírus. Porém, não se sabe exatamente se estes morcegos
clinicamente normais, os quais apresentam anticorpos, estão: i) incubando o vírus e
podem eventualmente sucumbir aos seus efeitos ou ii) recuperando-se de uma infecção
passada e são possivelmente imunes (STEECE & ALTENBACH, 1989).
8
Já foram detectados, em quantidades variadas, anticorpos neutralizantes do vírus
produzido naturalmente por morcegos hematófagos e diversos indivíduos de espécies
não-hematófagas, considerados clinicamente normais (BRASS, 1994). No entanto,
segundo Campbell & Charlton (1988), alguns indivíduos podem apresentar infecção
subclínica, onde o RABV passa a multiplicar-se no tecido adiposo sem afetar o SNC,
tornando esses indivíduos eficientes reservatórios. Esses mesmos autores, afirmam que
o RABV pode permanecer por meses ou anos no corpo desses indivíduos infectados e
ser eliminado através de secreções respiratórias e saliva, ainda com capacidade de
virulência para disseminar a doença entre humanos e outras espécies de mamíferos.
A disseminação intra e interespecífica pode causar a forma aguda da doença em
alguns indivíduos, enquanto que em outros a infecção abortiva resulta na soroconversão,
ou seja, produção de anticorpos no soro do animal com imunidade bem estabelecida
(LANGONI et al., 2008). Para Constantine (1988), a Raiva pode manifestar-se
predominantemente em morcegos imunodeficientes, indivíduos incapazes de estabelecer
uma imunidade efetiva a um antígeno, enquanto que em imunocompetentes, indivíduos
com imunidade eficiente contra um antígeno, sua manifestação é rara devido à relação
equilibrada estabelecida entre o vírus, normalmente fatal, e seu hospedeiro. Alguns
morcegos, expostos ao vírus, nunca apresentam evidências clínicas da doença, ao passo
que outros podem sobreviver após uma recuperação (BAER & BALES, 1967;
CONSTANTINE, 1967). Eles parecem sobreviver à exposição, desde que apresentem
um alto nível de anticorpos neutralizantes em seu soro e não apresentem vírus em seus
tecidos (CONSTANTINE, 1967). No entanto, nada se sabe sobre as dosagens ou níveis
médios de anticorpos determinantes de indivíduos imunocompetentes entre as
populações de morcegos.
Testes sorológicos permitem avaliar a situação epidemiológica, sendo a
soropositividade em uma colônia o reflexo da sua exposição ao vírus, enquanto que a
9
alta prevalência associada a altos títulos de anticorpos indica os surtos recentes
(CUBAS et al., 2007).
De acordo com Smith et al. (1973), independente da resposta imunológica ser ou
não efetiva, o uso de métodos sorológicos determinantes da presença ou ausência de
anticorpos neutralizantes para o RABV pode revelar o contato do vetor com o agente
etiológico. No caso dos morcegos, tal estudo pode, no mínimo, indicar dentre os
hematófagos e não-hematófagos quais os vetores de maior interesse para o controle em
um determinado local durante o monitoramento pela vigilância sanitária. Isto evita, a
formação de focos, o consequente aparecimento de surtos e a morte generalizada de
espécies ecologicamente importantes. Portanto, a titulação de anticorpos torna-se
importante na prevenção, controle e vigilância das áreas de risco para o ciclo da Raiva
na zona rural.
1.4. A RAIVA NO ESTADO DO PARÁ
No ano de 2005 um grande número de surtos de Raiva foi registrado na
Amazônia brasileira. Nesse ano, em particular, a quantidade de casos no Brasil foi
bastante representativa diante dos anos anteriores, principalmente na região norte
(SCHINEIDER et al., 2009). Dos 64 casos de Raiva humana transmitida por morcegos
hematófagos, 62 são relatados em surtos nos Estados do Pará e Maranhão (CASTILHO
et al. 2010). Mas, de acordo com a Secretaria de Vigilância Sanitária do Ministério da
Saúde (2004), as notificações de óbitos tiveram início no Pará no ano de 2004, com dois
focos de raiva humana transmitida por morcegos hematófagos nos municípios de Portel
(15 casos) e Viseu (6 casos).
No ano seguinte foram diagnosticados mais 41 casos, sendo 17 no Pará (dois no
município de Viseu e 15 no município de Augusto Corrêa) e 24 no Maranhão (três no
município de Godofredo Viana, dois em Candido Mendes, dois em Carutapera e 17 em
10
Turiaçu) (MINISTÉRIO DA SAÚDE 2004). Assim, na Amazônia brasileira, a partir de
2004, houve uma importante mudança do perfil epidemiológico da raiva no Brasil e na
América Latina, particularmente, na região amazônica. Nesse período o morcego
hematófago ou vampiro comum (D. rotundus) passa a ser considerado como o principal
responsável pelos casos de Raiva humana.
Os registros de Raiva em humanos e em herbívoros ruminantes descritos para o
Pará referem-se a um dos mais sérios casos de surto de Raiva em humanos no Brasil.
Este episódio foi considerado o maior em um período tão curto pelo Ministério da
Saúde (2004) e, provavelmente, os casos registrados refletem o relato precedente de
Mayen (2003) acerca do desequilíbrio que se estabelece gradativamente na dinâmica
natural do agente patogênico com o hospedeiro silvestre, em virtude da destruição dos
ambientes naturais.
A partir de então, a mesorregião nordeste do Pará tornou-se uma área focal para
estudos de quirópteros e Raiva em todos os campos, disciplinas e aspectos relacionados
à doença, pois tem sido o principal foco da circulação do RABV transmitido por
morcegos hematófagos no Brasil. Durante os últimos anos alguns procedimentos para o
controle das populações de morcegos foram adotados. Contudo, devido à falta de
conhecimento sobre quais espécies estão mais envolvidas na transmissão da doença, tais
procedimentos envolveram outras espécies que podem não estar agindo diretamente na
transmissão dessa zoonose.
Assim, o presente trabalho, através da técnica de titulação de anticorpos aplicada
aos morcegos capturados nas localidades de ocorrência de surto, pretende gerar
informações
sobre
o
possível
contato
desses
indivíduos
com
o
RABV,
consequentemente, determinando as espécies envolvidas na transmissão dessa doença.
Paralelamente, o inventário da quiropterofauna local torna-se relevante tanto
para a mesorregião nordeste do Pará, que é uma das mais antropizadas do Estado (IBGE
11
2006), quanto para a região amazônica brasileira como um todo, uma vez que dados
sobre a fauna de morcegos dessa parte da Amazônia ainda são escassos, sendo os únicos
registros conhecidos, os provenientes da península de Ajuruteua, no município de
Bragança (ANDRADE et al., 2008).
12
2. OBJETIVOS
2.1. OBJETIVO GERAL
Descrever a composição da fauna de morcegos e relacionar a soroprevalência de
anticorpos contra o Vírus da Raiva onde houve surtos de raiva humana na costa
nordeste do Estado do Pará em 2004 e 2005.
2.2. OBJETIVOS ESPECÍFICOS
Como objetivos específicos pretende-se:
•
Elaborar a lista das espécies de morcegos capturados nos municípios de
Bragança, Augusto Corrêa e Viseu;
•
Estimar e comparar a abundância e a diversidade dessa fauna de morcegos
entre os municípios inventariados;
•
Determinar a razão sexual e a proporção entre classes etárias dos indivíduos
de maior número de captura;
•
Diferenciar a influência da variação sazonal (período seco e chuvoso) entre
as categorias reprodutivas e entre os municípios;
•
Verificar a soroprevalência de anticorpos contra o RABV em populações de
morcegos;
•
Comparar a positividade sorológica entre as espécies de morcegos
capturados, os municípios e a variação estacional da região.
13
3. METODOLOGIA
3.1. ÁREA DE ESTUDO
A área de estudo do presente trabalho abrange municípios notificados na rota de
circulação do RABV nos anos de 2004 e 2005. A Figura 1 apresenta esta área, com os
municípios-alvo e suas respectivas localidades:
- Município de Bragança:
Localidades: Mata do Lobão, Benjamin Constant e Treme;
- Município de Augusto Corrêa:
Localidades: Vila do Araí, Vila Soares e Bacanga;
- Município de Viseu:
Localidades: Firmiana, Açaiteua e Serra do Piriá.
As coletas foram realizadas em fragmentos de matas de terra firme encontradas
nessas localidades. Tais matas encontram-se em estado de degradação e fragmentação, e
são principalmente constituídas por espécies vegetais pioneiras de sub-bosques.
O clima da região é quente e úmido por todo ano. Possui uma estação
considerada como chuvosa, que vai de janeiro a agosto, e outra considerada como seca,
que vai de setembro a dezembro (MORAIS et al., 2005). Tais estações serão retratadas
nesse trabalho como períodos chuvoso e seco.
14
Bragança
Augusto
Correa
Viseu
(00°59’S, 46°40’W)
(01°04’S, 46°22’W)
(01°04’S, 46°30’W)
(01°09’S, 46°21’W)
(01°10’S, 46°41’W)
(01°12’S, 46°17’W)
(01°16’S, 46°31’W)
(01°18’S, 46°24’W)
Malha Rodoviária
Augusto Correa
Bragança
Viseu
Local de coleta
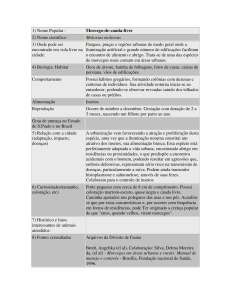
Figura 1. Mapa ilustrando os municípios e suas respectivas localidades-alvo na mesorregião Nordeste do
Estado do Pará.
15
3.2. CAPTURA DE MORCEGOS
Para a realização do inventário da quiropterofauna foram realizadas capturas
noturnas entre os meses de abril a novembro de 2009, abrangendo as duas estações,
levando em conta que a estação considerada como chuvosa, vai de janeiro a agosto, e a
considerada como seca, vai de setembro a dezembro (MORAIS et al., 2005).
Foram utilizadas 10 redes de espera (12 x 3 m), ao nível do solo, expostas por
duas noites em cada localidade, das 18:00 à 1:00 h, sendo vistoriadas em intervalos de
meia hora durante as luas minguante e nova, perfazendo um total de 18 noites por
estação (seca e chuvosa). As redes foram abertas em áreas de floresta de terra firme,
algumas transversalmente e outras de forma paralela em trilhas pré-existentes, corpos
d’água e campo aberto, visando amostrar uma maior variedade de microhábitats.
3.3. IDENTIFICAÇÃO DOS ESPÉCIMES
Os indivíduos capturados foram mantidos individualmente em sacolas de pano
para a obtenção das seguintes medidas morfométricas: comprimentos do antebraço,
folha nasal, orelha e trago. Essas medidas foram utilizadas para auxiliar na identificação
das espécies capturadas as quais foram baseadas nas chaves de identificação de Handley
(1987), Linares (1987), Marques-Aguiar (1994) e Eisenberg & Redford (1999).
Espécimes com identificação duvidosa foram fixados em solução de formol
(10%), sendo, posteriormente, conservados em etanol (70%) e devidamente etiquetados.
Tal procedimento também foi aplicado aos exemplares capturados que não resistiram ao
manuseio em campo, os quais também foram destinados à formação de uma coleção de
referência do presente estudo. O material-testemunho foi depositado na Coleção de
Zoologia do Campus de Bragança (CZB), Bragança-PA. A coleta e o transporte dos
morcegos foram autorizados segundo a determinação da Licença de Coleta/Transporte
16
No.16839-1 emitida pelo Instituto Brasileiro do Meio Ambiente e Recursos Naturais
Renováveis (IBAMA).
3.4. DETERMINAÇÃO DO ESTADO REPRODUTIVO
São considerados machos ativos sexualmente aqueles exemplares com testículos
na bolsa escrotal, também denominados como “machos com descida testicular” (MDT),
ou ainda “machos com testículo escrotado”; os inativos são aqueles com os testículos na
cavidade abdominal, também chamados “machos sem descida testicular” (MSDT), ou
“machos com testículo abdominal”.
A gravidez das fêmeas foi determinada pela palpação de seu abdômen, para
detectar a presença de feto. Fêmeas lactantes foram reconhecidas por apresentarem as
mamas intumescidas e sem pelos e com presença de leite, que pode ser observada
comprimindo o mamilo com uma pinça. Algumas fêmeas foram consideradas póslactantes em função da ausência de pelos e leite. As fêmeas sem evidência de
características reprodutivas foram consideradas como “fêmeas não reprodutivas”
(FNR).
3.5. DENSIDADE, DIVERSIDADE E ESFORÇO DE CAPTURA
As dimensões das redes de espera foram importantes para o cálculo do esforço
de captura em rede/hora, sendo que uma rede/hora corresponde a cada 12 m de rede
aberta por hora. Para a avaliação do esforço de captura da quiropterofauna foi calculada
a Densidade por Indivíduos (DI), Densidade por Espécie (DE) e a Razão
Espécies/Capturas (REC) (BERNARD & FENTON 2002), calculados pelas seguintes
formulas:
DI = N° total de indivíduos / hora.rede
(Equação 1)
DE = N° total de espécies / hora.rede
(Equação 2)
17
REC = N° total de espécies / N° total de capturas
(Equação 3)
Para estimar a diversidade de espécie foi utilizado o índice de Shannon (H’)
acompanhado pela Equitabilidade (E) (MAGURRAN, 1988).
O H’ é representado pela seguinte fórmula:
H’ = - Σ (ni / N) ln (ni / N)
(Equação 4)
Onde:
ni = no total de indivíduos da espécie i;
N = no total de indivíduos na amostra;
ni/N = pi abundância proporcional de cada espécie na amostra total.
Enquanto o valor de Equitabilidade pode ser obtido através do seguinte cálculo:
E= H’ / ln S
(Equação 5)
Onde:
S = no total de espécies na amostra;
H’ = valor obtido do índice de Shannon.
3.6. COLETA DE SANGUE
De cada morcego capturado foram obtidas amostras de sangue com cerca de 3
mL, as quais foram, posteriormente, individualizadas em tubos Eppendorf, contendo
anticoagulante (Heparina Sódica). Nos espécimes que compuseram o materialtestemunho, as amostras de sangue foram obtidas por punção cardíaca, enquanto que
nos indivíduos liberados este processo foi realizado por punção venosa. Todas as
amostras foram conservadas a uma temperatura de 15°C.
18
Em laboratório, as amostras foram centrifugadas a 4.000 rpm por cinco minutos.
Após este procedimento, aproximadamente 0,2 mL do plasma sobrenadante foi retirado
e colocado em frascos esterilizados e identificados com códigos individualizados e,
então, resfriados em temperaturas entre 2 e 8°C. As amostras, devidamente
acondicionadas e identificadas, foram enviadas ao Laboratório de Zoonoses e Doenças
Transmitidas por Vetores no Centro de Controle de Zoonoses (CCZ-SP) em São PauloSP, sob responsabilidade da Dra. Luzia de Fátima Alves Martorelle e Ana Paula
Cataoka, onde foram realizadas as análises de titulação de anticorpos estimulados
devido ao contato do hospedeiro com o RABV.
3.7. TÉCNICA DE SORONEUTRALIZAÇÃO EM CULTIVO CELULAR
O nível de anticorpos neutralizantes contra o RABV testado através do Teste
Rápido de Inibição de Foco de Fluorescência (RFFIT - Rapid Fluorescent Focus
Inibition Test), uma técnica desenvolvida por Smith et al. (1973), que se trata da
soroneutralização em cultura celular para determinação de anticorpos neutralizantes
contra RABV. Segundo esses autores, para iniciar o procedimento deve-se determinar a
linhagem celular a ser usada. A linhagem de fibroblasto de hamster (BHK 21 - Baby
Hamster Kidney) e a mais utilizada, mas independente do tipo de célula usada, existem
fatores que apresentam profundo efeito na realização dessa técnica, entre eles o pH do
meio de cultura, a presença ou ausência de fatores de crescimento, o nível de CO2, entre
outros.
Na primeira etapa da técnica ocorre a replicação do RABV em linhagem celular
BHK 21. Devem ser usadas células que estejam em fase logarítmica de crescimento (24
horas), o vírus liofilizado deve ser de procedência conhecida e com título >105.0, esse
título em condições adequadas será elevado e mantido a cada lote produzido.
19
Apenas na segunda etapa ocorre a titulação de RABV em linhagem celular BHK
21, onde deve ser feita a diluição seriada dos soros. Cada laboratório determina qual a
menor e qual a maior diluição que irá utilizar no teste, desde que frente aos padrões a
técnica tenha reprodutibilidade. No caso do Laboratório de Zoonoses e Doenças
Transmitidas por Vetores no CCZ-SP, inicia-se com uma diluição 1:5, tendo um limite
de detecção de 0,16 Unidades Internacionais/mililitro (UI/mL).
Seguido à diluição, ocorre a leitura e o cálculo dos resultados, onde para cada
orifício registra-se o resultado positivo para o campo que apresentar um ou mais focos
de fluorescência e negativo para os que não apresentarem nenhum foco. Os títulos são
calculados pelo método matemático estimativo de Spearman-Kärber ou por interpolação
matemática entre o soro teste e o soro padrão de unidades internacionais conhecidas.
No presente trabalho foram considerados soropositivos indivíduos com títulos ≥
0,16 UI/mL, pois, partindo da diluição 1:5, apresentam evidência da produção de
anticorpos contra o RABV. Indivíduos com resultado < 0,16 UI/mL foram considerados
soronegativos.
3.8. ANÁLISE DE DADOS
3.8.1. DENSIDADE E DIVERSIDADE E SIMILARIDADE
A variação na densidade entre os municípios inventariados foi testada através da
análise de similaridade ANOSIM do pacote estatístico Primer v5 (CLARKE &
GORLEY, 2001). Esse teste multivariado foi realizado a partir de uma matriz de
similaridade, com base na abundância dos táxons de cada amostra, gerada com esses
dados transformados pela raiz quadrada, utilizando-se o coeficiente de Bray-Curtis
(CLARKE & GORLEY, 2001).
20
Para comparar os valores dos índices de diversidade entre os municípios foi
realizada a análise de variância de Kruskal Wallis através do programa BioEstat 5.0
(AYRES et al., 2007).
3.8.2. RAZÃO SEXUAL, CLASSES DE IDADE E VARIAÇÃO ESTACIONAL
Para as espécies representadas com maior quantidade de indivíduos capturados
foram avaliados os desvios i) da razão sexual 1:1 e ii) da proporção entre classes etárias
(adultos e jovens) com uso do teste de Qui-quadrado (χ2) para proporções esperadas
iguais.
No intuito de avaliar a relação entre a variação estacional e o número de
indivíduos capturados de cada categoria reprodutiva foi também realizado um teste de
Qui-quadrado (χ2) tanto para fêmeas lactantes, pós-lactantes, grávidas e FNR; os valores
para MDT e MSDT foram somados e testados juntos também através do χ2. Para
verificar a relação entre a variação estacional e os municípios, baseado no número de
indivíduos e espécies, foi utilizado o χ2 de Partição.
Para realização dos χ2 utilizados nessas análises foi utilizado o pacote estatístico
BioEstat 5.0 (AYRES et al., 2007).
3.8.3. SOROLOGIA
Um teste de Qui-quadrado (χ2) de Partição foi realizado para comparar o
número de indivíduos soropositivos e soronegativos entre os municípios visitados, tanto
para os indivíduos de todas as espécies quanto para as quatro espécies com maior
número de amostras sorológicas. O mesmo teste foi utilizado para verificar a diferença
entre o número de soropositivos entre cada uma das quatro espécies, bem como para
avaliar a diferença entre o número de soronegativos e soropositivos, considerando a
razão sexual, a faixa etária e a variação estacional. Todas as análises referentes a esta
21
seção (3.8.3. Sorologia) foram realizadas no pacote estatístico BioEstat 5.0 (AYRES et
al., 2007).
22
4. RESULTADOS
4.1. ESFORÇO DE CAPTURA, ABUNDÂNCIA E DIVERSIDADE
O presente estudo realizou um esforço amostral de 2.520 hora.rede (H.R.),
perfazendo 840 H.R. por município. Este esforço resultou na coleta de 949 indivíduos,
com uma taxa de captura de 0,38 ind/hora.rede, destacando-se o município de Bragança
com o valor de 0,48 ind/hora.rede, através do cálculo para DI (Tabela 1).
Tabela 1. Proporções de capturas realizadas com redes de espera nos municípios
de Bragança, Augusto Corrêa e Viseu - Pará.
MUNICÍPIO
H.R.
NI
NE
DI
DE
REC
Bragança
840
406
27
0,48
0,03
0,07
Augusto Corrêa
840
218
24
0,26
0,03
0,11
Viseu
840
325
19
0,39
0,02
0,06
GERAL
2.520
949
36
0,38
0,01
0,04
A análise comparativa entre os três municípios mostrou uma diferença
significativa no número de morcegos capturados (ANOSIM, R=0,31; p<0,05), isso pode
ser notado visualizando os valores de NI da Tabela 1, onde o município de Bragança se
destaca com 406 indivíduos. O mesmo município também apresenta maior número de
espécies (NE), seguido por Augusto Corrêa e Viseu (Tabela 1).
O H’ estimado para a área de estudo foi de 2,1, enquanto que os valores para os
municípios de Bragança, Augusto Corrêa e Viseu foram bastante similares (Tabela 2). A
análise comparativa dos valores de diversidade não mostrou diferença significativa entre
os municípios estudados (Kruskal Wallis, H=1,40; gl=2; p>0,05).
23
Tabela 2. Índice de Shannon (H’),
), Equitabilidade (E) e o número de espécies (NE)
estimados para a área de trabalho e para os municípios de Bragança, Augusto Corrêa e
Viseu, no Estado do Pará.
Índices
Bragança
Augusto Corrêa
Viseu
Geral
NE
27
24
19
36
H’
1,9
2,1
1,9
2,1
E
0,6
0,7
0,6
0,5
Os 949 indivíduos capturados distribuem-se
distribuem se em 36 espécies e quatro famílias
(Tabela 3). A família Phyllostomidae,
Phyllostomidae, como esperado, apresentou maior percentual de
capturas (98%), os outros 2% foram representados pelas famílias Vespertilionidae,
Emballorunidae e Thyropteridae, sendo que esta última família contou
contou com apenas um
representante: Thyroptera tricolor.
tricolor
Os filostomídeos
ostomídeos capturados pertencem a cinco subfamílias (Figura 2),
2 sendo
Carolliinae a que se destacou com 44% (n=407) de abundância. Esta subfamília foi
representada quase que exclusivamente pela espécie Carollia perspicillata,
perspicillata cujo
percentual (93%; n=307) dominou
ominou essa subfamília, bem como alcançou o maior número
de indivíduos registrados de todas as espécies (40%; n=377) (Tabela 3).
.
Figura 2.. Abundância relativa das subfamílias de Phyllostomidae capturadas nos
municípios de Bragança, Augusto Corrêa e Viseu,
Viseu, no Estado do Pará.
24
Tabela 3. Morcegos capturados nos municípios de Bragança (B), Augusto Corrêa (AG) e Viseu (V), Nordeste do Pará. Guildas: Frugívora (F), Insetívora (I),
Nectarívora (N), Sanguívora (S).
Família
Phyllostomidae
Subfamília
Stenodermatinae
Phyllostominae
Glossophaginae
Carolliinae
Vespertilionidae
Desmodontinae
Vespertilioninae
Myotinae
Emballorunidae
Thyropteridae
Total
7
Espécie
Dermanura cinerea (Gervais, 1856)
Artibeus concolor Peters, 1865
Artibeus gnomus Handley, 1987
Artibeus lituratus (Olfers, 1818)
Artibeus obscurus (Schinz, 1821)
Artibeus planirostris Spix, 1823
Platyrrhinus brachycephalus ( Rouk & Carter, 1972)
Platyrrhinus incarum (Thomas, 1912)
Sturnira lilium (E. Geoffroy, 1810)
Uroderma bilobatum Peters, 1866
Uroderma magnirostrum Davis, 1968
Vampyriscus bidens (Dobson, 1878)
Lophostoma brasiliense Peters, 1866
Lophostoma silvicolum d’Orbigny, 1836
Micronycteris megalotis (Gray, 1842)
Mimon crenulatum (E. Geoffroy, 1803)
Phyllostomus discolor Wagner, 1843
Phyllostomus hastatus (Pallas, 1767)
Tonatia saurophila Koopman & William, 1951
Trinycteris nicefori (Sanborn, 1949)
Glossophaga soricina (Pallas, 1766)
Lichonycteris obscura Thomas, 1895
Lionycteris spurreli Thomas, 1913
Lonchophylla thomasi J. A. Allen, 1904
Carollia perspicillata (Linnaeus, 1758)
Rhinophylla fischerae Carter, 1966
Rhinophylla pumilio Peters, 1865
Desmodus rotundus (E. Geoffroy, 1810)
Eptesicus brasiliensis (Desmarest, 1819)
Myotis nigricans (Schinz, 1821)
Peropteryx macrotis (Wagner, 1843)
Saccopteryx bilineata (Temminck, 1838)
Saccopteryx canescens Thomas, 1901
Saccopteryx gymnura Thomas, 1901
Saccopteryx leptura (Schreber, 1774)
Thyroptera tricolor Spix, 1823
36
Guilda
F
F
F
F
F
F
F
F
F
F
F
F
I
I
I
I
F
F
I
I
N
N
N
N
F
F
F
S
I
I
I
I
I
I
I
I
4
B
44
0
3
2
7
54
0
6
2
19
0
2
1
0
0
2
0
1
3
1
6
1
1
7
208
15
5
1
0
8
2
1
2
0
2
0
406
AG
21
1
0
0
2
17
1
7
0
3
1
3
3
1
1
0
2
1
0
1
53
0
0
1
79
6
3
7
0
2
0
0
0
1
1
0
218
V
6
0
10
1
1
116
0
7
3
43
0
3
0
0
0
0
4
2
0
0
22
0
0
4
90
1
0
0
3
7
0
0
0
0
1
1
325
Total
71
1
13
3
10
187
1
20
5
65
1
8
4
1
1
2
6
4
3
2
81
1
1
12
377
22
8
8
3
17
2
1
2
1
4
1
949
25
A subfamília Desmodontinae, constituída pelos indivíduos hematófagos, foi
representada por apenas 1% (Figura
(
2),
), com os oito indivíduos capturados pertencentes
à espécie D. rotundus,, o principal transmissor
tra
da Raiva
aiva para os mamíferos.
Foram registradas quatro guildas (Figura 3),
), sendo frugívora a mais
representativa dentre os espécimes capturados (n= 802; 85%), enquanto a guilda
Sanguívora obteve abundância relativa de apenas 1%. Apesar da metodologia
metodologi utilizada
não favorecer a captura de indivíduos da guilda insetívora, esta foi representada por 14
espécies distintas, sendo M. nigricans a espécie mais abundante deste grupo (n=17;
61%),, as demais espécies dessa guilda encontram-se
encontram se listadas na Tabela 3.
3
Figura 3.. Abundância relativa das guildas de morcegos capturados nos municípios de
Bragança, Augusto Corrêa e Viseu, no Estado do Pará.
CLASSES ETÁRIAS
4.2. RAZÃO SEXUAL E PROPORÇÃO ENTRE CLASSES
Dentre as cinco espécies com mais indivíduos capturados apenas duas
apresentaram razão sexual desviada para fêmeas: C. perspicillata (2 fêmeas: 1 macho;
χ2=4,03; gl=1; p<0,05) e G. soricina (1,5 fêmeas: 1 macho; χ2=4,03; gl=1; p>0,05). D.
cinerea e U. bilobatum apresentaram razão sexual de 1:1 ((χ2=1,14; gl=1; p>0,05 e
26
χ2=0,754 gl=1; p>0,05, respectivamente), enquanto A. planirostris apresentou razão
sexual desviada para machos (2 machos: 1 fêmea; χ2=4,497; gl=1; p<0,05).
Quanto às classes etárias, as duas espécies mais abundantes apresentaram maior
proporção de indivíduos adultos: C. perspicillata (4 adultos: 1 jovem; χ2=573,95; gl=1;
p<0,001), A. planirostris (5 adultos: 1 jovem; χ2=65,88; gl=1; p<0,001); em G. soricina
a proporção de jovens é maior (2 jovens: 1 adulto; χ2=10,38; gl=1; p<0,05), ao passo
que para D. cinerea e U. bilobatum não houve desvios (1:1; χ2=1,14; gl=1; p>0,05 e
χ2=0,01; p>0,05, respectivamente).
4.3. CATEGORIAS REPRODUTIVAS E SUA VARIAÇÃO ESTACIONAL
Das 484 fêmeas de morcegos capturadas, 46 foram classificadas como póslactantes, 49 lactantes e 147 grávidas. A maioria das fêmeas (n=242) não apresentou
características reprodutivas evidentes, sendo definidas como não reprodutivas (FNR).
Dos 465 machos, 417 não apresentavam descida testicular (MSDT). Este processo
reprodutivo somente foi encontrado em 48 machos, porém a descida testicular pode ter
outras causas, que incluem o estresse gerado pela captura e manipulação do animal.
Analisando o estado reprodutivo dos indivíduos em relação à variação
estacional, nota-se que o número de FNR foi bem mais elevado durante o período seco
(Figura 4), havendo uma diferença bastante significativa entre esses valores (χ2=15,88;
gl=1; p<0,001). Ao contrário, as fêmeas pertencentes às demais categorias reprodutivas
foram mais numerosas durante o período chuvoso. A Figura 4 apresenta a diferença
entre o número de fêmeas pós-lactantes capturadas durante o período seco e chuvoso
(χ2=5,56; gl=1; p<0,05). Os valores para as fêmeas lactantes não apresentaram diferença
significativa (χ2=2,46; gl=1; p>0,05), muito embora tenham sido maiores durante o
período chuvoso, ao passo que o número de fêmeas grávidas foi superior durante esse
27
período, refletindo
do em uma diferença estatística bastante significativa ((χ2=77,88; gl=1;
p<0,001).
Considerando as categorias reprodutivas masculinas, observa-se
observa se que os MDT
foram mais numerosos durante o período seco, enquanto aqueles MSDT foram mais
frequentes durante o período
eríodo chuvoso, resultando em uma diferença significativa no que
se refere à variação estacional (χ
( 2=43,48; gl=2; p<0,001).
MSDT
MDT
FNR
Seco
Grávida
Chuvoso
Pós-lactante
lactante
Lactante
0
20
40
60
80
100
120
Percentual de indivíduos
Figura 4.. Percentual de indivíduos por categoria reprodutiva nos períodos seco
e chuvoso. MSDT (machos sem descida testicular), MDT (machos com descida
testicular), FNR (fêmeas não reprodutivas).
4.4. VARIAÇÃO ESTACIONAL
ONAL ENTRE OS MUNICÍPIOS
MUNICÍ
A maioria dos indivíduos das
da áreas de trabalho (n=556; 59%) foi capturada
durante a o período seco. Para cada município os valores variaram, porém apenas no
município de Augusto Corrêa ocorreu o inverso, 57% (n=125) dos indivíduos foram
capturados durante o período chuvoso, e a diferença entre
entre o número de espécimes foi
maior em Viseu, onde 71% (n=230) dos indivíduos foram capturados durante o período
28
seco (Figura 5).
). Essa diferença entre o número de capturas nos municípios foi bastante
significativa (χ2= 42,9102; gl=2; p< 0,001).
Os valores de riqueza para os municípios combinados foram exatamente os
mesmos em ambos os períodos do ano (n=29). Para cada município separadamente,
esses valores variaram pouco, não apresentando diferença significativa ((χ2=2,76; gl=2;
p>0,05) apesar de apenas em Viseu esse valor ter sido maior durante a estação seca
(Figura 6).
Municípios Combinados
Viseu
Chuvoso
A. Corrêa
Seco
Bragança
0
50 100 150 200 250 300 350 400 450 500 550 600
Figura 5.. Comparação entre os valores absolutos de espécimes de morcegos registrados para os períodos seco
e chuvoso nos municípios inventariados, de forma separada e combinada, no Estado
Estado do Pará.
Ao todo foram registradas 36 espécies, algumas delas foram exclusivas de um
determinado período, como por exemplo: E. brasiliensis (n=3),, L. spurreli (n=1), L.
silvicolum (n=1),, M. megalotis (n=1), P. brachycephalus (n=1),, S. leptura (n=4), T.
tricolor (n=1) ocorreram apenas durante o período seco. Por outro lado, A. concolor
(n=1), L. obscura (n=1),, P. macrotis (n=2), S. bilineata (n=1),, S. gymnura (n=1), T.
saurophila (n=3) e U. magnirostrum (n=1) foram registrados somente no período
chuvoso.
o. Embora várias espécies tenham sido registradas exclusivamente em um dado
período do ano, o número de indivíduos para cada uma dessas espécies foi baixo.
29
Municípios Combinados
Viseu
Chuvoso
A. Corrêa
Seco
Bragança
0
5
10
15
20
25
30
35
Figura 6.. Comparação entre os valores absolutos das espécies de morcegos registrados nos
períodos seco e chuvoso nos municípios inventariados, de forma separada e combinada no
Estado do Pará.
4.5. PREVALÊNCIA SOROLÓGICA
SOR
Foram analisados soros de 28 espécies diferentes, pertencentes a quatro guildas
(Tabela 4), totalizado 307 amostras de soro. Deste total,
total, 51% (n=156) foram
consideradas soronegativas para a produção de anticorpos. Entretanto, as amostras do
município de Viseu apresentaram elevado percentual de indivíduos soropositivos (n=72;
62%), enquanto que para Bragança ocorreu o inverso. O município
município de Augusto Corrêa
apresentou exatamente 50% para cada condição (Figura 7).
). Através do χ2 de Partição,
percebesse que a diferença entre esses locais, considerando a quantidade de indivíduos
soropositivos é significativa (χ
( 2=10,32; gl= 2; p<0,05), sendo essa diferença ocasionada
pela adição das amostras do município de Viseu na análise, já que a partição entre
Bragança e Augusto Corrêa não apresentou diferença significativa ((χ2=1,62; gl= 1;
p>0,05).
30
Tabela 4. Número de indivíduos positivos e negativos para produção de anticorpos em Bragança, Augusto Corrêa e Viseu, no
Estado do Pará.
Bragança
Augusto Corrêa
Viseu
Guilda/Espécies
Total
Positivo
Negativo
Positivo
Negativo
Positivo
Negativo
Carollia perspicillata
16
22
11
14
12
10
85
Artibeus planirostris
4
9
5
6
15
7
46
Uroderma bilobatum
4
6
0
2
11
14
37
Dermanura cinerea
7
14
3
5
6
0
35
Platyrrhinus incarum
2
1
1
-
3
2
9
Artibeus gnomus
2
-
-
-
3
3
8
Rhinophyla fischerae
4
2
1
-
-
1
8
Frugívora
Phyllostomus discolor
-
-
-
1
4
1
6
Artibeus obscurus
1
2
-
-
1
-
4
Sturnira lilium
1
-
-
-
1
2
4
Rhinophyla pumilio
-
1
2
-
-
-
3
Vampyriscus bidens
-
-
-
-
1
2
3
Phyllostomus hastatus
1
-
-
-
1
-
2
Artibeus lituratus
-
1
-
-
1
-
2
Uroderma magnirostrum
-
-
1
-
-
-
1
Platyrrhinus brachycephalus
-
-
-
1
-
-
1
Myotis nigricans
2
1
-
-
6
1
10
Tonatia saurophila
-
3
-
-
-
-
3
Lophostoma brasiliense
-
1
-
1
-
-
2
Lophostoma silvicolum
-
-
1
1
-
-
2
Mimon crenulatum
-
2
-
-
-
-
2
Eptesicus brasiliensis
-
-
-
-
1
1
2
Micronycteris megalotis
-
-
1
-
-
-
1
Trinycteris nicefori
-
-
1
-
-
-
1
Glossophaga soricina
1
2
7
3
6
-
19
Lonchophylla thomasi
1
1
-
-
-
1
3
Lichonycteris obscura
1
-
-
-
-
-
1
-
1
3
3
-
-
7
47
69
37
37
72
45
307
Insetívora
Nectarívora
Sanguívora
Desmodus rotundus
Total
31
positivo
Municípios Combinados
49%
Viseu
A. Corrêa
Bragança
negativo
51%
62%
38%
50%
50%
41%
59%
Percentual de indivíduos
Figura 7.. Comparação dos valores percentuais de morcegos soropositivos e soronegativos para a
produção de anticorpos capturados em Bragança, Augusto Corrêa e Viseu, e entre os três municípios
combinados no Estado do Pará.
Os resultados baseados no número de indivíduos soropositivos e
soronegativos nos diferentes períodos do ano (seco e chuvoso) mostraram diferença
significativa (χ2=28,61; gl=1 p<0,001). Salientando-se
Salientando se que o percentual de
indivíduos
víduos soropositivos durante o período chuvoso é bem maior (n=95; 67%),
enquanto que o de soronegativos é mais elevado durante o período seco (n=105;
63%). No município de Viseu essa diferença é bem evidente, onde 96% (n=47) dos
indivíduos capturados durante
durante o período chuvoso são positivos. A mesma tendência
foi registrada para Augusto Corrêa, onde 75% (n=15) dos indivíduos capturados
nesse período são soropositivos. Apenas em Bragança os valores de soronegativos
soronegativo
foram mais elevados em ambos
ambo os períodos (Figura 8).
Não foi registrada diferença significativa entre o número de soropositivos de
jovens e adultos (χ2=0,08; gl=1; p>0.05) e machos e fêmeas ((χ2= 2,15; gl=1;
p>0.05) (Tabela 5).
32
postivo
negativo
Percentual de indivíduos
4%
25%
54%
68%
59%
33%
63%
63%
96%
75%
46%
41%
Chuvoso
Seco
32%
Seco
Bragança
67%
37%
Chuvoso
Seco
A.Corrêa
37%
Chuvoso
Viseu
Seco
Chuvoso
Municípios
Combinados
Figura 8.. Comparação entre os valores percentuais de indivíduos soropositivos e soronegativos nos períodos
seco e chuvoso nos municípios inventariados de forma separada e combinada no Estado do Pará.
Apenas para essas espécies, assim como para todos os indivíduos,
indivíduos, o número de
soropositivos é elevado, e o município de Bragança continua apresentando maior
número de soronegativos. Anteriormente, considerando todas as espécies, Augusto
Corrêa apresentou o mesmo percentual para soronegativos e soropositivos (50%).
(50%) Por
outro lado, considerando as quatro espécies separadas, o percentual de indivíduos
negativos para a produção de anticorpos aumentou
aumentou para 59% (Tabela 6, Figura 9).
9
Devido ao número analisado de amostras de soro ter variado consideravelmente
dentre as espécies, foram escolhidas as mais abundantes para efeito de comparação,
co
totalizando quatro espécies e 203 amostras (Tabela 6).
33
Tabela 5. Soroprevalência relacionada ao sexo e faixa etária dos morcegos
registrados nos municípios de Bragança, Augusto Corrêa e Viseu, no Estado
do Pará.
Positivo
Negativo
Total
Feminino
76 (55%)
61 (45%)
137
Masculino
80 (47%)
90 (53%)
170
156
151
307
Jovem
69 (51%)
66 (49%)
135
Adulto
87 (51%)
85 (49%)
172
156
151
307
Total
Total
A análise comparativa, baseada no número de soropositivos das quatro espécies
mais abundantes, entre os três municípios foi significativa (χ2= 7,45; gl=2; p<0,05).
Essa diferença novamente foi ocasionada pela adição das amostras do município de
Viseu na análise, já que a partição entre Bragança e Augusto Corrêa não apresentou
diferença significativa (χ2= 0,14; gl=1; p>0,05).
Dentre as quatro espécies mais abundantes, três apresentaram maior percentual
de indivíduos soronegativos, exceto A. planirostris cujo resultado apontou 52% (n=24)
dos indivíduos como soropositivos (Tabela 6, Figura 10). Contudo, todos os valores
foram muito aproximados, sendo a diferença entre os soropositivos e os soronegativos
não significativa (χ2= 1,14; gl=3; p>0,05).
34
Tabela 6. Número de indivíduos das quatro espécies mais abundantes com
maior número de amostras positivas e negativas para produção de anticorpos
nos municípios de Bragança, Augusto Corrêa e Viseu, no Estado do Pará.
Situação
Município
Total
Positivo
Negativo
Bragança
16 (42%)
22 (58%)
38
Augusto Corrêa
11 (44%)
14 (56%)
25
Carollia perspicillata
Viseu
Total
12 (55%)
10 (45%)
22
39 (46%)
46 (54%)
85
4 (31%)
9 (69%)
13
Artibeus planirostris
Bragança
Augusto Corrêa
5 (45%)
6 (55%)
11
Viseu
15 (68%)
7 (32%)
22
24 (52%)
22 (48%)
46
Bragança
7 (33%)
14 (67%)
21
Augusto Corrêa
3 (38%)
5 (62%)
8
Viseu
6 (100%)
0 (0%)
6
16 (46%)
19 (54%)
35
Bragança
4 (40%)
6 (60%)
10
Augusto Corrêa
0 (0%)
2 (100%)
2
11 (44%)
14 (56%)
25
15 (41%)
22 (59%)
37
Total
Dermanura cinerea
Total
Uroderma bilobatum
Viseu
Total
Espécies combinadas
Bragança
31 (38%)
51 (52%)
82
Augusto Corrêa
19 (41%)
27 (59%)
46
Viseu
Total
44 (59%)
31 (41%)
75
94 (46%)
109 (54%)
203
35
Positivo
Municípios Combinados
46%
Viseu
A. Corrêa
Bragança
Negativo
54%
59%
41%
41%
59%
38%
62%
Percentual de indivíduos
Figura 9.. Comparação dos valores percentuais de espécimes de morcegos soropositivos e
soronegativos para a produção de anticorpos da raiva nos municípios de Bragança, Augusto
Corrêa e Viseu, e para os três municípios combinados no Estado do Pará.
Positivo
Dermanura cinerea
Uroderma bilobatum
46%
41%
Artibeus planirostris
Carollia perspicillata
52%
46%
Negativo
54%
59%
48%
54%
Percentual de indivíduos
Figura 10.. Comparação dos valores percentuais de indivíduos das quatro
espécies mais abundantes de morcegos soropositivos e soronegativos para a
produção de anticorpos da raiva nos municípios de Bragança,
Bragança, Augusto
Corrêa e Viseu, no Estado do Pará.
36
5. DISCUSSÃO
Entre os três municípios estudados dois estiveram diretamente envolvidos nos
surtos de Raiva Humana ocorridos em 2004 (Augusto Corrêa) e 2004 - 2005 (Augusto
Corrêa e Viseu) (MINISTÉRIO DA SAÚDE 2004). Durante este período não foram
registrados casos de Raiva Humana para o município de Bragança. No entanto, devido à
proximidade com os outros municípios, viu-se a necessidade de avaliar a composição da
fauna de morcegos local e sua soroprevalência de anticorpos contra a Raiva, no intuito
de comparar a produção de anticorpos em diferentes espécies entre áreas com e sem
registros dessa zoonose.
5.1. COMPOSIÇÃO DA QUIROPTEROFAUNA
A maior riqueza e abundância de morcegos presente em Bragança dão-se pelas
áreas de florestas, as quais foram utilizadas para as capturas, apresentarem maiores
quantidades de recursos alimentares e abrigos. Além do que, sabe-se que durante os
períodos de surto, alguns procedimentos foram adotados para o controle de populações
de morcegos nas áreas afetadas. Procedimentos estes que envolveram espécies
hematófagas e não-hematófagas e que deve ter influenciado na composição da
quiropterofauna atual de localidades pertencentes aos municípios de Viseu e Augusto
Corrêa.
Apesar de Bragança apresentar maiores números de espécies e indivíduos,
Augusto Corrêa foi o que apresentou maior valor de diversidade, contudo os valores dos
três foram muito aproximados, e a diversidade da área geral, ou seja, dos três
municípios combinados, foi bastante elevada (H’=2,1). Este valor foi bastante
aproximado ao de outro trabalho feito para região (ANDRADE et al., 2008), onde a
quiropterofauna de áreas de manguezal e terra firme na península bragantina foi
37
inventariada obtendo um H’= 1,9. Pedro & Taddei (1997) sugerem que embora haja
mudanças na composição de espécies em diferentes ecossistemas, para morcegos o H’
em áreas neotropicais geralmente situa-se em torno de 2,0.
Da quiropterofauna de morcegos registrada para a região, nota-se uma grande
predominância de morcegos filostomídeos, o que já era esperado devido à metodologia
utilizada favorecer a captura desses indivíduos (ROCHA et al., 2010). Os morcegos
dessa família apresentam uma grande versatilidade quanto à exploração de alimentos,
por possuírem diferentes técnicas de forrageio e utilizarem diferentes tipos de abrigo
(BREDT et al., 1998); e também por estes serem os mais abundantes em regiões
neotropicais (FENTON et al., 1992).
Morcegos vespertilionídeos parecem ser hábeis em detectar as redes, enquanto
que emballorunídeos e thyropterídeos apresentam características de vôo que dificultam
ou não permitem sua captura, por forragearem acima das copas das árvores (PEDRO &
TADDEI, 1997), por isso o total de capturas desses indivíduos no presente trabalho foi
baixo, totalizando apenas 3%.
A grande predominância relatada de C. perspicillata e de Artibeus no presente
estudo, já foi registrada em diversos trabalhos (REIS, 1984; PEDRO et al., 1995; REIS
et al., 2000; BERNARD, 2002; BIANCONI et al., 2004; CALOURO et al., 2010; LUZ
et al., 2011). Segundo Faria (2006), isso parece estar relacionado ao fato de que essas
são espécies que se adaptam bem aos ambientes perturbados, pois elas consomem frutos
de espécies vegetais pioneiras em sub-bosques, tipo de vegetação frequentemente
encontrado nas florestas de terra firme dessa região. Este evento já foi registrado,
principalmente, com morcegos do gênero Carollia (BERNARD, 2002), e de forma mais
oportunista, como no caso do gênero Artibeus quando ocorre escassez de frutos nas
38
copas das árvores da floresta (BONACCORSO & GUSH, 1987; BERNARD, 2001;
KALKO & HANDLEY, 2001).
Artibeus planirostris aparece como uma das espécies mais comuns para a região,
pois, assim como em outro trabalho realizado na região bragantina (ANDRADE et al.,
2008), essa espécie apresenta grande número de registros. No entanto, os resultados dos
inventários da quiropterofauna, de uma maneira geral, mostraram que a espécie mais
comum do gênero Artibeus é A. lituratus, tanto em áreas urbanas como em áreas de
floresta. Isto ocorre devido à maioria dos estudos ter sido realizada nas regiões Sudeste,
Sul e Centro-Oeste, onde essa espécie é mais comum (BARROS et al., 2006; REIS et
al., 2003; LIMA, 2008; BRITO et al., 2010; CALOURO et al., 2010).
Em contrapartida, poucos indivíduos de D. rotundus (n=8) foram capturados,
isso é reflexo do fato de que os locais escolhidos pra armar as redes não são comumente
explorados por essa espécie, já que esta parece estar estreitamente associada às áreas
com presença de herbívoros domésticos, como: bovinos, caprinos e eqüinos (BREDT et
al., 1998) e as redes foram armadas em florestas de terra firme não próximas a criações
desses animais.
Em se tratando da razão sexual sabe-se que muitas espécies de morcegos
apresentam sistema de acasalamento poligínico, com a formação de haréns organizados
a partir de machos adultos, principalmente, em morcegos filostomídeos, (KUNZ et al.,
1983; FLEMING, 1992; FISCHER & FISCHER, 1995; MELLO & FERNANDEZ,
2000; ZORTÉA, 2003; COSTA et al., 2007; MELLO et al., 2009). Isso certamente
explica a ocorrência, no presente trabalho, da razão sexual desviada para fêmeas nas
espécies C. perspicillata e G. soricina. Por outro lado, em espécies como D. cinerea e
U. bilobatum a proporção de machos e fêmeas foi a mesma, e diferente do que se
esperava, em A. planirostris houve desvio para machos. Essa última espécie, também de
39
forma peculiar, apresentou maior proporção de indivíduos adultos, mas, no entanto, não
houve a formação de haréns, o que segundo Ferreira et al. (2010) é o esperado em
grupos com maior número de adultos, fato este registrado para C. perspicillata, que
apresentou maior proporção de adultos e razão sexual desviada para fêmeas.
A maior proporção de indivíduos adultos em A. planirostris e C. perspicillata
pode ser explicada pela baixa quantidade de filhotes por ano (um ou dois por fêmea)
comum a muitas espécies de filostomídeos (FLEMING et al., 1972; MELLO &
FERNANDEZ, 2000), apesar disso D. cinerea e U. bilobatum apresentaram a mesma
proporção para jovens e adultos, enquanto G. soricina apresentou maior número de
jovens. O fato dessas três últimas espécies apresentarem elevado número de jovens pode
estar relacionado ao fato delas terem sido capturadas, principalmente, durante o período
seco, período no qual o número de jovens é comumente mais numeroso.
Adicionalmente, os resultados também apontaram para o fato de que as fêmeas
lactantes, pós-lactantes e, principalmente, as grávidas são mais numerosas durante o
período chuvoso.
As espécies de morcegos fitófagas relacionam seu período de reprodução aos
picos de floração e frutificação, devido à alta disponibilidade de alimentos (BREDT et
al., 1998), o que ocorre durante a estação chuvosa, por isso o número de fêmeas em
estado reprodutivo é maior durante esse período, enquanto que fêmeas não reprodutivas
são mais numerosas durante o período seco. Nesse período de escassez, foi registrada a
presença de um grande número de machos sexualmente ativos, o que sugere um período
de acasalamento. O nascimento dos filhotes ocorre com mais freqüência na estação
chuvosa, uma vez que o tempo de gestação é prolongado (dois a sete meses,
dependendo da espécie) (ALVES et al., 2009; GOMES & UIEDA, 2004; BREDT et al.,
1998). Contudo, é importante ressaltar que tais interpretações acerca do período de
40
reprodução dessas espécies são um reflexo do número de indivíduos capturados. A
maioria dos indivíduos foi capturada durante o período seco, pois durante o período
chuvoso os morcegos passam maior parte do tempo recolhidos em seus abrigos devido à
chuva, não saindo para forragear. Este fato é bem ilustrado com os resultados para os
municípios de Viseu e Bragança, mas não para o município de Augusto Corrêa. Por
outro lado, considerando o número de espécies capturadas no presente trabalho, valores
similares foram registrados para as duas estações, ocorrendo uma pequena variação por
localidade.
5.2. PREVALÊNCIA SOROLÓGICA
O estudo da soroprevalência da quiropterofauna dessa região mostrou que o
número de soropositivos e soronegativos para a produção de anticorpos foi muito
aproximado, indicando que boa parte dos morcegos dessa região, em algum momento,
teve contato com RABV, ou estão infectados com o vírus. Isso é bem evidente nos
municípios de Viseu e Augusto Corrêa onde foram registrados altos valores percentuais
de soropositividade.
Segundo Cubas et al. (2007), essa alta prevalência indica a
ocorrência de surtos recentes.
Apesar da proximidade com os municípios anteriormente citados para o Estado
do Pará, Bragança não apresentou surtos de Raiva nos anos de 2004 e 2005, sendo
assim os morcegos deste local tiveram menos contato com o vírus da raiva, o que pode
explicar o seu menor percentual de soropositivos.
As duas diferentes e marcadas estações do ano na área de trabalho parece
influenciar no percentual de indivíduos soropositivos. O maior percentual de
soropositivos durante a estação chuvosa parece ser resultado do fato de que durante esse
período os morcegos saem menos para forragear, ficando a maior parte do tempo em
seus abrigos onde mantêm maior contato com outros indivíduos da colônia. Assim, é de
41
se esperar que ocorra maior probabilidade de transmissão do vírus entre eles, já que esta
transmissão ocorre pelo contato direto, como: lambedura e mordedura (ALVES et al.,
2009), promovendo, consequentemente, a maior introdução de anticorpos.
Essa alta na introdução de anticorpos durante o período chuvoso ocorre em todos
o três municípios estudados, e é bem mais evidente em Viseu, onde quase a totalidade
dos indivíduos capturados durante este período era soropositiva. Esse elevado valor
parece estar relacionado com o fato de que nesse município existem muitas áreas com
cavernas, o que de acordo com Bredt et al. (1999), servem de abrigos com grande
concentração de colônias, promovendo maior facilitação na transmissão do vírus através
do contato direto.
Embora a transmissão do RABV pareça ocorrer muito cedo na vida desses
indivíduos, devido ao contato direto, ingestão de leite produzido pela mãe infectada ou
infecção transplacental (SIMS et al., 1963; CONSTANTINE, 1966, 1967;
CONSTANTINE et al., 1968; STEECE & CALISHER, 1989), no presente estudo a
diferença na soroprevalência entre adultos e jovens não foi significativa. Diante disso,
vemos que a introdução de anticorpos ocorre em ambos os estágios de desenvolvimento.
Da mesma forma, os resultados do presente trabalho não diferiram
significativamente quanto aos valores de soropositivos e soronegativos para machos e
fêmeas. Contudo, é comum indivíduos do sexo masculino apresentarem maior
introdução de anticorpos, já que machos dominantes, em interações intraespecíficas,
podem morder e ser mordidos por machos subalternos e intrusos e expulsá-los da sua
colônia (CORTÊS et al., 1994). Esses machos expulsos poderiam deslocar-se para
outras áreas na tentativa de formar ou encontrar uma nova colônia, sendo dessa forma
considerados importantes veículos de propagação do RABV quando infectados
(CORTÊS et al., 1994).
42
Apesar da diferença entre o número de positivos e negativos não ter sido
significativa entre os indivíduos analisados de A. planirostris, esta apresentou mais da
metade de indivíduos soropositivos (52%), vale a pena ressaltar que esta espécie
encontra-se presente na lista de morcegos brasileiros positivos para a Raiva (SODRÉ et
al. 2010).
Das quatro espécies analisadas, D. cinerea é a única que não está presente na
lista de Sodré et al. (2010), muito embora tenha sido, no presente estudo, registrada
produzindo anticorpos. É importante salientar que todos os indivíduos dessa espécie
apresentaram soropositividade para o município de Viseu.
De maneira geral, a alta produção de anticorpos encontrada em indivíduos de
diferentes espécies de morcegos não hematófagos nos três municípios estudados sugere
que o RABV circula muito ativamente nessa região. Em suma, na região do nordeste do
Pará, representada no presente trabalho pelos municípios de Bragança, Augusto Corrêa
e Viseu, foi registrada a circulação do fluxo viral entre morcegos de diversas espécies
não hematófagas, sendo necessário um constante monitoramento por medidas sanitárias
e epidemiológicas, no intuito de manter o controle da epizootia da Raiva.
43
6. REFÊNCIAS BIBLIOGRÁFICAS
ALVES, A. P. F.; ABREU, M. A. B. L. & LESSA, P. G. Ocorrência da raiva em
herbívoros no município de Pedra Bela durante o Período de 1999 a 2008. Curso de
Especialização Latu Sensu em Defesa e Vigilância Sanitária Animal – UCB. São
Paulo.36p. 2009.
ANDRADE, F. A. G.; FERNANDES, M. B.; MARQUES-AGUIAR, S. A. & LIMA, G.
B. Comparasion between the chiropteran fauna from terra firme and mangrove forests
on the Bragança península in Pará, Brazil. Studies on Neotropical Fauna an
Environment, 43 (3): 169-176. 2008.
ARAI, Y.T.; KUZMIN, I.V.; KAMEOKA, Y.; BOTVINKIN, A.D. New Lyssavirus
Genotype from the Lesser Mouse-eared Bat (Myotis blythi), Kyrghyzstan. Emerging
Infectious Diseases, 9 (3): 333-337. 2003.
AYRES, M.; AYRES, M. J.; AYRES, D. L. & SANTOS, A. A. BIOESTAT –
Aplicações estatísticas nas áreas das ciências bio-médicas. Ong Mamiraua. Belém, PA.
2007.
BADRANE, H.; TORDO, N. Host Switching in Lyssavirus History from the Chiroptera
to the Carnivora Orders. Journal of Virology, 75 (17): 8096-8104. 2001.
BAER, G. M. & BALES, G. L. Experimental rabies infection in the Mexican free-tailed
bat. Journal of infectious Diseases, 117: 82-90. 1967.
44
BARROS, R. S.; BISAGGIO, E. L. & BORGES, R. C. Morcegos (Mammalia,
Chiroptera) em fragmentos florestais urbanos no Município de Juiz de Fora, Minas
Gerais, Sudeste do Brasil. Biota Neotropical 6 (1). 2006.
BERNARD, E. Vertical stratifi cation of bat communities in primary forest of Central
Amazon, Brazil. Journal of Tropical Ecology, 17: 115-126. 2001.
BERNARD, E. Diet, activity and reproduction of bats species (Mammalia, Chiroptera)
in Central Amazonia, Brazil. Revista Brasileira de Zoologia, 19 (1): 173-188. 2002.
BERNARD, E. & FENTON, M. B. Species diversity of bats (Mammalia: Chiroptera)
in forest fragments, primary forest, and savannas in central Amazonia, Brazil.
Canadian Journal of Zoology, 80: 1124-1140. 2002.
BIANCONI, G. V.; MIKICH, S. B. & PEDRO, W. A. Diversidade de morcegos
(Mammalia, Chiroptera) em remanescentes florestais do município de Fênix, noroeste
do Paraná, Brasil. Revista Brasileira de Zoologia, 21 (4): 943-954. 2004.
BONACCORSO, F. J. & GUSH, T. J. Feeding behavior and foraging strategies of
captive phyllostomid fruit bats: an experimental study. The Journal of Animal Ecology,
56 (3): 907-920. 1987.
BORDIGNONG, M. O. Predação de morcegos por Chrotopterus auritus (Peters)
(Mammalia, Chiroptera) no pantanal de Mato Grosso do Sul, Brasil. Curitiba. Revista
Brasileira de Zoologia, 22 (4): 1207-1208. 2005.
45
BOTVINKIN, A.D.; POLESCHUK, E.M.; KUZMIN, I.V.; BORISOVA, T.I.;
GAZARYAN, S.V.; YAGER, P.; RUPPRECHT, C.E. Novel Lyssaviruses Isolated
from Bats in Russia. Emerging Infectious Diseases, 9 (12):1623-1625. 2003.
BOURHY, H.; KISSI, B; TORDO, N. Molecular diversity of the Lyssavirus Genus.
Virology, 194:70-81. 1993.
BRASIL. Ministério da Saúde. Secretaria de Vigilância em Saúde. Boletim eletrônico
Epidemiológico : SVS – Surto de raiva humana transmitida por morcegos no município
de Portel – Pará, março/abril de 2004, v.4, n.6, 2004. Disponível em:
<http://portal.saude.gov.br/portal/arquivos/pdf/boletim_eletronico_06_ano04.pdf>.
BRASS D. A. Rabies in Bats: natural history and public health implications. Livia
Press, Connecticut. 352p. 1994.
BREDT, A.; ARAÚJO, F. A. A.; JÚNIOR, J. C.; RODRIGUES, M. G. R.;
YOSHIZAWA, M.; SILVA, M. M. S.; HARMANI, N. M. S.; MASSUNAGA, P. N. T.;
BURER, S. P.; PORTO, V. A. R.; UIEDA, W. Morcegos em áreas urbanas e rurais:
manual de manejo e controle. Brasília: Fundação nacional de Saúde, 117p. 1998.
BRITO, J. E. C.; GAZARINI, J. & ZAUADZKI, C. H. Abundância e frugivoria da
quiropterofauna (Mammalia, Chiroptera) de um fragmento no nordeste do Estado do
Paraná, Brasil. Acta Scientiarum. Bilogical Sciences, 32 (3): 265-271. 2010.
46
CALISHER, C. H.; CHILDS, J. E.; FIELD, H. E.; HOLMES, K. V. & SCHOUNTZ, T.
Bats: important reservoir hosts of emerging viruses. Clinical Microbiology Reviews, 19:
531–545. 2006.
CALOURO, A. M.; SANTOS, F. G. A.; FAUSTINO,C. L.; SOUZA, S. F.; LAGUE, B.
M.; MARCIETE, R.; SANTOS, G. J. L. & CUNHA, A. O. Riqueza e abundância de
morcegos capturados na borda e no interior de um fragmento florestal do estado do
Acre, Brasil. Biotemas, 23 (4): 109-117. 2010.
CAMPBELL, J. B. & CHARLTON, K. M. Rabies. London: Kluwer Academic. 431 p.
1988.
CASTILHO, C. V.; MAGNUSSON, W. E.; ARAÚJO, R. N. O.; LUIZÃO, F. J. Shortterm temporal changes in tree live biomass in a Central Amazonian forest, Brazil.
Biotropica, 42 (1): 95 - 103. 2010.
CLARKE, K.R. & GORLEY, R.N. Primer v.5: User manual / Tutorial. Primer-E:
Plymouth. 91p. 2001.
CONSTANTINE, D. G.; TIERKEL, E. S.; KLECKNER, M. D.; HAWKINS, D. M.
Rabies in New Mexico cavern bats. Public Health Report, 83: 303–316. 1968.
CONSTANTINE, D. G. Ecological observations on lasiurine bats in Iowa. Journal of
Mammalogy, 47: 34–41. 1966.
47
CONSTANTINE, D. G. Bats rabies in the southwestern United States. Public Health
Service Publication No. 1617, 51p. 1967.
CONSTANTINE, D. G. Health precautions for bat researchers, 491-526p. In: KUNZ,
T.H. (Ed.). Ecological and Behaviorial Methods for the Study of Bats. Washington
D.C., London: Smithsonian Institution Press, 533p. 1988.
CORTÊS, V. A.; SOUZA, L. C.; UIEDA, W. & FIGUEIREDO, A. C. Abrigos diurnos
e infecção rábica em morcegos de Botucatu, São Paulo, Brasil. Veterinária e Zootecnia,
6: 179-186. 1994.
COSTA, L. M.; ALMEIDA, J. C. & ESBERARD, C. E. L. Dados de reprodução de
Platyrrhinus lineatus em estudo de longo prazo no Estado do Rio de Janeiro
(Mammalia, Chiroptera, Phyllostomidae). Iheringia, Séria Zoologia, 97 (2): 152-156.
2007.
CUBAS, Z. S.; SILVA, J. C. R. & CATÃO DIAS, J. L. Tratado de animais selvagens –
medicina veterinária. São Paulo: Roca. 785-98p. 2007.
EISENBERG, J. F. & REDFORD, K. H. Mammals of the Neotropics. The Central
Neotropicaics. Vol. 3. Ecuador, Peru, Bolívia, Brazil. The University of Chicago Press,
Chicago and London, 609p. 1999.
48
FAVORETTO, S.R.; CARRIERI, M.L.; CUNHA, E.M.S.; AGUIAR, E.A.C.; SILVA,
L.H.Q.; SODRÉ, M.M.; SOUZA, M.C.A.M.; KOTAIT, I. Antigenic Typing of
Brazilian Rabies Virus Samples Isolated from Animals and Humans, 1989-2000.
Revista do Instituto de Medicina Tropical de São Paulo,44 (2): 91-95. 2002.
FENTON, M. B.; ACHARYA L.; AUDET D.; HICKEY M. B. C.; MERRIMAN C.;
OBRIST M. K. & SYME D. M. Phyllostomid bats (Chiroptera: Phyllostomidae) as
indicators of habitat disruption in the Neotropics. Biotropica, 24: 440-446. 1992.
FERREIRA, C. M. M.; FISCHER, E. & PULCHÉRI-LEITE, A. Fauna de morcegos em
remanescentes urbanos de Cerrado em Campo Grande, Mato Grosso do Sul. Biota
Neotropica, 10 (3): 155-160. 2010.
FLEMING, T.; HOOPER, E. & WILSON, D. Three Central American bat
communities: structure reproductive cycles, and movement patterns. Ecology, 53: 555569. 1972.
FLEMING, T.H. How do fruit- and nectar-feeding birds and Mammals track their food
resources? In Effects of resource distribution on animal-plant interactions (M.D.
Hunter, T. Ohgushi & P.W. Price, Ed.). Academic Press, 355-391pp. 1992.
FISCHER, W. A. & FISCHER, E. A. Comportamento social e reprodutivo do
morcego-cara-branca, Artibeus lituratus. In: Ecologia e preservação de uma floresta
tropical urbana (H.F.L. Filho & L.P.C. Morellato, Org.). Editora da UNICAMP,
Campinas, SP. 1995.
49
FORNES, A.; LORD, D.L.; KUNS, M.L.; LARGHI, O.P.; FUENZALIDA, E. &
LAZARA, L. Control of bovine rabies through vampire bat control. Journal of Wildlife
Diseases, 10: 310-316. 1974.
GOMES, M. N. & UIEDA, W. Abrigos diurnos, composição de colônias, dismorfismo
sexual e reprodução do morcego hematófago Desmodus rotundus (E. Geoffroy)
(Chiroptera, Phyllostomidae) no Estado de São Paulo, Brasil. Revista Brasileira de
Zoologia, 21 (3): 629-634. 2004.
GOULD, A.R.; HYATT, A.D.; LUNT, R.; KATTENBELT, J.A.; HENGSTBERGER,
S.; BLACKSELL, S.D. Characterisation of a novel lyssavirus isolated from Pteropid
bats in Australia. Virus Research, 54: 165-187. 1998.
GREENHALL, A. M.; JOERMANN, G.; SCHMIDT, U. Desmodus rotundus.
Mammalian Species, 202: 1-6. 1983.
HANDLEY C. O. JR. New species of mammals from northern South America: fruiteating bats, genus Artibeus Leach. Fieldiana 29: 163-172. 1987.
HILL, J. E. & SMITH, J. D. Bats: natural history. 2nd Ed. University of Texas Press,
USA, 243p. 1984.
FINDLEY. Bats: a community perspective. Cambridge University Press. 167p. 1988.
50
HUTSON, A. M., MICKLEBURGH, S. P., RACEY, P. A. Microchiropteran bats: global
status survey and conservation action plan. IUCN/SSC Chiroptera Specialist Group. IUCN,
Gland, Switzerland and Cambridge, UK. x + 258 pp. 2001.
ICTV – INTERNATIONAL COMMITTEE ON VIRUS TAXONOMY. Vírus Taxonomy:
Classification and Nomenclature of Vírus. Eighth Report of th International Committee on
the Taxonomy of virus. In: FAUGUET, C. M.; MAYO, M. A.; MANILOFF, J.;
DESSEBERGER, U.; BALL, L. A. (eds), San Diego: Elsevier Academic press, 981- 998.
2005.
ICTV – INTERNATIONAL COMMITTEE ON VIRUS TAXONOMY. Official
Taxonomy: Updates Since the 8th Report, Vertebrate. 2009. Disponível em:
<http://talk.ictvonline.org/media/p/1208.aspx>
INPPAZ – INSTITUTO PANAMERICANO DE PROTECCION DE ALIMENTOS Y
ZOONOSIS. Vigilância Epidemiologica de la Rabia em lãs Americas. Boletin de Vigilancia
de la Rabia em lãs Americas. Buenos Aires: Organizacion Panamericana de la Salud –
Oficina Sanitaria Panamericana. Oficinal Regional de la Organizacion Mundial de la Salud.
Division de Prevencion y Control de Enfermidades v.28. 1996.
KALKO, E. K. V. & HANDLEY, C. O. Neotropical bats in the canopy: Diversity
community structure, and implications for conservation. Plant Ecology, 153: 319-333.
2001.
51
KUNZ, T.H.; AUGUST, P.V. & BURNETT, C.D. Harem social organization in cave
roosting Artibeus jamaicensis (Chiroptera: Phyllostomidae). Biotropica, 15 (2): 133138. 1983.
KUZMIN, I.V.; MAYER, A.E.; NIEZGODA, M.; MARKOTTER, W.; AGWANDA,
B.; BREIMAN, R.F.; RUPPRECHT, C.E. Shimoni bat virus, a new representative of
the Lyssavirus genus. Virus Research, 149: 197-210. 2010.
KUZMIN, I.V.; ORCIARI, L.A.; ARAI, Y.T.; SMITH, J.S.; HANLON, C.A.;
KAMEOKA, Y.; RUPPRECHT, C.E. Bat lyssaviruses (Aravan and Khujand) from
Central Asia: phylogenetic relationships according to N, P and G gene sequences. Virus
Research, 97: 65-79. 2003.
LANGONI H., SOUZA L. C., ZETUN C. B., T. C. C., HOFFMANN J. L., SILVA R.
C. Serological survey for rabies in serum samples from vampire bats (Desmodus
rotundus) in Botucatu region, SP, Brazil. The Journal of Venomous Animals and Toxins
Including Tropical Diseases, 14 (4): 653p. 2008.
LIMA, I. S. Espécies de morcegos (Mammalia, Chiroptera) registradas em parques nas
áreas urbanas do Brasil e suas implicações no uso deste ambiente. In: REIS, N. R.;
PERACCHI, A. L.; SANTOS, G. A. S. D. (Ed.). Ecologia de morcegos. Londrina:
Technical Books. 71-85pp. 2008.
LINARES, O.J. Murcielagos de Venezuela. Cuadernos Lagoven, Departamento de
Relaciones Públicas de Lagoven S. A., Caracas. 122p. 1987.
52
LUZ, J.L., COSTA, L.M., LOURENÇO, E.C. & ESBÉRARD, C.E.L. Morcegos
(Mammalia, Chiroptera) da Reserva Rio das Pedras, Rio de Janeiro, Sudeste do Brasil.
Biota Neotropica, 11 (1). 2011.
MARGURRAN, A. E. Ecological diversity and its measurement. Princeton, Princeton
University, 179p. 1988.
MARQUES-AGUIAR, S. A. A systematic review of the large species of Artibeus
Leach, 1821 (Mammalia: Chiroptera) with some phylogenetic inferences. Belém,
Boletim do Museu Paraense Emílio Goeldi (Zoologia), 10 (1): 3-83. 1994.
MAYEN, F. Hematophagous bats in Brazil, their role in rabies transmission, impact on
public health, livestock industry and alternatives to an indiscriminate reduction of bat
population. Berlin. Journal Veterinary Medicine, 50: 469-472. 2003.
MEDELLIN, R. A.; EQUIHUA, M. & AMIN, M. A. Bat diversity and abundance as
indicators of disturbance in neotropical rainforest. Conservation Biology, 4 (6):16661675. 2000.
MELLO, M. A. R. & FERNANDEZ, F. A. S. Reproductive ecology of bat Carollia
perspicillata (Chiroptera: Phyllostomidae) in a fragment of the Brazilian Atlantic
coastal forest. Z. Saeugetierkd, 65: 340-349. 2000.
53
MELLO, M. A. R.; KALKO, E. K. V.; SILVA, W. R. Ambient temperature is more
important than food availability in explaining reproductive timing of the bat Sturnira
lilium (Mammalia: Chiroptera) in a montane Atlantic Forest. Canadian Journal of
Zoology, 87: 239-245. 2009.
MINISTÉRIO DA SAÚDE. Surto de raiva humana transmitida por morcegos no
município de Portel-Pará, Março/Abril de 2004. Brasília. Boletim Eletrônico
Epidemiológico, 4: 2-5. 2004.
MIRETZI, M. Morcegos do Estado do Paraná, Brasil (Mammalia, Chiroptera): riqueza
de espécies, distribuição e síntese do conhecimento atual. Papeis Avulsos de Zoology,
43 (6): 101-138. 2003.
MORAES, B.C.; COSTA, J. M. N.; COSTA, A. C. L. & COSTA, E M. H. Variação
espacial e temporal da precipitação no Estado do Pará. Acta Amazônica, 35 (2): 207214. 2005.
OPAS - ORGANIZAÇÃO PAN-AMÉRICANA DE SAÚDE. Curso de Controle da
Raiva Silvestre (D. rotundus) no Brasil. 48p. 2007.
PEDRO, W. A.; GERALDES, M. P.; LOPEZ, G. G. & ALHO, C. J. R. Fragmentação
de habitat e a estrutura de uma taxocenose de morcegos em São Paulo (Brasil).
Chiroptera Neotropical, 1 (1):4-6. 1995.
PEDRO, W. A. & TADDEI, W. A. Taxonomic assemblage of bats from Panga Reserve,
Southeastern Brazil: abundance patterns and trophic relations in the Phyllostomidae
(Chiroptera). Boletim do Museu de Biologia, 6: 3-21. 1997.
54
PERACCHI, A.L., LIMA, I.P., REIS, N.L., NOGUEIRA, M.L. & ORTÊNCIO-FILHO,
H. Ordem Chiroptera. In: REIS, N.R., PERACCHI, A.L., PEDRO, W.A. & LIMA, I.P
(Eds). Mamíferos do Brasil. Editora da Universidade Estadual de Londrina. 153230pp. 2006.
REIS, N. R. Estrutura de comunidades de morcegos na região de Manaus, Amazonas.
Revista Brasileira de Biologia, 44 (3): 247-254. 1984.
REIS, N. R.; PERACCHI, A. L.; SEKIAMA, M. L. & LIMA, I. P. Diversidade de
morcegos (Chiroptera, Mammalia) em fragmentos florestais no estado do Paraná,
Brasil. Revista Brasileira de Zoologia, 17 (3): 697-704. 2000.
REIS, N. R.; LIMA, I. P. & PERACCHI, A. L. Morcegos (Chiroptera) da Área urbana
de Londrina, Paraná, Brasil. Revista Brasileira de Zoologia, 19 (3): 739 - 746. 2003.
REIS, N. R.; PERACCHI, A. L.; PEDRO, W. A. & LIMA, I. P. Morcegos do Brasil.
Londrina, p. 17-25. 2007.
ROCHA, P. A.; MIKALAUSKAS, J. S.; GOUVEIA, S. F.; SILVEIRA, V. V. B. &
PERACCHI, A. L. Morcegos (Mammalia, Chiroptera) capturados no Campus da
Universidade Federal de Sergipe, com oito novos registros para o estado. Biota
Neotropica, 10 (3). 2010.
RUPPRECHT, C.E.; HANLON, C.A.; HEMACHUDHA, T. Rabies re-examined. The
Lancet Infectious Diseases, 2: 327-343. 2002.
55
SCHNEIDER, L.G.; DIETZSCHOLD, B.; DIERKS, R.E.;MATTHAEUS, W.;
ENZMANN, P.J.; STROHMAIER, K. Rabies Group-Specific Ribonucleoprotein
Antigen and a Test System for Grouping and Typing of Rhabdoviruses. Journal of
Virology, 11(5): 748-755. 1973.
SCHNEIDER, M. C.; ROMIJN, P. C.; UIEDA, W.; TAMAYO, H.; SILVA, D. F.;
BELOTTO, A.; SILVA, J. B. & LEANES, L. F. Rabies transmitted by vampire bats to
humans: An emerging zoonotic disease in Latin America? Revista Panamericana de
Saúde Pública, 25 (3): 260-269. 2009.
SIMS, R. A.; ALLEN, R. & SULKIK, S. E. Studies on the pathogenesis of rabies in
insectivorous bats. Influence of the gravid state. Journal of Infection Disease 112: 1727. 1963.
SIMMONS, N. B. Order chiroptera. In: Mammal species of the world: a taxonomic and
geographic reference (D.E. Wilson & D.M. Reeder, eds.). Smithsonian Institution
Press, Washington, p. 312-529. 2005.
SMITH, J.; YAGER, P.; & BAER, G. A rapid reproducible test for determining rabies
neutralizing antibodies. Bulletin of the World Health Organization, 48: 535-541. 1973.
SODRÉ, M.M.; GAMA, A.R. & ALMEIDA, M.F. Updated
List of Bat Species
Positive for rabies in Brazil. Rev. Inst. Med. Tropical, 51: 75-81. 2010.
56
SOUZA, L. C.; LANGONI, H.; SILVA, R. C. & LUCHEIS, S. B. Vigilância
epidemiológica da raiva na região de Botucatu-SP: importância dos quirópteros na
manutenção do vírus na natureza. Jaboticabal, SP. ARS Veterinária, 21 (1): 62-68. 2005.
STEECE, R. S. & ALTENBACH J. S. Prevealence of rabies specific antibodies in the
Mexican free-tailed bat (Tadarida brasiliensis mexicana) at lava cave, New Mexico.
Journal of Wildlife Disease, 25 (4): 490-496. 1989.
STEECE, R. S. & CALISHER C. H. Evidence for prenatal transfer of rabies virus in the
Mexican free-tailed bat (Tadarida brasiliensis mexicana). Journal of Wildlife Diseases,
25 (3): 329-334. 1989.
TAVARES, V. C.; GREGORIN, R. & PERACCHI, A. L. A diversidade de morcegos
no Brasil: lista atualizada com comentários sobre distribuição e taxonomia. In
PACHECO, S. M.; MARQUES, R. V. & ESBÉRARD, CEL. (Eds.). Morcegos no
Brasil: biologia, sistemática, ecologia e conservação. Porto Alegre: Armazém Digital.
25-60pp. 2008.
TEIXEIRA, T. F.; BATISTA, H. B. C. R.; SCHMIDT, E. & ROEHE, P. M. Estudo
antigênico de amostras do vírus da raiva isoladas no Rio Grande do Sul, Brasil. Acta
Scientiae Veterinariae, 33 (3): 271-275. 2005.
THIELE, J. & WINTER, Y. Hierarchical strategy for relocating food targets in flower
bats: spatial memory versus cue-directed search. Animal Behaviour, 69: 315-327. 2005.
57
TORDO, N.; SACRAMENTO, D.; BADRANE, H.; BAHLOUL, C.; AGUILARSETIEN, A.; LOZA-RUBIO, E.; GAVILAN-SALINAS, A.; BROCHIER, B.;
PASTORET, P.P.; DESMEZIERES, E.; JACOB, Y.; PERRIN, P. Genetic diversity of
lyssaviruses: implications in vaccinology. In: SEMINÁRIO INTERNACIONAL DE
RAIVA, 2000, São Paulo. Programa e resumos. São Paulo: Instituto Pasteur, p.26-27.
2000.
UIEDA, W. O vírus da raiva nos morcegos e sua transmissão ao homem no Brasil.
Virologica, 93: 243-246. 1998.
VONHOF, M. J.; WHITEHEAD, H. & FENTON, M. B. Analysis of Spix’s discwinged bat association patterns and roosting home ranges reveal a novel social structure
among bats. Animal Behaviour, 68 (3): 507-521. 2004.
ZORTÉA, M. Reproductive patterns and feeding habits of three nectarivorous bats
(Phyllostomidae: Glossophaginae) from de Brazilian Cerrado. Brazilian Journal
Biology, 63 (1): 159-168. 2003.
WARRELL, M. J.; WARREL, D. A. M. Rabies and other lyssavirus diseases. Lacent,
363: 959-969. 2004.
WALKER, S. M. Conservation progress in Latin America. Bats Magazine, 19: 1-2.
2001.
58
WHO – WORLD HEALTH ORGANIZATION. Expert Consultation on Rabies: first
report. WHO technical report series, 931. Geneva: WHO, 121p. 2005.
WHITTAKER, R.J. & JONES, S. H. The role of frugivorous bats and birds in the
rebuilding of a tropical forest ecosystem, Krakatau, Indonesia. Journal Biogeography,
21: 245-258. 1994.
WOLF, W. W.; WESTBROOK, J. K.; RAULSTON, J. R.; PAIR, S. D. & HOBBS, S.
E. Recent airborne radar observations of migrant pests in the United States.
Philosophical Transactions of the Royal Society of London, B: Biological Sciences,
328: 619–630. 1990.
ZAHN, A.; HASELBACH, H. & GÜTTINGER, R. Foraging activity of central
European Myotis myotis in a landscape dominated by spruce monocultures. Mammal
Biology, 70: 265-270. 2005.