2º
Química B
Priscila
Av. Subst./Optat.
EM
24/11/14
INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA
LEIA COM MUITA ATENÇÃO
1.
Verifique, no cabeçalho desta prova, se seu nome, número e turma estão corretos.
2.
Esta prova contém 10 questões dissertativas.
3.
Leia todas as questões com atenção.
4.
A prova deverá ser feita com caneta esferográfica de tinta azul ou preta.
5.
É vedada a utilização de qualquer material de consulta, eletrônico ou impresso.
6.
É terminantemente proibido retirar-se do local da prova antes de ocorrido o tempo mínimo estipulado,
qualquer que seja o motivo.
7.
Tempo de duração da avaliação - Mínimo: 50 min
Máximo: 50 min
8.
Ao final, entregue a prova ao professor aplicador.
BOA PROVA!
Assinatura do Aluno: _________________________________________________
QUESTÕES
1/6
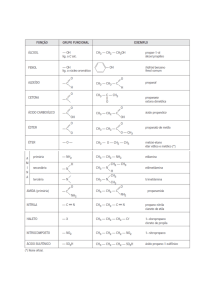
1.
(1,0) (FUVEST) O aldeído valérico, mais conhecido por pentanal, apresenta que fórmula
molecular?
Assinale a alternativa correta, justificando através da sua fórmula estrutural.
a)
C5H10O
b)
C5H5O2
c)
C5H10O2
d)
C5H8O
e)
C5H12O2
2.
(2,0) Complete as reações, indicando o nome das substâncias presentes na equação,
conforme os modelos a seguir:
a)
b)
2/6
3.
(1,0) (CEFET – MG Adaptada) As estruturas moleculares do ácido acetilsalicílico,
substância ativa da aspirina e em vários analgésicos, e do estireno, monômero utilizado na
produção de plásticos, são:
Quais são suas fórmulas moleculares?
4.
(1,0) Coube a Robert Robinson, prêmio Nobel de Química de 1947, o privilégio de chegar à
estrutura química da brasilina, substância responsável pela cor vermelha do pau-brasil.
Quais as funções orgânicas presentes na brasilina? Circule seus nomes funcionais indicando
ao lado os nomes.
3/6
5.
(1,0) (PUC – RS Adaptada) Para responder à questão a seguir, numere a coluna B, que
contém alguns nomes de compostos orgânicos, de acordo com a coluna A, na qual estão
citadas as funções orgânicas.
6.
Coluna A
Coluna B
I) benzeno
(
) éster
II) etoxietano
(
) hidrocarboneto
III) metanoato de etila
(
) éter
IV) propanona
(
) cetona
V) metanal
(
) aldeído
(1,0) (UFRJ) A solubilidade dos compostos é um conhecimento muito importante em
química.
Sabe-se que, de uma forma geral, substâncias polares dissolvem substâncias polares e
substâncias apolares dissolvem substâncias apolares.
Em um laboratório, massas iguais de tetracloreto de carbono, água e etanol foram colocadas
em três recipientes idênticos, conforme se vê na figura a seguir.
a) Mostre por meio de desenhos semelhantes ao apresentado, como fica a mistura I e II,
identificando cada substância, e como fica a mistura II e III.
4/6
b) A graxa lubrificante utilizada em automóveis é uma mistura de hidrocarbonetos pesados
derivados de petróleo com aditivos diversos.
Indique qual, dentre os três solventes apresentados, é o mais adequado para remover uma
mancha de graxa em uma camisa. Justifique sua resposta.
7.
(1,0) Escreva as fórmulas estruturais de quatro álcoois e três éteres que apresentam a
fórmula molecular C4H10O.
8.
(1,0) Escreva as estruturas de:
a) Dois isômeros de cadeia com fórmula C4H10
b) Dois isômeros de posição com fórmula C4H9NH2.
5/6
9.
(1,0) Escreva as fórmulas estruturais do but-1-eno e do but-2-eno.
Analisando os dois compostos, indique qual deles apresenta isomeria geométrica e desenhe as
fórmulas de projeção dos isômeros cis e trans.
10. (Bônus 1,0) (UNICAMP) A ureia (CH4N2O) é o produto mais importante de excreção do
nitrogênio pelo organismo humano. Na molécula da ureia, formada por oito átomos, o carbono
apresenta duas ligações simples e uma dupla, o oxigênio, uma ligação dupla, cada átomo de
nitrogênio, três ligações simples, e cada átomo de hidrogênio, uma ligação simples. Átomos
iguais não se ligam entre si.
Baseando-se nessas informações, escreva a fórmula estrutural da ureia, representando
ligações simples por traço e ligações duplas por dois traços.
6/6