Síntese e Avaliação do Potencial anti-HCV, anti-Glicosidases e antitumoral
de Chalconas Derivadas de Apocinina
Beatriz de Carvalho Marques, Mariana Bastos dos Santos, Gabriela Miranda Ayusso, Luis Octávio Regasini.
Universidade Estadual Paulista – Instituto de Biociências Letras e Ciências Exatas (IBILCE), Ciências
Biológicas.
[email protected]
Palavras Chave: chalconas, apocinina, HCV.
Introdução
Resultados e Discussão
A Hepatite C é uma degeneração do fígado causada
pelo vírus HCV, e que segundo a Organização
Mundial de Saúde (OMS), infecta mais de 3% da
1
população mundial. Infecção crónica que pode
2,3
progredir para carcinoma hepatocelular. Diabetes
melitus é um dos maiores problemas de saúde
4,5
pública, afetando dez milhões de brasileiros. As
glicosidases, são alvos terapêuticos para o
6
desenvolvimento de fármacos antidiabéticos. Há
diversas classes farmacológicas disponíveis de
agentes quimioterápicos para tratamento do câncer,
mas nenhuma delas mostra-se capaz de erradicar
as células cancerosas sem afetar tecidos normais,
7
causando prejuízo a saúde do paciente. Chalconas
são flavonóides de cadeia aberta, nos quais dois
anéis aromáticos encontram-se ligados por uma
cetona α,β-insaturada, compondo um esqueleto
8
biossintético C6C3C6.
Possuem
propriedades
9
antimicrobianas e antitumoral.
A 50 uM, as chalconas avaliadas exibiram
citotoxicidade
superior a 50% nos hepatócitos
testados. As chalconas contendo um grupo nitro no
anel B e nafitl ou piridil exibiram o efeito citotóxico
mais potente. A 10 uM, nitrochalconas 1 e 2
apresentaram inibição da replicação do HCV de 44 e
80%, respectivamente. A chalcona com um grupo
nitro na posição 4, apresentou 55% de inibição da
amilase e 10% de inibição da maltase.
Objetivos
O presente trabalho objetivo a síntese de vinte e
duas chalconas derivadas de apocinina; Avaliação
da inibição da replicação do vírus da Hepatite C
dessas chalconas em cultura de células Huh- 7
transfectadas
com
replicon
HCVJFH1
subgenômico, utilizando o ensaio de luciferase;
Avaliação da citotoxicidade das chalconas, em
hepatócitos Huh- 7 não transfectados, empregando
o ensaio de MTT; Avaliação do potencial
antidiabético
dessas
chalconas
contra
as
glicosidases ,maltase e amilase.
NO2
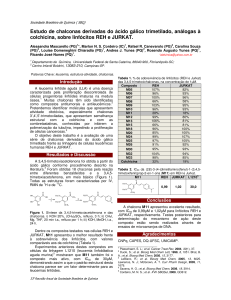
As chalconas foram sintetizadas por reações de
condensação aldólica de Claisen-Schmidt por
catálise básica e ácida, utilizando derivados de
benzaldeídos e apocinina.
O
HO
O
Ar NaOH ou H2SO4
H
O
EtOH
HO
Ar
O
O
Figure 1. Reação Geral da Condensação Aldólica
de Claisen-Schmidt
Os produtos impuros foram submetidos a
Cristalizações, Cromatografia em Coluna de Sílica e
a Cromatografia por Permeação em Gel.
As chalconas foram testadas nas concentrações de
0,08µM 0,4µM, 2µM, 10µM e 50µM.
XXVI Congresso de Iniciação Científica
HO
O
O
NO2
O
O
1
2
Figure 2. Chalconas que apresentaram atividade
contra o HCV e contra a amilase e a maltase.
Conclusões
A nitro chalcona 2 foi capaz de inibir a replicação de
HCV, indicando uma possível ação anti- HCV. A
nitrochalcona 2 inibiu, simultaneamente, a maltase e
a amilase, indicando uma possível ação
antidiabética. Todos os compostos apresentaram
atividade citotóxica potente contra os hepatócitos
testados, apresentando uma possível atividade
antitumoral.
Agradecimentos
CAPES, CNPq, Fapesp, PROPG, FAPERP, PROAP
e Unesp pelo apoio financeiro do presente trabalho.
_______________________________________
1
Ghany, M. G. et al. Hepatology, v. 49, p. 1335-1374, 2009.
Marcelin, P. (1999). The clinical spectrum of the disease. Em:
European Association for the Study of the Liver. Proceedings of the
Internacional Consensus Conference on Hepatitis C. França, 1, 1-6.
3
Thomson, B. J. & Finch, R. G. (2005). Clin Microbiol Infect, 11 (2),
86-94.
4
Skyler, J. S. Journal of Medicinal Chemistry, 47, 4113−4117, 2004.
5
Marcondes, J. A. M. Revista da Faculdade de Ciências Médicas de
Sorocaba,5, 18−26, 2003.
6
De Melo, E. B.; Gomes, A. S.; Carvalho, I. Tetrahedron, 62,
10277−10302, 2006.
7
SALMON, S. E.; SARTORELLI, A. C. Farmacologia básica e clínica.
8. ed. Rio de Janeiro: Guanabara, 2003. cap. 55, p. 803-832.
8
Batovska, D. et al. European Journal of Medicinal Chemistry, 44,
2211−2218, 2009.
9
Nowakowska, Z. Eur. J. Med. Chem., v. 42, p. 125-137, 2007.
2
Material e Métodos
HO