1
Pró-Reitoria de Graduação
Curso de Biomedicina
Trabalho de Conclusão de Curso
DIABETES MELLITUS: DIAGNÓSTICO E AVALIAÇÃO DO
CONTROLE GLICÊMICO
Autora: Isabella Baptista Mariano Hiyane
Orientador: Prof. MSc. Paulo Roberto Sabino
Junior
Brasília - DF
2013
2
ISABELLA BAPTISTA MARIANO HIYANE
DIABETES MELLITUS: DIAGNÓSTICO E AVALIAÇÃO DO
CONTROLE GLICÊMICO
Monografia
apresentada
ao
curso
de
graduação em Biomedicina da Universidade
Católica de Brasília como requisito parcial
para obtenção do título de Bacharel em
Biomedicina.
Orientador: MSc. Paulo Roberto Sabino Junior
Brasília
2013
3
Monografia de autoria de Isabella Baptista Mariano Hiyane, intitulada “Diabetes Mellitus:
Diagnóstico e Avaliação do Controle Glicêmico”, apresentada como requisito parcial para a
obtenção do grau de Bacharel em Biomedicina da Universidade Católica de Brasília, em 05 de
junho de 2013, defendida e aprovada pela banca examinadora abaixo assinada:
____________________________________________________
Prof. MSc. Paulo Roberto Sabino Junior
Orientador
Curso de Biomedicina – UCB
_____________________________________________________
Prof. Esp. Wislon Mendes Pereira
Curso de Farmácia – UCB
_____________________________________________________
Prof. Esp. Simone Cruz Longatti
Curso de Biomedicina– UCB
Brasília
2013
4
RESUMO
Referência: HIYANE, Isabella Baptista Mariano. Diabetes Mellitus: Diagnóstico e Avaliação
do Controle Glicêmico. 2013. 28 páginas. Monografia (Biomedicina) - Universidade Católica
de Brasília, Brasília, 2013.
O Diabetes mellitus é uma patologia crônica, de etiologia multifatorial, de elevada
prevalência, evolução ruim quando tratada de forma inadequada, sendo considerado um
problema de saúde pública mundial. Afeta indivíduos propensos e expostos a fatores de risco,
independente de classe social, idade e etnia. Existem fatores associados com a prevalência do
Diabetes mellitus, entre os quais se destacam: hábitos alimentares inadequados, sedentarismo,
obesidade e perfil lipídico alterado. Cerca de 350 milhões de pessoas apresentam a doença em
todo o mundo. A doença caracteriza-se pela hiperglicemia, onde a glicose circulante, em
concentrações elevadas, participa da glicação não enzimática das proteínas, e essas proteínas
glicadas podem acumular-se nos tecidos, resultando em algumas complicações como a
retinopatia, a nefropatia e doença arterial coronária. O diagnóstico do Diabetes mellitus
depende da demonstração de hiperglicemia. Para o diagnóstico do Diabetes mellitus utilizamse os exames de glicemia de jejum, pós-prandial, curva glicêmica, insulina basal e curva
insulínica. Para o monitoramento da doença dosa-se a Hemoglobina glicada, e em casos
específicos, a Frutosamina. Os exames laboratoriais devem ser solicitados e realizados
adequadamente, sendo primordial a expansão de medidas efetivas para o diagnóstico precoce e
o correto acompanhamento do paciente com Diabetes mellitus. O objetivo do presente
trabalho é apresentar e avaliar a importância do diagnóstico do Diabetes mellitus usando os
diferentes exames de rastreamento, e também ressaltar a relevância dos exames de
monitoramento da doença.
Palavras-chave: Diabetes mellitus. Diagnóstico. Monitoramento. Exames.
5
ABSTRACT
Diabetes mellitus is a chronic disease of multifactorial etiology, high prevalence, evolution
bad when improperly treated, being considered a public health problem worldwide. Affects
individuals prone and exposed to risk factors, regardless of social class, age and ethnicity.
There are factors associated with the prevalence of Diabetes mellitus, among which are: poor
eating habits, sedentary lifestyle, obesity and altered lipid profile. In a few years, about 350
million people will have the disease worldwide. The disease is characterized by
hyperglycemia, where circulating glucose at high concentrations participates in the nonenzymatic glycation of proteins, and these glycated proteins can accumulate in the tissue,
resulting in complications such as retinopathy, nephropathy and coronary artery disease. The
diagnosis of Diabetes mellitus depends on the demonstration of hyperglycemia. For the
diagnosis of Diabetes mellitus using up exams fasting glucose, postprandial glucose curve,
basal insulin and insulin curve. For monitoring disease dosa to glycated hemoglobin, and in
specific cases, the Fructosamine. Laboratory tests should be ordered and carried out properly,
it is paramount to expand effective measures to correct early diagnosis and monitoring of
patients with Diabetes mellitus. The aim of this paper is to present and evaluate the
importance of diagnosis of Diabetes mellitus using different screening tests, and also
emphasize the relevance of tests to monitor the disease.
Keywords: Diabetes mellitus. Diagnosis. Monitoring. Examinations.
6
SUMÁRIO
1. INTRODUÇÃO................................................................................................................7
2. DIABETES MELLITUS – DOENÇA, DIAGNÓSTICO E MONITORAMENTO 9
2.1 EPIDEMIOLOGIA. .............................................................................................
9
2.2 CLASSIFICAÇÃO..............................................................................................
10
2.2.1 Diabetes mellitus I. ..........................................................................................
10
2.2.2 Diabetes mellitus II...........................................................................................
11
2.2.3 Diabetes mellitus gestacional............................................................................
13
2.3 COMPLICAÇÕES DO DIABETES MELLITUS.................................................
13
2.3.1 Cetoacidose diabética......................................................................................
14
2.3.2 Nefropatia.........................................................................................................
14
2.3.3 Retinopatia.........................................................................................................
15
2.3.4 Complicações vasculares................................................................................
16
2.4 DIAGNÓSTICO E MONITORAMENTO.............................................................
18
2.4.1 Exames de Diagnóstico......................................................................................
18
2.4.1.1 Glicemia de jejum.............................................................................................
18
2.4.1.2 Glicemia de 2 horas após sobrecarga................................................................
18
2.4.2 Exames de monitoramento.............................................................................
19
2.4.2.1 Hemoglobina glicada....................................................................................
19
2.4.2.2 Frutosamina..................................................................................................
22
2.5 TRATAMENTO................................................................................................
23
3 CONCLUSÃO......................................................................................................
24
REFERÊNCIAS.............................................................................................................. 26
7
1. INTRODUÇÃO
O termo Diabetes mellitus (DM) aplica-se a um grupo heterogêneo de desordens
crônicas, decorrentes da deficiência e/ou da incapacidade da insulina de exercer
adequadamente seus efeitos no organismo (LIBERATORE, 2008).
O DM é um problema de saúde pública mundial, considerado um dos principais
problemas crônicos que atualmente afeta os indivíduos, e independem de classe social, etnia
e localização geográfica (SBD, 2003).
Vários fatores estão sendo associados com o aumento da prevalência do DM nas
últimas décadas, destacando-se o crescimento da expectativa de vida da população,
estritamente relacionado com a ingestão de gordura saturada, hábitos alimentares
inadequados, obesidade e sedentarismo (WILLETT et al., 2006; RODGERS et al., 2006;
SANTOS, 2006). A modernização e a urbanização progressiva, que consequentemente,
alteram o estilo de vida e os hábitos culturais, têm sido identificadas como fatores
desencadeantes do DM nos indivíduos (CESSE et al., 2009; TOSCANO, 2004; OLIVEIRA
et al, 2009; NAYARAN, 2000).
De acordo com estatísticas realizadas pela Organização Mundial da Saúde, 550
milhões de pessoas deverão apresentar a doença até 2020.
Quanto à mortalidade, Franco relata que, de modo geral, nos atestados de óbitos não
constam o DM como causa principal, aparecendo apenas às complicações decorrentes desta
patologia (CESSE, 2009). No Brasil, a proporção da mortalidade atribuível às doenças não
transmissíveis aumentou significativamente nas últimas décadas, estando o DM entre as dez
principais causas. Contribuindo para esse cenário desfavorável, existe a alta prevalência de
diabéticos não diagnosticados e expressiva proporção de casos com evidência de
complicações ao diagnóstico (BARBOSA, 2001).
Para o diagnóstico do DM utilizam-se os exames de glicemia de jejum, curva
glicêmica, pós-prandial, insulina basal e curva insulínica. Para o monitoramento da doença é
medida a Hemoglobina glicada, e em casos de hemoglobinopatias, por exemplo, utiliza-se a
Frutosamina (SBD, 2009).
Este trabalho tem o objetivo de estudar o DM, patologia de grande impacto na
atualidade, tanto em número de pessoas afetadas quanto nas consequências decorrentes de
suas complicações. Destacando a importância dos exames para diagnóstico e rastreamento
do DM e o monitoramento da doença.
8
Foi confeccionado por revisão de literatura com pesquisa de artigos publicados entre
os anos de 2001 e 2012 usando o portal CAPES como acesso às diversas bases de dados
disponíveis na internet, utilizando as seguintes palavras-chave: diabetes mellitus,
hemoglobina glicada, frutosamina, glicemia de jejum, monitoramento do diabético,
nefropatia, retinopatia, complicações vasculares e tratamento do diabetes.
9
2 DIABETES MELLITUS – DOENÇA, DIAGNÓSTICO E MONITORAMENTO
A síndrome de etiologia múltipla, Diabetes mellitus, é caracterizada pela
hiperglicemia, onde a glicose circulante em concentrações elevadas participa da glicação não
enzimática das proteínas, e essas proteínas glicadas podem acumular-se prejudicando os
tecidos e resultando em doença arterial coronária, retinopatia, nefropatia, catarata, entre
outras complicações. Também está frequentemente acompanhada de dislipidemia,
hipertensão arterial e disfunção arterial (SBD, 2003).
A concentração de glicose no organismo é controlada por um conjunto de vias
metabólicas
associadas
a
alguns
hormônios
hiperglicemiantes
e
um
hormônio
hipoglicemiante, que juntos, garantem a homeostase. O hormônio hipoglicemiante mais
importante é a insulina, que possui um eficiente sistema de controle de secreção. Os
hormônios hiperglicemiantes, tais como; glucagon, cortisol, adrenalina e hormônio do
crescimento, também garantem a oferta adequada de nutrientes aos tecidos (MOTTA, 2009).
A insulina é um hormônio polipeptídico constituído de 51 aminoácidos, secretada
pelas células β das ilhotas pancreáticas, responsável pela regulação da glicose, síntese de
proteínas e formação e armazenamento de triacilgliceróis (MOTTA, 2009).
2.1 EPIDEMIOLOGIA
A ocorrência do DM é um fenômeno universal que afeta países em qualquer dos
estágios de desenvolvimento. Observa-se o aumento da frequência da doença nas estatísticas
de mortalidade, tanto como causa básica quanto associada a doenças renais, cardiovasculares
e cerebrovasculares (FRANCO, 1998).
Números da Organização Mundial da Saúde 2003 estimam que 987.000 mortes em
todo o mundo, no ano de 2002, ocorreram por conta do Diabetes, representando 1,7% da
mortalidade geral.
De acordo com o programa VIGITEL (Vigilância de Fatores de Risco e Proteção para
Doenças Crônicas por Inquérito Telefônico) do Ministério da Saúde em 2007, a ocorrência
média de Diabetes no Brasil na população adulta é de 5,2%, mas a prevalência do Diabetes
atinge 18,6% da população com idade superior a 65 anos, sem distinção de sexo. Em 2008, a
prevalência observada entre idosos na mesma faixa etária foi de 20,7% (Ministério da Saúde,
2009).
10
Quanto à mortalidade, Franco (1998) relata que, de um modo geral, os dados obtidos
mediante atestados de óbito subestimam a importância do Diabetes como causa básica e,
frequentemente, essa enfermidade não aparece nos atestados de óbitos de diabéticos.
2.2 CLASSIFICAÇÃO
De acordo com as Diretrizes da Sociedade Brasileira de Diabetes, a classificação
proposta pela Organização Mundial da Saúde (OMS) e Associação Americana de Diabetes
(ADA) baseia-se na etiologia, classificando-a em quatro classes clínicas, de acordo com o
quadro 1: DM tipo I, DM tipo II, outros tipos específicos de DM e DM gestacional. Existem
duas categorias referidas como pré-diabetes, que são a tolerância à glicose diminuída e
glicemia de jejum alterada, entretanto, não são entidades clínicas, mas fatores de risco para o
desenvolvimento de DM (SBD, 2009).
Quadro 1. Classificação etiológica do DM
Fonte: SBD, 2009.
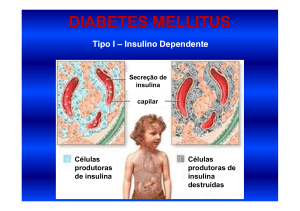
2.2.1 Diabetes mellitus I
O DM tipo I é caracterizado pela destruição das células β das ilhotas pancreáticas de
Langerhans, responsáveis pela produção de insulina, e consequentemente, deficiência desse
hormônio. O DM tipo I é uma doença autoimune e a sequência de eventos que conduzem à
destruição das células β das ilhotas, inicia-se com uma resposta inflamatória. A deficiência
na regulação imunológica permite a resposta autoimune no indivíduo predisposto, gerando a
deficiência de insulina (ABBAS, 2005). Existem casos que não foram comprovados
processos autoimunes, sendo referidos como forma idiopática (MOTTA, 2009). Geralmente
acomete crianças e adolescentes, mas também pode acometer pessoas adultas de forma
11
lentamente progressiva, sendo conhecida como LADA - Doença Autoimune Latente em
Adultos (Ministério da Saúde, 2009).
Os marcadores de autoimunidade são auto anticorpos anti-insulina, antidescarboxilase
do ácido glutâmico (GAD 65) e antitirosina-fosfatases (IA2 e IA2B). Esses anticorpos podem
estar presentes meses ou anos antes do diagnóstico clínico, na fase pré-clínica da doença, e
em até 90% dos indivíduos quando a hiperglicemia é detectada. Além do fator autoimune, o
DM apresenta forte associação com determinados genes do sistema antígeno leucocitário
humano (HLA). A taxa de destruição das células β é variável, sendo mais rápida entre
crianças. O DM idiopático corresponde a uma parcela pequena de pacientes e caracteriza-se
pela ausência de marcadores de autoimunidade (ABBAS, 2005).
2.2.2 Diabetes Mellitus II
O DM tipo II representa 90% dos casos de diabetes, onde a hiperglicemia resulta de
dois mecanismos: resistência periférica a ação da insulina e deficiência da produção de
insulina pelas células β do pâncreas. Tais mecanismos podem estar associados à
predisposição genética, fatores ambientais e comportamentais, destacando-se a obesidade,
dislipidemia, síndrome metabólica e sedentarismo (SBD, 2009).
O DM tipo II pode ocorrer em qualquer faixa etária, mas geralmente diagnostica-se
após os 40 anos (SBD, 2009).
A obesidade e o sedentarismo são os principais fatores relacionados ao
desenvolvimento de DM tipo II, como mostra a Figura 1, que podem ser induzidos por
adipocinas, ácidos graxos livres e processos inflamatórios crônicos no tecido adiposo, que
resultam na resistência à insulina. As células β hipersecretam a insulina ocasionando o DM
tipo II (KUMAR et al., 2010).
12
Figura 1 – Influência do sobrepeso e obesidade na ocorrência do Diabetes mellitus
Fonte: CERIELLO, 2004.
O diagnóstico dos distúrbios no metabolismo da glicose depende da demonstração de
alterações na concentração de glicose no sangue (GAVIN, 2001).
A regulação da glicemia depende basicamente da ação de dois hormônios produzidos
nas ilhotas de Langerhans no pâncreas: a insulina e o glucagon, sendo os responsáveis pela
homeostasia da glicose. Em pessoas saudáveis, a ação do glucagon é de estimular a produção
de glicose pelo fígado e a ação da insulina é de bloquear essa produção e aumentar a captação
da glicose pelos tecidos periféricos insulino-sensíveis, como o músculo e o tecido adiposo.
No estado normal de jejum, pequenos aumentos na glicemia levam a supressão da produção
de glucagon e aumento da produção de insulina. No jejum e no estado pré-prandial, o
consumo de glicose é representado pelo sistema nervoso central (50 %), músculo (25 %) e
pelos tecidos esplâncnicos (25 %) (GAVIN, 2001; GELONEZE et al., 2006).
O estado de jejum normal é caracterizado por níveis mais elevados de glucagon e
baixos de insulina, em conjunto com níveis fisiológicos de hormônios gastrointestinais como
13
o polipeptídeo inibitório gástrico (GIP) e o peptídeo semelhante ao glucagon (GLP-1). O
resultado desse equilíbrio é uma produção aumentada de glicose pelo fígado e pelo rim,
redução na captação periférica de glicose e aumento na proteólise muscular e na lipólise
adipocitária. Essas mudanças sincronizadas mantém a glicemia entre 70 e 100 mg/dL, e os
triglicérides abaixo de 125 mg/dL. Indivíduos com diabetes tipo II apresentam redução na
ação e produção de insulina, resultando em aumento na glicemia, ácidos graxos livres,
triglicérides e nos aminoácidos no estado de jejum (GAVIN, 2001; LEBOVITZ, 2001).
2.2.3 Diabetes mellitus gestacional
O Diabetes mellitus gestacional caracteriza-se pela hiperglicemia no período de
gravidez, podendo a mãe posteriormente vir a desenvolver o DM tipo II. (SBD, 2006).
Semelhante ao Diabetes mellitus II, o Diabetes mellitus gestacional associa-se tanto a
resistência à insulina quanto à diminuição da função das células beta (SBD, 2009).
2.3 COMPLICAÇÕES DO DIABETES MELLITUS
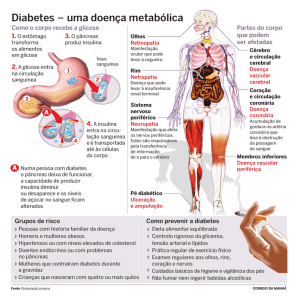
Ao longo dos anos, a hiperglicemia prolongada pode ocasionar lesões orgânicas
extensas e irreversíveis, como mostra a Figura 2, afetando órgãos e sistemas.
Os níveis de glicose sanguínea elevados são extremamente tóxicos ao organismo
devido à glicação das proteínas, hiperosmolalidade e pelo aumento do sorbitol presente dentro
das células (SBD, 2009).
Figura 2. Complicações decorrentes do Diabetes mellitus.
Fonte: SBD, 2009.
14
2.3.1 Cetoacidose diabética
A cetoacidose diabética é uma das principais complicações decorrentes da evolução do
Diabetes mellitus tipo I e II (KITABCHI, 2004).
Na cetoacidose diabética há redução de insulina circulante e liberação excessiva de
hormônios contra reguladores, como o glucagon, as catecolaminas, o hormônio do
crescimento e o cortisol. Essas alterações hormonais geram o aumento da produção hepática e
renal de glicose e diminuição da sua captação nos tecidos periféricos sensíveis à insulina,
resultando em hiperglicemia. Existem três mecanismos envolvidos nesse processo; a ativação
da gliconeogênese, da glicogenólise e redução do uso de glicose periférica (NEWTON, 2004).
A deficiência de insulina associada com os hormônios contra reguladores resulta na
liberação de ácidos graxos livres do tecido adiposo (lipólise), que, no fígado, são oxidados em
corpos cetônicos (ácidos beta-hidroxibutírico e ácido acetoacético), gerando cetonemia e
acidose metabólica (KITABCHI, 2006).
A avaliação laboratorial de pacientes com cetoacidose diabética deve incluir a
determinação de glicose plasmática, análise de eletrólitos, uréia, creatinina, osmolalidade,
análise urinária, cetonúria, gasometria, hemograma e eletrocardiograma. Os critérios
diagnósticos para este quadro são: glicemia > 250mg/dl; pH arterial < 7,3; bicarbonato sérico
< 15mEq/l e graus variáveis de cetonemia e cetonúria. O sódio sérico geralmente é baixo
devido à transferência osmótica de líquidos do meio intracelular para o meio extracelular
(SBD, 2006).
A cetoacidose diabética pode levar o paciente ao coma, e até mesmo, a óbito
(KITABCHI, 2006).
2.3.2 Nefropatia
A nefropatia diabética acomete pacientes com Diabetes mellitus, sendo uma das
maiores causas de morbidade e mortalidade. Essa complicação é caracterizada por lesões
glomerulares que comprometem o sistema renal (ABBAS, 2005).
O DM é uma das causas mais comuns de Insuficiência Renal Crônica no mundo,
sendo responsável por aproximadamente 45% dos casos de terapia de substituição renal nos
Estados Unidos (FINNE, 2005). Segundo o censo brasileiro de diálise, no Brasil as causas
mais frequentes de IRC são hipertensão arterial sistêmica (36%), seguida do Diabetes Mellitus
(26%).
15
A presença de pequenas quantidades de albumina na urina representa o estágio inicial
da nefropatia diabética, sendo a albumina utilizada como marcador de comprometimento
renal. O diagnóstico pode ser feito utilizando-se diferentes tipos de coleta de urina, mas deve
iniciar medindo-se, primeiramente, a albumina. (SBD, 2006).
2.3.3 Retinopatia
A retinopatia diabética é uma complicação comum do DM e está presente, em algum
nível nas pessoas com mais de 15 anos de evolução da doença. É considerada a principal
causa de cegueira legal em adultos na idade produtiva (BARBER, 2003).
Um dos sinais clínicos mais precocemente detectáveis é o aumento da permeabilidade
vascular, devido à quebra da barreira hemato-retiniana, que causa o edema macular. Mais
tardiamente, microaneurismas, exsudatos e, finalmente, proliferação vascular. Desses achados
clínicos, o edema macular é o mais correlacionado com o grau de perda visual (ANTONETTI,
2006).
A classificação da retinopatia diabética é baseada na observação direta da retina,
agrupando as alterações e relacionando com sua chance de evoluir para cegueira. Essa
classificação (quadro 2) foi criada durante o Congresso Mundial de Oftalmologia, realizada
em 2002 (SBD, 2009).
Quadro 2. Classificação da retinopatia diabética
Fonte: SBD, 2009.
16
2.3.4 Complicações vasculares
Embora o DM seja um distúrbio metabólico, atualmente está sendo considerado um
fator de risco para doenças vasculares. A doença arterial coronariana é uma das principais
causas de morte em pacientes diabéticos. O risco aumentado de complicações
cardiovasculares no paciente diabético pode ser decorrente dos fatores de risco, tais como
hipertensão, tabagismo, dislipidemia, obesidade, mas também pode ser o somatório de todos
esses fatores (SBD, 2009).
A hiperglicemia é um dos fatores que cursam para a macroangiopatia. Na gênese da
doença cardiovascular também participam outras anormalidades como a hipertensão arterial
(GROSS, 2003).
No DM, os vários sistemas que mantêm a homeostase e que garantem a estabilidade
dos fatores pró-trombóticos e mecanismos fibrinolíticos se rompem, comprometendo a
integridade e funcionalidade dos vasos, favorecendo a um estado pró-trombótico
(MUDALIARS, 2004). A aterosclerose acelerada observada nos diabéticos é atribuída, em
parte, a hiper-reatividade de plaquetas (GABBIANELLI, 2003). A hiper-reatividade
plaquetária está relacionada com a indução de elevação dos níveis séricos de fibrinogênio.
Pacientes com níveis de fibrinogênio séricos elevados apresentam um risco três vezes maior
de eventos coronarianos do que aqueles com fibrinogênio normal (PALMIERI et al., 2003).
Problemas vasculares associados com o DM, se não tratados e controlados, causam
consequências irreversíveis como necrose, amputação de membros entre outras complicações
vasculares (SBD, 2009).
2.4 DIAGNÓSTICO E MONITORAMENTO
O diagnóstico do DM depende da demonstração e avaliação da glicemia. Os
parâmetros laboratoriais utilizados para nortear as decisões terapêuticas, voltadas ao controle
glicêmico do DM, possuem vantagens e certas limitações (OLIVEIRA, 2005).
O grau de controle glicêmico no paciente diabético tem sido comumente avaliado
através de medidas da glicemia de jejum, glicemia após sobrecarga oral de glicose e/ou GPP
e através da determinação da Hemoglobina glicada. A glicemia de jejum é a mais utilizada na
avaliação do controle glicêmico; reflete os valores mais baixos de glicemia do dia. Uma de
suas principais limitações como parâmetro de controle é que esta não aumenta com a idade e,
17
por isso, torna-se menos sensível ainda para detectar alterações do metabolismo glicídico em
indivíduos com mais de 65 anos (TUOMILEHTO et al., 2002).
Na prática clínica, o diagnóstico e a avaliação do DM são realizados mediante alguns
critérios laboratoriais. Cada um com seu significado clínico específico, mas a análise
complementar entre eles é essencial para o paciente. Os testes de diagnóstico refletem o nível
glicêmico atual e instantâneo no momento exato do teste, enquanto que os testes de
monitoramento indicam a glicemia média pregressa dos últimos meses, como mostra a Figura
3 (SBD, 2009).
Figura 3. Testes tradicionais para avaliar glicemia
Fonte: SBD, 2009.
Segundo a Sociedade Brasileira de Diabetes são três os critérios aceitos para o
diagnóstico de DM; sintomas de poliúria, polidipsia e perda ponderal acrescidos de glicemia
casual acima de 200 mg/dL - compreende-se por glicemia casual aquela realizada a qualquer
hora do dia, independentemente do horário das refeições; ou glicemia de jejum igual ou
superior a 126 mg/dL em duas dosagens e dias alternados; ou glicemia de duas horas póssobrecarga de 75 g de glicose acima de 200 mg/dL. No quadro 3, seguem os valores
recomendados para a glicemia normal, tolerância à glicose diminuída e DM.
18
Quadro 3. Valores de glicose plasmática (mg/dL)
Fonte: SBD, 2009.
2.4.1 Exames de Diagnóstico
2.4.1.1 Glicemia de jejum
A determinação da glicemia é realizada com o paciente em jejum, de no período
máximo de 8 horas. Resultados dentro do valor recomendado, ≤ 100 mg/dL, não exclui o
diagnóstico de distúrbios metabólicos. A glicemia de jejum é a mais utilizada na avaliação do
controle glicêmico; reflete os valores mais baixos de glicemia do dia, sofre a menor
variabilidade. Uma de suas principais limitações como parâmetro de controle é que esta não
aumenta com a idade e, por isso, torna-se menos sensível ainda para detectar alterações do
metabolismo glicídico em indivíduos com mais de 65 anos (TUOMILEHTO, 2002).
2.4.1.2 Glicemia de 2 horas após sobrecarga
Para a realização desse teste, algumas considerações são importantes, entre elas, o
período de jejum de 8 horas, ingestão de pelo menos 150 g de carboidratos nos 3 dias que
antecedem a realização do teste. O paciente deve ingerir 75 g de glicose anidra ou 82,5 g de
glicose monoidratada dissolvidos em 250 a 300 mL de água em no máximo 5 minutos.
Normalmente após essa sobrecarga, a glicemia tende a retornar ao estado normal dentro de 2
horas. O valor recomendado é < 140 mg/dL (MOTTA, 2009).
A glicemia 2 horas pós-sobrecarga e a glicemia pós-prandial (GPP) medem os picos
atingidos em resposta, respectivamente, ao teste com 75 g de glicose oral (TOTG) ou à
19
refeição e têm sido consideradas equivalentes no que diz respeito ao seu significado
fisiopatológico. Ambas tendem a aumentar com a idade, de tal modo que este comportamento
pode ter implicações diagnósticas em indivíduos com faixa etária mais avançada
(TUOMILEHTO, 2002).
Existem alguns interferentes que elevam falsamente os resultados, entre eles estão o
paracetamol, ácido acetilsalicílico, ácido ascórbico, ácido etacrínico, ácido nalidíxico, ácido
nicotínico, adrenalina, benzodiazepínicos, cafeína, carbonato de lítio, cimetidina, clonidina,
corticoesteróides, dopamina, esteroides anabólicos, estrogênios, etanol, fenitoína, furosemida,
levodopa, tiazídicos, ECA, haloperidol, hipoglicemiantes orais, insulina, isoniazida, maconha,
nitrazepan, pentamida, propranolol (em diabéticos), quinidinas, salicilatos, sulfonamidas,
sulfonilureias (MOTTA, 2009).
2.4.2 Exames de monitoramento
2.4.2.1 Hemoglobina glicada
Refere-se a um conjunto de substâncias formadas com base em reações entre a
Hemoglobina A (HbA) e alguns açúcares. O processo de “glicação” de proteínas envolve uma
ligação não enzimática e permanente com açúcares redutores, como a glicose. Em termos de
avaliação do controle do DM, a fração HbA1c é a mais importante e a mais estudada, na qual
há um resíduo de glicose ligado ao grupo amino terminal (resíduo de valina) de uma ou de
ambas as cadeias beta da HbA (MOTTA, 2009).
Por esta razão, obedecendo à nomenclatura química, o termo correto é hemoglobina
glicada, devendo ser abandonado o termo hemoglobina glicosilada. A glicação ocorrerá em
maior ou menor grau, conforme o nível de glicemia. A hemoglobina glicada permanece
dentro das hemácias e a sua concentração, num determinado momento, dependerá,
basicamente, da taxa glicêmica média e da meia-vida das hemácias, que é de
aproximadamente 60 a 120 dias (ANDRIOLO, 2008; SACKS, 2006; SUMITA, 2006).
Os níveis de glicose sanguínea elevados são tóxicos ao organismo, através de três
mecanismos diferentes: mediante a promoção da glicação de proteínas, através da
hiperosmolaridade e por meio do aumento dos níveis de sorbitol dentro da célula. É através
desse processo de glicação das proteínas que a glicose sanguínea se liga à molécula de
hemoglobina, conforme mostra a Figura 4.
20
Figura 4. Moléculas de glicose ligadas à molécula de hemoglobina, formando a hemoglobina glicada.
Fonte: SBD, 2009
A quantidade de glicose ligada à hemoglobina é diretamente proporcional à
concentração média de glicose no sangue. Uma vez que os eritrócitos têm um tempo de vida
de aproximadamente 120 dias, a medida da quantidade de glicose ligada à hemoglobina pode
fornecer uma avaliação do controle glicêmico médio no período de 60 a 120 dias antes do
exame (SBD, 2009).
Tradicionalmente, a hemoglobina glicada tem sido considerada como representativa da
média ponderada global das glicemias médias diárias (incluindo glicemias de jejum e pósprandial) durante os últimos dois a quatro meses. Na verdade, a glicação da hemoglobina
ocorre ao longo de todo o período de vida do glóbulo vermelho, que é de aproximadamente
120 dias. Porém, dentro destes 120 dias, a glicemia recente é a que mais influencia o valor da
hemoglobina glicada. De fato, os modelos teóricos e os estudos clínicos sugerem que um
paciente em controle estável apresentará 50% de sua hemoglobina glicada formada no mês
precedente ao exame, 25% no mês anterior a este e os 25% remanescentes no terceiro ou
quarto mês antes do exame (SBD, 2009).
A hemoglobina glicada deve ser medida pelo menos duas vezes ao ano em todos os
pacientes com DM, para documentação do grau de controle glicêmico. E deve ser realizada
quatro vezes ao ano (a cada 3 meses) para pacientes que se submeterem a alterações do
esquema terapêutico ou que não estejam atingindo os objetivos recomendados com o
tratamento vigente (MOTTA, 2009).
De acordo com as Diretrizes da Sociedade Brasileira de Diabetes, níveis de
hemoglobina glicada acima de 7% estão associados a um risco progressivamente maior de
complicações crônicas.
21
A hemoglobina glicada pode ser determinada por três categorias de métodos baseados
no modo como os componentes glicados e não glicados são separados. São separados de
acordo com diferenças de carga (cromatografia de troca iônica, cromatografia líquida de alto
desempenho, eletroforese, focalização isoelétrica), reatividade química (colorimetria e
espectrofotometria) e diferenças estruturais (cromatografia por afinidade e imunoensaio)
(MOTTA, 2009).
a) Cromatografia de troca iônica: A hemoglobina não glicada apresenta uma carga positiva,
ajustando-se o pH do meio reacional, quando comparada à hemoglobina glicada, o que a faz
interagir mais com uma coluna catiônica, que possui carga negativa. O fluxo de um tampão
adequado na resina permite eluir a fração glicada, separando-a da não glicada pela carga da
molécula de hemoglobina.
b) Cromatografia de afinidade: A cromatografia de afinidade utiliza derivados do ácido
borônico, como o ácido m-aminofenilborônico, imobilizados em uma resina. O ácido
borônico reage com cis dióis (compostos que apresentam duas hidroxilas no mesmo lado,
como a molécula de glicose); portanto, a separação das frações glicada e não glicada se dá
pela porção açúcar, ficando a hemoglobina glicada retida na coluna, enquanto a não glicada é
eluída da mesma pelo fluxo de um tampão. Este princípio quantifica a hemoglobina glicada
total.
c) Eletroforese em gel de agarose: A separação eletroforética da hemoglobina A1 está baseada na
capacidade do N-terminal livre da hemoglobina não glicada de interagir com grupos
carregados negativamente. Esse método não é especifico para hemoglobina glicada.
d) Cromatografia líquida de alta pressão (HPLC): A hemoglobina não glicada apresenta carga
positiva, ajustando-se ao pH do meio reacional, quando comparada à hemoglobina glicada, o
que a faz interagir mais intensamente com uma coluna de carga negativa. O uso de um tampão
adequado de resina permite separar a fração glicada da não glicada e, desse modo, quantificála, diferindo da troca iônica pela passagem dos tampões sob pressão, o que acelera a corrida e
o fracionamento (MOTTA, 2009).
Recentemente, a partir de 2011 a WHO publicou estudos que estabelecem valores de
Hemoglobina glicada também para diagnóstico do Diabetes mellitus. Pacientes com
resultados acima de 6,5 teriam classificação como portador de Diabetes. Esse critério ainda
não foi retificado pela SBD e o exame não é usado com esta finalidade no Brasil. Porém,
existem interferentes que elevam falsamente o exame, tais como; anemia por carência de
ferro, vitamina B 12 ou ácido fólico, aumento de triglicerídeos, bilirrubinas e ureia e presença
de hemoglobinas anormais ou variantes (hemoglobinas S,C). Resultados falsamente
22
reduzidos: anemia hemolítica ou estados hemorrágicos, presença de grandes quantidades de
vitaminas C e E no sangue e presença de hemoglobinas anormais ou variantes (hemoglobinas
S, C) (MOTTA, 2009).
Atualmente, a hemoglobina glicada é o exame mais importante no controle do
Diabetes mellitus tipos I e II e na avaliação de risco das complicações crônicas (SBD, 2009).
2.4.2.2 Frutosamina
É o nome genérico das proteínas cetoaminas. A frutosamina é formada pela união não
enzimática de glicose a grupos amino de proteínas diferentes da hemoglobina (proteínas
séricas, proteínas de membrana e cristalino de lentes). Reflete o controle glicêmico de curto
prazo, das últimas 4 a 6 semanas, meia-vida das proteínas. A utilidade clínica do teste de
frutosamina não está bem estabelecida, sendo esse recurso, geralmente recomendado em
situações nas quais o teste de hemoglobina glicada apresente algum problema. Não há estudos
demonstrando a utilidade do teste como marcador do desenvolvimento de complicações
relacionadas ao diabetes (MOTTA, 2009).
O teste é sensível a variações nos teores das proteínas séricas, isto é, pacientes
exclusivamente nutridos por via parenteral apresentam nítidas variações na concentração da
frutosamina, apesar de glicemia normal estável. Há aumento de 1,3% da frutosamina
plasmática para cada 0,3 g/dL de aumento nos teores de proteinemia. Estados
hipoproteinêmicos (albumina sérica < 3,0 g/dL) podem produzir resultados falsamente baixos
para os níveis de frutosamina sérica. Valores recomendados: 1,8 a 2,8 mmol/L (MOTTA,
2009).
Para melhor compreensão do monitoramento do paciente diabético, segue-se uma
breve explanação sobre o tratamento e manutenção dos níveis de glicemia.
23
2.5 TRATAMENTO
O objetivo do tratamento do Diabetes mellitus é controlar os níveis de glicose no
sangue que se refletirá na redução da hemoglobina glicada e frutosamina. Os agentes
antidiabéticos orais são classificados de acordo com suas funções no organismo. Há aqueles
que incrementam a secreção pancreática de insulina (sulfonilureias e glinidas), os que
reduzem a velocidade de absorção de glicídios (inibidores das alfaglicosidades), os que
reduzem a produção hepática de glicose (biguanidas) e os que aumentam a utilização
periférica da glicose (glitazonas) (SBD, 2009).
Para a escolha do medicamento os seguintes aspectos devem ser analisados; valores
das glicemias de jejum, pós-prandial e o valor da Hemoglobina glicada, observando ainda, a
idade, o peso, patologias associadas, complicações decorrentes do Diabetes mellitus e
possíveis interações medicamentosas (SBD, 2009).
Pacientes diagnosticados precocemente recomenda-se mudanças no estilo de vida
associadas ao uso de metformina. Glicemia inferior a 150 mg/dL estão indicados
medicamentos que não promovam aumento na secreção de insulina. Os agentes antihiperglicemiantes e as gliptinas são recomendados aos pacientes obesos, pois não favorecem o
ganho de peso (SBD, 2009).
Pacientes com glicemia de jejum normal ou próximo do normal, mas coma
Hemoglobina glicada elevada, indica-se os anti-hiperglicemiantes, metformina ou glitazonas
(SBD, 2009).
24
3 CONCLUSÃO
O Diabetes mellitus se caracteriza, atualmente como uma epidemia de prognóstico
ruim quando não tratada de forma correta. A modernidade e a adoção de estilos de vida pouco
saudáveis estão relacionados com a incidência e prevalência do Diabetes.
O DM apresenta altas taxas de morbidade e mortalidade decorrentes das complicações
da doença. Acarreta problemas à sociedade em decorrência da perda de produtividade no
trabalho, aposentadoria antes do previsto e mortalidade prematura. Portadores do DM
apresentam um risco maior de desenvolverem complicações na microcirculação e na
macrocirculação, afetando a visão, os rins e outros órgãos e sistemas.
O DM tipo II é responsável por 85-90% de todos os casos do Diabetes, sendo
diretamente relacionados a diversos fatores de riscos, como sobrepeso, obesidade e
sedentarismo.
Recentemente a comunidade médica reconheceu a utilidade clínica da Hemoglobina
glicada, como exame de diagnóstico da doença, antes utilizada apenas para o monitoramento
do Diabetes mellitus. Em 2009, algumas das principais associações, entre elas a American
Diabetes Association (ADA), aceitaram o teste da Hemoglobina glicada para o diagnóstico do
Diabetes e também como identificação de pacientes em risco de desenvolverem a doença.
Comprovaram que a Hemoglobina glicada sofre poucas interferências comparando-se com os
outros exames de diagnóstico.
A principal vantagem da hemoglobina glicada é que pode ser dosada em qualquer
momento e não requer nenhuma preparação do paciente, ao contrário dos outros exames de
diagnóstico. Esse critério aceito mundialmente, já poderia ter sido aceito pela SBD, que ainda
não o fez. Há que se compreender, porém, que o exame de Hemoglobina glicada que
apresenta vantagens, aquele dosado por HPLC, tem custo ainda muito elevado e não pode ser
adotado pelos serviços públicos de saúde, além de não esta disponível em todos os lugares
devido à necessidade de equipamento específico.
A grandeza dessa epidemia requer, ainda, ações que ampliem a triagem para a doença,
com a utilização de métodos que possibilitem maior alcance da população e que auxiliem no
diagnóstico presumido precoce, ainda que seja necessária a confirmação posterior por exames
mais elaborados.
O uso de equipamentos portáteis com tiras reativas de química seca para dosagem de
glicemia capilar é uma ferramenta poderosa para triar a população e detectar novos casos de
Diabetes e de intolerância à glicose, a serem confirmados em laboratório clínico.
25
O presente trabalho buscou destacar a importância de estabelecer o diagnóstico do DM
e instituir terapêutica adequada, atingindo metas recomendadas no intuito de minimizar os
efeitos deletérios decorrentes desta patologia. A partir dos conhecimentos adquiridos,
entende-se a importância dos profissionais de saúde no diagnóstico e monitoramento do DM e
a necessidade de uma análise sensata da clínica do paciente associada a exames que possuem
sensibilidade e especificidade para detectá-lo e monitorá-lo.
Analisando a conjuntura da saúde pública do Brasil, pode-se inferir que o exame mais
apropriado para o diagnóstico e rastreamento do DM, ainda é a glicemia de jejum, levando-se
em consideração o método utilizado e o baixo custo. Em relação ao exame de monitoramento,
pode-se determinar a hemoglobina glicada utilizando métodos que possuem custos menos
elevados quando comparados com a metodologia HPLC, como por exemplo, o turbidimétrico.
Finalmente, os critérios para diagnóstico do DM estabelecidos em consenso pela SBD,
sempre revisados e atualizados, são claros e demonstram-se adequados, restando incluir a
dosagem de hemoglobina glicada como método diagnóstico.
26
REFERÊNCIAS
ABBAS, A. K.; LICHITMA, A. H. Imunologia celular e molecular. 5ª ed. Rio de Janeiro:
Elsevier, 2005.
ANDRIOLO, A.; VIEIRA, J. G. H. Diagnóstico e acompanhamento laboratorial do
diabetes mellitus. In: ANDRIOLO, A. (org.). Guias de medicina ambulatorial e
hospitalar/medicina laboratorial. 1. ed. São Paulo: Manole, 2008. p. 37-42.
ANTONETTI, D.A, Diabetic Retinopathy Center Group. Diabetic retinopathy: seeing
beyond glucose-induced microvascular disease. Diabetes. 2006; 55(9):2401-11.
BARBOSA, R. et al. Campanha nacional de detecção de casos suspeitos de diabetes
mellitus no Brasil: relatório preliminar. Rev. Panam Salud Publica 2001; 10:324-7.
BARBER, A. J. A new view of diabetic retinopathy: a neurodegenerative disease of the
eye. Prog Neuropsychopharmacol Biol Psychiatry 2003.
BRASIL. Secretaria de Políticas Públicas. Plano de reorganização da atenção à
hipertensão arterial e ao diabetes mellitus. Rev Saúde Pública. 2001;35(6):585-8.
BRASIL. Ministério da Saúde. Secretaria de Atenção à Saúde. Departamento de Atenção
Básica. Diabetes mellitus. Brasília: Ministério da Saúde, 2006. 64 p. il.- (Cadernos de
Atenção Básica, n. 16) (Série A. Normas e Manuais técnicos) ISBN 85-334-1183-9.
CESSE, E. A. P. et al . Tendência da mortalidade por diabetes melito no Brasil: 1950 a
2000. Arq Bras Endocrinol Metab, São Paulo, v. 53, n. 6, Aug. 2009.
Diretrizes da Sociedade Brasileira de Diabetes 2009/ Sociedade Brasileira de Diabetes. –[3.
ed.]- Itapevi, SP: A. Araújo Silva Farmacêutica, 2009. 400 p.:il.
Diretrizes da Sociedade Brasileira de Diabetes 2006. Tratamento e acompanhamento do
Diabetes mellitus. 2006.
FINNE P, REUNANEN A, STENMAN S, et al. Incidence of end-stage renal disease in
patients with type 1 diabetes. JAMA 2005; 294:1782.
FRANCO. Epidemiologia do diabetes mellitus. In: Lessa I. O adulto brasileiro e as doenças
da modernidade: epidemiologia das doenças crônicas não-transmissíveis. São Paulo/Rio
de Janeiro: Hucitec/Abrasco; 1998. p. 123-37.
GABBIANELLI P, et al. A new method to evaluate spontaneous platelet aggregation in
type 2 diabetes by cell facts. Clinica Chimica Acta. 2003; 329;95-102.
GAVIN III JR. Pathophysiologic mechanisms of postprandial hyperglycemia. Am J
Cardiol 2001; 88(suppl 1): 4H-8H.
27
GELONEZE, B. et al.. Hiperglicemia pós-prandial: tratamento do seu potencial
aterogênico. Arq. Bras. Cardiol., São Paulo, v. 87, n. 5, Nov. 2006 .
GROSS, J.L. Glicemia pós-prandial. Reunião: Discussão de Consensos da Sociedade
Brasileira de Diabetes. Arq Bras Endocrinol Metab vol 47 nº 6 Dezembro 2003.
KITABCHI, A.E. Hyperglycemic Crises in diabets. Diabetes Care. 2004; 27 (suppl. 1): 594102.
KITABCHI, A.E. Hyperglycemic Crises in adult patients with diabetes. Diabetes Care.
2006; 29 (12): 2739-48.
KUMAR,V. et al. Robbins & Cotran:Patologia -Bases Patológicas das Doenças. 7ª Ed.
Rio de Janeiro: Elsevier, 2010.
LEBOVITZ, H. E. A Symposium: Managing the atherogenic potential of the
postprandial state. Am J Cardiol 2001; 88(Suppl 1): 1H-3H.
LIBERATORE, R. et al . Prevalência de obesidade em crianças e adolescentes com
diabetes melito tipo 1. Rev. paul. pediatr. São Paulo, v. 26, n. 2, Junho de 2008.
MINISTÉRIO DA SAÚDE. Dia mundial do diabetes. Dados estatísticos no Brasil 2009.
Disponível em http://portal.saude.gov.br/portal/saude/area.cfm?id_area=1457. Acesso, março
de 2013.
MOTTA, V. T. Bioquímica clínica para o laboratório: princípios e interpretações. 5. Ed.
São Paulo, 2009.
MUDALIARS, S. Intense management of diabetes mellitus: role of glicose control and
antiplatelet agentes. Journal of Clinical Pharmacology. 2004; 44: 414-22.
NAYARAN, K. M. et al. Diabetes: a common, growing, serious, costly and potentially
preventable public health problem. Diabetes Res Clin Pract 2000; 50 Suppl 2:S77-84.
NEWTON, C.A. Diabetic Ketoacidosis in type 1 and type 2 diabetes mellitus. Arch Intern
Med. 2004; 164: 1925-31.
OLIVEIRA, A. F. et al . Global burden of disease attributable to diabetes mellitus in
Brazil. Cad. Saúde Pública, Rio de Janeiro, v. 25, n. 6, June 2009.
OLIVEIRA, C.H.M.C. de et al . Monitorização contínua de glicose: análise crítica baseada
em experiência ao longo de um ano. Arq Bras Endocrinol Metab, São Paulo, v. 49, n. 6,
Dec. 2005.
PALMIERI, V. et al. Relation of fibrinogen to cardiovascular events is independent of
preclinical cardiovascular disease: the Strong Heart Study. Am Heart J 2003;145(3):467-74.
28
RODGERS, A. The growing burden of risk from high blood pressure, cholesterol, and
bodyweight. In: Jamison DT, Breman JG, Measham AR, Alleyne G, Claeson M, Evans DB,
et al., editors. Disease control priorities in developing countries. New York: World
Bank/Oxford University Press; 2006. p. 851-68.
SACKS, D. B. Carbohydrates. Tietz textbook of clinical chemistry and molecular
diagnostics. St. Louis: Elsevier Saunders, 2006. p. 837-901.
SANTOS, A. M. Diagnóstico do diabete melito, drogas utilizadas no tratamento e terapia
combinada. In: Luna RL, Sabra A, organizadores. Medicina de família: saúde do adulto e do
idoso. Rio de Janeiro: Editora Guanabara Koogan; 2006. p. 849-57.
Sociedade Brasileira de Diabetes. Consenso Brasileiro sobre Diabetes 2002: diagnóstico e
classificação do diabetes melito e tratamento do diabetes melito tipo 2. Rio de Janeiro:
Diagraphic Editora; 2003.
SUMITA, N. M.; ANDRIOLO, A. Importância da determinação da hemoglobina glicada
no monitoramento do paciente portador de diabetes mellitus. J Bras Patol Med Lab, v. 42,
editorial, 2006.
TOSCANO, C. M. As campanhas nacionais para detecção das doenças crônicas nãotransmissíveis: diabetes e hipertensão arterial. Ciênc Saúde Coletiva 2004; 9:885-95.
TUOMILEHTO J, et al. Prevention of type 2 diabetes mellitus by changes in lifestyle
among subjects with impair red glucose tolerance. N Engl J Med. 2002.
WILLETT, W.C. Prevention of chronic disease by means of diet and lifestyle changes. In:
Jamison DT, Breman JG, Measham AR, Alleyne G, Claeson M, Evans DB, et al., editors.
Disease control priorities in developing countries. New York: World Bank/Oxford University
Press; 2006. p. 833-50.
World Health Organization. The World Health Report 2002: reducing risks, promoting
healthy life. Geneva: World Health Organization; 2002.
World Health Organization. The World Health Report 2003. Geneva:World Health
Organization; 2003.