Fundamentos de Química Orgânica
Professor Nelson Luís de Campos Domingues
Curso: Química Bacharelado/2009
Lista de Exercícios 2
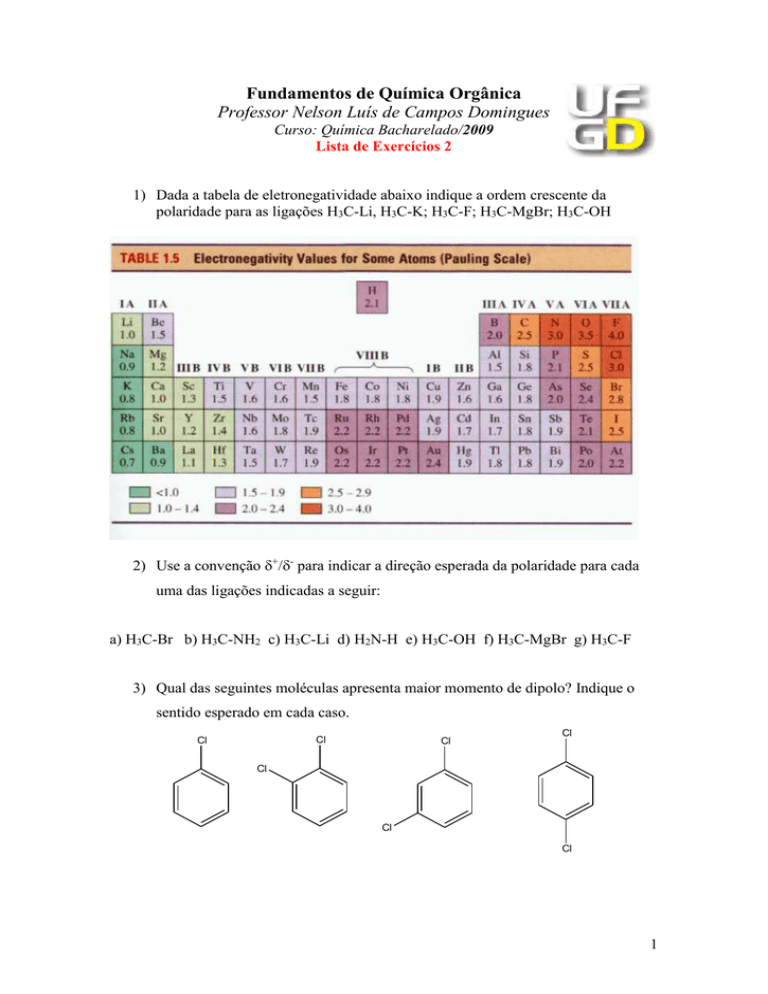
1) Dada a tabela de eletronegatividade abaixo indique a ordem crescente da
polaridade para as ligações H3C-Li, H3C-K; H3C-F; H3C-MgBr; H3C-OH
2) Use a convenção +/- para indicar a direção esperada da polaridade para cada
uma das ligações indicadas a seguir:
a) H3C-Br b) H3C-NH2 c) H3C-Li d) H2N-H e) H3C-OH f) H3C-MgBr g) H3C-F
3) Qual das seguintes moléculas apresenta maior momento de dipolo? Indique o
sentido esperado em cada caso.
Cl
Cl
Cl
Cl
Cl
Cl
Cl
1
4) O fosgênio Cl2C=O tem um momento de dipolo menor que o formaldeído,
CH2C=O, embora contenha átomos eletronegativos de cloro no lugar dos átomos
de hidrogênio. Explique
5) Calcule as cargas formais para os átomos destacados:
a) (CH3)2OBF3 b) H2C-N≡N c) H2C=N=N d) O=O-O
6) Qual dos seguintes pares de estruturas a seguir representa formas de
ressonância?
O
A)
B)
e
O
O
e
O
O
O
C)
e
D)
e
7) Os alcoóis podem reagir tanto com ácidos fracos quanto com bases fracas da
mesma maneira da água. Mostre a reação do álcool metílico CH3OH com um
ácido forte como o HCl e com uma base forte Na+ -NH2.
8) O hidrogênio O-H no ácido acético é muito mais ácido que qualquer hidrogênio
C-H. Explique.
O
H
C
C
H
H
H
O
Ácido acético.
2
9) Quais dos seguintes compostos atuarão como ácido de Lewis e quais atuarão
como bases de Lewis?
a) AlBr3 b) CH3CH2NH2 c) BH3 d) HF e) CH3SCH3 f) TiCl4
10) Desenhe todas as estruturas de ressonância possíveis para as seguintes espécies:
H
O
a)
b)
H3C
H
CH2
H
NH2
d)
c)
S
H2N
NH2
H3C
CH2
e)
3