Prof. Dr. Walter F. de Azevedo Jr.
[email protected] ou
[email protected]
1
© 2015 Dr. Walter F. de Azevedo Jr.
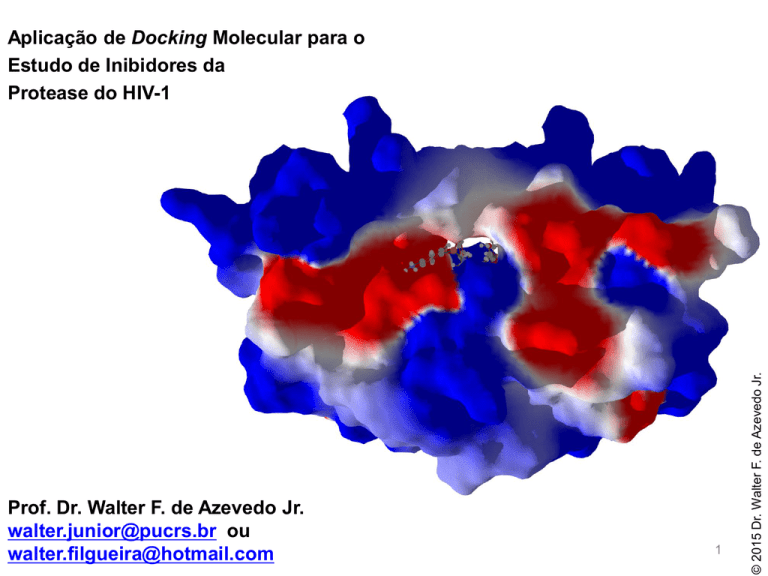
Aplicação de Docking Molecular para o
Estudo de Inibidores da
Protease do HIV-1
Protease do HIV
A AIDS surgiu como pandemia há
algumas décadas atrás e causou grande
temor, pois inicialmente não havia
conhecimento da sua causa. O estudo da
AIDS registra um dos maiores sucessos
da moderna abordagem do desenho de
fármacos,
usando-se
recursos
computacionais. A AIDS é causada pelo
HIV. Os vírus são formados por uma capa
de proteína que envolve seu material
genético, no caso do HIV é o RNA. Aqui
descreveremos o uso da protease do HIV,
como alvo para o desenvolvimento de
fármacos contra a AIDS.
Concepção artística da pesquisa de novos fármacos
contra a AIDS.
Imagem disponível em:
<http://www.sciencephoto.com/media/206187/view>
Acesso em: 6 de agosto de 2015.
2
Protease do HIV
As proteases são enzimas que catalisam
a clivagem de outras proteínas, a
protease do HIV catalisa tal clivagem.
Esta protease realiza uma importante
etapa no ciclo da infecção viral. Como em
outros vírus, o HIV leva a célula infectada
a produzir muitas cópias de suas
proteínas. Tais proteínas apresentam-se
inicialmente
como
uma
cadeia
polipeptídica (poliproteína), que apresenta
várias proteínas coladas numa cadeia. A
função da protease do HIV é catalisar a
clivagem da poliproteína em unidades
menores funcionais. A correta execução
de tal clivagem é crítica para o processo
de infecção viral.
Célula (linfócito T)(em verde) infectada com o HIV (em
vermelho). As esferas vermelhas são partículas repletas
de HIV, que saem da linfócito T para infectar outras
células.
Imagem disponível em:
http://www.sciencephoto.com/media/248205/enlarge
Acesso em: 6 de agosto de 2015.
3
Protease do HIV
A poliproteína intacta é necessária no
início do processo de infecção, quando
monta a forma imatura do vírus. Em
seguida a poliproteína tem que ser
clivada, para formar o vírus maduro, que
pode então infectar uma nova célula. As
reações de clivagem da poliproteína têm
que ser coordenadas perfeitamente, o que
permite a montagem do vírus. Devido a tal
sensibilidade e seu papel essencial para
infecção viral, a protease do HIV é um
alvo importante para o desenho de
fármacos contra a AIDS. A inibição da
protease do HIV impede a maturação do
vírus, cessando a progressão da infecção.
A estrutura da protease do HIV é dimérica, com duas
unidades idênticas. Os inibidores ligam-se na cavidade
entre as duas unidades. O inibidor está indicado pela
esferas, no meio da estrutura.
4
Regras de Lipinski
As regras de Lipinski (Lipinski et al., 1997,
2001) são um conjunto de parâmetros,
usados para avaliação do potencial que
uma molécula apresenta de ser absorvida
pelo organismo humano. Apesar de terem
sido publicadas em 1997, essas regras já
eram usadas há muito tempo pelo
laboratório farmacêutico Pfizer. O seu
sucesso na avaliação do potencial
farmacológico deve-se às seguintes
razões:
Fácil aplicação;
Fácil memorização;
São evidentes do ponto de vista físicoquímico;
São baseadas em pesquisa básica
sólida e funcionam efetivamente.
Fonte da imagem:
http://www.sciencephoto.com/media/268423/view
Acesso em: 6 de agosto de 2015.
Lipinski, C.A., Lombardo, F., Dominy, B.W., Feeney, P.J.. Adv
Drug Deliv Rev. 1997, 23(1-3):3-25.
Lipinski, C.A., Lombardo, F., Dominy, B.W., Feeney, P.J.. Adv
5
Drug Deliv Rev. 2001, 46(1-3):3-26
Regras de Lipinski
As regras de Lipinski são baseadas nas
propriedades
físico-químicas
de
compostos que formam a base de dados
USAN (United States Adopted Names
Directory), que apresentam moléculas que
passaram a fase 1 de testes clínicos.
Estudos
de
fase
1
envolvem
determinação de aspectos relacionados à
toxidade e farmacocinética. Compostos
que chegam à fase 2 são aqueles que
apresentam
absorção
e
toxidade
tolerável, o que sinaliza que investimentos
podem ser realizados em mais testes. As
regras de Lipinski analisam :
Doadores e aceitadores de ligação de
hidrogênio;
Fonte da imagem:
http://www.sciencephoto.com/media/268488/view
Acesso em: 6 de agosto de 2015.
LogP;
Massa molecular.
6
Regras de Lipinski
As regras de Lipinski baseiam-se em
critérios físico-químicos que as drogas
devem apresentar para serem absorvidas
pelo organismo humano. A absorção está
relacionada à solubilidade e à presença
de ligações de hidrogênio. Para um dado
composto é avaliado o número total de
potenciais átomos que podem estar
envolvidos
nessas
ligações,
aqui
separados em duas classes na análise.
1) Número de doadores de ligação de
hidrogênio (hydrogen-bond donors)(HBD).
Indica o número de hidrogênios presentes
na molécula que podem fazer ligação de
hidrogênio, principalmente ligados aos
oxigênio e nitrogênio.
2) Aceitadores de ligação de hidrogênio
(hydrogen-bond acceptors)(HBA). Indica o
número de aceitadores de ligação de
hidrogênio, na maioria das vezes átomos
de oxigênio e nitrogênio.
Fonte da imagem:
http://www.sciencephoto.com/media/350658/view
Acesso em: 6 de agosto de 2015.
7
Regras de Lipinski (Ligações de Hidrogênio)
A aplicação das regras de Lipinski baseia-se na avaliação da solubilidade do composto
em água, o aumento do número de ligações de hidrogênio contribui para esta
solubilidade, mas dificulta a passagem pela membrana, visto que aumenta o número
de ligações de hidrogênio que devem ser quebradas para a passagem da bicamada
fosfolipídica. Vamos ver um exemplo de como contar os doadores e aceitadores de
ligação
de
hidrogênio.
Usaremos
a
molécula
aspirina,
código
CID2244(http://pubchem.ncbi.nlm.nih.gov/summary/summary.cgi?cid=2244&loc=ec_rc
s).
Indicaremos o número de doadores como HBD e o de aceitadores como HBA. Na
molécula usaremos a seguinte notação:
Doador de ligação de hidrogênio (HBD)
Aceitador de ligação de hidrogênio (HBA)
8
Regras de Lipinski (Ligações de Hidrogênio)
Doador de ligação de hidrogênio (HBD)
Aceitador de ligação de hidrogênio (HBA)
Aspirina
HBA: 4
HBD: 1
9
Regras de Lipinski (Lipofilicidade)
Definimos a lipofilicidade de um composto, como a tendência deste para uma partição
numa matriz lipídica apolar contra uma matriz aquosa. Uma forma de determinarmos
experimentalmente a lipofilicidade de um composto, é a partir da partição deste entre
fases imiscíveis, tais como octanol (fase apolar) e um tampão aquoso (fase polar). Os
valores de partição podem ser expressos em termos de Log P, que é o coeficiente de
partição de um composto entre octanol e uma fase aquosa (tampão onde a molécula
está neutra),
Compostooctanol
Log P log
Compostoaquosa
onde [Composto]octanol é a concentração do composto na fase apolar, e
[Composto]aquosa é a concentração na fase aquosa. Há algoritmos estabelecidos para
determinarmos o Log P de um composto (Hansch et al., 1995; Cheng et al., 2007).
Hansch, C., Leo, A. and Hoekman, D. (1995) Exploring QSAR. Fundamental and applications in chemistry and biology, volume
I. Hydrophobic, electronic and steric constants, volume 2. New York: Oxford University Press.
Cheng, T.; Zhao, Y.; Li, X.; Lin, F.; Xu, Y.; Zhang, X.; Li, Y.; Wang, R.*; Lai, L. "Computation of Octanol-Water Partition
Coefficients by Guiding an Additive Model with Knowledge", J. Chem. Inf. Model. 2007, 47, 2140-2148.
10
Regras de Lipinski (Lipofilicidade)
Um guia geral para absorção gastrointestinal após administração oral da droga propõe
que o Log P deve estar na faixa de 0 a 3 para uma situação ótima, como indicado na
figura abaixo.
Biodisponibilidade oral
Alta
Baixa permeabilidade
da bicamada lipídica
Baixa solubilidade aquosa
Faixa ótima
Baixa
-4
-3
-2
-1
0
1
2
3
4
5
6
7
Log P
Figura baseada em Kerns, E. H. e Di, L. Drug-like properties; Concepts, structure, design and methods. Academic Press,
Elsevier, London, 2008. (pg. 45)
11
Regras de Lipinski (Aplicações)
Regras de Lipinski. A partir da estrutura
de um composto podemos avaliar
características da estrutura, tais como
ligações de hidrogênio, Log P e MW. Uma
absorção e permeabilidade adequadas
são esperadas para moléculas que
apresentem as seguintes características:
HBD 5
HBA 10 (5x2)
Log P 5
MW 500 (5x100)
Todos os aspectos considerados são
múltiplos de 5, por isso tal regra é
também chamada de regra dos 5 (rule of
five).
Fonte da imagem:
http://www.sciencephoto.com/media/350657/view
Acesso em: 6 de agosto de 2015.
12
Regras de Lipinski (Aplicações)
Como exemplo, vamos considerar a estrutura da molécula XK216, um inibidor da
protease do HIV (Ala et al., 1998). Identificaremos os doadores e aceitadores de ligação
de hidrogênio, como indicado abaixo.
Doador de ligação de hidrogênio (HBD)
Aceitador de ligação de hidrogênio (HBA)
XK216
Referência:
Ala PJ, Deloskey RJ, Huston EE, Jadhav PK, Lam PY,
Eyermann CJ, Hodge CN, Schadt MC, Lewandowski FA, Weber
PC, Mccabe DD, Duke JL, Chang CH. Molecular recognition of
cyclic urea hiv-1 protease inhibitors. J Biol Chem 1998: 273:
12325-12331.
13
Regras de Lipinski (Aplicações)
Para completar nossa análise, podemos usar as informações disponíveis sobre
fármacos do site PubChem (http://www.ncbi.nlm.nih.gov/pccompound/). No caso do
XK216, temos MW = 406,5173 g/mol g/mol e log P = 3,5.
Doador de ligação de hidrogênio (HBD)
Aceitador de ligação de hidrogênio (HBA)
XK216
Referência:
Ala PJ, Deloskey RJ, Huston EE, Jadhav PK, Lam PY,
Eyermann CJ, Hodge CN, Schadt MC, Lewandowski FA, Weber
PC, Mccabe DD, Duke JL, Chang CH. Molecular recognition of
cyclic urea hiv-1 protease inhibitors. J Biol Chem 1998: 273:
12325-12331.
14
Regras de Lipinski (Aplicações)
A tabela da direita mostra o resumo das informações para aplicação das regras de
Lipinski. Vemos que todas as regras de Lipinski são satisfeitas.
Doador de ligação de hidrogênio (HBD)
Aceitador de ligação de hidrogênio (HBA)
HBD = 2 5
HBA = 3 10 (5x2)
Log P = 3,6 5
MW 406,5173 500 (5x100)
Fonte:
http://pubchem.ncbi.nlm.nih.gov/compound/446158#sectio
n=Chemical-and-Physical-Properties
XK216
15
Referências Bibliográficas
ALBERTS, B. et al. Biologia Molecular da Célula. 4a edição. Artmed editora, Porto
Alegre, 2004 (Capítulo 3).
KERNS EH, DI L. Drug-like properties: Concepts, Structure, Design and Methods .
Academic Press, London, 2008.
LESK AM. Introduction to Protein Architecture. Oxford University Press, New York,
2001.
PATRICK GL. An Introduction to Medicinal Chemistry. 3ª Ed. New York: Oxford
University Press, 2005.
16












