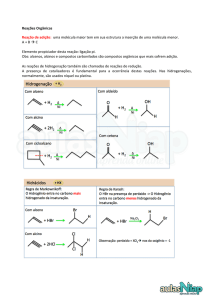
1A: Sal sódico da estrutura I (com um NH-Na+ no lugar de NH2 ao lado de SO2)
B: Porque em pH mais ácido haverá menor concentração da molécula ionizada (ânion
da sulfonamida sódica desenhada acima), que é solúvel, e conseqüentemente maior
concentração da molécula não-ionizada idêntica à da estrutura I, que é insulúvel,
aumentando, assim, a chance de cristalização.
C: A estrutura III, pois a conjugação também com o orbital pi do oxigênio da função
amida estabilizará a carga negativa da base conjugada em relação ao ácido, diminuindo
mais o pKa em relação às demais estruturas e, portanto, aumentando a concentração da
molécula ionizada, que é solúvel.
2- Não, pois a procaína é um éster do ácido para-aminobenzóico (PABA). In vivo, ela
será rapidamente metabolizada ao PABA. Tanto o sulfametoxazol (uma sulfa)
quanto a trimetoprima agem na via de síntese do ácido fólico, sendo que o
sulfametoxazol é um antimetabólito justamente do PABA para a enzima
diidropteroato sintetase. A administração da procaína vai aumentar a concentração
de PABA e prejudicar a ação inibitória competitiva da sulfa, comprometendo assim
a eficiência do antibacteriano.
3- Succinilsulfatiazol – Ação curta (pró-fármaco); sulfadiazina – Ação intermediária;
slfadoxina – ação prolongada
Quinolonas
1- C
2- Eu diria D, porque o cálcio vai prejudicar a absorção (quinolonas quelam metais
bivalentes) e os estrógenos vão ser imunossupressores.
3- A
4- Como a pergunta diz “quais”, acho que devemos assinalar todas. pKa pela
solubilidade, hidrofilicidade para penetrar nos tecidos, lipofilicidade para penetrar
na célula e parâmetros eletrônicos para interagir com o DNA
5- A;
6- B;
7- D.