GABARITO COMENTADO DE QUÍMICA
2a UNIDADE
PROFESSORES: CLÁUDIO E RODRIGUINHO
Data: 04/08/12
01. Por tratar-se de uma reação exotérmica, a entalpia dos reagentes é maior que a dos produtos.
Resposta: Há menos energia armazenada nos produtos do que nos reagentes.
02. O aquecimento de um ácido carboxílico causa a sua desidratação (perda de água), que caracteriza uma reação de
eliminação.
O
CH2
O
C
O
H
O
H
Resposta:
CH2
C
O
H 2O +
CH2
C
CH2
(Eliminação)
C
O
O
03. Percebe-se pelo gráfico que na câmara de combustão o valor de Kc é superior ao da câmara de exaustão, evidenciando um
maior rendimento da reação. Como Kc aumenta com a temperatura, podemos afirmar que a reação é endotérmica e a
inversa exotérmica, sendo favorecida pela redução na temperatura.
Resposta: Apenas I e III.
04. Como o reagente da reação I é saturado, sua reação é de substituição, enquanto que o reagente da reação III é insaturado
sua reação será de adição. Como o reagente da reação II é aromático, apesar de insaturado, excepcionalmente fará uma
reação de substituição.
Resposta: As reações I e II serão reações de substituição, enquanto que a reação III será uma adição.
05.
06. A substância do item II pode ser um álcool ou um aldeído, e a destilação da beterraba ou da batata produz etanol também.
E a hidrogenação do eteno é uma reação de adição que produz o etano.
Resposta: 2 e 3.
07.
08.
Resposta: metoxi-metano
09.
10. O nitrato de amônio é um sal proveniente de ácido forte e base fraca e tem, portanto, caráter ácido, o que leva a um
aumento na concentração de íons H+ no solo. Enquanto o que acontece no carbonato de cálcio é o inverso.
Resposta: O nitrato reduz o pH dos solos enquanto o carbonato aumenta.
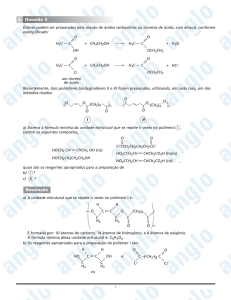
11. Um Ácido Carboxílico + álcool origina um éster, logo n moléculas de diácido com n moléculas de diácido origina um
poliéster.
Resposta: A reação entre n HOOC – (CH2)2 – COOH + n HO – CH2 – CH2 – OH n H2O + (– ?????? –)n tem como
produto principal um poliéster.
2
12. Afirmação I: incorreta; um aumento da pressão favorece reações que ocorrem com contração de volume e, nesse caso,
favoreceria a reação inversa, que ocorre com consumo de H 2;
Afirmação II: incorreta; a adição de um catalisador diminui o tempo necessário para que um sistema entre em equilíbrio,
mas não altera o rendimento;
Afirmação III: correta; um aumento da temperatura, nesse caso, favorece a reação de formação dos produtos, pois, de
acordo com a variação de entalpia, a reação direta é endotérmica e, portanto, a formação de gás hidrogênio é favorecida
pelo aquecimento.
Resposta: III.
13. Em lugares de maior altitude, a atmosfera é mais rarefeita e a concentração de gás oxigênio é menor que em áreas mais
próximas do nível do mar. A diminuição na concentração desse gás desloca o equilíbrio para a esquerda, de acordo com o
princípio de Le Chatelier.
Resposta: Devido ao ar rarefeito, o equilíbrio é deslocado para a esquerda.
14. A diminuição na concentração de dióxido de carbono, que tem caráter ácido, diminui a acidez e eleva o pH. De forma
oposta, numa situação de repouso, o aumento na concentração de dióxido de carbono aumenta a acidez e diminui o pH. O
pH sanguíneo é ligeiramente maior que 7,0 e, portanto, levemente básico. A acidose é caracterizada pela redução do pH
sanguíneo e a alcalose é caracterizada por sua elevação.
Resposta: básico, ácido, básico, redução, elevação.