HERPESVÍRUS HUMANOS
Os herpesvírus humanos (conhecidos)
TIPO
SINONIMIA
Sub-Família
PATOFISIOLOGIA
HHV-1
Vírus do Herpes simples (HSV-1)
Alfa (α)
Herpes oral ou genital (predomina orofacial)
HHV-2
Vírus do Herpes simples 2 (HSV-2)
Alfa (α)
Herpes oral ou genital (predomina genital)
HHV-3
Vírus varicela-zoster
Alfa (α)
Varicela ou catapora, herpes zoster
HHV-4
Epstein-Barr
virus (EBV), lymphocryptovirus
γ
(Gamma)
Mononucleose infecciosa, Linfoma de
Burkitt, Linfoma do CNS em pacientes com
AIDS,
sindrome linfoproliferativa pós-transplante
(PTLD), carcinoma nasofarínfgeo
HHV-5
Cytomegalovirus (CMV)
β (Beta)
Síndrome ~ à mononucleose infecciosa,
retinite, doença de inclusão citomegálica.
HHV6, 7
Roseolovirus
HHV-8
Herpesvírus associado ao
sarcoma de Kaposi
(KSHV), um tipo de rhadinovírus
β
γ
(Gamma)
Sexta doença (roséola infantum ou
exantema súbito)
Sarcoma de Kaposi e outros tumores
Família Herpesviridae
• Subfamília:
• Alfaherpesvirinae
– Simplexvirus (Herpes simples humano, ou HSV, ou
HHV-1 e HHV-2 (human herpesvirus type 1 or 2)
– Varicellovirus (vírus da varicela, ou catapora, ou
varicela-zoster, VZV (varicella-zoster virus)
ou HHV-3 (human herpesvirus type 3)
Vírus do Herpes
Simples Humano
- são alfaherpesvírus, latencia em neurônios
- envelopados
- Capsídeo icosaédrico, 162 capsômeros
- codifica cerca de 70 polipeptídeos
- tipos 1 e 2 muito semelhantes
- multiplicação intranuclear
Ver structure em:
F:\ENSINO\Animações\HSV\zipped exe
Latência
Infecção
Primária
Gânglio
Nervoso
Genoma
celular
Terminações
nervosas
Núcleo
Mini-cromossomo –
Genoma Viral+ Histonas
Reativação
Com ou
sem
lesões
neurônios
Pele/
mucosas
Gânglio
Nervoso
regional
• Herpes humanos tipos 1 e 2 (HHV-1 e 2)
SINAIS CLÍNICOS
HSV tipo 1; HHV-1:
Doenças associadas:
Herpes labial
Queratite
Estomatites (Aftas)
Herpes labial
(HSV tipo 1; HHV-1)
Herpes labial
(HSV tipo 1; HHV-1)
Lesões herpéticas
Herpes
Herpes neonatal
Lesões cutâneas
Encefalites
Herpes genital (HSV tipo 2; HHV-2)
Herpes genital
Herpes
DIAGNÓSTICO
Clínico
Diagnóstico laboratorial clássico:
1) Rápido: esfregaços de células
e exame por imunofluorescência
2) Isolamento de vírus:
fluido vesicular, suabes orais, nasais, conjuntivais,
tecidos de abortos, fragmentos de encéfalo, LCR
inoculação em células Vero, HEP e muitas outras
efeito citopático (ECP) característico em 1-3 dias
Atalho para PCR.lnk
Genoma viral
Diagnóstico atual:
PCR para detecção de
fragmentos de genoma viral
1
Eletroforese
1100 pb
Região alvo
PCR
Desenho de primers (18-20 nts)
1100 pb
2
3
1:positivo
2:marcador
3:negativo
Diagnóstico sorológico
Soroneutralização: em laboratórios especializados
Enzyme linked immunosorbent assay – ELISA
Permite inclusive diferenciar infecções por HSV-1 ou HSV-2
Positivos
Negativos
Família Herpesviridae
• Subfamília:
• Alfaherpesvirinae
– Simplexvirus (Herpes simples humano,
ou HSV, ou HHV-1 e 2)
– Varicellovirus (vírus da varicela, ou
catapora, ou varicela-zoster, VZV, ou
HHV-3)
VARICELA ou
“Catapora”
p.i. 14-20 DIAS
EVOLUÇÃO RÁPIDA
ALTAMENTE CONTAGIOSA
LESÕES EM DIFERENTES ESTÁGIOS
VARICELA
Lesões
VARICELA
Zoster
Zoster
VARICELA
DIAGNÓSTICO:
Geralmente clínico em imunocompetentes
No laboratório:
diagn. rápido em células da lesão (início):
IF, IPX
células gigantes
leucopenia
Isolamento em células: VERO, BHK, RK13
1árias de rim de
macaco
ECP em 2 a 14 dias
HERPES
Tratamento
- Idoxuridina (IDU) uso somente tópico
- Aciclovir e análogos (guanosina acíclica)
ação sobre a timidina quinase viral
- a longo prazo - efeito na recorrência
- ocular : idoxuridina, trifluridina (tópicos)
(resistentes: ácido fosfonofórmico)
NENHUMA DROGA EVITA COMPLETAMENTE
RECORRÊNCIAS !
NENHUMA DROGA AGE SOBRE A LATÊNCIA !
Família Herpesviridae
• Subfamília:
Gammaherpesvirinae
– Lymphocryptovirus (vírus Epstein-Barr,
EBV, ou herpesvírus humano tipo 4
(HHV-4)
- Latência em células
linfóides
MONONUCLEOSE INFECCIOSA
“Clássica”
ou
“Mononucleose Paul-Bunnel positiva”
Definição:
- Causada pelo vírus Epstein-Barr (EBV 1 e 2)
gamaherpesvírus (gênero lymphocryptovirus); - HHV 4
A mononucleose =
São linfócitos T atípicos,
maiores, com
citoplasma vacuolizado e
núcleo deformado e lobulado.
Mononucleose infecciosa
Transmissão / Patogenia
- transmissão por saliva (90% adultos +)
- vírus intermitente na saliva
- 10-5 a 10 -6 linfócitos infectados
- orofaringe => linf. B => Linf T reagem =>
muitas cópias do genoma no citoplasma;
poucas integradas no genoma.
Mononucleose infecciosa
CARACTERÍSTICAS CLÍNICAS:
- Síndrome agudo
- Febre, dor de garganta, mal-estar, linfadenopatia
- Esplenomegalia
- Eritema maculopapular (< 15%). Ampicilina eleva a >90%.
- Mononucleose com linfócitos T atípicos (10% - 30%)
- Linfocitose > 50% (incluso os 10%)
- Anticorpos heterófilos
- Anomalias de funções hepáticas são freqüentes.
Mononucleose Infecciosa
Mononucleose Infecciosa
Células alvo = Linfócitos B não sensibilizados
- 10 genes (EBNA 1-6, LMP1, 2a e 2b, EBER 1 e 2)
mantém a infecção latente em células linfóides
- Linfóc. B -> estimulados a proliferar continuamente
- podem se multiplicar seriadamente e dar origem a
linhagens linfoblastóides
- disseminação esporádica pela saliva
- linfócitos infectados se comportam como
linfócitos sensibilizados com Ag: secretam proteínas,
Igs, sofrem trocas de classe
Mononucleose infecciosa
Latência em três formas:
I e II = antígenos nucleares expressos:
EBNA 1; LMP 1, 2a e 2b
III = os 6 EBNA são expressos
EBNA 1: único expresso em todas as formas
sem ele não há latência
Mononucleose infecciosa
Diagnóstico:
- Paul Bunnel (Ac heterófilos)
- IgM específica anti-ag capsídeo viral
(ACV)
- IgG anti- ACV em elevação
- anti-EBNA: 3-4 semanas p.i. e
persiste por toda a vida
Exemplos de placas de
ELISAs
Revelada com OPD
Cor= +
Sem cor= Mais cor = mais positivo
Mononucleose
infecciosa - EBV
Associação com cânceres linfóides:
Linfoma de Burkitt em crianças africanas
Carcinoma nasofaríngeo (CNF) => (China)
Resto do mundo: CNF < 1/ 100 000
China:
15 a 30/ 100 000
Carcinoma de timo nos EUA
Hodgkins: EBV presente em 50% dos tumores
Linfoma de Burkitt
Linfoma de Burkitt: três formas
Currently Burkitt's lymphoma can be divided into three main clinical variants: the endemic, the
sporadic and the immunodeficiency-associated variants.
The endemic variant occurs in equatorial Africa. It is the most common malignancy of children in
this area. Children affected with the disease often also had chronic malaria, which is believed to have
reduced resistance to EBV, allowing it to take hold. The disease characteristically involves the jaw or
other facial bone, distal ileum, cecum, ovaries, kidney or the breast.
The sporadic type of Burkitt lymphoma (also known as "non-African") is another form of nonHodgkin lymphoma found outside of Africa. The tumor cells have a similar appearance to the cancer
cells of classical African or endemic Burkitt lymphoma. Again it is believed that impaired immunity
provides an opening for development of the Epstein Barr virus. Non-Hodgkin lymphoma, which
includes Burkitt's, accounts for 30-50% of childhood lymphoma. The jaw is less commonly involved,
compared to the endemic variant. The íleo-cecal region is the common site of involvement.
Immunodeficiency-associated Burkitt lymphoma is usually associated with HIV infection[3] or
occurs in the setting of post-transplant patients who are taking immunosuppressive drugs. Burkitt
lymphoma can be one of the diseases associated with the initial manifestation of AIDS.
By MORPHOLOGY(i.e. microscopic appearance) or immunophenotype, it is almost impossible to
differentiate these three clinical variants. Immunodeficiency-associated Burkitt lymphoma may
demonstrate more plasmacytic appearance or more pleomorphism, but these features are not specific.
Of all cancers involving the same class of blood cell, 2% of cases are
Burkitt's lymphoma.
The tumor consists of sheets of a monotonous (i.e. similar in size and morphology) population of medium
size lymphoid cells with high proliferative activity and apoptotic activity. The "starry sky" appearance
seen[5] under low power is due to scattered tingible body-laden macrophages (macrophages containing
dead body of apoptotic tumor cells). The old descriptive term of "small non-cleaved cell" is misleading. The
tumor cells are mostly medium in size (i.e. tumor nuclei size similar to that of histiocytes or endothelial
cells. "Small non-cleaved cells" are compared to "large non-cleaved cells" of normal germinal center
lymphocytes. Tumor cells possess small amount of basophilic cytoplasm. The cellular outline usually
appears squared off.
Immunohistochemistry
The tumor cells in Burkitt lymphoma generally strongly express markers of B cell differentiation (CD20,
CD22, CD19) as well as CD10, and BCL6. The tumour cells are generally negative for BCL2 and TdT. The
high mitotic activity of Burkitt lymphoma is confirmed by nearly 100% of the cells staining positive for Ki67.
Genetics
All types of Burkitt's lymphoma are characterized by disregulation of the c-myc gene by one of three
chromosomal translocations.[7] This gene is found at 8q24.
The most common variant is t(8;14)(q24;q32), which accounts for approximately 85% [7] of cases. This
involves c-myc and IGH@. A variant of this, a three-way translocation, t(8;14;18), has also been
identified.[8]
A rare variant is at t(2;8)(p12;q24).[9] This involves IGK@ and c-myc.
Another rare variant is t(8;22)(q24;q11).[9] This involves IGL@ and c-myc.
Combined, the two less-common translocations, t(2;8)(p12;q24) and t(8;22)(q24;q11), account for the
remaining 15% of cases not due to the t(8;14)(q24;q32) translocation.[7]
Treatment
Treatment includes dose-adjusted EPOCH with Rituxan (RITUXIMAB).[12]
The effects of the CHEMOTHERAPY, as with all cancers, depend on the time of
diagnosis. With faster growing cancers, such as Burkitt's, the cancer actually responds
faster than with slower growing cancers. This rapid response to chemotherapy can be
hazardous to the patient, as a phenomenon called “tumor lysis syndrome" could occur.
Close monitoring of the patient and adequate hydration is essential during the process.
Chemotherapy
Cyclophosphamide
Doxorubicin
Vincristine
Methotrextate
cytarabine
ifosfamide
etoposide
rituximab
Other treatments are immunotherapy, bone marrow transplants, stem cell transplant,
surgery to remove the tumor and radiotherapy.
Prognosis
Treatment with dose-adjusted EPOCH with Rituxan (rituximab) has shown an 8 year
survival rate of 91% for low risk, 90% for low-intermediate risk, 67% for highintermediate risk, and 31% for high risk cases with few of the side effects associated
with Burkitt's lymphoma chemotherapy.[12
Família Herpesviridae
• Subfamília Betaherpesvirinae
– Citomegalovírus (CMV ou HHV-5)
– Roseolovírus (vírus da roséola, HHV-6)
Citomegalovírus (CMV)
- é um betaherpesvírus; HHV-5, um só sorotipo
- infecção muito prevalente; doença muito rara
- neonatos: doença de inclusão citomegálica
- mononucleose infecciosa negativa para
Acs. Heterófilos
- pneumonia em imunocomprometidos
-
células gigantes => inclusão citomegálica
-
Latência em células linfóides
Citomegalovírus (CMV)
TRANSMISSÃO E EPIDEMIOLOGIA:
- Acs em ~80% adultos
- eliminação de vírus esporádica
- infecções:
-congênita
-pós-natal
CMV
INFECÇÃO PRÉ-NATAL:
- em qualquer estágio da gestação
- risco de transmissão: 0,2 a 2%
- 5 a 15% destes podem apresentar lesões congênitas
- infecção intrauterina => crianças disseminam o vírus
por mais tempo
- > risco = infecção 1ária na gestação
- infecção prévia = risco muito baixo
SÍNDROME CONGÊNITA
• Mãe infectada com reativação do vírus,
reinfecção ou persistente infecção primária.
• Causa danos severos no sistema nervoso, afeta
a formação de diferentes órgãos e tecidos
(ouvidos, olhos, fígado, rins, pele, etc),
• Anemia, trombocitopenia e leucopenia.
• Pode afetar a placenta.
RECÉM
NASCIDO
COM SÍNDROME
CONGÊNITA
RECÉM NASCIDO INFECTADO POR CMV
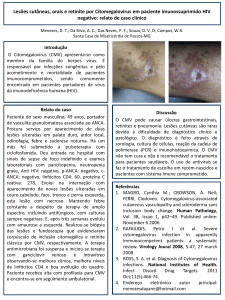
Retinite por CMV
CMV
Infecção intrauterina ou pré-natal
Achados clínicos:
- microcefalia
- convulsões
- icterícia
- hepatosplenomegalia
- retardo mental
- surdez (mais comum)
CMV
Congênito
Doença de
inclusão
citomegálica
INFECÇÃO PÓS-NATAL:
- geralmente na infância (MI rara)
- MI Paul Bunnel - negativa
- infecção em adultos > chance de MI
- pode ocorrer durante o parto
- através do leite => mais comum
- transmissão sexual (sêmen, secr. cervicais)
- transmissão por hemoderivados
- transplantados renais: reativação e disseminação
do vírus
CMV
Retinite por CMV
Doença de inclusão citomegálica
CMV
EBV
CMV
Infecção pós-natal:
- MI heterófilo- negativa;
- Febre, letargia, linfócitos anormais no
sangue periférico;
- usualmente sem faringite ou linfadenopatia
-retinites
- às vezes após transfusão com sangue fresco
(vírus inativado em refrigeração)
CMV
Em imunodeprimidos:
-
infecções frequentes
-
transplantes renais: assintomáticas
-
grave em transplantados de medula e coração =>
pneumonia intersticial e retinite
Diagnóstico laboratorial (2)
1. Teste para antigenemia (CMV) - Antígenos do CMV detectados na
superfície de leucócitos polimorfonucleares por imunoperoxidase
(IPX) ou imunofluorescência direta (IFD).
2. Polymerase chain reaction (PCR) – é hoje o método de escolha.
3. Sorologia - não confiável mas ocasionalmente pode ser detectado
aumento de IgG e presença de IgM.
Imunoperoxidase
Imunofluorescência
Direta
anticorpo marcado sobre material infectado
material infectado (suspeito)
+ anticorpo específico marcado com FITC
+ luz UV
________________________________________
reação colorida
CMV
Tratamento:
- acyclovir : não muito eficaz
- ganciclovir (em pneumonias e retinites)
- foscarnet (retinites): inibidor da
DNA polimerase viral
CMV
Prevenção:
- não há vacina
- Acompanhar a evolução da infecção em
transplantados e imunodeprimidosIniciar tratamento se viremia ocorrer.
Roséola (HHV-6 e HHV-7)
A apresentação clássica da roséola ocorre em crianças de 9- a 12 meses
que desenvolvem uma febre aguda e seguidamente uma convulsão febril
.
Após 3 dias , uma rápida defervescência ocorre e um exantema morbiliforme
aparece.
Roséola
Patofisiologia
In the primary infection, replication of the virus occurs in the leukocytes and the salivary glands.
HHV-6 is present in saliva. Early invasion of the CNS is believed to occur, thus accounting for
seizures and other CNS complications.
Although rare in the primary disease of infancy, generalized organ involvement has been reported
with gastrointestinal, hematopathic syndromes; hepatitis; and hepatosplenomegaly.
Following the acute primary infection, HHV-6 remains latent in lymphocytes and monocytes and has
been found in low levels in many tissues. Peripheral blood mononuclear cell cultures develop
enlarged balloonlike cells. Cells supporting virus growth are CD4+ T lymphocytes. HHV-6 downregulates the host immune response through several mechanisms, including molecular mimicry by
production of functional chemokine and chemokine receptors.
The 2 variants of HHV-6 are A and B. The genomes of HHV-6A/B have been sequenced. HHV-6B,
the main cause of roseola, consists of 97 unique genes. CD46 is the cell receptor for HHV-6, which
imparts the virus' broad tissue tropism.
A possible association of HHV-6 and multiple sclerosis has been suggested but is still inconclusive.
HHV-6 has been isolated in Kaposi’s sarcoma (caused by human herpesvirus 8), in which it may
contribute to tumor progression. HHV-6 may facilitate oncogenic potential in lymphoma and has
been associated with chronic fatigue syndrome.
HHV-7
•
•
•
•
Signs and symptoms
HHV-6B and HHV-7, as well as other viruses, can cause a skin condition in
infants known as exantema subitum , although HHV-7 causes the disease less
frequently than HHV-6B.[4] HHV-7 infection also leads to or is associated with a
number of other symptoms, including acute febrile respiratory disease, fever,
rash, vomiting, diarrhea, low lymphocyte counts,[5] and febrile seizures,[6] though
most often no symptoms present at all.[7]
There are indications that HHV-7 can contribute to the development of
syndrome de hipersensibilidade induzida por medicamentos,[8] encefalopatia[9]
sindrome hemiplegia, hemiconvulsão- epiplepsia,[10] hepatite,[11] postinfectious
myeloradiculoneuropathy,[12] pitiríase rósea,[13] e reativação de EBV HHV-4,
levando a doença “mononucleose-like".[14]
Complications with HHV-7 infection has been shown to be a factor in a great
variety of transplant types.[
HHV-7
•
•
•
•
•
•
Structure
A mature virus particle measures about 170 nanometres (1,700 Å) in
diameter.[15]
The genome of HHV-7 is very similar to that of HHV-6, although it is about 10%
smaller,[16] with a DNA genome of about 145,000 base pairs.[7] There are a
number of key differences between the genome of HHV-7 and that of HHV-6,
but the importance of them for viral DNA replication is not yet known.[7]
Cellular effects
HHV-7 resides mostly in CD4+ T cells[17] albeit only in certain strains of them.[18]
To enter CD4+ T cells, HHV-7, unlike HHV-6, uses CD4 and possibly some cellsurface glycoproteins to enter CD4+ T cells.[19] About a week after HHV-7 has
infected a cell, it begins to downregulate CD4 transcription,[20] which interferes
with HIV-1 infection[21] but may reactivate HHV-6 infection.[22] It is however
unclear exactly what effect HHV-7 has on HIV infection.[7]
HHV-7 also has a number of other effects on cells. Among these include
membrane leaking, the presence of lityic syncytia,[23] occasional apoptosis,[24]
the supporting of latent infection,[25] and increases and decreases in levels of
certain cytokines.[26]
HHV-7
•
•
•
•
•
•
Diagnóstico e tratamento
Em adultos, os effects de HHV-7 separados de HHV-6 ainda não são bem
documentados. Isto porque a detecção de HHV-7 era inicialmente difícil de ser feita
rapidamente. Uma técnica denominada loop-mediated isothermal amplification (LAMP)
foi recentemente introduzida.
No reliable serological test has been developed yet for HHV-7 alone, but multiple are in
the process of being developed.[7] The use of PCR assays to test for HHV-7 is also being
explored.[7][29]
No treatment for HHV-7 infection exists, but no clinical situation where such treatment
would be useful has yet been discovered.[7]
Epidemiological
Over 95% of adults have been infected and are immune to HHV-7,[30] and over three
quarters of those were infected before the age of six.[31] Primary infection of HHV-7
among children generally occurs between the ages of 2 and 5, which means it occurs
after primary infection of HHV-6.[32]
Herpesvírus Humano 8 (HHV-8)
•
Tumor associado à ocorrência do Sarcoma de Kaposi e outros linfomas menos
conhecidos (doença de Castleman e outros).
•
Tumor prevalente em homossexuais masculinos com AIDS.
•
DNA do vírus encontrado em 100% dos casos de KS.
•
A maioria dos pacientes com KS tem anticorpos anti-HHV-8.
•
A soroprevalência de anticorpos anti-HHV-8 é baixa na população em geral,
mas alta em suscetíveis ao KS, como homossexuais masculinos.
•
O tratamento com anti-retrovirais leva à regressão rápida dos tumores
•
Diferente dos demais herpes humanos, o HHV-8 não tem distribuição ubíqua.
Consulte nossa home page
•
•
•
•
•
•
www6.ufrgs.br/labvir
Referências adicionais:
Wikipedia
Site do CDC
Site: All the virology in the web (ATV)
Site de Vincent Racaniello (virology blog):
www.virology.ws