Lista Semana do Educador Química Marcelo Mota
01) (Unb 97) Cerca de 90% do ácido nítrico, principal matéria-prima dos adubos à base de
nitratos, são obtidos pela reação de oxidação da amônia pelo O‚, em presença de
catalisador-platina com 5% a 10% de paládio ou de ródio (ou de ambos) - a uma
temperatura de 950°C. A reação é representada pela equação
6NH3(g)+9 O2(g) ⇌ 2HNO3(g)+4NO(g)+8H2O(g).
Essa reação ocorre nas seguintes etapas:
⇌ 6NO(g)+9H2O(g)
II - 3NO(g)+3/2 O2(g) ⇌ 3NO2(g)
III - 3NO2(g)+H2O(g) ⇌ 2HNO3(g)+NO(g)
I - 6NH3(g)+15/2 O2(g)
ÐH=-1.359kJ
ÐH=-170kJ
ÐH=-135kJ
Considerando que as reações das etapas de obtenção do ácido nítrico, totalmente ionizável
em água, estão em equilíbrio,assinale a correta.
A) Um aumento de pressão no sistema reacional eleva a produção de ácido nítrico.
B) Pela equação global, verifica-se que a adição de água ao sistema não diminui o
rendimento da reação.
C) Sabendo-se que a constante de ionização do ácido acético é igual a 1,8×10¦mol/L, é
correto concluir que este é mais forte que o ácido nítrico.
D) A expressão para a constante de equilíbrio da reação global é
Kc=[HNO3][NO][H2O]/[NH3][O2].
E) O único fator capaz de deslocar esse sistema é a temperatura
02) (Ufsm 2004) As usinas hidroelétricas, que utilizam a água acumulada em represas
para fazer funcionar suas turbinas, são responsáveis pela perturbação no ciclo natural das
cheias e secas dos rios, pela inundação de áreas de terra cada vez maiores, pela retenção de
nutrientes que, se não fosse esse uso, estariam distribuídos mais ou menos uniformemente,
ao longo dos rios.
A queima de carvão mineral para a geração do vapor d'água que move as turbinas das
usinas termoelétricas lança, na atmosfera, além de dióxido de carbono, grandes
quantidades de enxofre e óxidos nitrogenados, gases que formam a chuva ácida. As usinas
nucleares causam impacto ambiental mesmo na ausência de acidentes, porque retiram a
água do mar ou dos rios para resfriar os núcleos de seus geradores, devolvendo-a a uma
temperatura bem mais alta. Esse aquecimento afeta os organismos aquáticos, pois o
aumento da temperatura deixa a água pobre em oxigênio pela diminuição da solubilidade.
Na construção de barragens, usa-se o concreto. Nos primeiros dias de confecção, o
concreto tem pH alcalino, o que protege a ferragem da oxidação. Com o tempo, o pH
diminui pela carbonatação do concreto que se dá pela reação com o H2CO3.
Em um teste de carbonatação feito em laboratório, foi usada uma solução de H2CO3 de
concentração 0,02 mol/L, a qual apresenta um grau de dissociação de 0,45%, a 25°C. O
valor da primeira constante de ionização do H2CO3, nessa temperatura, é,
aproximadamente,
a) 0,9 × 10-5
b) 9 × 10-5
c) 0,4 × 10-7
d) 9 ×10-7
e) 4 × 10-7
03) A determinação de acidez ou basicidade de uma solução pode ser realizada através de
um pHmetro ou por meio de substâncias denominadas indicadores são ácido/base. Uma
grande parte dos indicadores são ácidos orgânicos fracos, que podem ser representados
genericamente por Hln. A classificação da substância como sendo ácida básica é possível
devido à diferença de cor das espécies HIn e In, de acordo com o equilíbrio a seguir:
HIn (aq) ⇌ H+(aq) + In-(aq)
Cor A = Hln (aq)
Cor B = In-(aq)
Com base nas informações anteriores, é correto afirmar que:
A) Se adicionarmos um pouco deste indicador em um suco de limão, a solução apresentará
cor B.
B) HIn não é um ácido de Arrhenius.
C) A expressão da constante de equilíbrio é
Ka=([H+][In-])/[HIn] e dá uma informação quantitativa das espécies presentes.
D) Quanto maior for o número de hidrogênios na fórmula do ácido, maior será sua força.
E) A adição de OH- não perturba o sistema.
04) (Ime 96) A constante de ionização de um ácido monocarboxílico de massa molecular
60 é 4,0×10-5. Dissolvem-se 6,0g desse ácido em água até completar 1 litro de solução.
Determine:
a) a concentração de H+ na solução;
b) o pH da solução;
c) a expressão matemática da constante de ionização;
d) a concentração de H+ se o ácido for totalmente dissociado;
e) a solução que neutralizará uma maior quantidade de NaOH, considerando duas
soluções, de mesmo volume e de mesmo pH, do ácido monocarboxílico e de HCl.
05) (Unesp 90) Misturando soluções aquosas de K2CrO4 e HCl, ocorre o equilíbrio:
2CrO42-+ 2H+ ⇌ Cr2O72-+ H2O
a) Escrever a expressão da constante de equilíbrio.
b) Descrever e justificar o que ocorre no equilíbrio quando se adiciona:
I - solução de HCl;
II - solução de ZnCl2 sabendo-se que ZnCr2O7 é um sal solúvel, mas ZnCrO4 é um sal
pouco solúvel.
06) (Puccamp 94) A equação química, não balanceada,
C6H12O6 + NO3- + H+ ⇌ CO2 + H2O + N2
representa a reação que ocorre em solos pouco aerados e envolve a redução de nitrato a
nitrogênio, em meio ácido, na presença de carboidrato. O fenômeno, conhecido como
desnitrificação prejudica a fixação de NO3-- pelas plantas. É possível aumentar a
concentração do NO3-- no equilíbrio adicionando-se, no solo,espécie química capaz de
a) liberar íons OHb) liberar íons H+
c) absorver CO2
d) reagir com N2
e) consumir H2O
07) (Puccamp 94) A hidroxiapatita, fosfato naturalmente encontrado no solo, apresenta em
meio ácido a reação
Ca5(OH)(PO4)3(s) + 4H+(aq)
⇌
⇌5Ca2+(aq) + 3HPO42-(aq) + H2O (l)
A adição de hidroxiapatita em determinados locais modifica o solo, pois
a) aumenta o pH, devido à formação de ácidos.
b) diminui o pH, devido à formação de ácidos.
c) aumenta o pH, porque consome H+ (aq).
d) diminui o pH, porque produz sais ácidos.
e) aumenta o pH, porque produz água.
08) [PUCCAMP-2005] Mares absorvem grande parte do CO2 concentrado na atmosfera,
tornando-se mais ácidos e quentes, segundo cientistas.
A Royal Society, do Reino Unido, começou um estudo para medir os níveis de acidez dos
oceanos sob a influência do aumento da concentração de dióxido de carbono. O CO 2
concentrado na atmosfera é responsável pelo efeito estufa.
Na água, elevando a acidez, o gás interfere na vida de corais e seres dotados de concha,
assim como diminui a reprodução do plâncton, comprometendo a cadeia alimentar de animais
marinhos. ("Estado de S. Paulo", 24/08/2004)
Em uma solução aquosa 0,10 mol/L de carbonato de sódio ocorre a hidrólise do íon carbonato:
⇌
CO32- (aq) + H2O (l)
HCO3- (aq) + OH-(aq)
Constante de hidrólise, K(h) = 2,5 × 104
Calculando-se, para essa solução, o valor de [OH-] em mol/L, encontra-se
a) 5 × 103
b) 4 × 103
c) 3 × 103
d) 2 × 103
e) 1 × 103
09) - (ENEM/2010)
Devido ao seu teor de sais, a água do mar é imprópria para o consumo humano e para a
maioria dos usos da água doce. No entanto, para a indústria, a água do mar é de grande
interesse, uma vez que os sais presentes podem servir de matérias-primas importantes para
diversos processos. Nesse contexto, devido a sua simplicidade e ao seu baixo potencial de
impacto ambiental, o método da precipitação fracionada tem sido utilizado para a obtenção
dos sais presentes na água do mar.
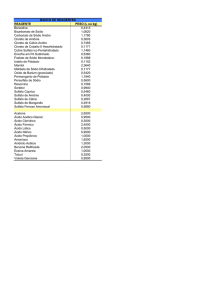
Tabela 1: Solubilidade em água de alguns compostos presentes na água do mar a 25ºC
Suponha que uma indústria objetiva separar determinados sais de uma amostra de água do
mar a 25ºC, por meio da precipitação fracionada. Se essa amostra contiver somente os sais
destacados na tabela, a seguinte ordem de precipitação será verificada:
a) Carbonato de cálcio, sulfato de cálcio, cloreto de sódio e sulfato de magnésio, cloreto de
magnésio e, por último, brometo de sódio.
b) Brometo de sódio, cloreto de magnésio, cloreto de sódio e sulfato de magnésio, sulfato
de cálcio e, por último, carbonato de cálcio.
c) Cloreto de magnésio, sulfato de magnésio e cloreto de sódio, sulfato de cálcio,
carbonato de cálcio e, por último, brometo de sódio.
d) Brometo de sódio, carbonato de cálcio, sulfato de cálcio, cloreto de sódio e sulfato de
magnésio e, por último, cloreto de magnésio.
e) Cloreto de sódio, sulfato de magnésio, carbonato de cálcio, sulfato de cálcio, cloreto de
magnésio e, por último, brometo de sódio.
10) - (ENEM/2010)
Às vezes, ao cobrir um refrigerante, percebe-se que uma parte do produto vaza
rapidamente pela extremidade do recipiente. A explicação para esse fato está relacionada à
perturbação do equilíbrio química existente entre alguns dos ingredientes do produto, de
acordo com a equação:
CO2(g) + H2O(l) ⇌ H2CO3(aq)
A alteração do equilíbrio anterior, relacionada ao vazamento do refrigerante nas condições
descritas, tem como consequência a
a) liberação de CO2 para o ambiente.
b) elevação da temperatura do recipiente.
c) elevação da pressão interna no recipiente.
d) elevação da concentração de CO2 no líquido.
e) formação de uma quantidade significativa de H2O.
11) - (ENEM/2009)
Sabões são sais de ácidos carboxílicos de cadeia longa utilizados com a finalidade de
facilitar, durante processos de lavagem, a remoção de substâncias de baixa solubilidade em
água, por exemplo, óleos e gorduras. A figura a seguir representa a estrutura de uma
molécula de sabão.
Em solução, os ânions do sabão podem hidrolisar a água e, desse modo, formar o ácido
carboxílico correspondente. Por exemplo, para o estearato de sódio, é estabelecido o
seguinte equilíbrio:
CH3(CH2)16COO- + H2O
⇌
CH3(CH2)16COOH + OH-
Uma vez que o ácido carboxílico formado é pouco solúvel em água e menos eficiente na
remoção de gorduras, o pH do meio deve ser controlado de maneira a evitar que o
equilíbrio acima seja deslocado para a direita.
Com base nas informações do texto, é correto concluir que os sabões atuam de maneira
a) mais eficiente em pH básico.
b) mais eficiente em pH ácido.
c) mais eficiente em pH neutro.
d) eficiente em qualquer faixa de pH.
e) mais eficiente em pH ácido ou neutro.
12) - (ENEM/2010)
O despejo de dejetos de esgotos domésticos e industriais vem causando sérios problemas
aos rios brasileiros. Esses poluentes são ricos em substâncias que contribuem para a
eutrofização de ecossistemas, que é um enriquecimento da água por nutrientes, o que
provoca um grande crescimento bacteriano e, por fim, pode promover escassez de
oxigênio.
Uma maneira de evitar a diminuição da concentração de oxigênio no ambiente é:
a) Aquecer as águas dos rios para aumentar a velocidade de decomposição dos dejetos.
b) Retirar do esgoto os materiais ricos em nutrientes para diminuir a sua concentração nos
rios.
c) Adicionar bactérias anaeróbicas às águas dos rios para que elas sobrevivam mesmo sem
o oxigênio.
d) Substituir produtos não degradáveis por biodegradáveis para que as bactérias possam
utilizar os nutrientes.
e) Aumentar a solubilidade dos dejetos no esgoto para que os nutrientes fiquem mais
acessíveis às bactérias.
RESPOSTAS
01) [A]
02) [E]
03) [C]
-3
04) a) [H+] = 2,0 x 10 mol/L
b) pH = 2,7
c) Ki = [H+] [R - COO] / [R -COOH]
d) [H+] = 0,1 mol/L
e) As quantidades de NaOH neutralizadas serão iguais.
05) a) Ki = [Cr2O72-] / [CrO42-]2 . [H+]2
b) I - deslocamento para a direita (Princípio de Le Chatelier)
II - deslocamento para a esquerda (Princípio de Le Chatelier)
06) [A]
07) [C]
08) [A]
09) [A]
10) [A]
11) [A]
12) [A]