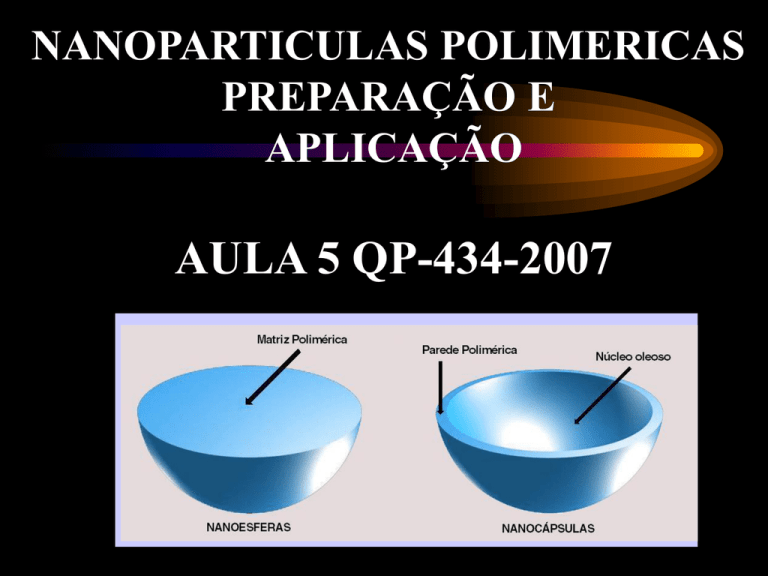
NANOPARTICULAS POLIMERICAS
PREPARAÇÃOSistemas
E Poliméricos
APLICAÇÃO
Nanopartículas:
Diâmetro das partícula: 100 a1000nm
AULA 5 QP-434-2007
Introdução
Liberação Controlada de Fármacos
• Liberação de fármacos a uma velocidade
e/ou numa localização indicada para a
necessidade do corpo ou estado da
doença em um período especificado de
tempo:
– Liberação temporal: controle sobre a
velocidade da liberação do fármaco
– Liberação espacial: controle sobre a
localização do fármaco
Hamid Ghandehari in <[email protected] >
Introdução
Liberação espacial
= Molécula do fármaco
TUMOR
LIBERAÇÃO EXCLUSIVA DO FÁRMACO A TIPOS ESPECÍFICOS DE CÉLULAS
Hamid Ghandehari in <[email protected]>.
Introdução
Liberação temporal
P
L
s
m
a
Convencional
Liberação ordem zero
Efeitos adversos
Níveis tóxicos
Faixa terapéutica
Concentração
Min. efetiva
Sem efeito
l
e
v
e
l
Tempo/dosagem administrada
Sistema de Liberação Controlada
• O comportamento do fármaco in vivo pode ser mudado
drasticamente ao incorpora-lo num carregador. Os veículos de
liberação de fármacos coloidais podem prover:
– Liberação lenta de compostos as vezes tóxicos
– Habilidade de guiar uma distribuição sistêmica
– Habilidade de proteger fármacos de degradação ambiental
– Habilidade de direcionar a alvos específicos diretamente em
tecidos
• Sistemas coloidais em uso são:
–
–
–
–
Nanopartículas
Microesferas
Emulsões
Lipossomas
d<1mm
d>1mm
100nm<d<5mm
20nm<d<2mm
Micro/nanoesferas e capsulas
NANOESFERAS
Monoliticas
NANOPARTICULAS
NANOCAPSULAS
Adapted of Lambert,G. Oligonucleotide and Nanoparticles Page,
<http://perso.clubinternet.fr/ajetudes/nano/index. html> dez/ 2003.
Reservatorio
METODOS DE PREPARAÇÃO
• 1- Através de polimerização de monômeros
• Problemas:
obtidas
induzindo-se
a
polimerização. Difícil controle da extensão
da reação-massa molar não controlada.
Purificação posterior. Interação do polímero
com o ativo.
• 2- Diretamente da macromolécula
ou
polímero pré-formado.
Polímeros biodegradaveis
O
O
O
CH2
C
n
Poli(acido glicolico)
ou PGA
CH3
O
CH
O
C
n
C
(CH2)5
O
Poli (-caprolactona)
ou PCL
n
Poli(acido lactico)
ou PLA
Poly(3-hydroxybutyrate-co-valerate) or PHBV
CH3
O
CH2CH3
O
I
II
I
II
H–[ O– CH – CH2 – C –O– ]m –co – CH – CH2 – C ]n –OH
BIOPOLÍMEROS TÍPICOS
Polímeros biodegradáveis e bioabsorvíveis;
Degradação depende de: MM, estrutura, solubilidade,composição
da cadeia,grau de cristalinidade.
(PLGA)
EMULSIFICAÇÃO/EVAPORAÇÃO DE SOLVENTE
• Trata-se de um método simples, de fácil
transposição de escala e cuja realização em
condições assépticas garante a esterilidade
final do produto.
• Em linhas gerais o polímero é dissolvido
em solvente volátil em água, como CHCl3
ou CH2Cl2. Se dispersa em água por
emulsificação com temnsoativo apropriado.
Algumas revisões: Couvreur et al. Eur. J. Pharm. 41, 2 (1995); Alonso. Nanoparticulate drug
carrier technology. In Cohgen (Ed). Microparticuate Systems for the delivery of proteins and
Vaccines. M. Dekkrt, N.Y. 2996, p. 203; Soppomath et al., J. Control. Rel. 70, 1 (2001).
MÉTODOS MAIS IMPORTANTES DE
PREPARAÇÃO DE NANOPARTÍCULAS
Maria I. Rê e M.F.A. Rodrigues-IPT-2004
1-MÉTODO DE EMULSIFICAÇÃO/EVAPORAÇÃO
DE SOLVENTE
Sanchez et al. Int. J. Pharm. 99, 263
(1993); Zambaux et al. J. Control.
Rel. 50, 31 (1998); Verrechia et al.,
J. Biom. Mater. Res. 27, 1019 (1993)
FASE AQUOSA
Água destilada
Tensoativo
FASE ORGÂNICA
Solvente orgânico
Polímero
Agente ativo
Homogenizaçào
Sonicação
Após a formação da nanoemulsão, o solvente
EMULSÃO
se difunde para a fase externa (extração para
a fase aquosa) até saturação da mesma. Com a
Óleo em água
evaporação das moléculas do solvente que
atingem a interfase fase aquosa-ar, reestabelece-se
o gradiente de concentração, ou seja, a força motriz
para a difusão do solvente orgânico das nanogotas para
a fase aquosa. Ao ser eliminado o solvente, o polímero
precipita levando a formação das nanoesferas.
Extração do solvente
Evaporação do solvente
SUSPENSÃO DE NANOPARTÍCULAS
PREPARAÇÃO
Evaporação de solvente modificado
(nanoesferas).
2 solventes
solúveis
entre si
(um é nãosolvente
para o
polímero)
SEI, 22.000x, 20 kV, topografia
Laboratório -
Preparação: 10% (surfatante), 0,8%
SEI, 2.300 x, 20 kV, topografia
(polímero), 40%etanol/acetona
APLICAÇÃO
1- Formação de nanoesferas para substâncias lipofílicas. Este método
tem sido modificado para uma emulsão múltipla do tipo água/óleo/água.
2- Limitações: a) Emulsão óleo/água deve ter uma fase dispersa (óleo)
bastante fina e homogênea (requer bastante tensoativo e técnicas de
agitação elevada). b) Solventes orgânicos (clorados) e tensoativos usados
(álcool polivinílico, p.ex.) não são compatíveis com aplicações biológicas.
3- Alternativas: Uso de tensoativos como albumina de soro humano .
4- Propriedades otimizadas: diâmetro médio e distribuição de tamanho;
re-suspensão num veículo aquoso sem agregação; teor de fármaco; taxa
de liberação, taxa de degradação; esterilidade; apirogenecidade; e teor de
solvente residual.
5- Variáveis: Volume da fase aquosa para a fase orgânica; concentração
do polímero na fase orgânica; concentração do fármaco na fase orgânica;
presença de tensoativo em ambas fases (orgânica e aquosa); solubilidade
do fármaco na fase aquosa (nível de saturação); método e velocidade de
agitação.
-2-MÉTODO
DE
EMULSIFICAÇÃO
ESPONTÂNEA/DIFUSÃO DE SOLVENTE
(Niwa et al. J. Pharm. Biopharm. 25, 89 91993).
Um solvente miscível em água (acetona, etanol ou
metanol) é misturado ao solvente immiscível (CHCl3,
ou CH2Cl2). A difusão espontânea do solvente miscívil
no meio aquoso cria uma turbulência interfacial entre
as duas fases levando a formação de partículas menores.
Fase aquosa
Fase
orgânica
Difusão rápida do
solvente miscível
com água
Quanto maior a proporção do solvente miscívil na mistura
menores as partículas formadas.
Nanopartículas
3-MÉTODO DE NANOPRECIPITAÇÃO
Envolve o uso de um solvente orgânico que é completamente solúvel na fase
aquosa externa consequentemente a extração e a evaporação do solvente
não são nescesárias para a precipitação do polímero.
FASE AQUOSA
Água destilada
Tensoativo
FASE ORGÂNICA
Solvente orgânico
Óleo
Polímero
Agente ativo
p.ex. acetona
FASE ORGÂNICA
Solvente orgânico
Polímero
Agente ativo
Agitação
nanoesferas
nanocapsulas
SUSPENSÃO DE NANOPARTÍCULAS
Fessi et al. Eur Pat. 0275796 B1 (1987).
Metodo – Encapsulação de agente
ativo
“Nanoprecipitação” – método de deslocação de
solvente
CH 3
HO
CH 2 CH 2 O
CH CH 2 O
m/2
CH 2 CH 2O H
n
m/2
1,2% PLURONIC (1)
3% (PLGA / acetona) + 4 mg de agente ativo (2)
(2) colocado em (1)
PLGA nanoesferas – Encapsulamento de violaceina
PLGA-PLURONIC-PVA system
4-MÉTODO DE SALTING-0UT
Esta é baseada na formação de uma emulsão pela incorporação, sob agitação, de uma
solução aquosa saturada de alcool polivinílico (PVA) em uma solução de polímero dissolvido
em acetona. O PVA tem o papel de estabilizar a dispersão. Aqui a miscibilidade das duas
fases é impossibilitada pela saturação da fase aquosa com PVA. A precipitação do polímero
ocorre quando uma quantidade
FASE ORGÂNICA
adicional de água é adicionada
Solvente orgânico
permitindo então a difusão
Polímero
da acetona para a fase aquosa.
Agente ativo
Este método é adequado quando
ativo e polímeros são solúveis em solventes
FASE AQUOSA
polares como acetona ou etanol.
(sal)
Água destilada
Tensoativo (PVA)
Agitação
Ibrahim et al. Int. J. Pharm.
87, 239 (1992); Allemann et
al., Int. J. Pharm. 87, 247 (1992).
EMULSÃO
Água em óleo
Água destilada
SUSPENSÃO DE NANOPARTÍCULAS
5-MÉTODO DE EMULSIFICAÇÃO/DIFUSÃO DE
SOLVENTE
Envolve o uso de um solvente parcialmente miscível em água, que é previamente saturado
em água para garantir o equilíbrio termodinâmico inicial de ambas as fases. A precipitação
Ocorre quando uma quantidade adicional de água é adicionado ao sistema, permitindo
então a difusão do solvente para a fase aquosa.
Leroux et al. Eur. J. Pharm.
Biopharm. 41, 14 (1995).
Quintanar-Guerreo et al.
Pharm Res. 15, 1056 (1998).
Formada a emulsão do tipo
óleo/água e o tensoativo é
adsorvido na superfície das
gotas da fase orgânica
dispersas na fase aquosa
FASE AQUOSA
(saturada em solvente orgânico)
Água destilada
Tensoativo
Agitação
FASE ORGÂNICA
(saturada em água)
Solvente orgânico
Polímero
Agente ativo
EMULSÃO
A adição de água ao sistema
Óleo em água
desestabiliza o estado de equilíbrio
e promove a difusão do solvente
Água destilada
na fase aquosa levando à formação
das nanopartículas
SUSPENSÃO DE NANOPARTÍCULAS
VANTAGENS
Este método apresenta algumas vantagens sobre
o método de nanoprecipitação como a possibilidade
de controle do tamanho das nanopartículas. Estas
apresentam tamanhos superiores àquelas
preparadas por nanoprecipitação, normalmente
entre 250-600 nm, dependendo de vários
parâmetros como tipo e concentração do
tensoativo e do polímero, tempo e velocidade
de agitação.
Métodos para a preparação de nanopartículas carregadas
com fármacos convencionais
-------------------------------------------------------------Método
Polímero Fármaco Tamanho(nm)
o/w
o/w
o/w
o/w
solv-disp
solv-disp
solv-disp
solv-disp
solv-disp
o/w
o/w
PLA, PLA-b-PEG
PLA-PEG-PLA
PLGA
PEO-b-PBLA
PMLAiPr
PMLAnHe
PLGA
PLGA
PCL, PLA,
PCL-co-PLA
PEO-b-PCL
PLA
Lidocaine
Progesterone
Dexamethasone
Doxorubicin
Halofantrin
Halofantrin
Vancomycin
Procaine Hydr.
Nimodipine
Enalapril maleate
Lidocaine
247-817
193-335
109-155
37
150-160
90-190
160-170
<210
81-132
50
115-123b
PBLG = poly(g-benzyl L-glutamate); PBLA = poly(b-benzyl L-aspartate); PMLAiPr =
poly(b-malic acid isopropil ester); PMLAnHe = poly(b-malic acid neohexil ester).
b Dimension of unloaded particles.
a
PREPARAÇÃO DE MICRO E NANOPARTICULAS CARREGADAS COM
FÁRMACOS PROTEÍCOS.a
Método
Polímero
Proteina
Tamanho (nm)
w/o/w
w/o/w
w/o/w
w/o/w
w/o/w
w/o/w
w/o/w
w/o/w
w/o/w
w/o/w
w/o/w
PLGA
PLGA
PLGA
PLGA, PLA
PLGA/PLA blend
PLGA, PCL
PLA
PLGA
FITC-HRP
PLGA
PLGA
PLGA
Biod. polym.
PLGA
PLGA
PEG-PLGA
PEG-co-PBT
w/o/w
PLGA-b-PEO
w/o/w
w/o/w
o/w
o/w
L-asparaginase
BSA
BSA
BSA
BSA
BSA
Protein C
FITC-BSA
196-226
ms
100-200
ms
ms
20-1000
230-340
ms
TRH
IL-1a+BSA
Rism. porcine ms
Peptides
BSA
rhBMP
BSA
BSA
250-800
ms
BSA
300-600
ms
ms
ms
ms = microsize; CP = coprecipitation; FITC-BSA = fluorescein isothiocyanate-labeled BSA; FITC-HRP = fluorescein
isothiocyanate-labeled horseradish peroxidase; IL-1a = recombinant human interleukin-1a; rhBMP = recombinant
human bone morphogenetic protein-2
a
Exemplo de encapsulação
utilizando nanocápsulas.
PREPARAÇÃO
Controle das variáveis de processo
temperatura
[tensoativo]
[polímero]
evaporação
Não
solvente
Sim
agitação
Precipitação
coágulos
agregados
grandes
espuma
Modo adição
Formas
arredondadas
superfície lisa
baixa
polidispersidade
BSA/PHB159
BSA/PHBV140
BSA/PHB540
BSA/PHB273
1.- PHBV140 libera menos BSA que PHB159 (Diferencias de porosidade nas matrizes) PHBV é
menos porosa que PHB.
2.- Pouca diferencia entre PHB540 e o 273. (Conway et al. J. Control. Rel. 49, 1 (1997)
The effect of type of organic phase solvents on the
particle size of
poly(d,l-lactide-co-glycolide) nanoparticles.
Song et al. Colloids and Surfaces A: Physicochem. Eng.
Aspects 276 (2006) 162–167
Nanoparticulas de PLGA foram preparadas por método de
emulsificação/difusão.
Efeito de 4 solventes no tamanho da partícula: acetato de etila,
carbonato de propileno, acetona e diclorometano.
Tres estabilizadores foram usados: Didodecil dimetil brometo de amonio
(DMAB), poli(vinil alcool) (PVA) e Pluronic F68.
Preparação: 100 mg de PLGA foi dissolvido em 10 ml de vários solventes (EA,
PC, ACE,e DCM). As fases orgânicas foram adicionadas em 20 ml de uma fase
aquosa contendo o estabilizador. Após uma saturação mutua da fase orgãnica
e a aquosa, a mistura foi emulsificada por 1 min com um sonicador de ponta.
Para permitir a difusão do solvente orgânico na água, um volume constante de
água (80 ml) foi subsequentemente adicionado a emulsão o/w sob uma
agitação magnética moderada formando as nanopartículas de PLGA
A distribuição do valor médio de tamanho da
partícula forma medidas por espectroscopia de
correlação de fótons (NICOMP, model 380, CA,
USA). O tamanho da partícula foi expressa como
diâmetro médio em volume-peso em nanômetro, e
obtido de medidas de três bateladas de
nanopartículas.
Partículas pequenas foram obtidas usando solventes parcialmente solúveis em
água (EA, PC), entretanto partículas grandes foram obtidas usando solvente
totalmente solúveis em água (ACE) e solvente imiscíveis em água (DCM). Como as
nanopartículas são formadas das gotas de emulsão após difusão do solvente
orgânico, seu tamanho é dependente da estabilidade das gotas da emulsão, que
colidem e coalescem ou aderem ou aglutinam entre elas. Quando o estabilizador
permanece na interfase liquido–liquido durante o processo de difusão, e seu efeito
protetor é adequado e logo as nanopartículas são formadas. As partículas
pequenas para EA e PC foram atribuídas tanto a a proteção adequada do
estabilizador contra a coalescencia e a baixa tensão interfacial entre as fases
aquosa e orgânica, resultante de sua natureza de solubilidade parcial em água.
EA
DCM
ACE
AC
Quando EA, um solvente orgânico parcialmente solúvel em água foi usado, foram
formadas uma pequena e discreta partículas de tamanho de 40–70 nm. Por outro lado,
partículas grandes e agregados de 350–450 nm foram observados em DCM como
solvente orgânico imiscível em água. Quando ACE, solvente orgânico completamente
solúvel em água foi usado, partículas grandes e discretas de 250–400 nm foram
obtidas. Das imagens de AFM, pode ser visto que nanopartículas abaixo de 70 nm são
obtidas usando um solvente parcialmente solúvel em água (EA) que quando usou-se
um solvente imiscível em água (DCM) ou um solvente completamente solúvel em água
(ACE). Isto está de acordo com os resultados da distribuição de tamanho de partícula
nas Figura 1.
OS AUTORES EXPLICAM ISTO DA SEGUINTE MANEIRA
As partículas pequenas para EA e PC foram atribuídas tanto a proteção
adequada do estabilizador contra a coalescencia e a baixa tensão interfacial entre
as fases aquosa e orgânica, resultante de sua natureza de solubilidade parcial
em água. Entretanto, quando DCM foi usado como solvente na fase orgânica
praticamente cada formulação resultou em agregação significativa devido a sua
natureza imiscível com água e o estabilizador DMAB não foi capaz de prevenir
completamente a agregação dos gotas de emulsão, levando a tamanhos de
partículas grandes (390 nm). de outra maneira, como ACE é completamente
miscível com água, emulsões estáveis entre as fases orgânicas e aquosas não
são formadas a pesar da presença de um estabilizador. Logo após de misturar
as duas fases, PLGA imediatamente precipita como partículas sub-micron
resultando em partículas de tamanho grande.
Contrariamente ao resultado de DMAB na Fig. 1, pequenos tamanhos de partículas
abaixo de 70 nm não foram, obtidas por PC e EA, e não houve uma grande diferencia
na distribuição do tamanho das partículas entre solvente parcialmente solúveis em água
(EA e PC) ou solvente totalmente solúvel em água (ACE) e em solvente imiscível em água
(MCD) em PVA ou Pluronic F68. Em particular, os tamanhos médios de partículas de
nanopartículas de PLGA estabilizadas com PVA mostraram valores similares na Fig. 3,
independente na diferencia do solvente na fase orgânica. Também interessante para
Pluronic F68 na Fig. 4 que EA mostra tamanho menor que em PC, que mostra diferente
perfil com os resultados de DMAB e PVA na Figs. 1 e 3, respectivamente. Em sistemas de
estabilizante não iônicos (PVA e Pluronic F68), as partículas estão estabilizadas por
impedimento estérico, mas num sistema de estabilizador iônico (DMAB), as partículas
são estabilizadas por repulsão eletrostática. Os resultados acima significam que o
efeito do tipo de solvente na fase orgânica para obter nanopartículas pequenas de
PLGA abaixo de 70 nm chega a ser mais importante quando partículas são estabilizadas
por repulsão eletrostática que impedimento estérico.
As partículas menores (50 nm) foram obtidas usando DMAB (estabilizador) e PC
(solvente na fase orgânica), entretanto, as partículas maiores (461 nm) foram
obtidas usando Pluronic F68 (estabilizador) e DCM (solvente na fase orgânica).
Estes resultados indicam que a escolha adequada do solvente na fase orgânica
e estabilizador é o fator chave na determinação do diâmetro médio das
nanopartículas de PLGA.
SOLVENTE: PC
O tamanho das partículas para PVA e Pluronic F68 diminui rapidamente com
pequenas mudanças na concentração mas muito pouco para DMAB. Isto indica que
com aumento da concentração do estabilizador para PVA e Pluronic F68, mais
moléculas do estabilizador são adsorvidas na interfase das gotas de emulsão,
permitindo um aumento na proteção contra a coalescencia e resultando em gotas
menores da emulsão. Outros autores prepararam nanopartículas de
poli(metilmetacrilato)
(PMMA)
usando
PVA
como
estabilizante
por
emulsificação/difusão, e pesquisaram o efeito da concentração do PVA no tamanho
das nanopartículas de PMMA. Eles observaram que a estabilidade física das
nanopartículas de PMMA aumentou com aumento de concentração de PVA, levando
a nanopartículas de tamanhos menores. Entretanto, para DMAB, somente uma
pequena quantidade de estabilizador é adsorvida na interfase das gotas da emulsão.
O excesso permanece na fase aquosa continua e não joga nenhum papel
significativo na emulsificação. O tamanho médio das nanopartículas de PLGA
preparadas usando DMAB como estabilizante é menor que aqueles com PVA e
Pluronic F68, que está de acordo com os resultados dos outros autores.
Quando EA e PC, solventes parcialmente solúveis em água, o tamanho médio
diminui rapidamente quando aumenta o volume de água adicionado na faixa
de 20–40 ml, mas pouca mudança foi observada acima de 80 ml. Entretanto,
para ACE, um solvente totalmente solúvel em água, o volume de água adicionado
não joga papel importante no tamanho da partícula comparado EA e PC, e o
tamanho da partícula diminui moderadamente quando aumenta o volume de
água adicionado. Estes resultados significam que o volume adicionado de água
é um fator importante na determinação do tamanho da partícula de PLGA
para solventes parcialmente solúveis em água como PC e EA. Também, foi
observado que o tamanho médio das partículas de PLGA preparadas usando
ACE são maiores que aquelas com EA e PC, que estão de acordo com os
resultados da distribuição do tamanho das partículas na Fig. 1.
CONCLUSÕES
A solubilidade dos solventes na fase orgânica em água foi
um parâmetro importante afetando o tamanho médio de
nanopartículas de PLGA, quando DMAB, um
estabilizador iônico é usado. nanopartículas abaixo de 70
nm foram obtidas usando solventes parcialmente solúveis
em água (EA e PC) que quando usados um solvente
totalmente solúvel em água (ACE) ou solventes imiscíveis
em água (DCM). Em particular, quando PC foi usado
como solvente na fase orgânica, nanopartículas de PLGA
abaixo de 50 nm foram obtidas. Entretanto, quando PVA e
Pluronic F68, estabilizadores não iônicos foram usados,
uma grande diferencia na distribuição do tamanho das
partículas entre solvente parcialmente solúvel em água ou
totalmente solúveis em água e em solvente imiscível em
água não foi observado, e todas as partículas mostraram
um grande diâmetro acima de 110 nm, independentemente
do tipo de solventes orgânicos.
MODOS DE INTERAÇÃO DE PVA DURANTE
PROCESSO DE EMULSIFICAÇÃO
(enredado)
Fig. 1. Diagrama ilustartivo de sistemas de longa circulação. Nanopartículas de
poliestireno coberta com Poloxameros e Poloxaminas. (b)nanopartículas de Poliestireno
grafted com PEO. (c) nanopartículas de copolímero de Polilactideoglicolideo com
polilactideo/glicolideo-PEO, coberto (A) ou preparado de um solvente comum (B) .
(d) (‘Self-forming’) Sistema de copolímero em bloco polilactideoglicolideo-PEO.
Stolnik et al., Advan. Drug Deliver. Rev. 16, 195 (1995).
NANOPARTICULAS DE
MACROMOLÉCULAS
Pinto Reis et al. / Nanomedicine: Nanotechnology, Biology, and Medicine 2 (2006) 8– 21
• NANOPARTICULAS DE ALGINATO
• Produzidas por extrusão de gotas de uma solução
alginato sódico numa solução de cloreto de cálcio. Os
tamanhos das partículas de alginato dependem do
tamanho das gotas iniciais. Num avanço adicional as
partículas de alginato tem sido produzidas usando um
método de gelação modificado de emulsificação/gelação
interna como ilustrada na Figura
NANOPARTICULAS DE
MACROMOLÉCULAS
Pinto Reis et al. / Nanomedicine: Nanotechnology, Biology, and Medicine 2 (2006) 8– 21
• NANOPARTICULAS DE QUITOSANO
• Os métodos propostos para preparar nanopartículas de
quitosano estão baseadas na formação espontânea do
complexo entre quitosano e polianios (tripolifostato) ou
gelação de uma solução de quitosano disperso numa emulsão
de óleo. Vários métodos para produzir nanopartículas de
quitosano são descrito na literatura. nanopartículas de
quitosano produzidos por gelação num método baseado na
emulsificação está ilustrado na Figure
NANOPARTICULAS DE
MACROMOLÉCULAS
Pinto Reis et al. / Nanomedicine: Nanotechnology, Biology, and Medicine 2 (2006) 8– 21
• NANOPARTICULAS DE AGAROSE
• Nanopartículas de agarose foram desenvolvidas para a
administração de terapêuticos de proteínas e peptídeos.
• nanopartículas de agarose foram produzidos pela
tecnologia baseada em emulsão como ilustrado na Figura
Preparação de nanocapsulas de PCL e PCL-PEG
Determinação de encapsulação
Caracterização das nanocapsulas
Determinação de toxicidade aguda (LD50)
Eficácia antimalaria
Determinação de parâmetros cardiovasculares
Estatistica
Nota: halofantrine é um fármaco mais
cardiotóxico dos usados em malaria. Induz uma
prolonga intervalo de QT já que é responsável de
alterar os canais de potássio produzindo uma repolarização
que determina o intervalo QT
Efeito cardiotóxico
Percentage variation of QT interval (A). The values represent means±S.E.M. (standard error mean) for 30 min after
IV injection of halofantrine solution (Hf. HCl), halofantrine entrapped in nanocapsules (Hf-NC) in doses of 100 mg/kg
(n=6) or 150 mg/kg (n=8), unloaded NC (n=8) and DMA/PEG solution (n=8).
QT= interval between the beginning of the Q wave and the end of the T wave of ECG
AGRADECIMENTOS