EEB. HÉLIO WASUM – SUL BRASIL – SC
PROJETO DE UTILIZAÇÃO DA
INFORMATICA EM SALA DE AULA
Prof. Rosilene Verde Brustolin
Química Orgânica – 3 série- Ensino Médio
2008
1
QUÍMICA ORGÂNICA
LIGAÇÕES QUÍMICAS
GEOMETRIA MOLECULAR
HIBRIDIZAÇÃO
Prof. Rosilene Verde Brustolin
Química Orgânica – 3 série - Ensino Médio
2008
2
Geometria molecular
• O arranjo tri-dimensional dos átomos em
uma molécula geometria molecular
• A teoria da repulsão dos pares de elétrons
(ligantes e não-ligantes) procura explicar o
arranjo dos átomos numa molécula.
3
Teoria da repulsão dos elétrons
• Eletrons são partículas carregadas negativamente,
portanto se repelem mutuamente.
• Os elétrons ocuparão posições tais que minimizem os
efeitos de suas repulsões (ocupando regiões o mais
afastado possível uns dos outros).
• Num átomo os elétrons ocupam determinados
espaços chamados orbitais (máximo 2e num orbital).
• Tipos de orbitais mais comuns: orbitais s ; p ;
4
REVENDO O ORBITAL s
FORMA DOS ORBITAIS
z
y
x
orbital s
5
REVENDO OS 3 ORBITAIS p
FORMAS DOS ORBITAIS
z
y
x
pz orbital
px orbital
py orbital
6
Exemplo da geometria de uma molécula
com mais de um átomo central
• Observa-se que um dos carbonos da molécula é
tetraédrico e o outro é trigonal plano (explicação
fica para após o conceito de hibridação).
7
Momento dipolar
• A molécula de HF tem uma ligação polar –
uma separação de cargas devido a diferença
de eletronegatividade existente entre o F e o
H.
• A forma da molécula e a grandeza do dipolo
explicam a polaridade total da molécula.
+H-F
8
Momento dipolar e geometria
•
Moléculas diatômicas homonucleares não
apresentam momento dipolar (O2, F2, Cl2, etc);
•
Moléculas triatômicas ou maiores ( dependem
do efeito resultante de todas ligações polares
existentes na molécula).
•
Em moléculas como CCl4 (tetraédricas) BF3
(trigonal planar) todos vetores das ligações
polares individuais se cancelam resultando
em nenhum momento dipolar(zero).
9
O momento dipolar depende da
geometria da molécula
10
Mais exemplos polaridade e geometria
11
Ligações covalentes
• Resultam da sobreposição dos orbitais
atômicos dos átomos que participam da
ligação.
• Os átomos compartilham o par eletrônico
existente na ligação.
• A ligação covalente pode ser polar ou
apolar.
• Podem ser do tipo sigma (σ) ou pi (π)
12
A molécula de H2
• Observa-se uma ligação covalente simples
resultante da sobreposição de um orbital 1s
de cada um dos átomos de hidrogênio.
• Observa-se que a ligação tem uma simetria
cilíndrica sobre o eixo que une o centro dos dois
átomos. Isto é conhecido como ligação .
• A ligação no H2 (H-H”) pode ser resumida em:
1s (H) – 1s(H”) ligação
13
A ligação covalente no H2
• Interpenetração de orbitais (ligação sigma s-s)
H
H
Região da sobreposição
14
A ligação no H2
• SIMETRIA CILÍNDRICA DA LIGAÇÃO SIGMA
H
H
15
2 átomos de H separados
Cada átomo de H apresenta 1 eletron no orbital do subnível
1s. Este elétron encontra-se atraído pelo único próton
existente no núcleo do átomo de H.
16
Início da formação do H2
Os átomos de H se aproximam acontecendo a sobreposição
dos orbitais 1s. Cada elétron começa a sentir a força
atrativa de ambos prótons dos núcleos.
17
Ligação sigma s-s quase completa no H2
18
Molécula de H2 com seu orbital molecular
Na molécula de H2 os dois orbitais atômicos 1 s dão origem
a um orbital molecular que engloba os dois elétrons
existentes na ligação covalente.
19
A molécula de Cl2
• Observa-se uma ligação simples originada
da união de dois orbitais 3p, cada um
pertencente a um dos átomos de cloro.
Cl
Resumo
Cl
3pz (Cl ) – 3pz (Cl”)ligação sigma
20
A ligação p-p
• Simetria cilíndrica
Cl
Cl
21
Uma Molécula Linear
A molécula de BeH2
Região da ligação
H
Be
H
22
23
GEOMETRIA DAS MOLÉCULAS
• Muitas propriedades (ex:reatividade) das
moléculas estão relacionados com sua forma.
• A forma é dependente do ângulo das ligações
e do comprimento das ligações.
• Utiliza-se o conceito de hibridização dos
átomos numa molécula para explicar a forma
dessa molécula.
24
Hibridização de orbitais atômicos
• É a mistura de orbitais pertencentes a um mesmo
átomo, originando novos orbitais iguais entre si,
mas diferentes dos orbitais originais.
• A diferença destes novos orbitais atômicos,
denominados orbitais híbridos, acontece tanto na
geometria(forma) como no conteúdo energético.
• O número dos orbitais híbridos obtidos será o
mesmo dos orbitais existentes antes de serem
misturados.
25
ORBITAIS ANTES DA
HIBRIDAÇÃO
x
hibridização
s orbital
px orbital
z
y
pz orbital
py orbital
26
ORBITAIS APÓS
HIBRIDAÇÃO (sp3)
z
x
4 x sp3
orbitais híbridos
27
Hibridização sp3
• É a mistura de 3 orbitais p “puros” com um
orbital s “puro”, formando 4 novos orbitais
“híbridos” denominados sp3.
• A geometria dos 4 orbitais sp3 é tetraédrica (os 4
orbitais partem do centro do tetraédro e dirigemse, cada um, para um dos vértices do tetraédro).
• O ângulo entre os orbitais sp3 será de aprox.109°.
• Acontece no C que se liga através de 4 ligações
simples ( o C é tetravalente).
28
A formação dos híbridos
3
sp
29
Exemplo de hibridação sp3 CH4
• No CH4, os 4 orbitais híbridos sp3 do C se
ligam com os orbitais s de 4 átomos de H,
formando 4 ligações sigma C-H
[sp3 (C) – 1s (H) ] x 4
ligação
30
.
.
C. .
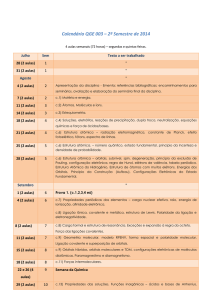
O carbono possui 4 elétrons de valência 2s22p2
O carbono é tetravalente.
O carbono pode formar ligações simples, duplas e
triplas.
O carbono pode apresentar orbitais híbridos do tipo sp, sp2
e sp3.
31
2p
hibridação
2s
sp3
32
H
H
H
H
33
Fórmula molecular do metano: CH4
H
Fórmula estrutural do metano: H
C
H
H
Lembrando, 4 ligações simples sp3 ( 4 orbitais híbridos).
Hidrogênio possui 1s orbital não hibridizado.
34
Metano
35
FORMA DAS MOLÉCULAS
sp3 - tetraédrica
H
C
N
H
H
H
sp3
H
H
O
H
H
sp3
H
sp3
36
FORMA DAS MOLÉCULAS
esta ligação está se
afastando de você
H
C
H
H
H
esta ligação está indo em sua direção
37
MOLÉCULA DO CH4
38
39
A molécula de CH4
40
Hibridização
2
sp
• É a mistura de um orbital s com dois orbitais p
(pertencentes a um mesmo átomo), resultando em
3 novos orbitais denominados híbridos sp2.
• Os três orbitais híbridos sp2 situam-se num mesmo
plano formando ângulos de 120° entre si
(geometria plana triangular).
• Acontece com C que possua uma dupla ligação.
• Num C do tipo sp2 existirá um orbital p “puro”
que será responsável pela ligação covalente do
tipo pi.
41
HIBRIDIZAÇÃO DO CARBONO sp2
Etileno
H
H
C
C
H
H
Cada carbono é hibrido sp2 . O hidrogênio é 1s.
Uma ligação da dupla é sp2 - sp2. A outra é p - p.
2p
2p
hibridação
2s
sp2
42
C
C
Observe que a dupla ligação consiste numa ligação
do tipo e outra do tipo p.
43
H
H
C C
H
H
H
H
C
H
C
H
44
Exemplo de hibridação sp2 H2C=CH2
• Molécula de eteno (etileno).
• Os dois átomos de C encontram-se ligados
por uma dupla ligação Uma ligação sigma
sp2-sp2 e uma ligação pi).
• Cada átomo de C encontra-se ligado a dois
átomos de H (duas ligações sigma s-sp2).
45
A Molécula de C2H4
46
Os ângulos de ligações no C2H4
• Como os átomos centrais são dois carbonos
de hibridação sp2 o ângulo entre as ligações
sigma será de 120. observe que a ligação
p é perpendicular ao plano que contém a
molécula.
• C com uma dupla ligação hibridação sp2
Numa dupla ligação uma ligação e uma ligação p
47
HIBRIDIZAÇÃO sp2
sp2 - trigonal planar
p ligação
H
H
C
H
H
C
H
C
H
eteno
(etileno)
H
H
120°
C
C
H
H
H
C
H
ligação
48
FORMA DA MOLÉCULA
sp2 - trigonal planar
C
ligação
C p ligação
H
H
C
orbital p vazio
H
C
H
49
50
51
OUTRAS MOLÉCULAS PLANAS
TRIGONAIS
hibridação sp2 geometria trigonal planar
H
C O
H
H
C N
H
H
H
H
H
H
H
H
neste exemplo, cada
carbono é sp2
52
Hibridação sp
• É a mistura de um orbital s com 1 orbital p,
produzindo dois novos orbitais denominados
híbridos sp.
• Os orbitais híbridos sp formam um ângulo de 180
entre si.
• A geometria molecular será linear.
• Surge em C com duas duplas ou C com uma tripla
ligação.
• Numa tripla ligação ter-se-á uma ligação sigma e
duas pi.
53
Etino (Acetileno)
54
Exemplo de hibridação sp C2H2
• Etino (acetileno)
• Em torno dos átomos de C existem dois orbitais híbridos sp
e dois orbitais p “puros”.
• Os dois orbitais híbridos se ligarão através de ligações
sigma s-sp (H-C) e sigma sp-sp(C-C).
• Os dois orbitais p de cada carbono se ligarão produzindo
duas ligações pi entre os carbonos (resultando numa tripla
ligação entre os dois carbonos).
• Liga tripla uma ligação e duas ligações p
55
Fórmula estrutural do acetileno
H C
C
H
Cada átomo de carbono é um híbrido sp.
Os hidrogênios possuem orbitais 1s, não hibridizados.
2p
2p
hibridação
sp
2s
Observe que a tripla ligação consiste de uma e 2p .
As duas ligações p provem dos orbitais p, não hibridizados.
56
H C C H
H
C
C
H
57
A Molécula de C2H2
58
Tipos de ligações no C2H2
• No acetileno existem 3 tipos de ligações:
ligações sigma s-sp; ligação sigma sp-sp;
ligações pi
[sp (C 1 ) – 1s (H) ] x 2
tipo
[sp (C 1 ) – sp (C 2 ) ]
tipo
[2py (C 1 ) – 2py (C 2 ) ]
tipo p
[2pz (C 1 ) – 2pz (C 2 ) ]
tipo p
59
Dúvidas?
Perguntas?
60