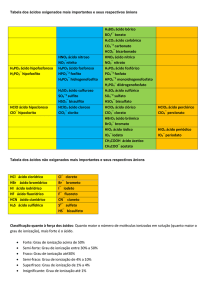
Funções Inorgânicas 4 – ácidos
Ácidos
Segundo Arrhenius, são compostos que, em solução aquosa, fornecem um único tipo de cátion, o
íon H+, num fenômeno físico conhecido como ionização.
Exemplos:
HCl(aq)
Ácido clorídrico
HNO3 (aq)
Ácido nítrico
H+(aq)
H+(aq)
+
Cl-(aq)
ânion cloreto
+
NO31- (aq)
ânion nitrato
As representações acima são simplificadas. Na verdade, o que ocorre é a ligação do H + com a
água, formando o cátion H3O+ (“hidrônio” ou “hidroxônio”).
Exemplos:
HCl
+
Ácido clorídrico
HNO3
Ácido nítrico
H3O+(aq)
H2O
+
H2O
+
H3O+(aq)
Cl-(aq)
ânion cloreto
+
NO31- (aq)
ânion nitrato
Note que, apesar de serem compostos moleculares, os ácidos são capazes de liberar íons
em meio aquoso. Essa é uma importante particularidade dos ácidos, pois, na qualidade de
substâncias moleculares (puros), eles não conduzem corrente elétrica. Mas, quando dissolvidos
em água, conseguem conduzir eletricidade, pois há íons em solução aquosa, como se fossem
substâncias iônicas dissolvidas.
Quanto mais forte é o ácido, maior a quantidade de íons em solução e maior sua condutividade
elétrica em solução aquosa. Quando um ácido é fraco, significa que um pequeno percentual de
suas moléculas sofreu ionização em contato com a água, ficando a maior parte delas, intactas,
apenas dissolvidas em água, sem sofrer ionização. Mesmo um ácido forte, se não estiver
dissolvido em água, não será condutor de eletricidade, pois suas moléculas não estarão
“quebradas” na forma de íons.
Notação dos “hidrácidos” (ácidos sem oxigênio)
Fórmula geral: HxE
“E” é, geralmente, um elemento da coluna VIA ou VIIA.
E “x” é o índice do hidrogênio, que corresponde ao Nox negativo do elemento “E”.
Exemplos: HBr (ácido bromídrico), H2S (ácido sulfídrico) e HCN (ácido cianídrico)
Notação dos “oxiácidos” (ácidos com oxigênio)
Fórmula geral: HxEOy
“E” é, geralmente, um elemento da coluna VIA ou VIIA.
O “x” é o índice do hidrogênio, que corresponde à carga do ânion EOyx-.
O “y” é o número de oxigênios no ânion e no ácido.
Exemplos: HClO3 (ácido clórico), H2SO4 (ácido sulfúrico) e HSO3 (ácido sulfuroso)
Importante (chuva ácida, a origem)
A fórmula de um oxiácido é obtida pela soma de uma molécula de água com um óxido ácido
(anidrido) de mesmo nome que o ácido.
Exemplos
CO2
+
Anidrido carbônico
H2O
↔
H2CO3
(reação reversível)
ácido carbônico
SO3
+
Anidrido sulfúrico
H2O
→
H2SO4
ácido sulfúrico
N2O5
Anidrido nítrico
+
H2O
→
2 HNO3
ácido nítrico
Como os óxidos ametálicos são geralmente poluentes atmosféricos produzidos a partir da queima
de combustíveis fósseis, eles reagem com a água da atmosfera e produzem ácidos dissolvidos na
água da chuva (chuva ácida). O ácido carbônico contribui com a acidez natural da chuva, que é
uma acidez fraca (pH entre 7 e 5,5), pois o ácido carbônico é um ácido fraco, além de se
decompor facilmente em gás carbônico e água novamente. Mas os ácidos nítrico e sulfúrico são
bem mais fortes e os mais presentes na chuva poluída, denominada “chuva ácida” (pH abaixo de
5,5).
Importante (ácidos orgânicos)
Observe que, tanto nos hidrácidos quanto nos oxiácidos, a fórmula é iniciada por um ou mais
átomos de hidrogênio. Mas, nos ácidos orgânicos, isso não ocorre. O hidrogênio que ioniza é o
último da fórmula.
Exemplo de ácido orgânico mais comum:
CH3COOH(aq)
“ácido acético” ou
“ácido etanóico”
(presente no vinagre)
→
CH3COO-(aq)
+
ânion “acetato”
ou “etanoato”
H+(aq)
Importante (força dos ácidos orgânicos)
Todos os ácidos orgânicos são fracos, ou seja, menos de 5% de suas moléculas ionizam em meio
aquoso e as demais permanecem apenas dissolvidas, porém “inteiras”; por isso, conduzem
fracamente a eletricidade em solução aquosa.
Obs.: Ácidos fortes ionizam mais de 50% de suas moléculas em água; e ácidos moderados
ionizam entre 5 e 50%.
Nomenclatura dos ácidos (hidrácidos)
Os hidrácidos não são derivados da reação de óxidos com água. Por isso, não possuem oxigênio
e o Nox do elemento ligado ao hidrogênio é sempre negativo.
Ácido _______________________________+ ídrico
(nome do elemento)
Exemplos: HCl (ácido clorídrico),
H2S (ácido sulfídrico),
HCN (ácido cianídrico).
Nomenclatura dos ácidos (oxiácidos)
Ácido _______________________________
(nome do óxido ácido que gera o ácido em reação com água)
Exemplos:
CO2
óxido (ou anidrido)
carbônico
+
H2O
H2CO3
ácido carbônico
SO3
+
óxido (ou anidrido)
sulfúrico
H2O
H2SO4
ácido sulfúrico
SO2
+
óxido (ou anidrido)
sulfuroso
H2O
H2SO3
ácido sulfuroso
Observação: Se o elemento central tiver dois Nox, pode-se, a partir da fórmula do ácido, calcular
o Nox do elemento central e determinar se o sufixo do nome do ácido será “oso” (menor Nox) ou
“ico” (maior Nox). Para isso, basta considerar cada hidrogênio com Nox = 1+, cada oxigênio com
Nox = 2- e a soma de todos os Nox da fórmula como zero.
Exemplo:
H2SO4
2 (+1) + S + 4(-2) = 0
S = +8-2 = +6
(+6 é o maior Nox positivo do enxofre, que possui Nox +4 e +6;
portanto, sufixo “ico”, ácido sulfúrico)
Casos especiais de ácidos
1) Óxidos que reagem com uma, duas ou três moléculas de água
Os elementos boro (5B), de Nox 3+, arsênio (33As), fósforo (15P) e antimônio (51Sb), os três de Nox
3+ e 5+, formam ácidos diferentes, a partir da reação de seus óxidos com 1, 2 ou 3 moléculas de
água. O nome dos ácidos será acrescido dos prefixos “meta” (1H2O), “piro” (2H2O) ou “orto”
(3H2O), sendo este último facultativo.
Óxido ácido
+ 1H2O
→ ácido meta _____________
(nome do óxido)
Óxido ácido
+ 2H2O
→ ácido piro _____________
(nome do óxido)
Óxido ácido
+ 3H2O
→ ácido (orto) _____________
(nome do óxido)
Exemplos:
P2O3: óxido (ou anidrido) fosforoso
P2O3
+
1H2O (→ H2P2O4 , simplificando os índices por dois) → 2 HPO2
ácido metafosforoso
P2O3
+
2H2O
P2O3
+
3H2O (→ H6P2O6 , simplificando os índices por dois) → 2 H3PO3
ácido fosforoso
→ H4P2O5
ácido pirofosforoso
P2O5: óxido (ou anidrido) fosfórico
P2O5
+
1H2O → (H2P2O6 , simplificando os índices por dois)→ 2 HPO3
ácido metafosfórico
P2O5 +
2H2O
→
H4P2O7
ácido pirofosfórico
P2O5
+ 3 H2O → (H6P2O8 , simplificando os índices por dois)→ 2 H3PO4
ácido fosfórico
2) O caso do boro (5B)
O boro é capaz de formar um quarto ácido, a partir da reação de DUAS moléculas de seu óxido
com UMA molécula de água.
2 B2O3
+
óxido (ou anidrido) bórico
H2O
H2B4O7
ácido tetrabórico
3) O caso do cromo (24Cr)
O cromo pode formar dois ácidos, variando a quantidade de óxido com água:
CrO3
+ H2O
óxido (ou anidrido) crômico
H2CrO4
ácido crômico
2 CrO3 + H2O
óxido (ou anidrido) crômico
H2Cr2O7
ácido bicrômico (ou dicrômico)
Classificação dos ácidos
Quanto à presença de oxigênio
a)
b)
Hidrácidos
Exemplos: HCl, H2Se, HCN
Oxiácidos
Exemplos: H2SO4, HNO3, H3PO4
Quanto ao número de hidrogênios ionizáveis
a)
Monoácidos ou ácidos monopróticos.
Exemplo: HMnO4
b)
Diácidos ou ácidos dipróticos.
Exemplo: H2SO3
c)
Triácidos ou ácidos tripóticos, etc.
Exemplo: H3BO3
Obs.: a palavra “prótico” se refere ao hidrogênio (1H) na forma de H+; que, tendo perdido o único
elétron que possuía, restou apenas o próton em seu núcleo atômico, e sua eletrosfera ficou
vazia. Assim, o ácido capaz de ionizar apenas um hidrogênio (H +) é monoprótico, pois libera um
próton para o meio aquoso.
Quanto à força do ácido
a)
Ácidos fortes: apresentam elevada tendência de sofrer ionização. Se mais de 50% de
suas moléculas ionizam (coeficiente ou grau de ionização), o ácido é considerado forte.
b)
Ácidos fracos: apresentam baixa tendência de sofrer ionização. Se um ácido ioniza
menos de 5% de suas moléculas em água, o ácido é considerado fraco.
c)
Ácidos moderados: possuem grau de ionização entre 5% e 50% de suas
moléculas.
Como deduzir a força dos ácidos pela fórmula
A força dos ácidos é definida experimentalmente. Mas pode-se ter uma ideia comparativa da
força entre eles, a partir da fórmula.
Para os oxiácidos, subtraindo-se o número de oxigênios pelo número de hidrogênios da fórmula,
quanto maior a diferença, maior a força do ácido.
a) Oxiácidos: HxEOy
b)
se y – x
se y – x < 2
2
ácido forte
ácido fraco
Hidrácidos: Família 7A: HF, HCl, HBr, HI
(fortes, sendo HF fraco)
(aumenta a força da esquerda para a direita
; ou melhor, de cima para baixo na
tabela periódica)
Família 6A e HCN
todos fracos
Ionização parcial e total de poliácidos
Um ácido com mais de um hidrogênio ionizável pode liberá-los no meio aquoso de várias formas,
podendo ser todos (ionização total) ou alguns (ionização parcial). Isso depende de vários fatores
do ambiente, como temperatura, concentração do ácido na água, presença ou não de outras
substâncias ácidas ou básicas etc.
Exemplo: ácido sulfúrico (H2SO4)
H2SO4 (aq) →
H+(aq) +
ácido
HSO41- (aq) →
H+(aq)
+
hidrogenosulfato
H2SO4(aq) →
HSO41-(aq)
(etapa 1 da ionização parcial, liberando o 1º H+)
hidrogenosulfato
SO42- (aq)
(etapa 2 da ionização parcial, liberando o 2º H+)
sulfato
2H+(aq)
+
ácido
SO42-
(aq)
(ionização total)
sulfato
Exemplo: ácido fosfórico (H3PO4)
H3PO4 (aq) →
H+(aq) +
ácido
H2PO41-(aq) →
H+(aq)
H+(aq)
H1PO42-(aq)
+
PO43-(aq)
hidrogenofosfato
H3PO4(aq) →
3H+(aq)
ácido
(etapa 1 da ionização parcial, liberando o 1º H+)
dihidrogenofosfato
+
dihidrogenofosfato
H1PO42-(aq) →
H2PO41-(aq)
(etapa 2 da ionização parcial, liberando o 2º H+)
hidrogenofosfato
(etapa 3 da ionização parcial, liberando o 3º H+)
fosfato
+
PO43-
(aq)
(ionização total)
sulfato
Propriedades dos ácidos
Têm sabor azedo.
Conduzem a corrente elétrica em solução aquosa, pois liberam íons (ionização). Os ácidos
fortes conduzem melhor a eletricidade, pois liberam mais íons em solução do que os ácidos
fracos.
Produzem pH < 7. Quanto mais baixo o valor do pH, maior a acidez do meio. A escala de pH
é formada por expoentes na base 10 da concentração de íons hidrogênio; isto significa que
um meio de pH 4 é dez vezes mais ácido que outro de pH 5. Abaixo de pH 7, o meio é ácido;
acima de pH 7, o meio é básico ou alcalino; o pH 7 é o meio neutro, que corresponde, por
exemplo, ao da água destilada.
Consequência da “chuva ácida”: a chuva ácida abaixa o pH da água de rios, lagos e do
solo; agride as folhas das árvores e plantas em geral, destruindo florestas inteiras.
Floresta localizada nas montanhas da República Tcheca destruída pela chuva ácida.
Disponível (acesso: 4.4.2014): http://commons.wikimedia.org/wiki/File:Acid_rain_woods1.JPG
Ação sobre indicadores: torna a solução alcoólica de fenolftaleína incolor; o papel tornassol
azul fica vermelho; o papel tornassol vermelho permanece vermelho; o alaranjado de metila
fica vermelho; o chá de repolho roxo fica vermelho.
Corroem a maioria dos metais, ionizando-os e liberando gás hidrogênio.
Consequência da “chuva ácida”: a chuva ácida acelera a corrosão de estruturas metálicas
expostas ao tempo, especialmente as de metais comuns, como ferro, zinco e alumínio.
Feº (s)
+
2 Alº (s)
H2SO4 (aq)
+
→
3 H2SO4 (aq)
FeSO4 (aq)
→
+
Al2(SO4)3 (aq)
H2 (g)
+ 3 H2 (g)
Experimento
Assista ao vídeo disponível no link abaixo, que mostra o ácido clorídrico atacando o metal
alumínio e produzindo gás hidrogênio (que é combustível) e o sal cloreto de alumínio.
https://www.youtube.com/watch?v=uTMhyZ_uTjc
Corroem carbonatos e bicarbonatos em geral, produzindo gás carbônico, um sal e água.
Consequência da “chuva ácida”: a chuva ácida corrói monumentos de mármore
(carbonato de cálcio, CaCO3), muitos deles com milhares de anos e de inestimável valor
histórico, como as ruínas e esculturas da antiga Atenas, na Grécia, ou o palácio Taj Mahal,
na Índia, transformando-as em gesso (sulfato de cálcio, CaSO4), que é uma substância que,
aos poucos, vai dissolvendo na água.
Por outro lado, se quisermos neutralizar um ácido, podemos usar bicarbonatos. Um recurso
muito usado na culinária, para neutralizar a acidez do limão, é adicionar um pouco de
bicarbonato de sódio (NaHCO3) ao suco da fruta.
CaCO3 (s)
+
H2SO4 (aq)
→
CaSO4 (aq)
+
H2O(l)
+
CO2 (g)
NaHCO3 (s)
+
HNO3 (aq)
→
NaNO3 (aq)
+
H2O(l)
+
CO2 (g)
Gárgula de mármore em monumento da Bavária, desgastada pela chuva ácida.
Disponível (acesso: 4.4.2014): http://commons.wikimedia.org/wiki/File:-_Acid_rain_damaged_gargoyle_-.jpg
Por serem compostos moleculares, apresentam propriedades físicas comuns a este grupo
de substâncias; ou seja, podem ser voláteis (baixos pontos de fusão e de ebulição), não
conduzem eletricidade (quando puros).
Ácidos mais comuns na química do cotidiano
Ácido clorídrico (HCl)
O ácido impuro (técnico) é vendido no comércio com o nome ácido muriático.
É encontrado no suco gástrico.
É um reagente muito usado na indústria e no laboratório.
É usado na limpeza de edifícios após a sua caiação (pintura a cal), para remover os
respingos de cal.
É usado na limpeza de superfícies metálicas antes da soldagem dos respectivos metais.
Ácido sulfúrico (H2SO4)
É o ácido mais importante na indústria e no laboratório. O poder econômico de um país
também pode ser avaliado pela quantidade de ácido sulfúrico que ele fabrica e consome.
O maior consumo de ácido sulfúrico ocorre na fabricação de fertilizantes, tais como os
superfosfatos e o sulfato de amônio.
É o ácido dos acumuladores de chumbo (baterias), usados nos automóveis.
É consumido em enormes quantidades, em inúmeros processos industriais, tais como
processos da indústria petroquímica, fabricação de papel, corantes, etc.
O ácido sulfúrico concentrado é um dos desidratantes mais energéticos. Assim, ele
carboniza os hidratos de carbono, como os açúcares, o amido e a celulose; a carbonização
é devida à desidratação desses materiais.
→
C12H22O11
sacarose
12 C(s)
H2SO4 concentrado
→
(C6H10O5)n
celulose
6nC(s)
H2SO4 concentrado
+
11H2O
carvão
+
5nH2O
carvão
O ácido sulfúrico "destrói" o papel, o tecido de algodão, a madeira, o açúcar e outros
materiais, devido à sua enérgica ação “desidratante”: ele “arranca” os átomos de hidrogênio
e oxigênio, na forma de moléculas de água, das grandes moléculas orgânicas desses
materiais.
O ácido sulfúrico concentrado tem ação corrosiva sobre os tecidos dos organismos vivos,
também devido à sua ação desidratante. Produz sérias queimaduras na pele. Por isso, é
necessário extremo cuidado ao manusear esse ácido.
As chuvas ácidas em ambientes poluídos com dióxido de enxofre contêm H 2SO4 e causam
grande impacto ambiental.
Ácido nítrico (HNO3)
Depois do ácido sulfúrico, é o ácido mais fabricado e mais consumido na indústria.
Seu maior consumo ocorre na fabricação de explosivos, tais como: nitroglicerina (dinamite),
trinitrotolueno (TNT), trinitrocelulose (algodão pólvora), ácido pícrico e picrato de amônio.
É usado na fabricação do salitre, fertilizante na agricultura, e na fabricação da pólvora negra
(salitre + carvão + enxofre ). Obs: Salitre = NaNO3 e KNO3
As chuvas ácidas em ambientes poluídos com óxidos do nitrogênio contêm HNO 3 e causam
sério impacto ambiental.
Em ambientes não poluídos, mas na presença de raios (descargas elétricas), a chuva ácida
também contém HNO3. O gás nitrogênio (N2) reage como oxigênio, aquecido pelos raios. O
anidrido nítrico (N2O5) formado reage com a água da atmosfera, produzindo ácido nítrico.
Por sua vez, o ácido ioniza em meio aquoso, formando ânions nitrato. Ecologicamente, esse
fato é muito importante, pois as plantas precisam muito de nitrogênio, mas têm dificuldade
de obtê-lo diretamente do ar atmosférico: as moléculas de N 2 são muito difíceis de serem
quebradas. Mas, com os raios, a quebra das moléculas é feita e o nitrato produzido e
dissolvido na água das chuvas pode ser absorvido pelas raízes das plantas. O nitrogênio é
importante para a fabricação dos aminoácidos e proteínas.
2 N2 (g)
+
→
5 O2 (g)
2 N2O5 (g)
raios
N2O5
+
H2O
HNO3
→
H+ (aq)
→
+
2 HNO3
NO31- (aq)
nitrato
O ácido nítrico concentrado é um líquido muito volátil; seus vapores são muito tóxicos. É um
ácido muito corrosivo e, como o ácido sulfúrico, é necessário muito cuidado para manuseálo.
Ácido fosfórico (H3PO4)
1. Os seus sais (fosfatos) têm grande aplicação como fertilizantes na agricultura.
2. É usado como aditivo conservante em alguns refrigerantes.
Ácido acético (CH3COOH)
É o ácido do vinagre, produto indispensável na cozinha (preparo de saladas e maioneses).
Ácido fluorídrico (HF)
Tem a particularidade de corroer o vidro. Por isso, não pode ser guardado em frascos de vidro. É
guardado em frascos de polietileno. É usado para gravar sobre o vidro.
Ácido carbônico (H2CO3)
É o ácido das águas minerais gaseificadas e dos refrigerantes, que se forma na reação do gás
carbônico com a água:
CO2 (g)
+
H2O (l) → H2CO3 (aq)
Quando o refrigerante é deixado aberto, em ambiente aquecido, a reação ocorre no sentido
contrário, liberando o gás carbônico novamente para a atmosfera.
H2CO3 (aq)
→
CO2 (g)
+
H2O (l)
Ácido sulfídrico (H2S)
O sulfeto de hidrogênio é um gás muito tóxico, de cheiro muito desagradável. É o responsável
pelo cheiro do ovo podre. Forma-se na decomposição de proteínas que contêm enxofre, que
estão presentes no ovo. Por isso, costuma-se dizer que o H2S tem cheiro de ovo podre.
Ácido cianídrico (HCN)
É terrivelmente tóxico. O cianeto de hidrogênio (HCN gasoso) é o gás das "câmaras de gás"
usadas na execução de pessoas.
Curiosidade: corte cebola sem chorar
Quando cortamos cebola, há liberação de vários gases, que, com o contato com a atmosfera,
sofrem modificações. Um desses gases contém um átomo de enxofre (16S) ligado a um oxigênio
(8O), cuja molécula sofre uma redução na cadeia carbônica (transformação I) e, depois, sofre
duas insaturações (ligações duplas) do enxofre (transformação II).
A terceira mudança ocorre, quando o gás entra em contato com a água que está nos nossos
olhos, formando ácido sulfúrico (H2SO4). Como o ácido começa a irritar nossos olhos, o
organismo se manifesta, produzindo grande quantidade de lágrimas para diluir o ácido,
diminuindo sua concentração e, consequentemente, diminuindo a irritação.
A melhor maneira de evitar que os olhos se irritem é cortar a cebola dentro de uma vasilha com
água, pois os gases ficarão dissolvidos, não se misturando com o ar e, por isso, não chegando
aos olhos. Se preferir outro método, usar óculos de mergulho também resolve, embora seja um
acessório um pouco estranho para um cozinheiro...
Assista aos vídeos:
Como cortar cebola sem chorar: https://www.youtube.com/watch?v=QaN7UoR2vjk
Segredos bizarros para não chorar na cozinha:
https://www.youtube.com/watch?v=S9w0kqIXtfI
Exercícios
1) Complete o quadro:
Fórmula
do ácido
HCl
Nox do
elemento
Nome do ácido
H2SO4
HIO4
H2SO3
H4P2O5
H2CrO4
HIO3
HClO2
HNO2
HBrO3
HBO2
H4P2O7
H4B2O5
H3PO3
H3PO4
Br+1
Cl+5
S-2
CNCl+7
I+1
Br+3
I-1
F-1
Mn+7
N+5
Ácido bromídrico
Ácido metafosfórico
Ácido perbrômico
Ácido piroantimonioso
Ácido bórico
Ácido carbônico
Ácido arsênico
Ácido hipocloroso
Ácido tetrabórico
Ácido bicrômico
Ácido mangânico
2) ESCREVA as equações de ionização (parciais e total) dos ácidos abaixo, dando os nomes
dos radicais formados (faça no caderno):
3)
Equação de ionização
H2CO3
→
H+
HCO31-
H2CO3
H2CO3
→
+
2H+
(total)
+
Nome do ânion
CO32-
Carbonato
(parcial)
HNO3
H2SO4
(total)
(parcial)
HMnO4
(total)
H3PO4
(parcial)
(parcial)
HClO4
(total)
H3PO4
(parcial)
(parcial)
HNO2
HCl
H2SO3
(total)
(parcial)
(total)
H4P2O7
(parcial)
(parcial)
(parcial)
HBr
HCN
H3BO3
(total)
(parcial)
bicarbonato ou
hidrogenocarbonato
(parcial)
H2S
(total)
(parcial)
HClO3
HBrO2
HI
HIO
H2MnO4
(total)
(parcial)
H2Cr2O7
H2Se
HClO4
HClO2
(total)
(parcial)