MODELO DE INSTRUÇÕES DE USO
STENT CORONÁRIO DE TROCA RÁPIDA COM ELUIÇÃO DE ZOTAROLIMUS
ENDEAVOR SPRINT
1.0 Descrição do dispositivo
O sistema de Stent Coronário de Troca Rápida com Eluição de Zotarolimus Endeavor
Sprint é constituído por quarto subsistemas:
1) stent Endeavor - um stent pré-montado à base de uma liga de cobalto
2) sistema introdutor - sistema coronário de troca rápida (RX)
3) tecnologia de fosforilcolina (PC) ¹
4) fármaco Zotarolimus
1.1 Stent
O stent Endeavor é fabricado a partir de uma liga de cobalto. Os stents são fornecidos
numa gama de tamanhos desde 2,25 mm a 4,0 mm de diâmetro e 8 mm a 30 mm de
comprimento.
Os diâmetros de stent de 2,25, 2,5 e 2,75 mm estão disponíveis em tamanhos de 8, 2,
4, 8, 24 e 30 mm.
Os diâmetros de stent de 3,0, 3,5 e 4,0 mm estão disponíveis em tamanhos de 9, 2, 5,
8, 24 e 30 mm.
1.2 Sistema introdutor
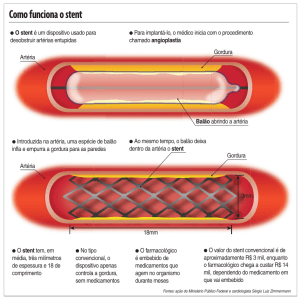
O sistema introdutor é constituído por um stent intracoronário expansível por balão,
previamente montado num sistema introdutor RX. O sistema introdutor possui dois
marcadores radiopacos para facilitar o posicionamento do stent durante a fluoroscopia.
O sistema introdutor é compatível com fios-guia de 0,36 mm (0,014 in.) e cateteresguia de 5 Fr. ( 0,4 mm).
1.3 Revestimento de polímero de fosforilcolina
(PC)
O stent encontra-se coberto com um revestimento de fosforilcolina (PC), um polímero
que age como um acondicionador do fármaco Zotarolimus. O polímero de PC é
composto por 2-metacriloiloxietil fosforilcolina.
Instruções de Uso
1
1.4 Fármaco Zotarolimus
O fármaco Zotarolimus (semelhante à rapamicina) é um novo composto químico
específico licenciado pela Abbott Laboratories. O Zotarolimus é um imunossupressor
macrocíclico que contém tetrazol. O mecanismo de ação sugerido do Zotarolimus é a
ligação ao FKBP 2, originando a formação de um complexo trimérico com a proteína
quinase mTOR (alvo mamífero da rapamicina), inibindo a sua atividade. A inibição da
mTOR origina a inibição de eventos de fosforilação de proteínas associados à tradução
da mRNA e ao controle do ciclo celular. O fármaco Zotarolimus destina-se a reduzir a
restenose, como complemento da intervenção coronária com o stent Endeavor.
O stent Endeavor tem uma dose nominal de 10µg de Zotarolimus por mm do
comprimento do stent.
1.5 Informações sobre o produto
Tabela 1 - Informações sobre o produto sistema de stent
Endeavor sprint da Medtronic
2.0 Forma de apresentação do produto
ESTERILIZADO, APENAS PARA UMA ÚNICA UTILIZAÇÃO.
O sistema de stent Endeavor sprint é esterilizado por óxido de etileno (EtO) e é
apirogênico. NÃO REESTERILIZE. Não utilize o produto se a embalagem estiver aberta
ou danificada.
Conteúdo: A embalagem contém um (1) stent coronário Endeavor sprint Zotarolimus.
Armazenamento: ARMAZENE NO RECIPIENTE ORIGINAL. Armazene entre 5 °C e 30
°C. Utilize antes da data de validade indicada na embalagem.
A bolsa exterior contém 2 pacotes pequenos (um utilizado para retirar o oxigênio da
bolsa e outro utilizado para retirar a umidade). Elimine estes pacotes depois de abrir a
bolsa.
3.0 Utilização recomendada
O Stent Coronário de Troca Rápida com Eluição de Zotarolimus Endeavor Sprint foi
concebido para doentes elegíveis para angioplastia coronária transluminal percutânea
(PTCA) com um diâmetro do vaso de referência de 2,25 mm a 4,0 mm e um
comprimento de lesão ¡Ü 27 mm. O sistema de stent Endeavor sprint foi concebido
Instruções de Uso
2
para melhorar os diâmetros luminais coronários, como um auxiliar das intervenções
coronárias e para reduzir a restenose. Os stents destinam-se a ser utilizados como
dispositivos de implante permanente.
4.0 Indicações para utilização
O Stent Coronário de Troca Rápida com Eluição de Zotarolimus Endeavor Sprint é
indicado para melhorar o diâmetro luminal coronário e reduzir a restenose em doentes
com doença coronária isquêmica sintomática em lesões da artéria coronária de novo,
nas artérias coronárias nativas, com um diâmetro do vaso de referência de 2,25 mm a
4,0 mm e um comprimento de lesão ¡Ü 27 mm.
5.0 Contra-indicações para utilização
O Stent Coronário de Troca Rápida com Eluição de Zotarolimus Endeavor Sprint é
contra-indicado para utilização em:
Doentes com hipersensibilidade ou alergias a aspirina, heparina, clopidrogel,
ticlopidina, fármacos como Zotarolimus, rapamicina, tacrolimus, sirolimus ou
semelhantes, ou quaisquer análogos ou derivados, cobalto, crômio, níquel, molibdênio
ou meio de contraste. Doentes nos quais a terapêutica anticoagulante e/ou
antiplaquetária é contra-indicada. Doentes que se julgue terem uma lesão que impeça
a insuflação completa de um balão de angioplastia.
6.0 Advertências e precauções
Os efeitos a longo prazo do Zotarolimus são de momento desconhecidos.
A exposição do doente ao fármaco encontra-se diretamente relacionada com a
quantidade total do comprimento do stent implantado.
A segurança e eficácia no que diz respeito à colocação direta de stents ainda não foram
estabelecidas.
A segurança e eficácia no que diz respeito à utilização de stents em enxertos da veia
safena ainda não foram estabelecidas.
A seleção judiciosa de doentes é necessária, uma vez que a utilização deste dispositivo
acarreta o risco associado de complicações enunciadas na Secção 7.0
Efeitos adversos possíveis.
Os efeitos a longo prazo dos stents e os riscos associados a estes implantes são
desconhecidos. Esta falta de informações deve ser tida em consideração ao realizar-se
a avaliação dos riscos/benefícios para o doente antes do implante.
A administração de terapêutica apropriada anticoagulante, antiplaquetária e
vasodilatadora coronária é vital para a implantação bem sucedida de um stent.
Nota: nos ensaios clínicos realizados com o stent Endeavor, foi administrado
clopidrogel ou ticlopidina antes do procedimento e durante um período de, pelo menos,
12 semanas após o procedimento. A administração de aspirina foi realizada
concomitantemente com clopidrogel ou ticlopidina, tendo em seguida sido continuada
indefinidamente para reduzir o risco de trombose.
Consulte a Secção 5.0 Contra-indicações para utilização.
Nota: O stent não é equipado com ou conectado a fontes de energia, portanto, não há
riscos de criação de campos eletromagnéticos que poderiam interferir na operação de
outros materiais ou equipamentos em um ambiente normal.
Apenas médicos com a devida formação devem realizar a implantação de stents.
A colocação de stents deve ser efetuada em hospitais nos quais seja possível realizar
uma cirurgia de emergência para enxerto de bypass na artéria coronária.
Instruções de Uso
3
A restenose subseqüente pode necessitar de uma dilatação repetida do segmento
arterial que contém o stent. Os resultados a longo prazo a seguir à repetição da
dilatação de stents coronários endotelializados são, de momento, desconhecidos.
Enquanto não estiverem disponíveis quaisquer dados clínicos, fármacos, tal como o
tacrolimus, que atua através da mesma proteína de ligação (FKBP), poderão interferir
com a eficácia do Zotarolimus. Não foram concluídos estudos de interação de
fármacos. O Zotarolimus é metabolizado pela CYP3A4. Inibidores fortes da CYP3A4
(como, por exemplo, o quetoconazol) podem provocar uma maior exposição ao
Zotarolimus até níveis associados a efeitos sistêmicos, especialmente se forem
desdobrados múltiplos stents. A exposição sistêmica ao Zotarolimus também deve ser
tida em conta se o doente for tratado ao mesmo tempo com uma terapêutica
imunossupressora sistêmica.
Não existem para este produto quaisquer estudos específicos ou de controle rigoroso
que tenham sido realizados em mulheres grávidas, mulheres lactantes ou em homens
que estejam a planear ter filhos. Estudos de fertilidade realizados em animais
demonstraram embriotoxicidade, incluindo embrioletalidade. Não se recomenda que o
Stent Coronário de Troca Rápida com Eluição de Zotarolimus Endeavor Sprintseja
utilizado em mulheres que estejam a tentar ter filhos, ou em mulheres que estejam
grávidas ou a amamentar. Estudos realizados em ratos machos resultaram numa
toxicidade testicular associada à dose. Quando for necessária a utilização de vários
stents, os materiais dos stents deverão ter uma composição semelhante. A colocação
de vários stents de composição diferente em contato uns com os outros poderá
aumentar o risco de corrosão. Os dados obtidos
através de testes de corrosão efetuados in vitro utilizando um stent de liga de cobaltocrômio F562 (stent coronário Driver da Medtronic) em combinação com um stent de
liga de aço inoxidável 3 6L (stent coronário S7 da Medtronic) não sugerem
um maior risco de corrosão in vivo.
Manuseio do stent - Precauções
Não utilize o produto se a embalagem estiver aberta ou danificada.
Para uma única utilização. Não reesterilize nem reutilize. Verifique a data de
validade do produto.
Não remova o stent do sistema introdutor visto que a remoção poderá danificá-lo
e/ou conduzir à sua embolização. O Stent Coronário de Troca Rápida com Eluição de
Zotarolimus Endeavor Sprint destina-se a funcionar como um sistema. O stent não foi
concebido para utilização com outro dispositivo introdutor. O sistema introdutor do
Stent Coronário de Troca Rápida com Eluição de Zotarolimus Endeavor Sprint não deve
ser utilizado em conjunto com outros stents ou para a pós-dilatação.
A manipulação excessiva (por ex., rodar um stent montado) pode causar o
deslocamento do stent do balão introdutor. Deve ter-se cuidado especial para não
manusear ou, de alguma forma, interferir com a posição do stent no dispositivo
introdutor. Isto é especialmente importante durante a remoção do cateter da
embalagem, durante a sua colocação sobre o fio-guia, o seu avanço através do
adaptador da válvula hemostática rotativa e ao longo do centro do cateter-guia.
O stent Endeavor não deve ser exposto a qualquer espécie de manuseamento
direto (por exemplo, prensagem do stent) nem deverá entrar em contacto
com líquidos antes da preparação e introdução, visto que o revestimento pode
ser susceptível a danos ou eluição prematura do fármaco.
Não exponha nem limpe o dispositivo com solventes orgânicos, como por exemplo
álcool. Use apenas o meio para insuflação do balão apropriado. Não utilize ar nem
Instruções de Uso
4
nenhum outro meio gasoso para insuflar o balão pois isto pode causar uma expansão
desigual e dificuldades no desdobramento do stent.
Não utilize o dispositivo se este estiver dobrado.
6.2 Colocação do stent - Precauções
Não prepare nem insufle previamente o balão antes do desdobramento,
utilizando procedimentos diferentes dos indicados nas instruções. Utilize a técnica de
purga do balão descrita na Secção 9.3 Preparação do sistema introdutor.
A segurança e eficácia dos comprimentos totais de stents superiores a 48 mm ainda
não foram estabelecidas. Caso seja necessário introduzir stents adicionais, devem ser
utilizados materiais de stent de composição semelhante.
O implante de um stent pode provocar a dissecação do vaso distal e/ou proximal à
porção do stent e causar a oclusão aguda do vaso, o que exigirá uma intervenção
adicional (por ex., CABG - cirurgia de bypass da artéria coronária, dilatação adicional
ou introdução de stents adicionais).
Não expanda o stent se este não estiver corretamente posicionado no vaso (consulte a
Secção 9.7 Remoção do stent/ sistema introdutor - Precauções).
Os resultados a longo prazo a seguir à repetição da dilatação de stents coronários
endotelializados são, de momento, desconhecidos.
A colocação do stent poderá comprometer a desobstrução da ramificação periférica.
Não exceda a pressão de ruptura nominal indicada no rótulo do produto. As
pressões do balão devem ser monitorizadas durante a insuflação do balão. A utilização
de pressões mais elevadas do que as especificadas no rótulo do produto poderá
resultar na ruptura do balão, em danos potenciais na íntima e dissecção do vaso
(consulte a tabela ).
Os métodos de remoção do stent (a utilização de fios, alças ou pinças adicionais)
podem resultar em traumas adicionais à vasculatura coronária e/ou ao local de acesso
vascular.
As complicações podem incluir sangramento, hematoma ou pseudoaneurisma.
6.3 Após o implante - Precauções
Deve ter-se muito cuidado ao cruzar um stent que foi recentemente desdobrado
com um cateter ecográfico intravascular (IVUS), com um fio-guia coronário ou com um
cateter por balão, para evitar modificar o revestimento e/ou a geometria do stent
Endeavor.
O teste não clínico de deflexão e torção induzidas magneticamente a 3 Tesla, com um
gradiente espacial máximo de 525 gauss/cm (5,25 Tesla/metro) indica que o stent
Endeavor não se deverá mover ou migrar imediatamente após o implante.
O stent Endeavor produz um aumento de temperatura inferior a 0,5 °C, quando
associado a ressonâncias magnéticas (RM) efetuadas a uma taxa de absorção
específica (SAR) média de corpo inteiro de 2,0 W/kg, com um pico de taxa de absorção
específica (SAR) de 4,0 W/kg durante 20 minutos. Não foi ainda determinado o efeito
dos procedimentos de ressonância magnética nuclear (RMN) a níveis de energia de
radiofreqüência (RF) mais elevados num doente com um stent Endeavor implantado.
Os resultados poderão não se aplicar a stents sobrepostos. O efeito do aquecimento
em associação com a ressonância magnética nuclear (RMN) no fármaco ou
revestimento do polímero é desconhecido.
A qualidade da imagem por ressonância magnética (RM) poderá ser comprometida se
a área de interesse ficar próxima ou estiver na mesma posição do stent.
Após a dilatação: Devem-se fazer todos os esforços possíveis para que o stent não
fique sub-expandido. Se o stent desdobrado não se encontrar completamente colocado
Instruções de Uso
5
de encontro à parede do vaso, o stent pode ser expandido um pouco mais, utilizando
um balão com um diâmetro superior que seja ligeiramente mais curto (cerca de 2 mm)
do que o stent. O processo após a dilatação pode ser efetuado utilizando um cateter
por balão de baixo perfil, pressão elevada e resistente a deformações e o balão não se
deve estender para além da região onde se encontra colocado o stent.
7.0 Efeitos adversos possíveis
As seguintes complicações podem estar associadas à utilização de stents coronários,
IVUS ou angioplastia coronária transluminal percutânea (PTCA) (enunciadas por ordem
de gravidade):
Morte
Aneurisma, pseudoaneurisma ou fístula arteriovenosa
Danos no stent ou lesão da artéria exigindo uma cirurgia de emergência para
enxerto de bypass na artéria coronária (CABG)
Trombose/ataque isquêmico passageiro
Tamponamento cardíaco
Dissecção, perfuração ou ruptura da artéria coronária
Embolia (ar, tecidos, dispositivo ou trombo)
Trombose ou oclusão do stent
Oclusão total da artéria
Enfarte agudo do miocárdio
Restenose da artéria onde o stent foi colocado
Arritmias
Hemorragia, com necessidade de transfusão
Choque/edema pulmonar
Fecho ou espasmo abrupto do vaso
Hipotensão ou hipertensão
Reação alérgica (ao meio de contraste, terapia antiplaquetária, material do
stent ou revestimento de fármaco)
Isquemia periférica/lesão do nervo periférico
Infecções ou febre
Angina instável
Dores/reação no local de introdução do cateter
Ruptura do balão
Migração do stent
Falha na introdução do stent
Má colocação do stent
Hematoma
A ocorrência das complicações mencionadas anteriormente pode originar a
necessidade de uma cateterização repetida e/ou intervenção coronária percutânea,
enfarte do miocárdio, cirurgia de emergência de bypass ou morte. Os seguintes efeitos
secundários/complicações adicionais podem estar associados, mas não estão limitados,
à utilização de Zotarolimus, incluindo a sua administração intravenosa (enunciados por
ordem alfabética):
Anemia
Parestesia circumoral
Diarréia
Pele seca
Dores de cabeça
Hematúria
Instruções de Uso
6
Infecção
Reação no local de injeção
Dores (abdominais, artralgia, local da injeção)
Erupção cutânea
8.0 Tratamento e seleção de doentes
Os riscos e benefícios descritos acima devem ser cuidadosamente analisados para cada
doente antes da utilização do stent coronário Endeavor sprint Zotarolimus.
Não foram ainda determinadas a segurança e eficácia da utilização de dispositivos para
aterectomia mecânica (cateteres para aterectomia direcional, cateteres para
aterectomia rotacional) ou cateteres para angioplastia por laser para tratamento de
estenoses dentro do stent.
9.0 Informações sobre a utilização clínica
9.1 Inspeção antes da utilização
Inspecione cuidadosamente a embalagem esterilizada antes de abrir. Não utilize o
produto se a embalagem estiver danificada ou aberta. Não use o produto depois do
vencimento do prazo de validade. Se a embalagem esterilizada parecer estar intacta,
retire o sistema da embalagem cuidadosamente e procure dobras, torções ou outros
danos. Certifique-se de que o stent se encontra localizado entre os marcadores
radiopacos. Não utilize se detectar quaisquer defeitos.
9.2 Materiais necessários
Cateter-guia de 5 Fr. com um diâmetro interno mínimo de 1,4 mm (0,056 in.)
Seringa de 20 cc
Solução salina heparinizada normal
Fio-guia de 0,036 mm (0,0 4 in.)
Válvula hemostática rotativa
Meio de contraste diluído com solução salina normal heparinizada, numa relação
de 1 para 1.
Dispositivo de insuflação
Dispositivo de torção
Válvula reguladora de três vias
9.3 Preparação do sistema introdutor
Prepare o cateter-guia e o fio-guia de acordo com as instruções do fabricante. O
sistema de stent Endeavor é compatível com fios-guia de 0,036 mm (0.014 in.).
Consulte o rótulo do produto ou a Secção 9.2 para confirmar a compatibilidade do
cateter-guia específico.
A escolha cuidadosa do tamanho do stent é importante para uma colocação bem
sucedida do mesmo. Selecione um comprimento de stent apropriado para a lesão alvo
(3 mm ou mais do que o comprimento da lesão). Certifique-se de que o stent
selecionado é suficientemente comprido para cobrir a lesão completamente.
Nota: o diâmetro do balão insuflado mede ligeiramente mais do que o diâmetro
interno do stent indicado no rótulo para permitir o recuo do stent após a expansão.
Retire o sistema introdutor do stent da embalagem. Retire a bainha protetora do
stent/balão. Deverá ter-se extremo cuidado para não manusear o stent de forma que
possa perturbar o seu posicionamento no balão. Inspecione o stent para se assegurar
de que este não está danificado nem foi movido da sua posição original no balão.
Verifique se o stent está localizado entre os marcadores proximal e distal do balão.
Nota: se o stent tiver sido movido ou estiver danificado, não o utilize.
Instruções de Uso
7
Irrigue o lúmen do fio-guia do sistema introdutor do stent com solução salina normal
heparinizada até sair líquido através da ponta distal.
Encha uma seringa de 20 cc com 5 cc de uma mistura de meio de contraste/solução
salina normal heparinizada, numa relação de 1 para 1.
Encaixe no sistema introdutor e exerça pressão negativa durante 20 a 30 segundos.
Liberte, lentamente, a pressão, permitindo que a pressão negativa extraia a mistura
para o lúmen do balão. Retire a seringa, deixando um menisco de mistura no centro do
lúmen do balão. Prepare o dispositivo de insuflação de acordo com os procedimentos
normais e purgue para retirar todo o ar da seringa e da tubagem.
Encaixe o dispositivo de insuflação diretamente no cateter, certificando-se de que não
permanecem quaisquer bolhas na ligação.
Deixe à pressão ambiente (posição neutra).
Nota: não aplique pressão negativa no dispositivo de insuflação após a
preparação do balão e antes de introduzir o stent.
9.4 Procedimento de introdução
Prepare o local de acesso vascular seguindo as práticas de norma para PTCA.
Dilate previamente a lesão com um balão com um diâmetro 0,5 mm menor do que o
stent e um balão com um comprimento igual ou menor do que o comprimento da lesão
alvo. O comprimento do balão de dilatação prévia deve ser menor do que o stent a ser
implantado.
Mantenha uma pressão neutra no dispositivo de insuflação. Abra a válvula hemostática
rotativa para permitir a fácil passagem do stent.
Nota: se encontrar resistência, NÃO FORCE A PASSAGEM. A resistência pode
indicar um problema e pode resultar em danos no stent se este for forçado.
Remova o sistema e examine-o.
Assegure-se da estabilidade do cateter-guia antes de fazer avançar o sistema
introdutor do stent para dentro da artéria coronária. Faça avançar cuidadosamente o
sistema introdutor do stent no centro do cateter-guia.
Nota: se encontrar resistência ao sistema introdutor do stent antes de sair do cateterguia, não force a passagem.
A resistência pode indicar um problema e pode resultar em danos no stent se este for
forçado. Mantenha a posição do fio-guia ao longo da lesão e retire o sistema introdutor
do stent como uma unidade. (Consulte a Secção 9.7 Remoção do sistema introdutor do
stent - Precauções).
Faça avançar o sistema introdutor do stent sobre o fio-guia até à lesão alvo sob
visualização fluoroscópica direta. Utilize os marcadores radiopacos proximal e distal no
balão como pontos de referência. Se a posição do stent não for a ideal, este deverá ser
cuidadosamente reposicionado ou retirado (consulte a Secção 9.7 Remoção do sistema
introdutor do stent - Precauções). A expansão do stent não deve ser feita se o stent
não estiver colocado devidamente no segmento da lesão alvo do vaso.
Feche a válvula hemostática rotativa de forma adequada, se esta estiver presente. O
stent está agora pronto para ser desdobrado.
9.5 Procedimento de desdobramento do stent
Antes da expansão do stent, utilize fluoroscopia de alta resolução para verificar se o
stent foi danificado ou movido durante o posicionamento.
Mantenha a pressão de insuflação durante 5 a 30 segundos para expandir o stent
completamente.
Instruções de Uso
8
Não exceda a pressão de ruptura nominal. O Stent Coronário de Troca Rápida
com Eluição de Zotarolimus Endeavor Sprint não deve ser expandido até um
diâmetro para além dos 0,5 mm da sua expansão nominal.
Nota: em vasos menores ou difusamente doentes, a utilização de pressões elevadas
de insuflação do balão pode provocar uma sobre-expansão do vaso distalmente ao
stent, o que pode originar uma dissecção do vaso.
Nota: a sub-expansão do stent pode provocar o movimento do stent. Deve ter-se
cuidado ao determinar o tamanho adequado do stent para garantir que este fica em
perfeito contacto com a parede arterial após a desinsuflação do balão.
9.6 Procedimento de remoção
Desinsufle o balão aplicando uma pressão negativa no dispositivo de insuflação.
Permita um tempo adequado, pelo menos 5 segundos, para a desinsuflação completa
do balão. Os stents mais compridos podem necessitar de mais tempo de desinsuflação.
A desinsuflação do balão pode ser confirmada pela ausência de meio de
contraste dentro do mesmo.
Abra a válvula hemostática para permitir a remoção do sistema introdutor.
Mantenha a posição do cateter-guia e do fio-guia para evitar que sejam puxados para
o vaso. Retire muito lentamente o balão introdutor do stent desdobrado, mantendo
uma pressão negativa e permitindo o movimento da artéria renal de forma a desalojar
suavemente o balão do stent. Após a remoção do sistema introdutor, feche a válvula
hemostática. Repita a angiografia e avalie visualmente o vaso e o stent quanto à
expansão devida.
Nota: caso seja necessário colocar um segundo stent para cobrir adequadamente o
comprimento da lesão, a colocação do stent mais distalmente na artéria deve ser
efetuada, se possível, antes da colocação do stent proximal. A segurança e eficácia dos
comprimentos totais de stents superiores a 48 mm ainda não foram estabelecidas.
Nota: o doente deve ser mantido sob observação e deverá realizar-se regularmente
uma avaliação angiográfica do local do stent durante os primeiros 30 minutos após o
implante do stent. Se a colocação do stent estiver associada à ocorrência ou suspeita
de trombose na região do segmento onde foi implantado o stent, recomenda-se a
realização de infusões intracoronárias de um agente trombolítico.
9.7 Remoção do stent/sistema introdutor - Precauções
Se for necessário retirar o sistema de stent antes do desdobramento, assegure-se de
que o cateter-guia está posicionado coaxialmente em relação ao sistema introdutor do
stent e, com todo o cuidado, retraia o sistema introdutor do stent para dentro do
cateter-guia.
Se encontrar resistência fora do normal em qualquer momento ao retirar o
stent na direção do cateter-guia, o sistema introdutor do stent e o cateterguia devem ser retirados como uma única unidade. Isto deverá ser feito sob
visualização fluoroscópica direta.
Quando retirar o sistema introdutor do stent e o cateter-guia como uma unidade:
Não retraia o sistema introdutor do stent para dentro do cateter-guia.
Instruções de Uso
9
Mantenha a colocação do fio-guia através da lesão e puxe o sistema introdutor do
stent cuidadosamente para trás até o marcador do balão proximal do sistema
introdutor do stent ficar alinhado com a ponta distal do cateter-guia.
O sistema deve ser puxado para trás para a aorta descendente em direção à bainha
arterial. À medida que a extremidade distal do cateter-guia entra na bainha arterial, o
cateter endireita-se permitindo a remoção segura do sistema introdutor do stent para
dentro do cateter-guia e a remoção subseqüente do sistema introdutor do stent e do
cateter-guia da bainha arterial.
A não observação destes passos e/ou o uso de força excessiva no sistema
introdutor do stent pode resultar em perda ou danos no stent e/ou nos
componentes do sistema introdutor do stent, como por exemplo o balão.
Tabela 2 – Stent Coronário de Troca Rápida com Eluição de Zotarolimus Endeavor
Sprint de troca rápida
Diâmetro interno (mm) vs. pressão de insuflação (atm/kPa)
* Pressão de desdobramento nominal (9 atm/9 2 kPa)
**Pressão de ruptura nominal. 6 atm ( 62 kPa) para stents com diâmetros até 3,5
mm, 5 atm ( 520 kPa) para stents com 4,0 mm. NÃO EXCEDA
Nota: a especificação do dispositivo nominal in vitro não tem em conta a resistência
da lesão. O tamanho do stent deve ser confirmado angiograficamente.
Nota: Não dilate o Stent Coronário de Troca Rápida com Eluição de Zotarolimus
Endeavor Sprint para além dos dados fornecidos no quadro de conformidade fornecido
na embalagem. Não dilate o Stent Coronário de Troca Rápida com Eluição de
Zotarolimus Endeavor Sprint 0,5 mm para além da sua pressão nominal.
Nota: a pressão do balão deve ser observada de perto durante a insuflação. Não
exceda a pressão de ruptura nominal conforme especificado no rótulo do produto, visto
que tal poderá originar a ruptura do balão com possíveis danos na íntima e dissecção.
Instruções de Uso
10
Esterilizado por óxido de etileno
Fabricante:
Medtronic Ireland (A subsidiary of Medtronic, Inc.)
Parkmore Business Park West
Galway
Irlanda
Importado e Distribuído no Brasil por:
Medtronic Comercial Ltda
Rua Joaquim Floriano, 100 – 7º andar – CEP: 04534-000
Itaim Bibi – São Paulo – SP
Tel.: 11 2182-9200 Fax: 11 2182-9240
CNPJ: 01.772.798/0001-52
Resp. Técnico: André Gaban – CRF/SP 25500
Registro ANVISA nº: 1033919318
Responsável Legal
Lúcia Sze (Representante Legal)
Instruções de Uso
Responsável Técnico
André Gaban
CRF/SP 25500
11