Interferência da dieta hipoprotéica na síntese de
CX3CL1/Fractalquina e endotelina em modelo experimental de
infecção pelo Trypanosoma cruzi.
i
UNIVERSIDADE FEDERAL DE OURO PRETO
Reitor
João Luiz Martins
Vice-Reitor
Antenor Barbosa Junior
Pró-Reitor de Pesquisa e Pós-Graduação
Tanus Jorge Nagem
PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIAS BIOLÓGICAS
Coordenador
Prof. Dr. Luís Carlos Crocco Afonso.
ii
UNIVERSIDADE FEDERAL DE OURO PRETO
NÚCLEO DE PESQUISA EM CIÊNCIAS BIOLÓGICAS
PROGRAMA DE PÓS – GRADUÇÃO EM CIÊNCIAS BIOLÓGICAS
Interferência da dieta hipoprotéica na síntese de Fractalquina/CX3CL1 e
endotelina em modelo experimental de infecção pelo Trypanosoma cruzi.
Régia Ferreira Martins
Orientação: DSc. André Talvani
Co-Orientação: MSc. Fabiane Matos dos Santos
Dissertação apresentada ao Programa de Pós-Graduação em
Ciências Biológicas do Núcleo de Pesquisa em Ciências
Biológicas da Universidade Federal de Ouro Preto, como parte
integrante dos requisitos para obtenção do Título de Mestre em
Ciências Biológicas, área de concentração: Imunobiologia de
Protozoários.
Ouro Preto
2010
iii
.
“A coisa mais bela que podemos experimentar é o mistério.
Essa é a fonte de toda a arte e ciência verdadeiras.”
Albert Einstein
iv
Dedico este trabalho à vovó Regina, quem dedicou a
vida a nossa família e nos ensinou verdadeiros valores.
“Saudades: presença dos ausentes.”
Olavo Bilac
v
M386i
Martins, Régia Ferreira.
Interferência da dieta hipoprotéica na síntese de CX3CL1/fractalkine e endotelina
em modelo experimental de infecção pelo Trypanosoma cruzi
[manuscrito] / Régia Ferreira Martins. – 2010.
xi, 56f.: il., graf., tabs.
Orientador: Prof. Dr. André Talvani.
Co-orientadora: Profa. Dra. Fabiane Matos dos Santos.
Dissertação (Mestrado) - Universidade Federal de Ouro Preto. Instituto de Ciências
Exatas e Biológicas. Núcleo de Pesquisas em Ciências Biológicas.
Área de concentração: Imunobiologia de protozoários.
1. Desnutrição - Teses. 2. Endotelinas - Teses. 3. Chagas, Doença de - Teses.
I. Universidade Federal de Ouro Preto. II. Título.
CDU: 616.937
Catalogação: [email protected]
AGRADECIMENTOS
Agradeço a Deus por estar sempre comigo.
Aos meus pais, Cláudio e Adriana, pela família que me deram, por fazerem parte de mim. Pelo amor e
dedicação. A vocês meu eterno amor e gratidão!
Aos meus irmãos Raissa, Caio e Cláudio obrigada por tudo. Amo vocês com que há de melhor em mim.
À minha família. Vozinha Regina cuja ausência dói, mas as lembranças trazem para perto. Tia Gigi
exemplo de força, exemplo de vida! Tia Marcininha por participar de tudo que acontece na minha vida. Tio
André pelo carinho.
Ao Juliano que me faz tão feliz, que mesmo longe está dentro do meu coração o tempo todo.
Às minhas amigas de Cristina, irmãs de alma. Obrigada por fazerem a vida parecer tão doce.
À República 171 pelos anos incríveis. As estelionatárias pela amizade e por me receberem de braços
abertos. Amadas muito obrigada! De cada uma de vocês levo um pouco comigo.
Ao Bruno, Filippe e Guilherme por estarem sempre por perto. Pelos momentos agradáveis nos corredores
do ICEB, pelos cafés, conversas, por cada instante juntos. Amigos vocês me são muito especiais!
Aos colegas e professores do Laboratório de Doença de Chagas da UFOP, pelos ensinamentos e
conhecimentos compartilhados, especialmente a Professora Terezinha, Lívia e Ivo.
À Fabiane pelo interesse, disponibilidade e ajuda com o projeto.
À Ouro Preto, onde passei os melhores anos da minha vida. “Ah, Ouro Preto dos meus devaneios, das
minhas andanças, das minhas recordações.”
Ao Laboratório de Patologia da UFOP e à professora Camila pelo lindo trabalho e grande auxílio
histopatológico!
Ao Laboratório de Nutrição Experimental da UFOP e ao professor Marcelo Eustáquio pela ajuda e
colaboração com nosso projeto.
Ao Laboratório Professora Conceição Machado da UFMG. Professora Patrícia, Carlos e Luciano obrigada
pela disponibilidade, atenção e carinho.
Enfim, agradeço ao professor André Talvani pela oportunidade, compreensão, apóio e carinho. Por fazer
parte deste projeto e ajudar a concretizá-lo. Obrigada sempre!
Agradeço também, carinhosamente, aos animais deste projeto.
"A compaixão para com os animais é das mais nobres virtudes da natureza humana."
Charles Darwin
vi
RESUMO
A cardiopatia chagásica, desenvolvida após a infecção pelo Trypanosoma cruzi (T. cruzi) é uma
doença inflamatória crônica. Apresenta alterações vasculares significativas, a ponto de conduzir o
hospedeiro vertebrado ao óbito. Múltiplos fatores parecem contribuir para os eventos
cardiovasculares na doença de Chagas, mas a resposta imune do hospedeiro aparece como essencial
tanto em modelo humano quanto experimental. Em particular, a produção de quimiocinas e de outros
mediadores inflamatórios têm apresentado grande relevância na alteração da homeostase e
contribuído para o recrutamento leucocitário, eventos primordiais para a patogênese da doença de
Chagas. Conhecendo-se a precária situação nutricional das populações negligenciadas em áreas
endêmicas para a doença de Chagas, e também a relação direta entre fatores nutricionais e a resposta
imune do hospedeiro, este trabalho objetivou avaliar a interferência da deficiência protéica na
resposta inflamatória cardíaca em modelo experimental da doença de Chagas. Utilizando-se ratos
Fisher machos, induzimos uma desnutrição protéica nesses animais, seguida de infecção pelo
Trypanosoma cruzi (cepa Y) e avaliamos a síntese da quimiocina Fractalquina/CX3CL1 e do
peptídeo endotelina associados à lesão cardíaca durante as fases aguda e crônica da doença de
Chagas. Observou-se que a deficiência protéica foi capaz de potencializar a síntese sistêmica de
CX3CL1 e de endotelina, tanto na fase aguda quanto crônica da doença de Chagas, porém não foi
capaz de controlar o aumento da carga parasitária na circulação sanguínea. Nossos dados mostram,
pela primeira vez, a presença da CX3CL1 durante a infecção pelo Trypanosoma cruzi. E ainda,
demonstrou a importância do estado nutricional do hospedeiro nas alterações imunes, pertinentes à
doença de Chagas, no modelo experimental, sugerindo que a médio ou longo prazo, tais alterações
poderiam contribuir para a progressão clínica da doença.
Palavras chave: Desnutrição protéica; Fractalkine/CX3CL1; Endotelina; doença de Chagas.
vii
ABSTRACT
Chagas' heart disease developed after Trypanosoma cruzi infection, is a chronic inflammatory
disease. It presents significant vascular changes, the point of driving the vertebrate host to death.
Multiple factors seem to contribute to cardiovascular events in Chaga's disease, but the host immune
response appears to be essential both in human and experimental model. In particular, the production
of chemokines and other inflammatory mediators have shown great importance in altering the
homeostasis and contributing to leukocyte recruitment, events essential for the pathogenesis of the
disease. Knowing the precarious nutritional situation of neglected populations in areas endemic for
Chaga’s disease, and also the direct relationship between nutritional factors and host immune
response, this study aimed to evaluate the role of protein deficiency in the inflammatory response
rate during an experimental model of disease. Using Fisher male rats, we induced proteic
malnutrition in these animals, followed by infection with Trypanosoma cruzi (Y strain) and
evaluated the synthesis of the chemokine Fractalkine/CX3CL1 and peptide endothelin associated
with cardiac injury during the acute and chronic phases of Chaga’s disease. It was observed that
protein deficiency was able to enhance the systemic synthesis of CX3CL1 and endothelin in both
acute and chronic Chaga’s disease, but was not able to control the increase in parasite load in the
bloodstream. Our data show for the first time, the presence of CX3CL1 during infection with
Trypanosoma cruzi. Also, we demonstrated the importance of nutritional status in the host immune
changes, relevant to Chaga's disease in the experimental model, suggesting that the medium to long
term, such changes could contribute to the progression of the disease.
Keywords: Protein malnutrition; Fractalkine/CX3CL1; Endothelin; Chaga’s disease
viii
Tabela
Tabela 1: Composição das dietas experimentais...............................................................................25
Lista de Figuras
Figura 1: Morfologia do T. cruzi..........................................................................................................13
Figura 2: Esquema representativo da adaptação ao modelo de desnutrição protéica..........................23
Figura 3: Avaliação do ganho de peso dos animais.............................................................................29
Figura 4: Avaliação sérica das proteínas totais....................................................................................30
Figura 5: Avaliação dos níveis séricos de albumina............................................................................31
Figura 6: Avaliação dos níveis sanguíneos de hemoglobina...............................................................31
Figura 7: Parasitemia...........................................................................................................................32
Figura 8: Análise histopatológica do coração..................................................................................... .34
Figura 9: Análise morfométrica da celularidade do tecido cardíaco de ratos Fisher infectados com a
cepa Y do T.cruzi, com dieta hipoprotéica ou normoprotéica.............................................................35
Figura 10: Avaliação morfológica do coração (peso do coração/peso coporal)..................................35
Figura 11: Avaliação dos níveis séricos e cardíacos de Endotelina.....................................................37
Figura 12: Avaliação dos níveis de Fractalquina/CX3CL1 no soro e no tecido cardíaco...................38
Figura 13: Análise imuno-histoquímica dos receptores da Fractalquina/CX3CL1 (CX3CR1) no
tecido cardíaco.....................................................................................................................................40
Figura 14: Análise imuno-histoquímica de macrófagos no coração....................................................41
ix
SUMÁRIO
1.0. INTRODUÇÃO
1.1. Trypanosoma cruzi e a epidemiologia da doença de Chagas ................................................... 12
1.2. O sistema imune na doença de Chagas ................................................................................... 15
1.3. Fractalquina/CX3CL1 e Endotelina na biologia vascular ........................................................ 16
1.4. O estado nutricional: aspectos gerais e sua relevância nas doenças parasitárias ..................... 19
2.0. OBJETIVOS
2.1. Objetivo geral .......................................................................................................................... 22
2.2. Objetivos específicos............................................................................................................... 22
3.0. MATERIAL E MÉTODOS
3.1. Proposição de um modelo de dieta hipoprotéica em ratos para o estudo da infecção pelo T.
cruzi ................................................................................................................................................23
3.2. Animais ................................................................................................................................... 24
3.3. Dieta ........................................................................................................................................ 24
3.4. Avaliação nutricional .............................................................................................................. 25
3.5. Parasitemia .............................................................................................................................. 25
3.6. Histopatologia
3.6.1. Processamento histológico ............................................................................................... 25
3.6.2 Análise morfológica qualitativa e quantitativa dos tecidos ............................................... 26
3.7. Imunohistoquímica .................................................................................................................. 26
3.8. Reação imunoenzimática – ELISA
3.8.1. Fractalquina/CX3CL1 ...................................................................................................... 27
3.8.2. Endotelina......................................................................................................................... 27
3.9. Análises estatísticas ................................................................................................................. 28
x
4.0. RESULTADOS
4.1. Avaliação do estado nutricional: peso e dosagens bioquímicas .............................................. 29
4.2. Parasitemia e mortalidade ....................................................................................................... 32
4.3. Análise histopatológica e morfométrica do coração ............................................................... 33
4.4. Avaliação dos níveis cardíacos e séricos de Endotelina ......................................................... 36
4.5. Avaliação dos níveis da fractalquina/CX3CL1 no soro e no tecido cardíaco ......................... 37
4.6. Análise imunohistoquímica dos receptores da CX3CL1(CX3CR1) e macrófagos no
coração ........................................................................................................................................... 39
5.0. DISCUSSÃO .............................................................................................................................. 42
6.0. CONCLUSÃO ........................................................................................................................... 48
7.0. REFERÊNCIAS BIBLIOGRÁFICAS .................................................................................... 49
xi
1.0. INTRODUÇÃO
1.1. A epidemiologia da doença de Chagas e o Trypanosoma cruzi.
Acredita-se que a doença de Chagas exista desde a antiguidade. Fragmentos de DNA, únicos
de cinetoplasto de Trypanosoma cruzi (T. cruzi), foram isolados de múmias humanas do nordeste
Chileno que datavam de aproximadamente 2.000 anos a.C. (Guhl et al, 1999). No entanto, estudos
revelam que a primeiras infecções possam ter ocorrido há cerca de 7.000 anos a.C. Neste período, o
ciclo silvestre da doença foi provavelmente estabelecido, onde os primeiros seres humanos
(membros da cultura Chinchorro) junto com muitas outras espécies de mamíferos atuavam como
hospedeiros (Aufderheide et al, 2004).
Milhares de anos depois, em 1909, Carlos Ribeiro Justiniano das Chagas durante uma
expedição científica pelo interior de Minas onde a malária devastava o acampamento dos
trabalhadores da Estrada de Ferro Central do Brasil descobriu o parasito, chamado T. cruzi em
homenagem a Oswaldo Cruz, no sangue de uma menina de três anos, Berenice. Foi seu trabalho
memorável que descreveu a doença, a morfologia do parasito, bem como seu transmissor,
hospedeiros e seu ciclo de vida (Brener, 1989).
Atualmente, a doença Chagas representa um dos principais problemas médico-sociais
brasileiros, acometendo cerca de 4 a 6 milhões de pessoas em todo o país. É uma doença crônica,
incapacitante e debilitante de grande impacto sócio-econômico e cultural (WHO, 2002). A
distribuição geográfica da infecção chagásica, incluindo os seus reservatórios e seus vetores,
estende-se desde o sul dos Estados Unidos até o sul da Argentina e Chile. Assim, abrange todas as
Américas, onde cerca de 90 milhões de pessoas estão expostas à infecção. Além disso, estima-se que
15 milhões de pessoas estejam infectadas pelo T. cruzi ou sejam portadoras da doença de Chagas em
toda a América (Coura & Dias, 2009).
O T. cruzi é um protozoário intracelular flagelado da ordem Kinetoplastidae, sendo assim
classificado por apresentar em sua estrutura interna uma organela conhecida por cinetoplasto. Este
microorganismo patogênico possui uma grande diversidade genética, já bem caracterizada. Seu
ciclo biológico é bastante complexo, caracterizado pela presença de muitos estágios de
desenvolvimento os quais podem ser observados no hospedeiro vertebrado e invertebrado (de Souza
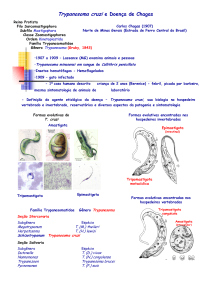
et al, 2002). Três formas do parasito são essencialmente estudas: amastigotas (Figura 1A),
12
epimastigotas (Figura 1B) e tripomastigotas (Figura 1C). As formas epimastigotas replicativas são
encontradas no intestino posterior, nas fezes e urina do inseto vetor, bem como as formas
tripomastigotas metacíclicas, infectivas para o homem. Tripomastigotas são encontradas nas células
de muitos tecidos, principalmente no tecido cardíaco, e na corrente sanguínea do homem. Essas
formas são incapazes de se replicar, tendo a função de interagir com a célula do hospedeiro a fim de
penetrá-la e garantir sua sobrevivência. Ainda no hospedeiro vertebrado podem ser encontradas
formas epimastigotas durante o final do ciclo intracelular, quando as amastigotas (formas
replicativas intracelulares sem flagelo) se transformam em tripomastigotas, ou vice-versa, dando
início a um novo ciclo (Ley et al, 1990). A infecção humana pode ocorrer através de transfusão
sanguínea, transmissão congênita, acidentes de laboratório, transmissão oral e transplantes de
órgãos, além da transmissão vetorial (principal forma de transmissão) (Prata, 2001).
A
B
C
Figura 1: Morfologia do T.cruzi. A) epimastigotas, formas replicativas; B) Ninho de amastigotas C) tripomastigota
sanguíneo, forma infectante. Fonte: de Souza, 2002.
Existe um grande número de insetos, família Ruduviidea, capazes de transmitir o T. cruzi,
fazendo com que a doença de Chagas tenha uma ampla distribuição geográfica. Além disso, muitos
mamíferos de grande importância epidemiológica servem como reservatórios naturais do parasito,
dentre eles roedores e desdentados. A doença foi considerada, inicialmente, uma zoonose presente
apenas no ambiente selvagem, mas após a invasão das matas pelo homem, houve uma dispersão dos
vetores triatomíneos que se adaptaram ao novo ambiente e passaram a usar o homem como fonte de
alimento, passando esta a ser considerada uma antropozoonose.
A doença no homem apresenta uma grande variedade de manifestações clínicas, que
provavelmente estão relacionadas à genética do parasito, bem como a do seu hospedeiro (Macedo et
al, 2004). Entretanto, outros aspectos devem ser ressaltados como o microambiente, a resposta
imune hospedeiro, a carga parasitária, o estado nutricional, dentre outro.
13
Sendo assim, a fase aguda ou inicial da doença é caracterizada pela curta duração e por sinais
clínicos brandos e inespecíficos como, febre, edema ganglionar, geralmente de difícil
reconhecimento ou específicos como, alta parasitemia e o sinal de Romaña ou chagoma de
inoculação, que corresponde a uma inflamação local no sítio de penetração do parasito. É menos
freqüente, porém provável, a ocorrência de miocardites, meningoencefalites, especialmente em
indivíduos imunossuprimidos (Hoff et al, 1978) ou a ocorrência de óbitos nessa fase (apenas 5% dos
casos de complicações cardíacas e neurológicas são fatais, especialmente em crianças). Nessa fase, o
parasito pode levar o indivíduo infectado a um comprometimento do sistema imune, resultado da
depleção de células do timo e intensa ativação policlonal de linfócitos (Reina-San-Martin et al,
2002). Após a fase aguda, a maioria dos indivíduos infectados pelo T. cruzi é conduzida para uma
fase latente da doença, também conhecida como forma crônica indeterminada, permanecendo sem
sintomatologia clínica detectável por décadas ou pela vida toda. Por outro lado, aqueles indivíduos
que desenvolvem a fase crônica sintomática da doença (aproximadamente 35%) podem apresentar
sinais patológicos característicos como cardiopatia (alterações eletrofuncionais cardíacas caracterizada por miocardite crônica que freqüentemente leva a cardiomegalia, falência congestiva
crônica e arritmias) (Rocha et al, 2007), além de danos ao sistema nervoso periférico, alterações na
motilidade esofágica e intestinal, levando ao quadro de megaesôfago e megacólon. Nessas alterações
patológicas, há infiltrado de linfócitos (Hoff et al, 1978)), perda das células miocárdicas na
cardiopatia (Palacius-Pru et al, 1989) e degeneração neuronal e denervação nos quadros digestivos
(Koeberle, 1968; Adad
et al, 1991). Podem ser observados também alterações neurológicas,
tromboembolismo venoso, acidentes cerebrovasculares e choque isquêmico, sendo estas últimas a
causa primária da morte súbita associada à doença (Rocha et al, 2007).
Excluindo os casos inesperados de morte súbita, que podem surgir em qualquer fase da
infecção (Prata et al, 1986), os demais casos relatados sucedem uma forma de acometimento
cardiovascular típico da doença, a cardiopatia chagásica. A cardiopatia chagásica possui como
característica principal um caráter progressivo e fibrosante, explicada por mecanismos como a
proliferação celular no miocárdio, especialmente fibroblastos e linfócitos T (Tanowitz et al, 2003),
necrose e apoptose das células cardíacas (Barcinski & DosReis, 1999), hiperplasia e hipertrofia
celular (Arnaiz et al, 2002), resposta imune devido à persistência do parasito nos tecidos (Gea et al,
1993) e autoimunidade (Leon & Engman, 2001).
14
1.2. A resposta inflamatória na infecção pelo T. cruzi.
A resposta inflamatória após a infecção pelo parasito é essencial para a resistência do
hospedeiro, mas também é responsável por diversas patologias observadas no curso da doença.
Uma vez na corrente sanguínea do hospedeiro, o parasito consegue escapar da lise pelo
complemento devido à existência de moléculas reguladoras de ativação do sistema complemento em
sua superfície celular (Krettli &Lima Pereira, 1981). No entanto, o reconhecimento de outras
moléculas de superfície estimula a síntese de citocinas pró-inflamatórias, bem como de quimiocinas
pelos macrófagos do hospedeiro. As citocinas produzidas durante a infecção como, TNF-α, IL-1,
IFN- γ, IL-10 e TGF-β, são capazes de induzir e regular a produção de diferentes quimiocinas e
alterar seu perfil de síntese por macrófagos e cardiomiócitos infectados (Teixeira et al, 2002). Estas
citocinas induzem a morte do parasito pela liberação de oxido nítrico (NO) pelos cardiomiócitos e
macrófagos, através da enzima óxido nítrico sintase (iNOS) (Aliberti et al, 1999). A eficiência da
resposta imune gerada contra o parasito na fase aguda da infecção é responsável pela redução, porém
não pela eliminação do parasito, conferindo resistência parcial ao hospedeiro (Krettli & Lima
Pereira, 1981).
A disseminação sistêmica do patógeno leva a um massivo infiltrado de células mononucleares
no miocárdio, levando a produção de citocinas, quimiocinas e mediadores como o NO. O perfil de
resposta imune, mediada por linfócitos T, que protege o hospedeiro e controla o parasitismo
apresenta um perfil chamado de Th1. Por outro lado, o controle da inflamação aguda, que gera dano
ao tecido, ocorre por meio de uma resposta de perfil Th2, através da produção das IL-4, IL-10 e
TGF-β. Sendo assim, Th2 limita a ação das citocinas pró-inflamatórias produzidas por Th1 e inibe a
liberação de NO (Mariano et al, 2008), o que possibilita a sobrevivência do parasito, previne a
hiperatividade da resposta imune e a imunopatologia dos tecidos afetados (Holscher et al, 2000;
Hughes & Kelly, 2006).
A falta de competência da resposta imune em eliminar completamente o parasito, se deve
também a existência de outra população de células T conhecidas como células T reguladoras (Treg)
(CD4+CD25+) que modulam a resposta imune. As T reg suprimem a proliferação de células T e
inibem a indução de autoreatividade destas células, função importante na prevenção de doenças
autoimunes. As células T regs podem entrar em ação devido à produção de TGF-β e IL-10, presentes
na infecção pelo T. cruzi (Mariano et al, 2008).
15
Dados mostraram que as lesões associadas à intensa resposta proliferativa e a liberação de
citocinas, que ocorrem durante a fase aguda da infecção, são também observadas em células de
pacientes chagásicos crônicos (da Silva et al, 2007). E, células T ativadas estão presentes em maior
quantidade no infiltrado inflamatório dos pacientes sintomáticos, o que demonstra uma estreita
relação entre essas células e o desenvolvimento da patologia na fase crônica (Cunha-Neto et al,
2005; Dutra et al, 1997). Além disso, Souza et al (2004) demonstraram que monócitos de pacientes
com lesões cardíacas expressam níveis elevados TNF-α, citocina associada à progressão das lesões
cardíacas, enquanto que em pacientes na fase indeterminada da infecção a citocina de expressão
prevalente é a IL-10, responsável por controlar a parasitemia. E ainda, o número de macrófagos e
monócitos é altamente elevado na doença de Chagas devido à potente reação inflamatória
desencadeada (Melo et al, 2003). Estudos mostraram que a depleção de macrófagos, causa um
aumento significativo no número de ninhos de amastigotas em cardiomiócitos. Esses dados indicam
que durante a fase aguda da infecção a rápida produção, maturação e ativação de macrófagos são
capazes de controlar a replicação do parasito, enfatizando o papel essencial dos macrófagos na
resistência de ratos a doença de Chagas (Melo & Machado, 2001).
Os macrófagos apresentam ao menos duas populações distintas (Itoh M et al, 1995). Os
macrófagos residentes, ou histiócitos, possuem um antígeno de superfície reconhecido pelo
anticorpo monoclonal ED2 (ou anti-CD68), enquanto que os monócitos apresentam um marcador
lisossômico, reconhecido pelo anticorpo monoclonal ED1(ou anti-CD163) (Dijkstra et al, 1985).
Alguns imunologistas consideram que as células ED1+ ED2- possam ser monócitos recém-chegados
ao tecido enquanto que os residentes (ED1- ED2+), ainda que originários dos monócitos teriam
passado, nos tecidos, a expressar novos antígenos (Barbé et al, 1990).
1.3. Fractalquina/CX3CL1 e endotelina na biologia vascular.
As quimiocinas constituem-se numa superfamília de proteínas de baixo peso molecular com
um papel fundamental nas reações inflamatórias (Mantovani et al, 2004). O recrutamento e a
transmigração leucocitária são descritos como suas funções mais características, porém as
quimiocinas também participam de eventos como angiogênese, produção de colágeno e homeostasia
de estruturas vitais como o sistema cardiovascular e órgãos hematopoiéticos (Bacon & Oppenheim
1998, Kim 2004). Assim, as quimiocinas podem ser divididas funcionalmente em duas categorias,
16
quimiocinas inflamatórias, as quais recrutam leucócitos em resposta ao estresse fisiológico e,
homeostáticas, responsáveis pelo tráfico basal de leucócitos e pela arquitetura de órgãos linfóides
secundários (Moser & Loetscher, 2001; Zlotnik & Yoshie, 2000; Gerard & Rollins, 2001). A
migração leucocitária em direção aos tecidos, durante um evento inflamatório, apresenta uma cascata
de eventos moleculares envolvendo tanto as quimiocinas quanto seus receptores, ambos integrados
as células co-participantes desses eventos: leucócitos e células endoteliais (Galkina & Ley 2007).
A CX3CL1 é o único membro da família das quimiocinas CX3C, e pode ser encontrada na
forma de proteína de membrana celular, agindo principalmente na retenção e adesão de leucócitos ou
ainda em sua forma solúvel, sendo capaz de atrair monócitos/ macrófagos, células natural killers
(NK) e células T (Bazan et al, 1997; Fong et al, 1998), onde seu receptor CX3CR1 é expresso. Pode
ser encontrada também nas células endoteliais ativadas por citocinas inflamatórias como IFN-γ e
TNF-α (McComb et al, 2008).
Além disso, é capaz de agir na proliferação de células da
musculatura lisa e, ainda ser expresso em plaquetas. Portanto, essas células, agindo separadamente
ou em conjunto, funcionam como mediadoras no efeito da CX3CL1 na resposta inflamatória
vascular (Liu et al, 2006).
Recentes evidências sugerem que a CX3CL1 pode agir na progressão direta da resposta
inflamatória, através da ativação de células NK e células dendríticas, desencadeando uma resposta
imune com perfil Th1 (Ryu et al, 2008). Esta resposta é capaz de provocar a exacerbação da
inflamação propiciando o envolvimento desta quimiocina na patofisiologia de diferentes doenças
inflamatórias como aterosclerose, glomerulonefrite, rejeição a transplantes cardíacos ou mesmo
doenças de caráter autoimune como artrite reumatóide (Galkina & Ley 2007; Schober, 2008). Além
disso, estudos descrevem que a CX3CL1 funciona como quimiocina angiogênica, ou seja, ela é
capaz de induzir a formação de novos vasos sanguíneos, crítica para a progressão do foco
inflamatório (Ryu et al, 2008).
A abundante expressão da CX3CL1 é detectada em cardiomiócitos, a qual estimula a expressão
de genes envolvidos no desenvolvimento da hipertrofia e falência cardíaca (Husberg et al, 2008). A
expressão da CX3CL1 está intimamente ligada ao processo inflamatório, sendo possível especular o
seu envolvimento na progressão doença de Chagas, uma vez que esta apresenta um caráter
tipicamente inflamatório. No entanto, o complexo de regulação dos mediadores inflamatórios e sua
expressão, especialmente no tecido cardíaco, está longe de ser completamente entendido (Husberg et
al, 2008).
17
Outro importante mediador inflamatório associado à biologia do endotélio é denominado
endotelina. De fato, as endotelinas são peptídeos produzidos pelo endotélio com potente atividade
vasoconstritora (especialmente a endotelina-1), normalmente estimuladas por mecanismos geradores
de danos vasculares. Após síntese e liberação, as endotelina exercem muitas funções como a
ativação de macrófagos, proliferação de fibroblastos na musculatura lisa vascular, regulação de
funções vasculares, liberação de peptídeos natriuréticos pelos cardiomiócitos, além de inibir a
liberação de renina pelos glomérulos e modular a ação da norepinefrina nas terminações nervosas
simpáticas (Davenport & Maguire 2006).
As endotelinas têm sido associadas aos processos ateromatosos e vários estados de doenças
cardiovasculares. A endotelina-1, a saber, tem participação comprovada na insuficiência cardíaca
congestiva, insuficiência renal, hipertensão arterial, hiperlipidemia e doença de Chagas (Giannessi et
al, 2001; Little et al, 2008). Distúrbios na produção e clearance da endotelina-1, contribuem
diretamente para a fisiopatologia cardiovascular experimental na doença de Chagas. Foi descrito, em
modelo murino, que alta expressão de endotelina no tecido cardíaco estaria associada diretamente à
infecção pelo T. cruzi e que esse perfil contribuiria para a elevada produção do óxido nítrico
(importante para o controle parasitário), para processo de fibrogênese e conseqüentemente para as
alterações fisiopatológicas graves no endotélio vascular (Petkova et al, 2001; Machado & Camargos
2008). Além disso, a ação da endotelina, principalmente através dos receptores ETA, pode estimular
os macrófagos a liberar citocinas, como TNF- α (Rae & Henriques, 1998), responsáveis por grande
parte dos danos causados aos tecidos durante a doença de Chagas.
Os altos níveis de IFN-γ e TNF-α, presentes durante a doença de Chagas, que coordenam a
expressão de quimiocinas e também das endotelinas (Talvani et al, 2000; Gomes et al. 2003; Talvani
et al, 2004), propiciam a ação de ambos os mediadores inflamatórios que também exercem
importante papel durante a patogênese da cardiopatia chagásica (Engman & Leon, 2002). Dessa
forma, torna-se evidente que tanto a CX3CL1 quanto a endotelinas constituem-se peças estruturais
importantes na patogênese da doença de Chagas, principalmente na biologia cardiovascular. A
compreensão do papel desses mediadores inflamatórios na geração dos eventos tromboembólicos
após a infecção pelo T. cruzi poderia, em longo prazo, contribuir para ações farmacoterápicas
preventivas na clínica da doença de Chagas. No entanto, a realidade da população afetada pelo T.
cruzi traduz outro aspecto indiretamente associado à resposta imune da doença: um extensivo quadro
de miséria e negligência ocasionado por diferentes instâncias sociais e políticas. Fruto dessa
18
condição precária surge uma inevitável condição de desnutrição em crianças e adultos pela
insuficiência tanto na quantidade quanto na qualidade dos constituintes nutricionais. E nesse
contexto, a redução drástica de proteínas na alimentação ocasionadas em diferentes momentos da
infecção chagásica poderia interferir diretamente na geração da resposta imune e, dessa forma,
alterar significativamente o curso clínico da doença.
1.4. O estado nutricional: aspectos gerais e sua relevância na doença de Chagas
A nutrição é conceituada como a ciência dos alimentos capaz de estabelecer uma íntima
relação entre a saúde e a vida dos indivíduos. Ela pode ser incluída entre os fatores capazes de alterar
a integridade física, a capacidade produtiva ou mesmo a resistência do homem frente às doenças
infecciosas e parasitárias. Em contrapartida, desnutrição compreende todas as inadequações
dietéticas, bem como as deficiências de absorção e má utilização dos alimentos, capazes de criar
condições para a ocorrência de doenças ou mesmo de desencadear ou exacerbar sintomas clínicos
associados a elas (Forbes, 1978).
A desnutrição é um dos maiores problemas socioeconômicos que ocorre em todo o mundo.
Ainda hoje é possível notar a deficiência que existe na qualidade da alimentação das populações,
especialmente dos países em desenvolvimento. As populações que vivem na linha da pobreza são as
que mais sofrem com o déficit nutricional, uma vez que são negligenciadas. As conseqüências de
uma má alimentação, ou a falta dela, podem ser desastrosas no que diz respeito ao crescimento,
desenvolvimento e sobrevivência do indivíduo. E ainda, a incidência da anemia entre mulheres
grávida, desses países, pode chegar a 80% (Sharma et al, 2003), o que atinge significativamente o
feto. Há evidências na literatura de que os tipos de deficiência nutricionais não resultam apenas em
anormalidades graves na anatomia do cérebro ou no retardamento mental ou fisiopatológico, mas
também no surgimento e progressão de deficiências cognitivas, de aprendizagem (Ranade et al,
2008) e de comportamento.
A Organização Mundial de Saúde (OMS) estima que 1/3 das crianças no mundo sofram com
a desnutrição e que aproximadamente 150 milhões de crianças com menos de cinco anos apresentam
peso inferior para sua idade (WHO 2007) e que cerca de 182 milhões (32,5%) possuem baixa
estatura (AACC/SCN 2000) devido à desnutrição. A desnutrição é responsável, direta ou
indiretamente por 54% das cerca de 8 a 10 milhões de mortes de crianças com menos de cinco anos
por ano, contribuindo com 53% das mortes associadas a doenças infecciosas entre crianças desta
19
faixa etária nos países em desenvolvimento (WHO 2002). Aproximadamente 20 a 30% das crianças
gravemente desnutridas vão a óbito durante o tratamento em hospitais públicos (Schofield &
Asworth, 1996). No Brasil, desde as décadas de 1970 e 1980 esse quadro vem tendo uma melhora,
onde a prevalência da desnutrição foi reduzida em cerca de 60%, representando mais de um milhão
de crianças (Ministério da Saúde 1996).
A deficiência nutricional é capaz de prejudicar fenômenos imunológicos essenciais para a
defesa no indivíduo. Especialmente na infância, tais deficiências podem ocasionar danos à formação
do sistema imune, com o comprometimento de sua capacidade durante a idade adulta (CunninghamRundles et al, 2005). Na desnutrição, a maioria dos mecanismos de defesa do organismo está
prejudicada (Chandra, 1997). Além disso, a infecção é a maior causa de morbidade e mortalidade em
indivíduos severamente desnutridos (Morgan, 1997). A desnutrição está diretamente relacionada à
debilidade do sistema imune, através do enfraquecimento da função fagocítica das células do sistema
mononuclear, do sistema de complemento, da concentração de anticorpos e da produção de citocinas
(Chandra, 2002). Nesta condição várias funções dos macrófagos encontram-se comprometidas
(Borelli et al, 1998). Estas células são de importância fundamental no controle e na resolução dos
processos infecciosos, na regulação da homeostase por participarem efetivamente da resposta
inflamatória e do processo de reparação tecidual e estarem envolvidas na resposta imune tanto inata
quanto adaptativa (Melo et al, 2006). Na infância os impactos e efeitos da desnutrição sobre o
sistema imune e a formação de estruturas orgânicas são ainda maiores.
A desnutrição protéica é causa secundária comum de imunodeficiência e susceptibilidade às
infecções (Katona & Katona, 2008). A deficiência protéica severa em crianças é caracterizada
clinicamente por manifestações como a redução de quase 70% do peso corporal, formação de edema
e presença de anemia. Além disso, a desnutrição severa durante a infância afeta o desenvolvimento
tímico, fato que compromete a imunidade através da redução prolongada da contagem de linfócitos
circulantes (Savino, 2002). Esta imunodeficiência parece ser um fator primordial na susceptibilidade
às infecções.
Os primeiros trabalhos descritos na literatura relacionando o estado nutricional com a doença
de Chagas foram desenvolvidos na década de 1960, utilizando o modelo murino, e demonstraram
que a deficiência de pantotenato, piridoxina ou tiamina aumentavam a ação fagocíticas das células
de defesa e o agravamento das lesões cardíacas, quando comparados aos animais com níveis
dietéticos padrões (Yaeger & Miller 1960). Ainda nesta mesma década, Yaeger & Miller (1963)
20
demonstraram que a deficiência de riboflavina e a vitamina A favorecem o aumento da
susceptibilidade dos animais à cepa Tulahuen do T. cruzi, fato que se mostrou mais justificado pelo
estado de inanição dos animais do que pela deficiência nutricional propriamente dita. E ainda,
Gomes et al., (1994) demonstraram que camundongos adultos submetidos a um grau severo de
restrição protéica (4.75%) e infectados com as cepas Y ou CL de T. cruzi, apresentaram uma
diminuição da resistência a infecção resultando em alta parasitemia e mortalidade, apesar das lesões
cardíacas terem sido menos extensivas. Além disso, muitos autores têm demonstrado a interferência
da deficiência dos micronutrientes (selênio, zinco e ferro) e vitaminas (vitamina E e A) no curso da
doença de Chagas, a qual favorece o aumento das complicações cardiovasculares (Rivera et al,
2002;Carvalho et al, 2006), afeta o desenvolvimento do sistema imune, e conseqüentemente
aumenta a carga parasitária na circulação sanguínea (Brazão V et al, 2008; Arantes et al, 2006; de
Souza et al, 2003; Yaeger & Miller, 1963 ).
Em especial, a desnutrição protéica, pelas limitações imunofisiológicas impostas ao
organismo, parece repercutir mais intensamente na capacidade de resistência às doenças infectoparasitárias (Caulfield et al, 2004; Emery, 2005; Hughes & Kelly, 2006). A limitação protéica afeta
diretamente a resposta imune inata e adquirida, havendo inclusive maior deficiência na resposta
celular sobre a humoral (Cunningham-Rundies et al, 2005). Como conseqüência clínica desta
deficiência alimentar, relata-se a presença de edemas, apatia, perda de massa muscular,
hepatomegalia e anemia. Além da repercussão da dieta hipoprotéica na imunidade do indivíduo,
algumas pesquisas demonstram sua interferência também nos mecanismos fisiológicos autonômicos
do organismo (Oliveira et al, 2004; Tropia et al 2001).
Portanto, a compreensão das alterações imuno-fisiológicas secundárias ao déficit protéico nos
indivíduos infectados pelo T. cruzi torna-se fundamental para o entendimento das alterações clínicas
associadas à doença de Chagas. Pela relevância da desnutrição em nosso país e, pelas décadas que
distanciam os estudos pioneiros em desnutrição na doença de Chagas, poucos trabalhos são descritos
na literatura científica envolvendo a infecção pelo T. cruzi. Diante da complexidade de variáveis que
interpõem a evolução clínica da infecção pelo T. cruzi, talvez o aspecto nutricional do hospedeiro
tenha sido um fato até hoje negligenciado, porém importante em processos imunofisiológicas tanto
da cardiopatia chagásica crônica quanto dos eventos vasculares largamente descritos e associados os
casos de morte súbita na doença de Chagas.
21
2.0. OBJETIVO
2.1. Objetivo geral
O objetivo deste trabalho foi avaliar a interferência da dieta hipoprotéica na síntese da
quimiocina CX3CL1 e do peptídeo vasoativo endotelina durante o processo inflamatório
cardiovascular em ratos Fisher experimentalmente infectados pela cepa Y do T. cruzi.
2.2. Objetivos específicos
•
Adaptar o modelo de desnutrição protéica em ratos Fisher, possibilitando a sobrevivência
dos animais infectados pelo T. cruzi por um longo período (120 dias, fase crônica);
•
Identificar as lesões no tecido cardíaco e vascular dos animais submetidos às dietas
normoprotéica e hipoprotéica em associação com a infecção pelo T. cruzi na fase aguda e
fase crônica da doença de Chagas;
•
Avaliar os níveis séricos e no coração da CX3CL1 e endotelina e, correlacioná-los a
intensidade do infiltrado inflamatório durante as fases aguda e crônica da doença de Chagas,
correlacionando esses achados ás respectivas dietas dos animais;
•
Avaliar a expressão qualitativa de receptores de CX3CL1, macrófagos residentes e
recrutados no tecido cardíaco dos animais infectados pelo T. cruzi submetidos às dietas
normoprotéica e hipoprotéica.
22
3.0. MATERIAL E MÉTODOS
3.1. Proposição de um modelo de dieta hipoprotéica em ratos para o estudo da infecção pelo T. cruzi.
A introdução da dieta hipoprotéica no modelo murino (ratos), proposta na metodologia, tem
sido largamente estuda e pré-testada no Laboratório de Nutrição Experimental, ENUT, UFOP.
Porém, mediante a presença da elevada carga parasitária (T. cruzi), houve a necessidade de
desenvolver um modelo capaz de se adequar à condição de “desnutrição” e “infecção”
concomitantemente e, que permanecesse nesse estado por um longo período após a infecção para a
caracterização da fase crônica da doença.
O esquema abaixo ilustra o modelo proposto e adequado por nosso laboratório, no qual são
explicitadas as várias etapas experimentais desenvolvidas desde o nascimento até o sacrifício dos
animais (Figura 2). Após o desmame, com 21 dias de vida, as dietas normoprotéica e hipoprotéicas
foram introduzidas aos grupos e oferecidas por um período necessário para o estabelecimento da
deficiência protéica (14 dias). Em seguida, formas tripomastigotas do T. cruzi foram inoculadas em
nos animais (grupo infectado), sendo estes sacrificados nos períodos estabelecidos como fase aguda
(15 dias) e fase crônica (120 dias) da doença de Chagas experimental.
Introdução
das dietas
0
Fase aguda
21
21dias
35
14 dias
Fase crônica
50
15 dias
170
120 dias
Dias
Nascimento
Desmame
Infecção
Sacrifício
Sacrifício
(420x103 tripo/70g)
Figura 2: Esquema representativo da adaptação ao modelo de desnutrição protéica. Modelo
pré-estabelecido pelo Laboratório de Nutrição Experimental da Escola de Nutrição da UFOP.
Durante as fases aguda e crônica da doença foram sacrificados 5 animais de cada grupo (Infectado
com dieta normoprotéica, infectado com dieta hipoprotéica, não infectado com dieta normoprotéica e
não infectado com dieta hipoprotéica).
23
3.2. Animais
Ratos Fisher machos, com 21dias de vida, provenientes do Biotério da Escola de Nutrição da
Universidade Federal de Ouro Preto, receberam uma dieta hipoprotéica contendo 6% de proteína
durante 14 dias, após o desmame. Os grupos foram separados aleatoriamente, de forma que a média
do peso dos animais de cada grupo não fosse superior a 2g, quando comparado aos demais grupos.
Realizada a desnutrição, dez desses animais foram infectados intraperitonealmente (i.p.) com 420 x
103 formas tripomastigota/70 g de peso (Camargos et al, 2000) com a cepa Y do T. cruzi. O grupo
controle recebeu a dieta normoprotéica contendo 15% de proteína. Desses animais, dez foram
infectados, assim como os ratos do grupo que recebeu a dieta hipoprotéica. Após a infecção e os
intervalos de tempo (15 dias fase aguda e 120 dias fase crônica) necessários para estabelecimento da
doença, os animais foram sacrificados, os corações foram extraídos, fragmentado e conservados (de
acordo com as técnicas utilizadas posteriormente) e o soro coletado para análises posteriores. O
projeto contou com duas etapas experimentais, a fim de adaptar o modelo de desnutrição protéica à
infecção pelo T. cruzi nas fases aguda e crônica da doença. Sendo assim, obtivemos quatro grupos
com dez animais, na primeira e na segunda etapa da experimentação que se diferenciavam apenas
pelo tempo de infecção. Todos os procedimentos e protocolos são realizados de acordo com a
conduta preconizada pelo COBEA (Colégio Brasileiro em experimentação Animal) sobre pesquisa
em animais. Projeto aprovado pelo Comitê de Ética em Pesquisa Animal da UFOP.
3.3. Dieta
A dieta hipoprotéica bem como a dieta normoprotéica empregadas neste procedimento, foram
desenvolvidas pelo Laboratório de Nutrição Experimental, da Escola de Nutrição da UFOP e, foram
ofertadas livremente, junto com água. Os animais permaneceram em salas com temperatura e
luminosidade controladas.
24
Tabela 1: Composição das dietas experimentais para cada 3000g da dieta (g/KG).
Ingredientes
Amido de milho
Caseína *
Sacarose
Óleo
Fibras (celulose)
Mistura de sais**
Mistura de vitaminas**
Colina
Dieta NP
Dieta HP
1597,5g
600g
300g
210g
150g
105g
30g
7,5g
1987,5g
210g
300g
210g
150g
105g
30g
7,5g
(*) O teor de caseína usado nas dietas normoprotéica e hipoprotéica foram de 6% e 15% respectivamente.
(**) Quantidades em gramas baseadas nos protocolos do Laboratório de Nutrição experimental do ENUTUFOP; teores de minerais e vitaminas baseados em Reeves et al (1993)
3.4. Avaliação nutricional
Como parâmetro de avaliação do status nutricional utilizou-se o peso dos animais, através da
pesagem semanal após o desmame, e dosagens bioquímicas. Além disso, após o sacrifício dos
animais os corações foram retirados e pesados, a fim de permitir a análise comparativa destes com o
peso corporal. O teor de albumina e proteínas totais foi determinado em soro e o teor de
hemoglobina de sangue total, coletados por animal utilizando kits comerciais (Labtest Diagnóstica
S.A®, Cat 99, Lagoa Santa, Minas Gerais, Brasil).
3.5. Parasitemia
Formas sanguíneas do T. cruzi foram contados em todos os animais infectados, diariamente,
através de observação direta ao microscópio óptico utilizando-se 5 µl de sangue fresco entre lâmina
e lamínula, coletados através da veia caudal dos animais (Brener Z, 1962).
3.6. Histopatologia
3.6.1. Processamento histológico
Os corações foram fixados em solução de formol a 10% em PBS, desidratados em álcoois de
concentrações crescentes (70%, 80%, 90%, 95% e 100%), diafanizados em xilol e incluídos em
25
parafina. Os blocos de parafina foram cortados em 4µm, corados pela técnica de hematoxilina e
eosina (HE) e montados em lâminas para avaliação morfológica do infiltrado inflamatório e da
presença de trombos.
3.6.2 Análise morfológica qualitativa e quantitativa dos tecidos cardíacos.
Aspectos qualitativos dos tecidos cardíacos foram analisados e documentados. Para
quantificação de celularidade dos tecidos cardíacos, 20 imagens de cada coração foram obtidas com
a objetiva de 40 X através do software de captura de imagens Leica Application Suite do Laboratório
multiusuário do NUPEB/UFOP. Posteriormente, as imagens foram avaliadas em um microscópio de
luz acoplado a uma câmera pelo programa Leica Qwin, no mesmo laboratório, através da seleção de
pixels com coloração característica para núcleos celulares corados por hematoxilina. O número de
células quantificadas por imagem do mesmo coração foi somado e a média do número de células
para cada grupo foi obtido.
3.7. Imuno-histoquímica
Os fragmentos coletados foram acondicionados em Optimum cutting temperature compound
médium (O.C.T.), congelado a -80oC. Posteriormente foram cortados a 7 µm de espessura em
criostato e colocados em lâminas silanizadas. O tecido foi tratado com H2O2 30% e azida sódica
(0,007g para 1 mL de PBS) em PBS por 10 min para bloquear a atividade de peroxidase endógena e
em PBS/BSA 2% durante 20 min para o bloqueio de sítios inespecíficos. Após lavar com PBS por
10 min, as lâminas foram incubadas por uma hora com o anticorpo primário em PBS/BSA 2%
(camundongo/coelho anti-rato anti-CD68, anti-CD163 (Abd Serotec, Kdlington, UK) e anti-CX3CR1
(BioVision, Cat 5537-100, Moutain view, USA) na diluição 1:400), lavadas novamente em PBS e
incubados por mais uma hora com o anticorpo secundário conjugado ao complexo biotina-avidianaperoxidase (1:50) em PBS/BSA 2% . A reação foi revelada com DAB (Sigma Co., S. Louis, EUA) e
DMSO por 10 minutos, usando sempre 100µl das soluções para cada lâmina.
26
3.8. Reação imunoenzimática - ELISA
3.8.1. Fractalquina/CX3CL1
O ensaio imunoenzimático para CX3CL1 foi realizado utilizando-se plasma e sobrenadante
de macerado cardíaco proveniente de animais infectados ou não e submetidos à dieta normoprotéica
ou hipoprotéica. De acordo com os Kits CX3CL1 (R&D System, Cat DY990, Abingdon, UK), foram
adicionados 50 µl do anticorpo de captura diluído em PBS (0.8 µg/mL de PBS) em cada poço e a
placa foi incubada overnight em temperatura ambiente. Após cada etapa eram adicionados 200 µl do
tampão de lavagem (PBS Tween 20®0.05%) em cada poço e aspirado por três vezes. Bloqueado
com reagente diluente (150 µl PBS/BSA 1%) por 1 hora, a placa recebeu as amostras e os padrões
(50µl) e depois de 2 horas de reação foi adicionado o anticorpo de detecção (300 ng/mL de reagente
diluente). Finalmente, 50 µl de estreptoavidina ligada à peroxidase na diluição de 1:200 foram
adicionados à placa. Após revelação (H2O2 e tetrametilbenzidina 1:1) a intensidade de marcação foi
realizada em leitor de ELISA utilizando-se o comprimento de onda de 450 nM.
3.8.2. Endotelina
O ELISA para endotelina utilizou plasma e sobrenadante de macerado cardíaco proveniente de
animais infectados ou não e submetidos à dieta normoprotéica ou hipoprotéica. De acordo com o Kit
endotelia (Cayman Chemical’s Co.), foram adicionados a placa, previamente incubada com
anticorpo de captura, 50 µl da amostra e do padrão (5ng/mL de tampão EIA) em cada poço
juntamente com 50 µl do conjugado (endthelin AChE-Fab’ conjugate) e 2.5 µl de soro de rato não
específico, a fim de bloquear anticorpos heterofílicos. Posteriormente, a placa é mantida overnight
em 4° C e, 250 µl do tampão de lavagem (PBS Tween 20® 0.005%) são adicionados em cada poço e
aspirados por cinco vezes. Após a lavagem, a placa é coberta com 100 µl de Reagente de Ellman,
incubada por 30 - 90 minutos em temperatura ambiente e suavemente movimentada. Enfim, a placa
é levada ao leitor de ELISA e lida utilizando-se o comprimento de onde de 405- 420 nM. Todos os
reagentes são fornecidos pelo kit, com exceção das amostras.
27
3.9. Análise estatística
Os parâmetros avaliados foram representados através da média de seus valores e respectivo
erro médio padrão ou então, pelos valores absolutos com respectiva média (gráficos de dispersão).
Utilizou-se One-way ANOVA para múltiplas comparações, testes de Tukey-Kramer HSD ou
student-Newman multiple comparisons). Foi empregada a regressão linear para alguns valores
bioquímicos, quando necessário. Todas as análises foram realizadas através dos programas INSTAT e
GraphPad Prism.
28
4.0. RESULTADOS
4.1. Avaliação do estado nutricional: pesos e dosagens bioquímicas.
Os dados da figura 3, utilizados na avaliação do estado nutricional dos animais, demonstram
que os animais com dieta hipoprotéica apresentam um pequeno aumento de peso corporal tendendo a
estabilidade após as primeiras semanas de infecção. Ao contrário, os animais com dieta
normoprotéica tiveram um ganho de peso durante todo este período até o momento do sacrifício
(Figura 2). Portanto, o ganho de peso corporal foi um dos parâmetros utilizados para avaliação do
estado nutricional dos animais.
NP - não infectado
Ganho de peso corporal (g)
HP - não infectado
140
NP - infectado
120
HP - infectado
100
80
60
40
*
*
20
*
0
0
1
2 semanas/dieta
hipoprotéica
Desmame
20
3
1
42
Semanas após a infecção
Infecção
com o T. cruzi
Figura 3: Avaliação do ganho de peso dos animais. Animais (ratos Fisher) pesados semanalmente após o desmame
(até 15 dias após a infecção). Os grupos submetidos à dieta normoprotéico (linhas pretas) apresentaram um aumento
significativo de massa corporal, durante as quatro semanas de vida, quando comparados aos grupos submetidos à dieta
hipoprotéica (linhas vermelhas), não havendo influencia da infecção pelo T. cruzi neste parâmetro. Os dados acima estão
apresentados como média+/- SEM e analisados por One-way ANOVA (Tukey-Kramer HSD). * p<0,05 quando
comparamos animais submetidos à dieta normoprotéica com animais submetidos à dieta hipoprotéica.
29
Para confirmar a eficácia do modelo de dieta hipoprotéica, amostras de soro dos animais foram
analisadas e demonstraram diferenças nos níveis de proteínas totais entre os animais que consumiam
as dietas normoproéica e hipoprotéica, tanto na fase inicial da doença de Chagas (Figura 4A) quanto
na fase crônica (Figura 4B). Isto nos permite afirmar que a dieta deficiente em proteína afetou
consideravelmente os níveis séricos de proteínas totais nos animais, não havendo novamente
interferência da infecção nesses parâmetros.
A
B
0.5
0.4
*
*
0.3
Proteínas totais
(mg/dL)
Proteínas totais
(mg/dL)
0.5
0.4
*
*
0.3
0.2
0.2
NP
HP
Não infectados
NP
NP
HP
HP
Não infectados
Infectados pelo
T. cruzi (15 dias)
NP
HP
Infectados pelo
T. cruzi (120 dias)
Figura 4: Avaliação sérica das proteínas totais. Tanto na fase aguda (A) quanto na fase crônica (B) da infecção, os
níveis séricos de proteínas totais foram significativamente menores nos animais que consumiam dieta hipoprotéica em
relação aos animais que consumiam dieta normoprotéica, infectados ou não. As dosagens foram feitas após o sacrifício
dos animais. Os dados acima estão apresentados como média+/- SEM e analisados por ANOVA One-way (TukeyKramer HSD). * p< 0,01.
Na figura 5, podemos observar que os níveis de albumina apresentaram-se significativamente
reduzidos no grupo com dieta hipoprotéica independentemente da ocorrência da infecção quando
comparados ao grupo de dieta normoprotéica. No entanto, apesar desta diferença, os animais que
consumiam a dieta hipoprotéica foram capazes de manter estáveis seus níveis de albumina mesmo
após um longo período de restrição de proteína.
30
0.4
Albumina (mg/dL)
Albumina (mg/dL)
0.4
0.3
*
*
0.2
*
0.3
*
0.2
0.1
0.1
NP
HP
Não infectados
NP
NP
HP
HP
Não infectados
Infectados pelo
T.cruzi (15 dias)
NP
HP
Infectados pelo
T. cruzi (120 dias)
Figura 5: Avaliação dos níveis séricos de albumina. Tanto na fase aguda (A) quanto na fase crônica (B) da infecção,
os níveis séricos de albumina foram significativamente menores nos animais que consumiam dieta hipoprotéica em
relação aos animais que consumiam dieta normoprotéica, infectados ou não, tanto na fase aguda quanto na fase crônica
da infecção. As dosagens foram feitas após o sacrifício dos animais. Os dados acima estão apresentados como média+/SEM e analisados por ANOVA One-way (Tukey-Kramer HSD).
O índice sanguíneo de hemoglobina utilizado para caracterizar o modelo de desnutrição em
ratos, demonstrou que na fase aguda da doença, apenas os animais deficientes em proteínas não
infectados (figura 5A) apresentaram diferenças em relação aos demais grupos. E, aos 120 dias de
infecção (fase crônica), após um tempo mais prolongado de dieta hipoprotéica, as diferenças entre os
estes grupos se exacerbaram (figura 5B).
B
A
0.50
Hemoglobina (g/dL)
Hemoglobina (g/dL)
0.5
0.4
*&
0.3
0.45
* &
0.40
0.35
0.2
NP
HP
Não infectados
NP
NP
HP
Infectados pelo
T. cruzi (15 dias)
HP
Não infectados
NP
HP
Infectados pelo
T. cruzi (120 dias)
Figura 6. Avaliação dos níveis sanguíneos de hemoglobina. Análise bioquímica realizada após o sacrifico dos animais
em fase aguda (15 dias de infecção) (A) e fase crônica (120 dias e infecção) (B). Os dados acima estão apresentados
como média+/- SEM e analisados por ANOVA One-way (Tukey-Kramer HSD). * p< 0,05; &: diferença entre os grupos
submetidos à mesma dieta.
31
4.2. Parasitemia e mortalidade.
Na figura 7, a curva de parasitemia, usada para caracterizar a infecção através da contagem de
formas tripomastigotas na circulação sanguínea, mostra que os animais com dieta hipoprotéica
apresentam um pico (3 dias após a infecção) significantemente maior (p <0,001) do que os animais
com dieta normoprotéica. Entretanto, os dois grupos mostraram o mesmo período pré-patente e
tempo de parasitemia (15 dias após a infecção).
*
Parasitos/0.1 ml de sangue
200000
*
Dieta normoprotéica (NP)
Dieta hipoprotéica (HP)
150000
100000
50000
0
0
2
4
6
8
10
12
Dias após infecção
Figura 7. Parasitemia. Ratos Fisher infetados com 420 x 103 tripomastigotas da cepa Y do T. cruzi. É evidente uma
diferença no pico de parasitemia dos animais com dieta HP (n=10) em relação aos animais com dieta NP (n=10). Os
dados acima estão apresentados como média+/- SEM e analisados por ANOVA (student-Newman multiple comparisons
test). * p<0,001 quando comparamos animais submetidos à dieta normoprotéica com animais submetidos à dieta
hipoprotéica.
As taxas de mortalidade foram determinadas em cada grupo de animais. Na fase aguda (15 dias
de infecção) a sobrevivência foi de 100% em todos os grupos, já na fase crônica (120 dias de
infecção) um animal de cada grupo morreu, exceto no grupo alimentado com dieta normoprotéica
não infectado (dados não mostrados).
32
4.3. Análise morfológica e morfométrica do coração.
A análise histopatológica dos tecidos cardíacos dos animais alimentados com dieta
normoprotéica (Figura 8C) e hipoprotéica (Figura 8D) infectados pelo T.cruzi na fase aguda da
infecção revelou a presença de intenso infiltrado inflamatório, sobretudo perivascular, com
predomínio de células mononucleares e áreas de necrose.
Na fase crônica (120 dias após a
infecção), os animais que consumiam dieta normoprotéica (Figura 8E) e hipoprotéica (Figura 8F)
apresentaram tecido cardíaco relativamente preservado, com focos discretos de inflamação, com
predomínio de células mononucleares. Tanto os animais não infectados e alimentados com dieta
normoprotéica (Figura 8A) quanto os animais não infectados e alimentados com dieta hipoprotéica
(Figura 8B) apresentaram tecido cardíaco preservado. Com relação à vasculatura cardíaca, a análise
qualitativa permitiu observar alterações morfológicas entre os grupos infectados, como a dilatação
dos vasos sanguíneos, além destes se mostrarem repletos de hemácias quando comparados aos
grupos não infectados (dados não mostrados). Além disso, em um coração foi verificado a presença
de vasos obstruídos por hemácias e fibrina (trombos) (dados não mostrados). Os outros tecidos
infectados encontram-se preservados com focos de inflamação discretos, principalmente
mononuclear.
A quantificação do infiltrado inflamatório, realizado através da contagem de núcleos celulares
dos fragmentos de tecido cardíaco, demonstrou que o número de células inflamatórias no coração
dos animais deficientes em proteínas é igual ao dos animais que consumiam a dieta normoprotéica,
não havendo influência do período de restrição protéica ou tempo de infecção, fase aguda (figura
9A) ou fase crônica (figura 9B).
33
A
B
C
D
E
F
Figura 8: Análise histopatológica do coração. Cortes histológicos de coração de ratos Fisher corados com
hematoxilina e eosina. Animais que consumiam dieta normoprotéica (A) e hipoprotéica (B) não infectados. Tecido
muscular estriado cardíaco preservado apresentado cardiomiócitos (seta) longos, ramificados e anastomosados com
núcleo central vesiculoso e fracamente corado. Entre as redes de cardiomiócitos é possível observar vasos sanguíneos.
Ratos que consumiam dieta normoprotéica (C) hipoprotéica (D) infectados por 15 dias (fase aguda). Miocardite difusa
com presença de infiltrado inflamatório predominantemente mononuclear (seta). Presença de fibras cardíacas necróticas
(cabeça de seta). Ratos que consumiam dieta normoprotéica (E) e hipoprotéica (F) infectados por 120 dias (fase
34
crônica). Miocárdio com presença focal de discreto infiltrado inflamatório predominantemente mononuclear (seta);
350
A
*
B
*
2
Núcleos celulares / 74931 µ m
2
Núcleos celulares / 74931 µ m
aumento de 400X.
300
250
200
150
100
50
0
NP
HP
NP
Não infectado
HP
250
*
*
NP
HP
200
150
100
50
0
NP
Infectado pelo
T. cruzi (15 dias)
HP
Não infectado
Infectado pelo
T. cruzi (120 dias)
Figura 9: Análise morfométrica da celularidade do tecido cardíaco de ratos Fisher infectados com a cepa Y do
T.cruzi, com dieta hipoprotéica ou normoprotéica. O número de células inflamatórias foi avaliado através da
contagem de núcleos presentes no tecido cardíaco. As amostras foram obtidas na fase aguda (A) e fase Crônica da
infecção (B) e não houve diferença entre o grupo infectado que consumia dieta hipoprotéica em relação ao grupo
infectado que consumia dieta normoprotéica. Os dados acima estão apresentados como média+/- SEM e analisados por
One - way ANOVA (Tukey-Kramer HSD). * p<0,05 quando comparamos os animais submetidos à dieta normoprotéica
infectados com os animais não infectados submetidos à mesma dieta e animais submetidos à dieta hipoprotéica
infectados quando comparados aos animais não infectados submetidos à mesma dieta.
A
B
coração/peso corporal
(g)
Coração/peso corporal (g)
*
0.006
*
0.004
0.002
0.000
NP
HP
Não infectados
NP
HP
0.006
0.002
0.000
NP
Infectados pelo
T. cruzi (15 dias)
HP
Não infectados
35
*
*
0.004
NP
HP
Infectados pelo
T. cruzi (120 dias)
Figura 10: Medida do coração de ratos Fisher infectados com a cepa Y do T.cruzi realizada através da fração peso do
coração pelo peso corporal. As medidas foram feitas durante o sacrifício dos animais na fase aguda e na fase crônica da
infecção. Os corações tiveram um aumento significativo (p<0,01) nos animais submetidos à dieta hipoprotéica infectados
ou infectados pelo T. cruzi quando comparados aos animais submetidos à dieta normoprotéica infectado ou não
infectados pelo T. cruzi, durante a fase aguda (15 dias após a infecção) (A) ou fase crônica da infecção (120 dias após a
infecção) (B). Os dados acima estão apresentados como média+/- SEM e analisados por One - way ANOVA (TukeyKramer HSD).
A análise do tamanho do coração realizada durante o sacrifício dos animais demonstrou que, os
ratos que consumiam a dieta hipoprotéica, estando infectados ou não pelo T.cruzi, tiveram um
aumento significativo (p<0,05) do coração quando comparados ao grupo que consumia dieta
normoprotéica infectados ou não infectados durante as fases aguda (figura 10A) e crônica (figura
10B) da infecção.
4.5. Avaliação dos níveis cardíacos e séricos de Endotelina.
Na figura 11A, podemos observar que os níveis séricos de endotelina apresentaram-se
significativamente mais altos (p<0,001) nos animais deficientes em proteínas quando comparados
aos demais grupos. E ainda, os animais infectados e deficientes em proteínas mostraram níveis mais
elevados de endotelina quando comparado ao grupo apenas infectado (p<0,05). Após um longo
período de restrição protéica, a diferença entre os grupos com dieta hipoprotéica se extingue,
permanecendo apenas diferença entre os animais que consumiam dietas distintas. Podemos notar
também, que após um tempo maior de infecção, os níveis de endotelina entre os grupos com dietas
normoprotéica e hipoprotéica infectados são invertidos e a diferença entre os grupos com dieta
normoprotéica fica evidente (p<0,001) (figura 11B).
A dosagem de endotelina no sobrenadante cardíaco mostrou que os animais deficientes em
proteínas e infectados pelo T. cruzi apresentaram diferenças (p<0,001) nos níveis desta proteína
quando comparados com o grupo que consumia a mesma dieta ou dieta normoprotéica, infectados ou
não (figura 11C). Depois de um tempo mais prolongado com a dieta hipoprotéica, os níveis de
endotelina cardíaco dos animais não infectados elevaram-se consideravelmente tornando clara a
diferença entre este grupo e os demais. Além disso, é possível notar que dentre os animais
infectados, os que possuem a restrição protéica apresentaram níveis significativamente mais
elevados do que aqueles consumidores de dieta normoprtéica (figura 11D).
36
A
B
Endotelina sérica (pg/ml)
Endotelina sérica (pg/ml)
150
&*
200
150
*
100
&
50
&
100
*
50
0
0
NP
HP
NP
Não infectados
NP
HP
HP
NP
Não infectados
Infectados pelo T. cruzi
(15 dias)
HP
Infectados peloT. cruzi
(120 dias)
D
C
250
*&
200
150
100
*
&
50
0
NP
HP
Não infectados
NP
*
150
Endotelina/coração
(pg/ml)
Endotelina/coração
(pg/ml)
*
&
100
50
0
HP
NP
Infectados pelo T. cruzi
(15 dias)
HP
Não infectados
NP
HP
Infectados pelo T. cruzi
(120 dias)
Figura 11: Avaliação dos níveis séricos e cardíacos de endotelina. Dosagem de endotelina obtida do soro (A e B) e
sobrenadante do macerado cardíaco (C e D) de ratos Fisher infectados pela cepa Y do T.cruzi, através do teste de
ELISA. Os dados acima estão apresentados como média+/- SEM e analisados por One – way ANOVA (Tukey-Kramer
HSD). p<0,05; &: diferença entre os grupos submetidos à mesma dieta.
4.6. Avaliação dos níveis de CX3CL1 no soro e no tecido cardíaco.
A figura 12A mostra que os níveis séricos da CX3CL1 encontram-se significativamente mais
elevados (p<0,05) nos animais deficientes em proteínas e infectados pelo T.cruzi quando
comparados ao grupo de animais infectados submetidos à dieta normoprotéica, durante a fase aguda
37
da infecção (15 dias). Durante a fase crônica (120 dias de infecção) (Figura 12B) e um período mais
prolongado de restrição protéica, os níveis séricos de CX3CL1 tornam-se mais elevados entre os
animais submetidos à dieta hipoprotéica não infectados quando comparados aos outros grupos,
incluindo o grupo submetido à dieta hipoprotéica infectado.
A dosagem de CX3CL1 no sobrenadante cardíaco não mostrou diferença entre os grupos, seja
durante a fase aguda (Figura 12C) ou fase crônica (Figura 12D) da infecção.
B
A
*
75
CX3CL1 sérica (pg/ml)
CX3CL1 sérica (pg/ml)
75
50
25
0
NP
HP
Não infectados
NP
HP
* &
50
25
0
NP
Infectados com o T. cruzi
(15 dias)
C
20
CX3CL1/coração pg/ml
CX3CL1/coração pg/ml
16
12
8
4
HP
Não infectados
NP
HP
Infectados com o T. cruzi
(120 dias)
D
15
10
5
0
0
NP
HP
Não infectados
NP
NP
HP
HP
Não infetados
Infetados pelo T.cruzi
(15 dias)
NP
HP
Infetados pelo T.cruzi
(120 dias)
Figura 12: Avaliaçãos dos níveis de Fractalquina/CX3CL1 no soro e no tecido cardíaco. Os níveis séricos de
CX3CL1 dosados em ratos Fisher infectados pelo T.cruzi, mostraram aumento significativo entre os animais do grupo
submetido à dieta hipoprotéica em relação aos demais na fase aguda da infecção (A). Na fase crônica os níveis séricos
de CX3CL1 ficaram significativamente elevados no grupo submetidos à dieta hipoprotéica não infectados quando
comparado com os demais grupos. As dosagens de CX3CL1 medidas no tecido cardíaco não apresentaram diferenças
tanto na fase aguda (C) quanto na fase crônica (D) da infecção. Os dados acima estão apresentados como média+/- SEM
e analisados por One – way ANOVA (Tukey-Kramer HSD). p<0,05; &: diferença entre os grupos submetidos à mesma
dieta (p<0,01).
38
4.7. Análise imuno-histoquímica dos receptores da CX3CL1 (CX3CR1) e macrófagos no coração.
A expressão de receptores CX3CR1 em células do tecido cardíaco caracterizada pela técnica
de imunohistoquímica, é demonstrada através da marcação de cardiomiócito e células de defesa de
ratos Fisher infectados pela cepa Y do T. cruzi alimentados com dieta normoprotéica (Figura 13C) e
hipoprotéica (Figura 13D). Os tecidos cardíacos dos animais submetidos à dieta normoprotéica e
infectados ou submetidos a dieta hipoprotéica e infectados apresentam o mesmo perfil de expressão
dos receptores de CX3CL1 (CX3CR1), sendo diferentes apenas quando comparados aos animais não
infectados.
ED1 é um marcador específico para micróglia, macrófagos ativados. Através da técnica de
imunohitoquímica, sua marcação revela a presença de resposta inflamatória em rato. Na figura 14,
podemos observar a marcação de macrófagos recrutados (ED1) no tecido cardíaco de ratos Fisher
infectados pelo T.cruzi, alimentados com dieta normoprotéica (Figura 14C) e hipoprotéica (Figura
14D). E ainda, macrófagos ED2 (macrófagos residentes) podem ser observados no coração dos
animais que consumiam dieta normoprotéica (Figura 14E) e dieta hipoprotéica (Figura 14F)
infectados pelo T. cruzi na fase aguda da infecção (15 dias).
39
A
B
C
D
Figura 13: Análise Imuno-histoquímica dos receptores de CX3CL1 (CX3CR1) no tecido cardíaco. Figura
ilustrativa. Ratos Fisher alimentados com dieta NP (A) e HP (B) não infectados. Animais submetidos à dieta
normoprotéica (C) hipoprotéica (D) infectados pelo T. cruzi na fase aguda (15 dias após a infecção) (n=2). Coloração
marrom de cardiomiócitos expressando receptores da CX3CL1 (CX3CR1). Aumento de 400X.
40
A
B
C
D
E
F
Figura 14: Análise Imuno-histoquímica de macrófagos do coração. Figura ilustrativa. Corte histológico de coração
de ratos Fisher corados pela técnica de imunoperoxidase. Animais submetidos à dieta normoprotéica (A) e hipoprotéica
(B) não infetados. Determinação de macrófagos recrutados (ED1) (setas) em ratos Fisher infectados pela cepa Y do
T.cruzi na fase aguda (15 dias de infecção) alimentados com dieta normoprotéica (C) e hipoprotéica (D) (n=2) e
macrófagos residentes (ED2) (setas) em ratos Fisher infectados pela cepa Y do T.cruzi na fase aguda (15 dias de
infecção) alimentados com dieta normoprotéica(C) e hipoprotéica (D) (n=2). Aumento de 200X.
41
5.0. DISCUSSÃO
O modelo experimental de desnutrição protéica proposto nesse trabalho teve como finalidade
permitir o estudo da associação entre infecção pelo T. cruzi e sua relação com o estado nutricional do
hospedeiro. Uma vez que o modelo de desnutrição (dieta constituída de 6% de caseína, uma redução
de 60 % da proteína oferecida na dieta normoprotéica) já estava pré-estabelecido pelo Laboratório de
Nutrição Experimental da Escola de Nutrição, houve a necessidade de adaptá-lo a infecção. A
necessidade de um inóculo com elevada carga parasitária (420x103 tripomastigotas/70g de peso)
deveu-se a grande resistência do rato a infecção, no entanto, Carvalho et al (2006) afirmam,
baseados em dados provenientes de pacientes chagásicos, que o rato representa um bom modelo no
estudo da imunopatologia comparativa para a doença de Chagas. Além disso, estes animais são
capazes de desenvolver rapidamente a deficiência alimentar por possuir um metabolismo acelerado
permitindo que os estudos ocorram em um curto espaço de tempo e, ainda, apresentam ciclo
reprodutivo curto e são de fácil manuseio. Modelos animais têm sido amplamente utilizados na
caracterização da desnutrição, a fim de se entender as suas conseqüências no desenvolvimento e no
metabolismo do indivíduo (Portman, 1987; Tonkiss et al, 1993; Morgane et al, 1993; Manjarrez et
al, 1998).
O estudo da desnutrição protéica é um importante fator ou ferramenta no estudo de diversas
doenças infecciosas, sendo reconhecida como a maior causa de imunodeficiência, uma vez que sua
ocorrência encontra-se intimamente relacionada à ineficiência da atuação do sistema imune contra
agentes patogênicos e ser, ainda hoje, comum em áreas sócio-economicamente precárias e
endêmicas para diversas parasitoses (Chandra, 1991). A interação entre a desnutrição e a infecção
parece enfraquecer ainda mais a resposta imune levando à alteração nas populações de células de
defesa e aumentando ativação de mediadores inflamatórios (Dulger et al, 2002). Dentre tais
mediadores podemos citar as citocinas pró-inflamatórias, largamente associadas às etapas iniciais de
algumas doenças parasitárias (ex. infecção pelo protozoário T. cruzi), levando a uma intensificação
da resposta inflamatória sistêmica. Durante este processo de infecção versus desnutrição, alguns
nutrientes são perdidos e a soma do gasto energético do hospedeiro para montar a resposta imune,
associado à limitação nutricional da sua dieta, pode resultar na diminuição da absorção de nutrientes
pelo intestino (Nova et al, 2002; Reid et al, 2002; Johann-Liang et al, 2000, Keusch, 2003)
agravando ainda mais o quadro da desnutrição. Sendo assim, a associação da infecção pelo T. cruzi a
42
uma dieta deficiente em proteínas, gera danos aos tecidos, especialmente ao tecido cardíaco, através
da exacerbação da resposta inflamatória.
A deficiência protéica, bem como outras carências nutricionais, gera conseqüências negativas
ao sistema imune facilitando o estabelecimento de infecções, muitas vezes pela incapacidade de
eliminar o patógeno do organismo. Silva et al (1987), observaram que tanto camundongos
convencionais (CV) quanto germ free (CFW) alimentados com dieta hipoprotéica e infectados com a
cepa CL do T. cruzi apresentam parasitemia mais elevada que os animais saudáveis. Corroborando
com a literatura, nossos dados demonstram que a carga parasitária presente na circulação sangüínea
dos animais que foram alimentados com dieta hipoprotéica foi significativamente superior que a dos
animais alimentados com dieta normoprotéica. Poucos estudos têm elucidado especificamente o
efeito do estado nutricional no curso da infecção pelo T.cruzi (de Andrade & Zincker, 1995).
Entretanto, o papel do status nutricional na prevenção de doenças já foi foco em muitos estudos
(Blumberg, 1995; Harrige, 1996), assim como a extensão de suas conseqüências no desenvolvimento
de patologias. Portanto nossos dados mostram-se importantes na tentativa de reforçar essa
compreensão da doença de Chagas em associação a um déficit protéico alimentar podendo, dessa
forma, interferir positivamente ou negativamente na eficácia da resposta imune e conseqüentemente,
no curso da infecção.
A fim de avaliar a eficácia da dieta hipoprotéica utilizada no modelo proposto, alguns
parâmetros bioquímicos (proteínas totais, hemoglobina e albumina) foram analisados. A análise das
proteínas totais é importante na avaliação do estado nutricional e no diagnóstico e tratamento de uma
série de doenças e perturbações metabólicas e/ou nutricionais (Motta, 2003). Nossos dados
mostraram, como na literatura, que o consumo deficiente de proteínas altera os níveis séricos de
proteínas totais provocando sua redução significativa tanto no modelo animal (Figura 4) quanto no
humano (Waterlow & Alleyne, 1974, Kim et al, 1994; Oliveira et al, 2004). Os níveis sanguíneos de
hemoglobina mostraram-se significativamente reduzidos no grupo de animais submetidos à dieta
hipoprotéica não infectados pelo T. cruzi quando comparado aos demais grupos. Por meio de vias
ainda não definidas, nossos dados mostraram que a infecção pelo T. cruzi em concomitância com a
dieta hipoprotéica parece ser capaz de estabilizar os níveis de hemoglobina no sangue destes animais
tanto na fase aguda (Figura 6A) quanto na fase crônica (Figura 6B).
Além de proteínas totais e hemoglobina, a albumina pode ser considerada um importante
marcador bioquímico na avaliação do estado nutricional e indicador prognóstico de várias doenças
43
(Cabral, et al, 2001). De acordo com o estudo de Oliveira & Angelis (2001), ratos Swiss submetidos
à dieta hipoprotéica (3% de caseína) tiveram uma redução significativa nos níveis de albumina
quando comparados aos animais submetidos à dieta normoprotéica. Estes dados corroboram com
nossos achados onde o consumo de dieta hipoprotéica também propiciou uma diminuição (p<0,05)
nos níveis de albumina (Figura 5).
Deste modo, a alimentação deficiente em proteínas, induziu nos animais (ratos) significativa
diferença no ganho de peso quando comparados com os animais alimentados com a dieta
normoprotéica (Figura 3). Segundo, Dubowitz (1965), Lhemelandu (1985) & Oliveira et al (1999), a
grande perda de massa muscular é ocasionada pela depleção de proteínas do tecido muscular
esquelético, rico reservatório protéico (Alves et al, 2008), decorrente da deficiência protéica. Além
disso, Vituri et al (2008) mostraram que animais alimentados com dieta hipoprotéica apresentaram
uma redução no consumo destas dietas, podendo favorecer a redução ou deficiência no ganho de
massa corpórea dos animais. E ainda, Cunha et al (2002) mostraram que corações de pacientes com
desnutrição crônica apresentaram o peso do coração pelo peso corporal significativamente (p< 0,05)
maior do que os indivíduos saudáveis. Este fenômeno pode ser interpretado como uma estratégia do
coração para manter sua preservação relativa em conseqüência à intensa perda de peso corporal. Em
concordância com os dados destes autores, nossas análises mostraram que em decorrência da
restrição protéica o grupo de animais alimentados com dieta hioprotéica apresentou peso do coração
proporcionalmente maior em relação ao peso do corpo, quando comparado ao grupo dos animais de
dieta normoprotéica tanto na fase aguda da infecção (Figura 10A) quanto na fase crônica (Figura
10B). Uma vez estabelecida a eficácia do modelo empregado de deficiência protéica, o próximo
passo foi avaliar sua interferência no mecanismo inflamatório dos animais, principalmente
envolvendo a participação de uma quimiocina em particular: a CX3CL1.
Em modelos animais de infecção pelo T. cruzi, foi descrita a participação de algumas
quimiocinas como a CCL2/MCP-1, a CCL3/MIP-1alfa, a CCL5/RANTES, a CXCL9/MIG e a
CXCL10/IP-10 em lesões cardíacas de camundongos em fase crônica da doença (Teixeira et al,
2002). Estas quimiocinas, expressas no miocárdio de camundongos infectados pelo T. cruzi, podem
contribuir para o intenso infiltrado inflamatório através do recrutamento de células T CD8+ e CD4+
e, portanto, para o estabelecimento e manutenção da miocardite (Machado et al, 2005). Foi
observado ainda que animais deficientes do receptor CCR5 apresentaram elevada redução do
infiltrado celular no coração, indicando a importância destes receptores na migração de linfócitos e
44
controle da replicação local do parasito (Machado et al, 2005). Por outro lado, apesar de inúmeros
relatos sobre a participação de uma quimiocinas denominada CX3CL1 em diversos processos
inflamatórios (Harrison, et al, 1998; Chakravorty et al, 2002), nenhuma inferência até o momento
havia sido feita para o processo inflamatório cardíaco associado à doença de Chagas. Sabe-se que
sua expressão é ativada pela presença de citocinas pró-inflamatórias como, IL-1, IFN-γ, TNF-α ou
ainda pela presença de LPS (Bazan et al, 1997; Pan et al, 1997). Através de seu único receptor,
CX3CR1, expresso em cardiomiócitos (Figura 14) ou em outras células inflamatórias como
monócitos/macrófagos ED1 (Figura 14 C e D) e ED2 (Figura 14 E e F), células NK, células
endoteliais e algumas células T (Imai et al, 1997), essa quimiocina representa um novo tipo de
molécula capaz de participar do tráfego leucocitário, além de exercer funções na adesão e
quimioatração de células circulantes para o sítio inflamatório (Al-Aoukaty et al, 1998). E nesse
sentido, alguns estudos demonstraram que a persistência do processo inflamatório e da ativação do
sistema imune podem favorecer o desenvolvimento da falência cardíaca (Mann, 2005; Aukrust et al,
2004).
Em um estudo desenvolvido por Melo & Machado (2001) sobre a contribuição dos fagócitos
mononucleares para resistência de ratos infectados com a cepa Y do T. cruzi, esse demonstrou que
durante a infecção aguda há significativa ativação de monócitos do sangue periférico. Além disso,
foi demonstrado, por análise do processo inflamatório cardíaco, um elevado parasitismo
acompanhado de processo inflamatório mononuclear intenso e difuso com grande número de
macrófagos ativados. Os dados destes autores mostraram então, que a fase inicial da infecção pelo T.
cruzi induz uma rápida produção, maturação e ativação dos monócitos/macrófagos do sistema imune
a fim de controlar a replicação do T. cruzi, enfatizando o papel fundamental dessas células para a
resistência do modelo murino (ratos) durante a doença de Chagas. Estes resultados corroboram com
nossos achados, onde todos os animais infectados apresentaram o mesmo perfil inflamatório sem
distinção para o tipo de dieta recebida (Figuras 8 e 9). Da mesma forma que não houve diferença na
análise qualitativa do infiltrado de macrófagos (Figura 14).
É sabido também, que a doença de Chagas provoca uma série de anormalidade das funções
cardíacas, podendo haver uma estreita relação entre estas alterações cardíacas com o aumento nos
níveis séricos de CX3CL1 visto em nossos resultados (Figura 12A). E ainda, estudos
epidemiológicos relataram a associação do estado nutricional, em fases iniciais da vida, ao
desenvolvimento de doenças cardiovasculares na vida adulta (Sawaya et al, 1995; Sawaya et al,
45
2003; Sawaya & Roberts, 2003). Tropia et al (2001) demonstraram os efeitos deletérios da
desnutrição protéica (6% de proteína), após o período de amamentação, sobre o sistema
cardiovascular, como o aumento do tônus vasomotor simpático dos animais. Ainda, animais
submetidos à dieta hipoprotéica apresentam níveis basais de freqüência cardíaca elevados, bem
como da pressão arterial (Oliveira et al, 2004), além de demonstrarem perturbação na homeostase
desse órgão (Loss et al, 2007). Desse modo, os níveis séricos elevados de CX3CL1, parecem estar
relacionados a algum tipo de desequilíbrio funcional do sistema cardiovascular uma vez que tanto a
dieta hipoprotéica quanto a infecção pelo T. cruzi favorecem as alterações cardíacas. No entanto, a
desnutrição protéica parece ser um fator determinante e acelerador, já que os animais apenas
infectados pelo T. cruzi não apresentaram aumento ou alteração nos níveis de CX3CL1.
Até o momento a quimiciocina CX3CL1 tem sido associada principalmente a doenças
cardiovasculares (Husberg et al, 2008). Na doença de Chagas, era esperado que tal quimiocina
pudesse exercer um papel definidor de patologia, uma vez que parte das lesões ocorre no endotélio,
local de sua ampla expressão, e ao longo do tecido cardíaco. Por outro lado, a análise dos receptores
de CX3CL1 (CX3CR1) no tecido cardíaco mostrou que estes eram igualmente expressos tanto nos
animais infectados com dieta hipoprotéica quanto naqueles com dieta normoprotéica (Figura 13).
Damås et al (2005) demonstraram que o tratamento com fármacos do grupo das estatinas reduz a
expressão de mediadores inflamatórios, bem como da resposta inflamatória mediadas por células
mononucleares do sangue periférico ativadas por CX3CL1. A proposta desse grupo é que o sistema
CX3CL1/CX3CR1 possa constituir, num futuro próximo, um alvo na terapêutica para as doenças
cardíacas. Como, ainda, na literatura não existem estudos relacionando a participação desta
quimiocina na progressão da doença de Chagas, nossos dados, ainda em modelo experimental,
abrem caminhos para maiores investigações em outros modelos empregando a CX3CL1 no processo
de imunopatogênese/prognóstico clínico para a doença.
Um outro mediador inflamatório que apresenta um papel na biologia vascular semelhante ao da
CX3CL1 é a endotelina. A endotelina participa do remodelamento cardíaco e dos processos
inflamatórios de doenças crônicas (Mulder et al, 1997; Kedzierski et al, 2001; Guarda et al, 1993).
Além disso, recentes evidências demonstraram que endotelina-1 exerce um importante papel na
progressão da patogênese da cardiopatia chagásica (Mulder et al, 1997; Kedzierski et al, 2001;
Guarda et al, 1993). Durante a infecção aguda pelo T.cruzi níveis séricos elevados de endotelina-1,
bem como de sua expressão no endotélio vascular e endocárdico, são observados. Nosso estudo
46
mostrou que durante a fase aguda da infecção pelo T. cruzi, também em ratos, os níveis séricos de
endotelina apresentaram-se elevados no grupo de animais alimentados com dieta normoprotéica
quando comparados aos animais não infectados que consumiam a mesma dieta. É possível observar
que após um período mais longo de infecção (120 dias) os níveis séricos de endotelina entre estes
dois grupos se exacerbam. No entanto, independente da fase da doença avaliada (aguda ou crônica),
tanto os níveis séricos quanto os níveis cardíacos de endotelina sofreram influência direta da dieta
hipoprotéica.
De forma geral, a deficiência protéica é capaz de alterar a homeostase vascular e cardíaca e
promover a liberação de mediadores inflamatórios (Oliveira et al, 2004; Loss et al, 2007) Da
mesma forma, a infecção pelo T. cruzi também é capaz de desencadear, por si só, uma resposta
inflamatória dependente de moléculas antigênicas do parasito que alteraria a hemodinâmica vascular,
autonômica, elétrica e funcional do órgão cardíaco (Kaysen, 2001; Rocha et al, 2007). Tendo em
foco a realidade de regiões específicas da América latina onde a infecção pelo T. cruzi e o precário
quadro nutricional coexistem, a hipótese que moveu esse estudo experimental nos direcionou para a
interferência nutricional sob a resposta inflamatória, em especial, sob a síntese de CX3CL1 e
endotelina. Estes mediadores sofreram interferências da infecção pelo T. cruzi e da dieta deficiente
em proteínas, levando a crer que tal coexistência poderia contribuir para a progressão da cardiopatia
chagásica ou outros danos vasculares associados a essa doença. Esse estudo, inédito pela
apresentação da CX3CL1 na infecção pelo T. cruzi, abrirá perspectivas para novos estudos
envolvendo essa quimiocina na doença de Chagas seja de forma isolada, seja em concomitância com
estratégias nutricionais e/ou terapêuticas.
47
6.0. CONCLUSÃO
O presente estudo envolvendo o modelo murino (rato) no estudo da dieta hipoprotéica
interferindo na síntese de CX3CL1 e endotelina durante as fases aguda e crônica da doença de
Chagas permitiu concluir que:
•
O modelo proposto de desnutrição foi adequado por permitir a sobrevida dos animais infectados
até a fase crônica da doença (120 dias);
•
As dietas hipoprotéica e normoprotéica, per si, não alteraram o padrão de lesão tecidual nos
animais infectados pelo T. cruzi;
•
Os níveis de CX3CL1 e endotelina foram afetados (elevados tanto no soro quanto no tecido
cardíaco) em função do tempo de infecção e da restrição protéica;
•
Os níveis de CX3CL1 e endotelina, bem como a qualidade da dieta não alteraram o padrão de
lesão tecidual cardíaco nos animais infectados pelo T. cruzi;
•
Os receptores da CX3CL1 (CX3CR1) mostraram-se mais expressivos nos animais infectados
pelo T. cruzi, no entanto não foi observado interferência da desnutrição protéica nesse padrão de
receptores, durante a fase aguda da infecção;
•
O infiltrado de macrófagos (residentes ou recrutados) mostrou-se mais expressivos nos animais
infectados pelo T. cruzi, no entanto não foi observado interferência da desnutrição protéica nesse
padrão, durante a fase aguda da infecção;
•
A dieta hipoprotéica, bem como a presença do T. cruzi, foram capazes de interferir positivamente
na síntese de mediadores inflamatórios CX3CL1 e endotelina, mas sem exercer interferência no
padrão inflamatório tecidual observado em modelo experimental (rato) da doença de Chagas.
48
•
A dieta hipoprotéica foi capaz de interferir na carga parasitária dos animais, mostrando que a
restrição alimentar de proteínas favorece o pico elevado de parasitemia.
•
A restrição protéica interferiu diretamente no peso do coração, favorecendo um aumento
proporcional deste em decorrência da deficiência protéica.
49
7.0. REFERÊNCIAS BIBLIOGRÁFICAS
ACC/SCN (2000). Nutrition throughout life. 4th Report on the world nutrition situation. Geneva;
ACC/SCN./World Health Organization.
Adad SJ et al (1991). Contribuição ao estudo da anatomia patológica do megaesôfago chagásico.
Rev. Inst. Med.Trop.; 33: 443-450.
Al-Aoukaty A et al (1998). MIP-3α, MIP-3β and fractalkine induce the locomotion and the
mobilization of intracellular calcium, and activate the heterotrimeric G proteins in human natural
killer cells. Immunology; 95: 618-24
Alibert JC et al (1999). β-chemikines enhance parasites uptake and promotes nitric oxide -dependent
microbiostatic activity in murine inflammatory macrophages infected with T. cruzi. Infct.Immun.;
67: 4819-4826.
Alves AP et al (2008). Efeito da desnutrição protéica pré e pós natal sobre a morfologia, a
diferenciação e o metabolismo do tecido muscular estriado esquelético m ratos. J Pediatr.; 84(3): 264
-271.
Arantes JM et al (2007). Trypanosoma cruzi: Treatment with the iron chelator desferrioxamine
reduces parasitemia and mortality in experimentally infected mice. Experimental Parasitology;
117:43–50.
Arnaiz, MR et al (2002). Cardiacmyocyte hypertrophy and proliferating cell nuclear antigen
expression in Wistar rats infected with Trypanosoma cruzi. J. Parasitol.; 88: 919–925.
Aufderheide AC et al (2004). Proc Natl Acad Sci U S A. 17; 101(7):2034-9.
Aukrust P et al (2004). Therapeutic potential of anticytokine therapy in congestive heart failure. Am
J Cardiovasc Drugs; 4: 169–77.
Bacon KB et al (1998). Chemokines in disease models and pathogenesis. Cytokine Growth Factor
Rev.; 9: 167-173.
Barbé E et al (1990). Characterization and expression of the antigen present on resident rat
macrophages recognized by monoclonal antibody ED2. Immunobiology; 182: 88–99.
Barcinski MA & DosReis GA (1999). Apoptosis in parasites and parasite-induced apoptosis in the
host immune system: a new approach to parasitic diseases. Braz. J. Med. Biol. Res.; 32: 395–401.
Bazan JF et al (1997). A new class of membrane-bound chemokine with a CX3C motif. Nature; 385:
640–4.
50
Borelli P et al (1998). Protein Malnutrition: Some Aspects of the in vitro adhesion of peritoneal
mouse macrophages. Ann Nutr Metab.; 42(6): 367-73.
Brazão V et al (2008). Zinc supplementation increases resistance to experimental infection by
Trypanosoma cruzi. Veterinary Parasitology; 154: 32–37
Brener Z et al (1962). Observations on immunity to superinfections in mice experimentally
inoculated with Trypanosoma cruzi and subjected to treatment. Rev Inst Med Trop. São Paulo;
4:119-23.
Brener Z et al (1989). A descoberta (Homenagem aos 80 anos da descoberta da Doença de Chagas).
Memórias do Instituto Oswaldo Cruz, Rio de Janeiro; 84:1-6.
Blumberg JB (1995). Considerations on the scientific substantiation for antioxidant vitamins and βcarotene in disease prevention. Am J Clin Nutr.; 62 : 1521S-1526S.
Cabral VL et al (2001). Importância da albumina sérica na avaliação nutricional e de atividade
inflamatória em pacientes com doença de Crohn+. Arq Gastroenterol; 38 (2): 104-108.
Camargos ER et al (2000). Infection with different Trypanosoma cruzi populations in rats:
myocarditis,cardiac sympathetic denervation and involvement of digestive organs. Am. J. Trop.
Med. Hyg.; 62(5): 604–612
Camargos ER et al (2004). Protective role of ETA endothelin receptors during the acute phase of
Trypanosoma cruzi infection in rats. Microbes Infect; 6: 650–656.
Carvalho LS et al (2006). Vitamin E deficiency enhances pathology in acute Trypanosoma cruziinfected rats. Soc Trop Med Hyg.; 100(11): 1025-31.
Caufield LE et al (2004). Under nutrition as an underlying cause of child deaths associated with
diarrhea, pneumonia, malaria and measles. Am J. Clin Nutr; 80: 193-8.
Chakravorty SJ et al (2002). Fractalkine expression on human renal tubular epithelial cells: potential
role in mononuclear cell adhesion. Clin Exp Immunol; 129: 150-9.
Chandra RK et al (1991). Nutrition and immunity:Lessons from the past and new insights into
future. Am J Clin Nutr; 53: 1087-1101.
the
Chandra RK (1997). Nutrition and the immune system: an introduction. Am J Clin Nutr.; 66(2): 4603.
Chandra RK (2002). Nutrition and the immune system from birth to old age. Eur J Clin Nutr.; 56(3):
S73-6.
Coura JR & Dias JC (2009). Epidemiology control and surveillance of Chagas disease: 100 years
after its discovery. Mem. Inst. Oswaldo Cruz; 1: 31-40.
51
Cunha DF et al (2002). Heart weight and heart weight/body weight coefficient in malnourished
adults. Arq. Bras. Cardiol.; 78(4): 382-7.
Cunha-Neto E et al (2005). Cardiac gene expression profiling provides evidence for cytokinopathy
as a molecular mechanism in Chagas disease cardiomyopathy. Am J Pathol.; 167:305 - 313.
Cunningham-Rundles et al (2005). Mechanisms of nutrient modulation of the immune response. J.
Allergy Clin Immunol.; 115: 1119-28.
Damås JK et al (2005). Expression of fractalkine (CX3CL1) and its receptor, CX3CR1, is
elevated in coronary artery disease and is reduced during statin therapy. Arterioscler Thromb Vasc
Biol.; 25: 2567–2572.
Da Silva AB et al (2007). Megacolon in Chagas disease : a study of inflammatory cells , enteric
nerves, and glial cells. Hum Pathol.; 38: 1256-1264.
Davenport AP & Maguire JJ (2006). Endothelin. Handb Exp Pharmacol.; 176: 295-329.
de Andrade AL et al (1995). Chronic malnutrition and Trypanosoma cruzi infection in childreJ Trop
Pediatr.; 41(2):112-5.
De Souza W (2002). Basic cell biology of Trypanosoma cruzi. Curr Pharm Des.; 8(4): 269-85.
Dijkstra CO et al (1985). The heterogeneity of mononuclear cells in lymphoid organs: distinct
macrophage subpopulations in the rat recognized by monoclonal antibodies ED1, ED2 and ED3.
Immunology; 54: 589–599.
Dubowitz, V (1965). Enzyme histochemistry of skeletal muscle. J Neurol Neurosurg
Psychiatry; 28: 516-24
Dulger H et al (2002). Pro-inflammatory cytokines in Turkish children with protein-energy
malnutrition. Mediators Inflamm.; 11: 363-5.
Dutra WO et al (1997). Citokine mRNA profile of peripheral blood mononuclear cells isolated from
individuals with trypanosoma cruzi chronic infection. Scand J Immunol.; 45: 74-80.
Emery PW (2005). Metabolic changes in malnutrition. Eye; 19: 1029-34.
Engman D & Leon J (2002). Pathogenesis of Chaga’s heart disease: role of autoimmunity. Acta
Trop.; 81: 123-132.
Fong AM et al (1998). Fractalkine and CX3CR1 mediate a novel mechanism of leukocyte capture,
firm adhesion, and activation under physiologic flow. J Exp Med.; 188: 1413–9.
52
Forbes WB et al (1978). Effect of chronic protein malnutrition on experimentally induced seizures in
the rat. Exp. Neurol.; 62: 475-481.
Galkina E & Ley K (2007). Leukocyte influx in atherosclerosis. Curr Drug Targets; 8: 1239-1248.
Gea S et al (1993). Chaga’s disease cardioneuropathy: association of anti-Trypanosoma cruzi and
anti-sciatic nerve antibodies. Am. J. Trop. Med. Hyg.; 49: 581–58.
Gerard C & Rollins BJ (2001). Chemokine and disease. Nat Immunol; 2: 108–115.
Giannessi D et al (2001). The role of endothelins and their receptors in heart failure. Pharmacol
Res.; 43: 111-126.
Gomes JA et al (2003). Evidence that development of severe cardiomyopathy in human Chagas’s
disease is due to a Th1-specific immune response. Infect. Immun.; 71: 1185-93.
Gomes NG et al (1994). Effects of severe protein restriction in levels of parasitemia and in mortality
of mice acutely infected with Trypanosoma cruzi. Rev Soc Bras Med Trop.; 27(1):19-24.
Guarda E et al (1993). Effects of endothelin on collagen turnover in cardiac fibroblasts Cardiovasc.
Res.; 27: 213–2134.
Guhl F et al (1999). Isolation of Trypanosoma cruzi DNA in 4,000-year-old mummified human
tissue from northern Chile. Am J Phys Anthropol. 108(4):401-7.
Harrison JK, Jiang Y, Chen S,
Harrige LS (1996). Nutrition and immunity with emphasis on infection and autoimmune disease.
Nutr Health; 10: 285–312.
Harrison JK et al (1998). Role for neuronally derived fractalkine in mediating interactions between
neurons and CX3CR1-expressing microglia. Proc Natl Acad Sci USA; 95: 10896-901.
Hoff R et al (1978). Trypanosoma cruzi in cerebrospinal fluid during the acute state of Chagas
disease. N. Engl. J. Med.; 298 (11): 604-606
Holscher C et al (2000). Tumor necrosis factor alpha-mediated toxic shock in Trypanosoma cruziinfected interleukin 10-deficient mice. Infect. Immun.; 68: 4075–4083.
Hughes S & Kelly P (2006). Interactions of malnutrition and immune impairment, with specific
reference to immunity against parasites. Parasite Immunol.; 28: 577-88
Husberg C et al (2008). Cytokine expression profling of the myocardium reveals a role for CX3CL1
(fractalkine) in heart failure. J Mol Cell Cardiol.; 45: 261–269.
Imai T et al (1997). Identification and molecular characterization of fractalkine receptor CX3CR1,
which mediates both leukocyte migration and adhesion. Cell; 91: 521-30.
53
Itoh M et al (1995). Phenotypic heterogeneity of testicular macrophages/dendritic cells in normal
adult mice: an immunohistochemical study. J Reprod Immunol.; 28: 217–232
Johann-Liang R et al (2000). Energy balance, viral burden, insulin-like growth factor-1, interleukin6 and growth impairment in children infected with human immunodeficiency virus. Aids; 14: 68390.
Katona P & Katona-Apte J (2008). The interation between nutrition and infection. Clin Infect Dis.;
46: 1582-1588.
Kaysen GA et al (2001). Inflammation and dietary protein intake exert compeling effects on
serum albumin and creatinine in hemodialysis patients. Kidney Int.; 60: 333.
Kedzierski RM & Yanagisawa M (2001). Endothelin system: the double-edged sword in health and
disease. Annu. Rev. Pharmacol. Toxicol.; 41: 851–876.
Keusch GT (2003). The history of nutrition: malnutrition, infection and immunity. J Nutr.; 133:
336S-40S.
Kim SW et al (1994) Dietary restriction modulates the norepinephrine content and uptake of the
heart and cardiac synaptosomes. Proc. Soc. Exp. Biol. Med.; 207: 43-47.
Kim CH (2004). Chemokine-chemokine receptor network in immune cell trafficking. Curr Drug
Targets Immune Endocr Metabol Disord.; 4: 343-361.
Köeberle F (1968). Chagas disease and Chagas syndromes: the pathology of American
trypanosomiasis. Adv Parasitol.; 6: 63-116.
Krettli AU & Lima Pereira FE (1981): Immunosupresion im Protozoan infection, Biochemistry and
Physiology of protozoan. In: Levandoviski M & Hutner SH (Org).2ed (New York Academic Press)
4: 431-461.
Leon JS & Engman DM (2001). Autoimmunity in Chagas heart disease. Intern. J. Parasitol.; 31,
555–56.
Ley V et al (1990). The exit of Trypanosoma cruzi from the phagosome is inhibited by raising the
pH of acidic compartments. J Exp Med.; 168: 649-659.
Lhemelandu EC (1985). Fibre number and sizes of mouse soleus muscle in early postnatal protein
malnutrition. Acta Anat (Basel); 121: 89-93.
Little PJ et al (2008). Endothelin-1 actions on vascular smooth muscle cell functions as a target for
the prevention of atherosclerosis. Curr Vasc Pharmacol.; 6: 195-203.
Liu P et al (2006). CX3CR1 Deficiency Confers Protection From Intimal Hyperplasia After Arterial
Injury. Arterioscler. Thromb. Vasc. Biol.; 26: 2056-2062.
54
Loss IO et al (2007) Barorreflex dysfunction in rats submitted to protein restriction. Life Sci.; 81:
944-950.
Macedo MM et al (2004). Trypanosoma cruzi: Genetic Structure of Population and Relevance of
Genetic Variability to the Pathogenesis of Chagas. Mem Inst Osvaldo Cruz; 99: 1-12.
Machado CR & Camargos ER (2008). Endothelins role in the control of the acute phase of
Trypanosoma cruzi infection.Mini Rev Med Chem.; 8(8):820-7.
Manjarrez G et al (1998). Free tryptophan as an indicator of brain serotonin synthesis in infants.
Pediatr Neurol 18(1): 57–62.
Mann DL (2005). Targeted anticytokine therapy and the failing heart. Am J Cardiol.; 95: 9C-16C.
Mantovani A et al (2004). The chemokine system in diverse forms of macrophages activations and
polarization. Trends Immunol; 25: 677-686.
Mariano FS et al (2008). The involvement of CD4+CD25+ T cells in the acute phase of
Trypanosoma cruzi infection. Microbes Infect.; 10(7): 825-33.
McComb JG et al (2008). CX3CL1 up-regulation is associatied with recruitment of CX3CR1
mononuclear phagocytes and T lymphocytes in the lungs during cigarette smoke-induced
emphysema. Am J Pathol.; 173: 949-961.
Melo RC et al (2006). Lipid bodies: Structural markers of inflammatory macrophages in innate
immunity.Inflamm Res.; 55(8):342-8.
Melo RC & Machado CR (2001). Trypanosoma cruzi: peripheral blood monocytes and heart
macrophages in the resistance to acute experimental infection in rats. Exp Parasitol.; 97(1):15-23.
Melo RC et al (2003). Production of hydrogen peroxide by peripheral blood monocytes and specific
macrophages during experimental infection with Trypanosoma cruzi in vivo. Cell Biol Int.; 27(10):
853-61.
Ministério da Saúde (1996). Metas governamentais para o ano 2000. Brasília: Ministério da Saúde.
Morgan G (1997). What if any is the effect of malnutrition on immunological competence? Lancet.;
349(9066): 1693-5.
Morgane PJ et al (1993). Prenatal malnutrition and development of the brain. Neurosci Biobehav
Rev.; 17: 91–128.
Moser B & Loetscher P (2001). Lymphocyte traffic control by chemokines. Nat Immunol.; 2: 123–
128.
55
Motta V (2003). Bioquímica clínica para o laboratório: princípios e interpretações – 4ªed. Porto
Alegre: Editora Médica Missau.
Mulder P et al (1997). Role of endogenous endothelin in chronic heart: effect of long-term treatment
with an endothelin antagonist on survival, hemodynamics, and cardiac remodeling. Circulation;
96(6):1976
Mukherjee S et al (2003). Role of vasoactive mediators in the pathogenesis of Chagas’ disease.
Front. Biosci; 8: E410–E419.
Nova E et al (2002). The adaptive response of the immune system to the particular malnutrition of
eating disorders. Eur J Clin Nutr; 56 (3): S34-S37.
Oliveira FL et al (1999). Desnutrição energética intra-uterina em ratos: alteração músculoesquelética na 1ª e 2ª gerações. J Pediatr.; 75:350-356.
Oliveira MV& Angelis RC (2001). Requisitos protéicos mínimos de diferentes fontes vegetais para r
atos de laboratório em fase de crescimento. Braz J Vet Res Anim Sci.; 38(1):23-28.
Oliveira et al (2004). Arterial pressure, heart rate and blood pressure variability in malnourished rats.
XXI Congress of the Latin American Association of Physiological Sciences; 1: 106.
Palacius-Pru E et al (1989). Ultrastructural characteristics of different stages of human chagasic
myocarditis. Am J Trop Med Hyg.; 41: 29-40.
Pan Y et al (1997). Neurotactin, a membrane-anchored chemokine upregulated in brain
inflammation. Nature; 387: 611–617.
Petkova SB et al (2000). Myocardial expression of endothelin-1 in murine Trypanosoma cruzi
infection. Cardiovasc. Pathol.; 9: 257–265
Petkova SB et al (2001). The role of endothelin in the pathogenesis of Chagas’ disease. Int. J.
Parasitol.; 31: 499–511.
Portman OW (1987). Effects of maternal and long-term postnatal protein malnutrition on brain size
and composition in rhesus monkeys. J Nutr.; 117(11): 1844–1851.
Prata A (2001). Clinical and epidemiological aspects of Chagas disease. Lancet Infect. Dis.; 1: 92–
100
Prata A et al (1986). Características da morte súbita tida como não esperada na doença de Chagas.
Rev Soc Bras Med Trop.; 19: 9-12.
Rae GA & Henriques MG (1998). Endothelins in inflammation. In Proinflammatory and
Antiinflammatory Peptides (Said, S.I, ed.); 163–202.
56
Ranade SC et al (2008). Different types of nutritional deficiencies affect different domains of spatial
memory function checked in a radial arm maze. Neuroscience; 152: 859-866.
Reeves PG et al (1993). Purified diets for laboratory rodents: final report of the American Institute
of Nutrition, Ad Hoc. Writing Committee on the Reformulation of the AIN-76, a rodent diet. J.
Nutr., Bethesda; 123:1939-1951.
Reid M et al (2002). The acute-phase protein response to infection in edematous and nonedematous
protein-energy malnutrition. Am J Clin Nutr.; 76(6):1409-1415.
Reina -San-Martin B et al (2002). Lymphocyte polyclonal activation: a pitfall for vaccine design
against infectious agents. Parasitol Today; 16: 62-67.
Rivera MT et al (2002). Progressive Chaga’s cardiomyopathy is associated with low selenium
levels. Am. J. Trop. Med. Hyg.; 66(6): 706–712
Rocha MO et al (2007). An update on the management of Chagas cardiomyopathy. Expert Rev. Anti
Infect.; 5(4): 727-743.
Ryu J et al (2008). Activation of fractalkine/CX3CR1 by vascular endothelial cells induces
angiogenesis through VEGF-A/KDR and reverses hindlimb ischaemia. Cardiovasc Res.; 78(2): 33340.
Savino W (2002). The thymus gland is a target in malnutrition. Eur. J. Clin Nutr.; 56 (3): S46-S49.
Sawaya AL et al (1995). Obesity and malnutrition in a Shantytown population in the city of Sao
Paulo, Brazil. Obes. Res.; 3 Suppl 2: 107s-115s.
Sawaya AL et al (2003). The link between childhood undernutrition and risk of chronic diseases in
adulthood: a case study of Brazil. Nutr. Rev.; 61: 168-175.
Sawaya AL & Roberts S (2003). Stunting and future risk of obesity: principal physiological
mechanisms. Cad.Saúde Pública; 19 (1): S21-S28
Sharma JB et al (2003). Effect of dietary habits on prevalence of anemia in pregnant women of
Delhi. J Obstet Gynaecol Res.; 29 (2): 73-78
Schober A (2008). Chemokines in vascular dysfunction and remodeling. Arterioscler Thromb Vasc
Biol.; 28: 1950-1959.
Schofield C & Asworth A (1996). Why have mortality rates for severe malnutrition remained so
high? Bull World Health Org.; 74: 223-9.
Silva ME et al (1987). American trypanosomiasis (Chagas’ disease) in conventional and germfree
rats and mice. Rev Inst Med Trop.; 29: 284–88.
57
Souza AP et al (2003). Selenium supplementation at low doses contributes to the decrease in heart
damage in experimental Trypanosoma cruzi infection. Parasitol Res.; 91: 51–54
Souza PE et al (2004) . Monocytes from patients with indeterminate and cardiac form of Chagas
disease display distinct phenotypic and functional characteristics associated with morbidity. Infect
Immun.; 72: 5283-5291.
Talvani A et al (2000). Kinetic of cytokine gene expression in experimental chagasic
cardiomyopathy tissue parasitism and endogenous IFN-g as important determinants of chemokine
mRNA expression during infection with Trypanosoma cruzi. Microbes and infection; 2: 851-866.
Talvani A et al (2004). Elevated concentrations of CCL2 and TNF-α in chagasic cardiomyopathy.
Clin Infect Dis.; 38: 943-50.
Tanowitz HB et al (2003). Recent developments in the pathology of Chagas disease with emphasis
on the cardiovascular system; 82–96.
Teixeira MM et al (2002). Chemokines, inflammations and Trypanosoma cruzi infection. Trends in
Parasitology; 18 (6): 262-265.
Tonkiss J et al (1993). Prenatal protein malnutrition and postnatal brain function. Ann N Y Acad
Sc.; 678: 215–227.
Tropia et al (2001). Effects of low-protein diet on the baroreflex and Belzold-Jarisch reflex in
conscious rats. Nutr Neurosci.; 4: 99-107.
Vituri CL et al (2008). Capacidade da matriz extracelular da medula óssea de induzir a proliferação
de células mielóides in vitro no modelo de desnutrição protéica em camundongos. Braz J Pharma
Sci.; 44 (3): 493-500
Waterlow JC (1997). Protein-energy malnutrition: the nature and extent of the problem. Clin Nutr.;
16 (1): 3-9.
WHO - World Health Organization (2007). Global database on child growth and malnutrition.
Disponível em: http://www.who.int/nutgrowthdh. Acessado em maio de 2009
World Health organization. Expert Committee (2002). Control of Chagas disease. World Health
Organ Tech Rep 905:109.
Yaeger RG & Miller ON (1960). Effect of malnutrition on susceptibility of rats to Trypanosoma
cruzi Pyridoxine deficiency. Exp. Parasitol.; 10: 238-44.
Yaeger RG & Miller O (1963). Effect of malnutrition on susceptibility of rats to Trypanosoma cruzi
vitamin A deficiency. Exp Parasitol.; 14: 9-14.
Zlotnik A & Yoshie O (2000). Chemokines: a new classification system and their role in immunity.
Immunity.; 12: 121–127.
58
59