Tópico 2 – Teoria
Atômica
Prof. Romis Attux – DCA/FEEC/UNICAMP
Primeiro Semestre / 2017
Obs.: O conteúdo dos slides se baseia
fortemente no livro texto [Callister, 2011].
EE410 - Turma A - Prof. Romis Attux
Prelúdio
•
Desde pelo menos a Grécia antiga, teve lugar na humanidade a visão de
que a matéria seria composta por partes indivisíveis (átomos), cujas
diferentes características explicariam a multiplicidade do universo como o
percebemos.
•
Com a descoberta do elétron, percebeu-se que o átomo não era indivisível
sendo composto de partículas com cargas negativa (elétrons) e partículas
com carga positiva (prótons). Posteriormente, juntar-se-ia à dupla a
partícula conhecida como nêutron, sem carga elétrica.
•
Os experimentos de Rutherford e colaboradores levaram à visão moderna
de um átomo composto por um núcleo positivamente carregado (formado
por prótons e nêutrons), portando virtualmente toda a massa do átomo, e
uma eletrosfera na qual os elétrons “orbitavam”. A dimensão do núcleo é
muito menor que a dimensão do átomo como um todo.
EE410 - Turma A - Prof. Romis Attux
Número Atômico e Massa Atômica
•
Tanto os elétrons quanto os prótons possuem carga de 1,60 x 10-19 C. A massa
de prótons e nêutrons é aproximadamente igual, com valor de
1,67 x 10-27 kg, e a massa do elétron é bem menor, de 9,11 x 10-31 kg.
•
O número atômico de um átomo, denotado por Z, define o elemento químico
ao qual o átomo se associa. Esse número corresponde ao número de prótons
presentes no núcleo atômico, que, em condições normais, é igual ao número
de elétrons na eletrosfera. São encontrados na natureza elementos com Z
variando de 1 (hidrogênio) a 92 (urânio).
•
A massa atômica A de um átomo é expressa, de modo aproximado e
conveniente, como a soma das massas dos prótons e nêutrons subjacentes ao
núcleo. Embora todos os átomos de um elemento tenham necessariamente o
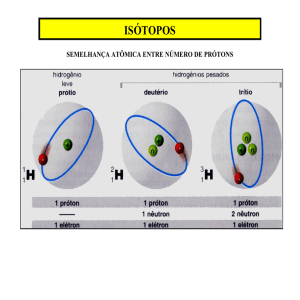
mesmo número de prótons, pode haver variedades com diferentes números de
nêutrons, denominadas isótopos. O “peso” atômico de um elemento é a média
ponderada das massas atômicas de seus isótopos naturais.
EE410 - Turma A - Prof. Romis Attux
Unidades
•
A unidade de massa atômica (uma) é usada para quantificar o “peso”
atômico. Definiu-se uma escala onde 1 uma corresponde a 1/12 da massa
atômica do isótopo mais comum do carbono, o carbono 12, com 6 prótons
e 6 nêutrons.
•
Note que isso faz com que as massas de prótons e nêutrons sejam
ligeiramente maiores que a unidade, mas se pode utilizar A Z + N, sendo
N o número de nêutrons.
•
“Pesos atômicos” e “pesos moleculares” podem ser expressos em uma /
átomo ou uma / molécula. Também se pode usar uma medida de massa
por mol de material. Um mol de uma substância contém 6,023 x 1023
átomos ou moléculas, o chamado número de Avogadro.
•
Por exemplo, o peso atômico do ferro é de 55,85 uma / átomo ou
55,85 g/mol.
EE410 - Turma A - Prof. Romis Attux
Modelos Atômicos - Bohr
•
O primeiro modelo quântico digno de nota do átomo foi o modelo de Bohr,
que é relativamente bem sucedido para explicar o comportamento do
átomo de hidrogênio.
•
Nesse modelo, considera-se o núcleo (um próton) em torno do qual orbita
um elétron. Uma condição de quantização do momento angular faz surgir
um número quântico n, que assume valores inteiros a partir de um. Cada
valor desse número representa um possível estado quântico do elétron, e
define, de maneira discreta, o raio da órbita associada e o valor de sua
energia.
•
Surge, dessa forma, o importante conceito de nível de energia, em
contraste com um contínuo de possíveis valores. A energia dos níveis do
átomo de hidrogênio, no modelo de Bohr, é dada pela fórmula
En = -13,6 eV / n2.
EE410 - Turma A - Prof. Romis Attux
Modelos Atômicos - Bohr
•
No modelo de Bohr, assim como nos modelos mais refinados que viriam, a
transição entre níveis energéticos se associa à emissão ou à absorção de
um fóton com energia igual à diferença de energia entre os níveis.
•
O modelo é “planetário” e não incorpora as noções de incerteza quântica
ou a função . Só usaremos para realizar ilustrações simples, pois se trata
de uma concepção superada.
EE410 - Turma A - Prof. Romis Attux
Modelos Atômicos – Mecânica Ondulatória
•
O modelo mais preciso de que se dispõe para descrever o átomo é baseado
na mecânica ondulatória, ou seja, trata o elétron de uma perspectiva de
partícula – onda. Não há mais órbitas, e sim nuvens de probabilidade para
os diferentes estados quânticos, que, naturalmente, continuam a ter
energias quantizadas.
•
Usando a mecânica ondulatória (Schrödinger e Dirac), chega-se a uma
descrição de estado quântico do elétron baseada em quatro números
quânticos. Três desses números, atingíveis via equação de Schrödinger,
definem o caráter da densidade de probabilidade associada ao elétron. O
quarto define seu spin.
•
Continua a haver a noção de nível atômico, mas surge a importantíssima
noção de subnível (ou subcamada). Os níveis (ou camadas) são
determinados pelo número quântico principal (n), que assume valores
inteiros a partir de 1 (n = 1, 2, 3, ... ).
EE410 - Turma A - Prof. Romis Attux
Modelos Atômicos – Mecânica Ondulatória
•
Por vezes, as respectivas camadas associadas a n = 1, 2, 3, ... são
denotadas pelas letras K, L, M, ... Esse número é “parente” do solitário
número quântico do modelo de Bohr.
•
O segundo número quântico (l), denominado por vezes azimutal, determina
a subcamada ocupada pelo elétron. O valor l = 0 define um orbital tipo s, o
valor l = 1 define um orbital tipo p, o valor l = 2 define um orbital tipo d e o
valor l = 3 define um orbital tipo f. Dado um número quântico principal n,
tem-se l variando de 0 a n-1.
•
O número de estados para cada subcamada é determinado pelo terceiro
número quântico, magnético (ml). O valor de ml vai de –l a l, ou seja,
orbitais s possuem uma única configuração, orbitais p possuem 3, orbitais
d possuem 5 e orbitais f possuem 7.
•
Por fim, para cada tripla (n, l, ml), há duas possibilidades para o quarto
número quântico - spin (ms), ms = -1/2 e ms = +1/2.
EE410 - Turma A - Prof. Romis Attux
Configurações Eletrônicas e Princípio da
Exclusão
•
Os elétrons tendem a ocupar sempre configurações de mínima energia (no
estado fundamental do átomo), respeitando o princípio da exclusão de
Pauli. Esse princípio garante que é impossível que dois elétrons possuam,
num mesmo sistema, configurações idênticas para os quatro números. Os
elétrons de um átomo, por consequência, sempre possuem quádruplas
distintas.
•
Ora, tendo em mãos a noção de mínima energia e o princípio da exclusão,
podemos tentar “montar a estrutura eletrônica” dos diferentes átomos.
Faltam-nos apenas alguns detalhes. Primeiramente, precisamos saber a
ordem energética das subcamadas, bem como as diferenças energéticas
suscitadas pelos números ml e ms. A regra de Hund nos fornece a segunda
resposta – começa-se por ml = +l e varre-se o escopo desse número
tomando sempre ms = +1/2. Em seguida, repete-se o ciclo com ms = -1/2.
EE410 - Turma A - Prof. Romis Attux
Ordem de Energia – Níveis e Subníveis
4d
4p
N-shell n = 4
3d
4s
Energy
Adapted from Fig. 2.6, Callister &
Rethwisch 9e.
(From K. M. Ralls, T. H. Courtney, and J. Wulff,
Introduction to Materials Science and
Engineering, p. 22. Copyright © 1976 by John
Wiley & Sons, New York. Reprinted by
permission of John Wiley & Sons, Inc.)
EE410 - Turma A - Prof. Romis Attux
3p
3s
M-shell n = 3
2p
2s
L-shell n = 2
1s
K-shell n = 1
Configurações Eletrônicas
•
Como o estado de menor energia é dado pela quádrupla (1, 0, 0, +1/2) essa é
a configuração do único elétron do átomo de hidrogênio. Essa configuração é
dada de maneira mais sucinta como 1s1. O segundo elétron, que caracteriza o
átomo de hélio (um gás nobre), é descrito como (1, 0, 0, -1/2), e a configuração
resultante é descrita como 1s2. Para o lítio (Z = 3), tem-se um novo elétron – (2,
0, 0, +1/2), e a descrição é 1s22s1. Para o berílio (Z = 4), acrescenta-se o
elétron (2, 0, 0, -1/2) e se tem 1s22s2. O boro traz pela primeira vez um orbital
p com o elétron (2, 1, +1, +1/2), levando a 1s22s22p1. Seguindo nossas regras,
e lembrando que nem sempre a energia segue a ordem dos orbitais (lembremse do tortuoso diagrama de Linus Pauling e da figura anterior), poderíamos
seguir “brincando de Lego” com a matéria. No entanto, saltaremos para a
configuração do gás nobre seguinte, o neônio – 1s22s22p6. Quando se tem uma
dupla s, p preenchida, chega-se, como regra, a uma configuração de gás nobre
(e ao lado direito da tabela periódica). Essa configuração é altamente estável, e
voltaremos a discuti-la quando falarmos de ligações químicas.
EE410 - Turma A - Prof. Romis Attux
Configurações Eletrônicas
Element
Atomic #
Hydrogen
1
Helium
2
Lithium
3
Beryllium
4
Boron
5
Carbon
6
...
Neon
10
Sodium
11
Magnesium
12
Aluminum
13
...
Electron configuration
1s 1
1s 2
(stable)
1s 2 2s 1
1s 2 2s2
1s 2 2s 2 2p 1
1s 2 2s 2 2p 2
...
Argon
...
Krypton
1s 2 2s 2 2p 6 3s 2 3p 6
(stable)
...
1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 (stable)
EE410 - Turma A - Prof. Romis Attux
18
...
36
1s 2 2s 2 2p 6
(stable)
1s 2 2s 2 2p 6 3s 1
1s 2 2s 2 2p 6 3s 2
1s 2 2s 2 2p 6 3s 2 3p 1
...
Elétrons de Valência e Orbitais Híbridos
•
Elétrons de valência são aqueles que se envolvem nas ligações químicas.
Para diversos elementos, eles são exatamente os elétrons da camada mais
externa.
•
Por fim, cabe mencionar que é possível ter orbitais híbridos do tipo spn,
surgidos de uma configuração de menor energia resultante. Esses orbitais
são estudados em certas aplicações de química orgânica, por exemplo.
EE410 - Turma A - Prof. Romis Attux
Tabela Periódica
•
Os elementos químicos são, muitas vezes, apresentados na forma da
chamada tabela periódica dos elementos, que busca agrupar nas mesmas
colunas átomos com características eletrônicas similares (do ponto de
vista dos elétrons de valência) e propriedades físicas e químicas análogas.
A ordem de disposição dos elementos é crescente com respeito a Z.
EE410 - Turma A - Prof. Romis Attux
H
accept 2eaccept 1einert gases
give up 1egive up 2egive up 3e-
Adapted from
Fig. 2.8,
Callister &
Rethwisch 9e.
Tabela Periódica
He
Li Be
O
F Ne
Na Mg
S
Cl Ar
K Ca Sc
Rb Sr
Y
Cs Ba
Se Br Kr
Te
I
Xe
Po At Rn
Fr Ra
Electropositive elements:
EE410 - Turma
A - Prof. Romis
Readily
giveAttux
up electrons
to become + ions.
Electronegative elements:
Readily acquire electrons
to become - ions.
Tabela Periódica
•
Os elementos da última coluna (“0”) são os gases nobres, que são inertes
pela enorme estabilidade de sua configuração eletrônica (como já
mencionado).
•
A maioria dos elementos é denotada normalmente como metal, e tem um
caráter eletropositivo, ou seja, de serem “doadores” de elétrons de valência
na formação de ligações químicas. Os elementos à direita (excluindo os
gases nobres) são eletronegativos, ou seja, tendem a atuar como
“receptores” de elétrons para formar ligações químicas. Em geral, a
eletronegatividade aumenta indo-se da esquerda para a direita na tabela.
EE410 - Turma A - Prof. Romis Attux