12
ARTIGO ORIGINAL
Luis Fernando Bouzas1
Mirna Calazans2
Tumores sólidos e hematológicos na
infância e na adolescência – Parte 2
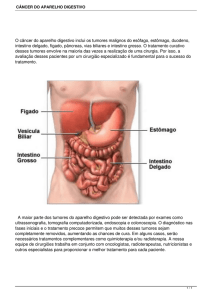
INTRODUÇÃO
O câncer na infância e na adolescência tem
fornecido oportunidades únicas para o avanço na
compreensão da causa e no sucesso terapêutico
das neoplasias como um todo.
O diagnóstico de neoplasia maligna em crianças é raro, correspondendo a apenas 3% de todos
os cânceres, em diferentes faixas etárias. Na maioria dos casos, a neoplasia maligna se origina de
tecidos germinativos, ao contrário do que ocorre
em adultos, quando deriva mais freqüentemente
de tecidos epiteliais. Nas crianças, essa origem
mais comum determina altas taxas de sobrevida de
longo prazo e de cura, uma vez que os tumores
apresentam alta sensibilidade à quimioterapia e à
radioterapia. Os excelentes resultados atingidos na
população pediátrica são resultado do tratamento
multidisciplinar efetivo e da detecção precoce.
As participações do pediatra e do cirurgião pediátrico são de fundamental importância para que o
diagnóstico e as intervenções de urgência pertinentes sejam realizados o mais precocemente possível,
o que influencia positivamente o resultado.
Em complementação ao que foi descrito na
parte 1 deste artigo, quando abordamos principalmente aspectos de leucemias e linfomas, serão descritos os principais achados clínicos e laboratoriais
relacionados às neoplasias da infância e da adolescência, no intuito de facilitar o reconhecimento
dessas patologias pelo profissional que realizará o
primeiro atendimento médico dos pacientes.
Médico pediatra; membro do Comitê de Onco-Hematologia da Sociedade de
Pediatria do Estado do Rio de Janeiro (SOPERJ); presidente da Sociedade Brasileira de
Transplante de Medula Óssea (SBTMO); mestre em Hematologia pela Universidade
Federal do Rio de Janeiro (UFRJ); diretor do Centro de Transplante de Medula Óssea
do Instituto Nacional de Câncer (INCa).
2
Médica hematologista do Centro de Transplante de Medula Óssea do INCa.
1
volume 4 nº 2 abril 2007
EPIDEMIOLOGIA
As neoplasias malignas estão entre as principais causas de morte em crianças entre 1 e 14 anos
de idade. Elas são a terceira causa de morte em
crianças de 1 a 4 anos e a segunda entre as de 5 a
Tabela 1
TIPOS DE MALIGNIDADE MAIS COMUNS EM CRIANÇAS COM O
PICO DE IDADE AO DIAGNÓSTICO E INCIDÊNCIA NOS EUA
Malignidade
Pico de idade
(anos)
Taxa de incidência
(milhão/ano)
2-5
24,7
Constante
5
Não-Hodgkin
6-16
9,3
Hodgkin
> 10
7,5
Constante
13,4
Meduloblastomas
5-10
4.9
Ependimoma
<5
2,1
Neuroblastoma
<3
8
Tumor de Wilms
<5
6,9
Retinoblastoma
<3
3
2-6 e 14-18
3,7
Sarcoma de Ewing/PNET
10-18
2,1
Osteossarcoma
10-18
3,1
<2
1,6
< 2 e > 14
0,4
Leucemia
Linfocítica aguda
Não-linfocítica aguda
Linfomas
Tumores de SNC
Gliomas
Tumores sólidos
Rabdomiossarcoma
Hepatoblastoma
Tumores de células
germinativas
Fonte: Surgical Clinics of North América.
SNC = sistema nervoso central; PNET = primitive neuroectodermal tumor.
Adolescência & Saúde
Bouzas & Calazans
TUMORES SÓLIDOS E HEMATOLÓGICOS NA INFÂNCIA E NA ADOLESCÊNCIA – PARTE 2
14 anos. As doenças neoplásicas mais comumente
diagnosticadas são leucemia aguda, linfoma nãoHodgkin, doença de Hodgkin e tumores primários
do sistema nervoso central (SNC). Entre os tumores sólidos pediátricos mais comuns estão neuroblastoma, tumor de Wilms, rabdomiossarcoma e
retinoblastoma(13) (Tabela 1).
TUMOR DE WILMS
Neoplasia renal primária mais comum nas
crianças, é discretamente menos comum em meninos do que em meninas. Os tumores unilaterais são
tipicamente diagnosticados no quarto ano de vida,
enquanto os bilaterais são geralmente encontrados
em idades mais precoces. As crianças com essa patologia apresentam outros achados ao exame físico
que chamam a atenção do pediatra: aniridia, hemihipertrofia, criptorquidia e hipospadia(8). A maioria
das crianças com tumor de Wilms é levada ao pediatra devido ao aumento da circunferência ou à
presença de massa abdominal, o que geralmente
é observado pelos pais no momento do banho ou
de vestir. Outras queixas comuns incluem dor abdominal, hematúria maciça e febre. Ao exame físico,
25% dos pacientes apresentam hipertensão arterial
sistêmica (HAS) devido ao aumento da atividade da
renina(3). Pode ocorrer varicocele secundária a obstrução da veia espermática por trombo na veia renal
ou cava inferior. Exames laboratoriais importantes
no diagnóstico incluem hemograma completo com
contagem de plaquetas, testes de função hepática e
renal, cálcio sérico (que pode estar elevado nos tumores rabdóides do rim e em nefroma mesoblástico
congênito) e elementos anormais e sedimentoscopia
(EAS). Os exames de imagem a serem solicitados inicialmente devem ser os necessários para identificar
uma lesão intra-renal, o que geralmente é obtido
com o exame ultra-sonográfico das lojas renais.
NEUROBLASTOMA
É o tumor maligno intra-abdominal mais
comum em crianças. É mais freqüente em meAdolescência & Saúde
13
ninos do que em meninas, sendo a idade média
ao diagnóstico de 2 anos para ambos os sexos(3).
Aproximadamente 70% dos pacientes apresentam doença metastática ao diagnóstico, sendo os
ossos, o fígado, a medula óssea e a pele mais freqüentemente envolvidos. O neuroblastoma pode
originar-se de qualquer tecido do sistema nervoso
simpático do organismo, sendo que os sítios mais
acometidos são os intra-abdominais. A glândula
supra-renal é o sítio primário em 38% dos casos.
Outros sítios intra-abdominais freqüentemente
acometidos incluem gânglios simpáticos paravertebrais, celíaco, mesentéricos superior e inferior.
Quando não são acometidos os sítios intra-abdominais, a doença geralmente se apresenta nas regiões cervical e torácica. Comumente as crianças
são levadas ao pediatra devido ao aumento da
circunferência ou massa abdominal. Os tumores
paravertebrais geralmente levam a sintomatologia
referente ao SNC. Os pacientes com metástases
hematogênicas podem queixar-se de dor óssea ou
apresentar edema periorbital e equimoses. A febre
está presente em 23% dos casos ao diagnóstico.
Apresentações clínicas incomuns incluem hidropisia fetal e diarréia crônica devido à secreção
tumoral de polipeptídios vasoativos intestinais(12).
Os tecidos nervosos simpáticos normalmente secretam epinefrina e norepinefrina. A maioria dos
pacientes com neuroblastoma apresenta aumento
da secreção urinária de ácido vanilmandélico, ácido homovanílico, diidroxifenilalanina, dopamina
e norepinefrina. O diagnóstico de neuroblastoma
se inicia com a obtenção de uma história clínica
detalhada, com questões referentes a alguns sinais e sintomas comuns na doença, como a presença de diarréia e ataxia. O exame físico deve
incluir a observação meticulosa da pele para que
possíveis metástases subcutâneas possam ser reconhecidas, as quais geralmente apresentam-se
como lesões vermelho-violáceas e elevadas, podendo ser solitárias. As equimoses periorbitárias
são comuns em crianças com doença disseminada
e comprometimento orbitário. Um exame neurológico detalhado deve ser realizado. Os exames
laboratoriais que auxiliam no diagnóstico incluem
volume 4 nº 2 abril 2007
14
TUMORES SÓLIDOS E HEMATOLÓGICOS NA INFÂNCIA E NA ADOLESCÊNCIA – PARTE 2
hemograma completo, EAS, testes de função hepática e renal, velocidade de hemossedimentação
(VHS), ferritina sérica e quantificação da excreção
urinária de ácido vanilmandélico e catecolaminas
totais. Inicialmente, os exames de imagem em
pacientes com massa abdominal devem incluir
uma radiografia simples de abdome em posição
supina, a qual poderá demonstrar uma massa,
possivelmente com calcificação. A ultra-sonografia de abdome pode demonstrar uma massa sólida, podendo conter áreas císticas. Os pacientes
com neuroblastoma torácico geralmente apresentam uma massa em mediastino posterior, menos
freqüentemente calcificada do que nos casos de
doença intra-abdominal e que pode ser demonstrada em radiografia simples de tórax.
RETINOBLASTOMA
É o tumor oftalmológico maligno mais comum na população pediátrica. A sobrevida excede 90%, sendo, assim, uma das neoplasias da
infância com a maior taxa de cura. Setenta a 75%
dos casos são unilaterais, com uma freqüência ligeiramente maior em meninos, especialmente naqueles com doença bilateral. Os casos de doença
unilateral são geralmente diagnosticados aos 2
anos de idade nos meninos e 1 ano nas meninas.
Nos pacientes com comprometimento bilateral,
geralmente o diagnóstico é realizado em menores
de 12 meses de idade(3). A maioria dos casos é esporádica, no entanto alguns são hereditários, seguindo um padrão de penetrância alto, como um
traço autossômico dominante(7). Assim, os pais e
irmãos dos pacientes com retinoblastoma devem
ser submetidos a exame oftalmológico cuidadoso,
uma vez que a doença pode sofrer regressão espontânea, deixando alterações características na
retina(11). Geralmente as crianças são levadas ao
pediatra devido a leucocoria, estrabismo, eritema
conjuntival ou diminuição da acuidade visual. O
exame físico revela um reflexo pupilar esbranquiçado e o oftalmoscópico pode demonstrar tumores que se localizam próximo à mácula. A necrose
volume 4 nº 2 abril 2007
Bouzas & Calazans
de tumores localizados na retina ou a presença de
glaucoma podem levar ao surgimento de uveíte,
com dor e eritema local. O diagnóstico da doença
se baseia em história clínica detalhada, incluindo
a familiar. Os pacientes com suspeita de retinoblastoma devem ser encaminhados a um oftalmologista pediátrico com experiência no tratamento
dessa patologia, uma vez que o exame de ambos
os olhos deve ser realizado sob anestesia geral.
RABDOMIOSSARCOMA
É a neoplasia de partes moles mais freqüente na infância. É discretamente mais comum em
meninos, com a idade média ao diagnóstico de
4 anos, sendo que as meninas são ligeiramente
mais velhas do que os meninos à apresentação(3).
O rabdomiossarcoma pode surgir em qualquer
sítio do organismo, mas 35% dos casos ocorrem
nas regiões de cabeça e pescoço, sendo a órbita o
sítio primário mais comum. O restante dos casos
que acometem a cabeça e o pescoço divide-se em
tumores parameníngeos (nasofaringe, seios paranasais, ouvido médio, mastóides, fossas pterigopalatina e infratemporal) e não-parameníngeos.
Outras regiões que podem ser acometidas por
esse tumor incluem abdome, trato geniturinário,
próstata, bexiga, vagina, útero, ductos biliares(3),
tórax, tronco, coxas e região inguinal. Os casos
com comprometimento das extremidades são
mais comuns na segunda década de vida e geralmente mais agressivos. Aproximadamente 25%
das crianças apresentam doença metastática ao
diagnóstico, e os principais locais de acometimento são pulmões, medula óssea, ossos e linfonodos.
A Tabela 2 mostra as apresentações clínicas mais
comuns desse tumor, de acordo com o sítio primário de acometimento(6).
Como o rabdomiossarcoma pode acometer
qualquer estrutura do corpo, o estudo radiológico
deve ser individualizado. O diagnóstico requer interpretação radiológica precisa, avaliação patológica da amostra obtida por cirurgia e o conhecimento do padrão de disseminação metastática.
Adolescência & Saúde
Bouzas & Calazans
TUMORES SÓLIDOS E HEMATOLÓGICOS NA INFÂNCIA E NA ADOLESCÊNCIA – PARTE 2
15
Tabela 2
APRESENTAÇÃO CLÍNICA DO RABDOMIOSSARCOMA
Sítio
Sintomas clínicos mais comuns
Cabeça e pescoço
Massa assintomática, podendo simular uma linfonodomegalia
Órbita
Proptose, quemose, paralisia ocular e massa palpebral
Nasofaringe
Rinorréia, voz anasalada, epistaxe, dor local e disfagia
Seios paranasais
Edema, dor, sinusite, obstrução, epistaxe e paralisia dos nervos cranianos
Ouvido médio
Otite média crônica, secreção hemorrágica, massas polipóides
Laringe
Rouquidão e tosse
Tronco
Massa assintomática
Trato biliar
Hepatomegalia e icterícia
Retroperitônio
Massa assintomática, ascite, obstrução dos tratos gastrointestinal ou geniturinário, compressão medular
Bexiga e próstata
Hematúria, retenção urinária, massa abdominal e constipação
Genitália feminina
Pólipos vaginais, nódulo vulvar
Genitália masculina
Massa escrotal
Extremidades
Massa indolor com comprometimento de linfonodos
SARCOMA DE EWING E TUMORES
NEUROECTODÉRMICOS PRIMITIVOS
PERIFÉRICOS
Esses tumores, se não idênticos, são altamente
relacionados. Eles podem apresentar-se como malignidades do tecido mole ou de tecidos ósseos. O sarcoma de Ewing é o segundo tumor ósseo primário
mais comum na população pediátrica, representando aproximadamente 4% das neoplasias, sendo que
a grande maioria surge na segunda década de vida.
Vinte a 25% dos casos apresentam acometimento
primário do fêmur e 20% acometem primariamente
a pelve. Outras áreas que podem ser atingidas incluem tíbia, fíbula, ossos dos pés, úmero, vértebras,
costelas, clavícula, mandíbula e calota craniana. O
principal sintoma que leva os pacientes ao pediatra
é a dor, inicialmente intermitente, evoluindo para
constante, podendo acordar a criança durante o
sono. O edema local pode ser notado pelo paciente
ou por seus pais, principalmente quando o tumor
acomete uma das extremidades. Outros sinais e sintomas podem ocorrer, dependendo da localização
da doença, como, por exemplo, claudicação, dor
Adolescência & Saúde
que se acentua com a respiração ou com características radiculares e paraplegia devida a tumor que
atinge a vértebra. A apresentação clínica pode simular a de pacientes com osteomielite(1). A febre pode
estar presente em 28% dos casos à apresentação(3).
Em 26% das crianças acometidas ocorrem metástases já ao diagnóstico, sendo que os pulmões e sítios ósseos são os locais metastáticos mais freqüentes. A avaliação inicial do paciente com suspeita de
sarcoma de Ewing inclui radiografias dos sítios
primários do tumor, documentação de possíveis
sítios metastáticos e avaliação laboratorial para
excluir outros diagnósticos. Geralmente as lesões
dos ósseos longos comprometem a diáfise, com
extensão para a metáfase e com características
líticas ou mistas (lítico-escleróticas). Os tumores pélvicos freqüentemente apresentam-se, aos
raios X simples, como lesões mistas, com componentes líticos e blásticos.
TUMORES HEPÁTICOS PRIMÁRIOS
Aproximadamente 60% a 70% de todos os
tumores hepáticos primários em crianças são mavolume 4 nº 2 abril 2007
16
TUMORES SÓLIDOS E HEMATOLÓGICOS NA INFÂNCIA E NA ADOLESCÊNCIA – PARTE 2
lignos, sendo que os mais comuns são o hepatoblastoma e o carcinoma hepatocelular. As lesões
benignas mais comuns são o hemangioma e os
hamartomas. O hepatoblastoma é mais freqüente
do que o carcinoma hepatocelular, sendo que o
primeiro afeta mais as crianças mais jovens, com a
idade média ao diagnóstico de 1 ano. Ao contrário,
o carcinoma hepatocelular atinge tipicamente as
crianças mais velhas, com idade média ao diagnóstico de 12 anos. Ambos os tumores ocorrem mais
em meninos(4). Geralmente as crianças com hepatoblastoma apresentam outras anormalidades associadas, incluindo hemi-hipertofia, divertículo de
Meckel, agenesia renal e de glândula supra-renal,
além de hérnia umbilical(10). Crianças prematuras
ou com peso muito baixo ao nascimento parecem
apresentar um risco maior de desenvolver o hepatoblastoma(5).
O carcinoma hepatocelular está fortemente
associado ao vírus da hepatite B, que pode ser adquirido por via vertical, através de mães soropositivas ou por exposição a produtos sangüíneos contaminados. Pacientes com várias outras doenças
de base têm apresentado o diagnóstico adicional
de carcinoma hepatocelular, como, por exemplo,
crianças com tirosinemia, galactosemia, atresia biliar, cirrose colestática familiar progressiva, anemia
de Fanconi, neurofibromatose, entre outros(3).
Geralmente as crianças com tumores hepáticos são levadas ao pediatra devido a uma
massa ou distensão abdominal, além de perda
de peso, anorexia e febre. A icterícia é rara. A história clínica deve ressaltar ocorrência prévia de
icterícia ou hepatite, uso pré-natal de hormônios
esteróides pela mãe, exposição prévia a agentes
hepatotóxicos e presença de casos de doenças
hepáticas ou biliares nos pais ou irmãos do paciente. A avaliação laboratorial inclui hemograma
completo e testes de função hepática e renal. O
nível sérico de alfafetoproteína está aumentado
em ambos os tumores. Os exames de imagem incluem tomografia computadorizada (TC) e ressonância magnética (RM) do abdome. Raramente
os tumores hepáticos malignos são calcificados.
A ultra-sonografia abdominal pode demonstrar
a presença e a extensão de uma massa sólida,
volume 4 nº 2 abril 2007
Bouzas & Calazans
além de avaliar as lojas renais e a veia cava inferior, o que é útil no diagnóstico diferencial e na
avaliação pré-cirúrgica.
TUMORES GERMINATIVOS
Três por cento de todos as malignidades
pediátricas são causados por tumores de células
germinativas originadas das gônadas ou de sítios
extragonadais. Em crianças, quase dois terços dos
tumores germinativos são extragonadais, sendo
que a região mais acometida é a sacrococcígea.
As regiões menos afetadas incluem o mediastino,
o retroperitônio, a vagina e a loja pineal. O comportamento biológico desses tumores varia da
forma benigna do teratoma maduro ao carcinoma
embrionário e o coriocarcinoma, ambos altamente
malignos. No entanto esses tumores de comportamento agressivo apresentam importante quimiossensibilidade, sendo que, após a introdução dos
regimes quimioterápicos baseados em derivados
da platina, há grande melhora na sobrevida dessas
crianças.
Apenas 2% dos teratomas pré-sacrais e sacrococcígeos diagnosticados antes dos 6 meses
de vida são malignos, enquanto o são 65% daqueles diagnosticados após essa idade. Acometem
mais freqüentemente as meninas. Geralmente o
diagnóstico é feito ao nascimento ou durante os
primeiros meses de vida, e com freqüência existem anomalias congênitas das vértebras, do trato
geniturinário ou anorretais associadas. Lesões malignas podem surgir em sítios de onde um tumor
benigno foi previamente retirado. Os pacientes
com teratomas pélvicos malignos se apresentam
com uma massa abdominal ou na região das nádegas, ou com sinais de obstrução urinária ou fecal. O toque retal revela uma massa entre o reto
e o sacro.
Dez por cento de todas as neoplasias de células germinativas pediátricas se apresentam como
tumores testiculares, sendo 80% malignos e 90%
localizados. A distribuição etária é bimodal, acometendo crianças muito jovens e adolescentes.
A maioria das crianças com tumores testiculares
Adolescência & Saúde
Bouzas & Calazans
TUMORES SÓLIDOS E HEMATOLÓGICOS NA INFÂNCIA E NA ADOLESCÊNCIA – PARTE 2
primários apresenta aumento indolor do testículo
acometido. Ascite, adenomegalia inguinal ou dor
abdominal aguda podem ocorrer nos raros casos
de doença metastática. O acometimento testicular
bilateral ao diagnóstico acontece em menos de 1%
dos casos(3).
Os tumores ovarianos representam aproximadamente 25% de todos os tumores germinativos
pediátricos, sendo que a maioria deles ocorre no final da infância, com pico de incidência aos 10 anos
de idade. Os mais comuns são os disgerminomas
e os tumores do seio endodérmico. Os teratomas
imaturos representam cerca de 10% das massas
ovarianas(2, 9). Essas pacientes geralmente são levadas ao pediatra devido a dor, que pode ser intensa
pela torção do pedículo, ou surgimento de massa
abdominal. Pode ocorrer febre ao diagnóstico. A
avaliação radiológica inicial deve incluir raios X simples de abdome, que podem mostrar calcificação
do tumor. A ultra-sonografia abdominal demonstra
se a massa tem natureza cística, e a TC mostra com
maior precisão o sítio de origem do tumor.
Os tumores germinativos que acometem primariamente o tórax em geral se apresentam como
massas no mediastino anterior em meninos adolescentes. A maior parte desses tumores é composta
de teratomas benignos, mas também podem ser
encontrados coriocarcinoma e tumores do saco
hialino nessa localização. A apresentação clínica
está relacionada à compressão traqueobrônquica,
incluindo tosse, dispnéia e dor torácica. A radiografia simples de tórax demonstra massa mediastinal anterior, e o diagnóstico é definido através
da biópsia do tumor primário ou de um linfonodo
supraclavicular comprometido.
A alfafetoproteína e a subunidade beta da gonadotrofina coriônica humana (β-HCG) apresentam
nível sérico elevado em alguns tumores germinativos, contribuindo para o diagnóstico da doença.
Níveis séricos de alfafetoproteína podem se elevar
em tumores de seio endodérmico, independentemente da localização. Pacientes com carcinoma
embrionário, coriocarcinoma e disgerminoma podem apresentar níveis elevados de β-HCG, o que
auxilia no diagnóstico dessas doenças.
Adolescência & Saúde
17
CONCLUSÃO
O prognóstico da doença maligna na infância
depende primariamente do tipo do tumor, da extensão da doença ao diagnóstico e da rápida resposta ao tratamento. Como a maioria dos tumores é passível de cura, o diagnóstico precoce é de
especial importância. Além disso, geralmente nas
doenças em estágios iniciais o tratamento indicado, apesar de curativo, é menos agressivo do que
os utilizados em estágios mais avançados da mesma patologia. Nas crianças esse aspecto assume
grande relevância por se tratar de uma população
cuja sobrevida é longa e o objetivo é evitar, sempre dentro do possível, mutilações ou patologias
secundárias ao tratamento indicado.
O diagnóstico precoce das neoplasias malignas nas crianças é de suma importância, uma
vez que aproximadamente 70% dos tumores são
potencialmente curáveis. Portanto os profissionais
que lidam com essa população de pacientes devem ter alto índice de suspeição diante de um caso
sugestivo.
O diagnóstico e o tratamento da criança com
câncer devem ser cuidadosamente orientados e explicados aos pais e, se a criança possuir idade para
tal, a ela também. Sempre que possível a criança e
seus familiares devem ser acompanhados por uma
equipe multidisciplinar, envolvendo profissionais
como assistentes sociais, psicólogos e psiquiatras
pediátricos e professores capacitados para lidar
com crianças e adolescentes com diagnóstico de
câncer.
A mensagem deste artigo (partes 1 e 2) é
clara e pode ser simplificada. O diagnóstico precoce das neoplasias da infância e da adolescência
está diretamente relacionado à adequada investigação clínica realizada por pediatras, clínicos
e cirurgiões, partindo do conhecimento epidemiológico, realizando anamnese, exame físico
minucioso e solicitando exames complementares
básicos. Diante da suspeita ou do diagnóstico já
confirmado, o especialista deve ser imediatamente acionado, proporcionando intervenção imediata, o que contribui para resultados positivos
no controle da doença.
volume 4 nº 2 abril 2007
18
TUMORES SÓLIDOS E HEMATOLÓGICOS NA INFÂNCIA E NA ADOLESCÊNCIA – PARTE 2
Bouzas & Calazans
REFERÊNCIAS
1. Durbin M, Randal RL, James M, et al. Ewing’s sarcoma masquerading as osteomyelitis. Clin Orthop. 1998; 357: 176.
2. Göbel V, Calaminus G, Engert J, et al. Teratomas of infancy and childhood. Med Pediatr Oncol. 1998; 31: 8.
3. Green DM. Diagnosis and management of solid tumors in infants and children. Boston: Martinus Nijhoff. 1985.
4. Greenberg H, Filler RM. Hepatic tumors. In: Pizzo PA, Poplack DG, eds. Principles and practice of pediatric oncology.
3rd ed. Philadelphia: Lippincott-Raven. 1997.
5. Ideda H, Matsuyama S, Tauimura M. Association between hepatoblastoma and very low birth weigth: a trend or a
chance? J Pediatr. 1997; 130: 557.
6. Macdowell HP. Update on childhood rhabdomyosarcoma. Arch Dis Child. 2003; 88: 354.
7. Matsunada E. Hereditary retinoblastoma. Penetrance, expressivity and age at onset. Hum Genet. 1976; 33: 1.
8. Miller RW, Fraumeni JF Jr, Manning MD. Association of Wilms’ tumor with aniridia, hemihypertrophy and other
congenital malformations. N England J Med. 1964; 270: 922.
9. Pinkerton CR. Malignant germ cell tumors in childhood. Eur J Cancer. 1997; 33: 895.
10. Reynolds M. Pediatric liver tumors. Semin Surg Oncol. 1999; 16: 159.
11. Sanborn GE, Augsburger JJ, Shields JA. Spontaneous regression of bilateral retinoblastoma. Br J Ophthalmol. 1982;
66: 685.
12. Schiebel E, Rechnitzer C, Fahrenkrug J, Hertz H. Vasoactive intestinal polypeptide (VIP) in children with neutral crest
tumours. Acta Paediatr Scand. 1982; 71: 721.
13. US Cancer Statistics Working Group. United States Cancer Statistics: 2000 incidence. Atlanta: Departament of
Health and Human Services; Centers of Disease Control and Prevention; National Cancer Institute. 2003.
volume 4 nº 2 abril 2007
Adolescência & Saúde