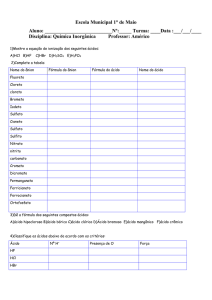
457. Indique, na afirmação a seguir, o que é
correto ou incorreto e justifique sua resposta
de forma resumida.
“Uma solução aquosa de cloreto de hidrogênio apresenta o número de cátions H + igual
ao de ânions Cl–, portanto é eletricamente
neutra e não conduz a eletricidade”.
458.Dentre as espécies químicas apresentadas, é classificado como não eletrólito o:
d) C6H12O6
a) Na2CO3
b) KOH
e) LiH
c) Na2O
459. A força de um eletrólito é medida pelo(a):
a) poder de corrosão de metais.
b) conteúdo de oxigênio.
c) velocidade de ionização.
d) grau de ionização.
e) poder de volatilidade.
460.Com base na tabela de graus de ionização
apresentada a seguir:
Ácido
Grau de ionização (a)
HF
8%
HCl
92%
EM1D-10-34
HCN
0,08%
H2SO4
61%
H3PO4
27%
podemos concluir que o ácido mais fraco é o:
a) HF
d) H2SO4
b) HCl
e) H3PO4
c) HCN
461.Dissolvendo-se 300 moléculas de uma
substância composta em água, verificou-se
que 18 moléculas sofreram dissociação. Com
essa informação, podemos afirmar que:
a) o grau de dissociação é 0,06% e o eletrólito é fraco.
b) o grau de dissociação é 0,6% e o eletrólito
é fraco.
c) o grau de dissociação é 6,0% e o eletrólito
é forte.
d) o grau de dissociação é 6,0% e o eletrólito
é moderado (semiforte).
462.Têm-se os três ácidos e os valores da tabela, que foram obtidos dissolvendo-se em
água à temperatura constante.
Com base no exposto acima, faça o que se
pede.
H 2S
Quantidade em
mols dissolvidos
10
Quantidade em
mols ionizados
1
H2SO4
3
2
HNO3
10
8
a) Calcule o grau de ionização para cada ácido e coloque-os em ordem crescente de sua
força de ionização.
b) Equacione a ionização do HNO3 em água.
463. O esquema a seguir mostra a aparelhagem que pode ser utilizada para testar a força
dos ácidos.
n
G
p
Em qual das soluções, todas com mesma
concentração e mesma temperatura, a lâmpada apresenta maior brilho?
a) HF (a = 8%)
b) C12H22O11
c) H3PO4 (a = 27%)
d) C2H6O
e) NaCl
464. Um ácido, quanto à força, classifica-se
como forte, moderado e fraco, conforme a escala de grau de ionização abaixo.
100%
50%
Forte
Moderado
466. De acordo com a tabela a seguir, podemos
afi rmar que:
Número
Ácido
Grau de ionização (%)
I
H3PO4
27
II
H2s
7,6 · 10–2
III
HClO4
97
IV
HCN
8,0 · 10–3
a)
b)
c)
d)
e)
467. X, Y e Z representam genericamente três
ácidos que, quando dissolvidos em um mesmo volume de água, à temperatura constante,
comportam-se de acordo com a tabela.
Número de mols
dissolvidos
Número de mols
ionizados
X
20
2
Y
10
7
Z
5
1
5%
Fraco
Assim, comparando-se o ácido A, cujo grau
de ionização é de 40%, com o B, no qual, na
ionização de 1 mol de moléculas, somente 2,4
· 1023 moléculas não se ionizam, podemos dizer que:
a) A é mais forte que B.
b) A e B são igualmente moderados.
c) A é tão fraco quanto B.
d) B é mais forte que A.
e) B é tão forte quanto A.
465. Sejam os seguintes ácidos, com seus
respectivos graus de ionização (a): HClO4
(a = 97%); H2SO4 (a = 61%); H3BO3 (a = 0,025%);
H3PO4 (a = 27%); HNO3 (a = 92%). Assinale a
afi rmativa correta.
a) H3PO4 é mais forte que H2SO4.
b) HNO3 é um ácido moderado.
c) HClO4 é mais fraco que HNO3.
d) H3PO4 é um ácido forte.
e) H3BO3 é um ácido fraco.
II é considerado forte.
III e IV são fortes.
IV é um ácido semiforte.
III é mais forte que I.
I é considerado ácido fraco.
Analise as afi rmações, considerando os
três ácidos.
I.
X representa o mais forte.
II. Z representa o mais fraco.
III. Y apresenta o maior grau de ionização.
Está(ão) correta(s):
a) apenas I.
b) apenas II.
c) apenas III.
d) apenas I e II.
e) I, II e III.
468. Em relação ao estudo dos ácidos e bases,
assinale a alternativa incorreta.
a) Quando um composto iônico é dissolvido
em água, os íons se separam em um processo
chamado ionização.
b) Os termos dissociação e ionização não são
sinônimos.
c) A teoria dos ácidos de Arrhenius é restrita
a soluções aquosas.
d) As substâncias que conduzem eletricidade
são chamadas eletrólitos.
e) Em geral, ao se colocarem substâncias iônicas em água, estas formam uma solução capaz de conduzir corrente elétrica.
469.Defina e exemplifique ácido segundo
Arrhenius.
470.Classifique os ácidos quanto à presença de oxigênio na molécula: HCl, H2SO4, HBr,
HNO3, HClO3 e HCN.
471. Classifique os ácidos quanto ao número
de hidrogênios ionizáveis: H4SiO4, HCl, H3PO3,
HNO3, H3PO2, H4P2O7, H3PO4, HBr, HNO3 e H2S.
472.Da série de ácidos abaixo representada,
qual apresenta a mesma classificação, dentro
do critério de número de hidrogênios ionizáveis?
a) HNO3, HNO2, H2S, H2SO3
b) H3PO4, H3AsO3, H3BO3, H3PO3
c) H2CrO4, H3AsO4, HIO3, HBr
d) H2SO4, H2S2O8, H2CO3, HMnO4
e) H3PO3, H2Cr2O7, H2SnO3, H2SO4
Podemos afirmar que:
a) HClO4 e HCN são triácidos.
b) H3PO4 e H2S são hidrácidos.
c) H3PO4 é considerado um ácido semiforte.
d) H2S é um ácido ternário.
475. Usando a regra prática para a determinação da força de um ácido, classifique os ácidos
quanto à presença de hidrogênio e sua força:
HCN, H3BO3, HCl, HClO4, H2SO4, H3PO3, HBr, HClO,
H3PO2, H3PO4, H2SO3, HF, HMnO4, HI, HNO3.
476. Classifique os seguintes ácidos quanto à
presença de oxigênio, ao número de hidrogênios ionizáveis e à força ácida.
a) HF
b) H3PO4
c) H2SO4
d) H2Se
e) H3SbO4
f) H4[Fe(CN) 6]
477. Em relação à classificação dos ácidos, podemos afirmar que:
a) HClO4 e HCN são hidrácidos.
b) H3PO4 e H2S são diácidos.
c) H3PO4 é considerado um ácido forte.
d) H2S é um ácido ternário.
EM1D-10-34
473. Classifique os seguintes ácidos quanto à
presença de oxigênio, ao número de hidrogênios ionizáveis e à força ácida.
a) HCl
b) H3PO3
c) H2SO3
d) H2S
e) H3PO4
478. O ácido classificado como oxiácido, diácido e formado por átomos de três elementos
químicos diferentes é o:
a) H2S
b) H4P2O7
c) HCN
d) H2SO3
e) HNO3
474. Considere os seguintes ácidos, com seus
respectivos graus de ionização (a 18 °C) e usos:
– H3PO4 (a = 27%): usado na preparação
de fertilizantes e como acidulante em bebidas
refrigerantes;
– H2S (α = 7,6 · 10–2 %): usado como redutor;
– HClO4 (α = 97%): usado na medicina, em
análises químicas e como catalisador em explosivos;
– HCN (α = 8,0 · 10 –3 %): usado na fabricação de plásticos, corantes e fumigantes para
orquídeas e poda de árvores.
479.Os ácidos podem ser classificados quanto ao número de hidrogênios ionizáveis. O
ácido hipofosforoso (H 3PO2), utilizado na fabricação de medicamentos, apresenta fórmula estrutural:
H
O
P
O
H
H
Quantos hidrogênios são ionizáveis no
ácido hipofosforoso? Justifique sua resposta.
480.Observe a tabela abaixo e julgue as afirmativas que se seguem:
Ácido
Grau de ionização (α)
H3PO4
α = 27%
H2S
α = 8 · 10–2 %
HClO4
α = 97%
HCN
α = 8 · 10–3 %
1a – O ácido mais forte, entre os indicados, é o
ácido perclórico, HClO4.
2a – O ácido fosfórico, H3PO4, é classificado
como um ácido semiforte.
3a – H2S, ácido sulfídrico, é um triácido.
4a – H3PO4 e H2S são hidrácidos.
5a – O ácido cianídrico, HCN, é mais fraco que
o ácido sulfídrico, H2S.
481.Monte a fórmula molecular dos hidrácidos abaixo:
a) Ácido fluorídrico
b) Ácido clorídrico e) Ácido cianídrico
c) Ácido bromídrico
d) Ácido iodídrico
482.Escreva a fórmula molecular do ácido cianídrico e do ácido isocianídrico e classifique-os quanto à presença de oxigênio.
483.Faça a correspondência:
a) Ácido clorídrico (( )HCN
b) Ácido sulfídrico (( )HF
c) Ácido cianídrico (( )H2S
d) Ácido fluorídrico (( )HCl
486.Escreva a fórmula estrutural dos seguintes hidrácidos.
Dados:
H
C
N
S
F
a) HF
b) H2S
c) HCN
487.Monte a fórmula molecular e dê o nome
para os hidrácidos formados pelos elementos
do grupo VI A.
488.Dados os íons abaixo, monte a fórmula
molecular e dê os respectivos nomes aos ácidos formados:
Br– = brometo S2– = sulfeto CN– = cianeto
489.Dê o nome oficial e monte a fórmula estrutural dos seguintes ácidos:
c) HCN
a) HCl
b) H2S
490.Dê o nome oficial dos seguintes ácidos:
a) HF
e) HI
b) HCl
f) HBr
c) HCN
g) HNC
d) H2S
491. Monte a fórmula molecular dos ácidos
abaixo:
a) Ácido ferricianídrico
b) Ácido ferrocianídrico
484.O ácido muriático é muito usado em
limpeza doméstica e de peças metálicas (decapagem). Sua fórmula molecular e seu nome
oficial são, respectivamente:
a) HClO, ácido clórico.
b) HCl, ácido clorídrico.
c) HCl, ácido clórico.
d) HClO3, ácido clorídrico
e) HClO, ácido clorídrico.
492. O ácido cianídrico é o gás de ação venenosa mais rápida que se conhece: uma concentração de 0,3 mg (miligrama) por litro de ar é
imediatamente mortal. É o gás usado nos estados americanos do norte que adotam a pena de
morte por câmara de gás. A primeira vítima foi
seu descobridor Carl Wilhelm Scheele, que morreu ao deixar cair um vidro contendo solução
de ácido cianídrico, cuja fórmula molecular é:
a) HCOOH
d) HCNO
b) HCN
e) H4[Fe(CN) 6]
c) HCNS
485.Dê o nome oficial dos ácidos abaixo:
a) H2S
b) H2Se
c) H2Te
493.A partir dos “ácidos chaves” abaixo,
monte a fórmula de seus ácidos derivados:
c) HIO3
a) HClO3
b) HBrO3
494.As seguintes soluções aquosas são ácidos
comuns encontrados em laboratórios:
1. HClO2
3. HClO
2. HClO3
4. HClO4
Assinale a alternativa que apresenta, respectivamente, os nomes corretos dos ácidos
mencionados acima.
a) Ácido clórico; ácido cloroso; ácido perclórico; ácido hipocloroso
b) Ácido hipocloroso; ácido perclórico; ácido
cloroso; ácido clórico
c) Ácido cloroso; ácido clórico; ácido clorídrico; ácido perclórico
d) Ácido cloroso; ácido clórico; ácido hipocloroso; ácido perclórico
e) Ácido clorídrico; ácido clórico; ácido hipocloroso; ácido perclórico
495.Dê o nome oficial do ácido-chave (oxiácido-padrão) e escreva a fórmula molecular e o
nome de seu derivado:
a) H2SO4
b) H2SeO4
c) H2TeO4
d) HNO3
496.Associe corretamente as duas colunas e
assinale a alternativa correta.
I.
H2SO4: ácido sulfúrico
II. HCl: ácido clorídrico
III. HClO2: ácido cloroso
IV. HClO4: ácido perclórico
V. H2S: ácido sulfídrico
(A) hidrácido, monoácido, forte, volátil
(B) hidrácido, diácido, fraco, volátil
(C) oxiácido, monoácido, forte, volátil
(D) oxiácido, diácido, forte, fixo
(E) oxiácido, monoácido, semiforte, volátil
a) I – A; II – B; III – C; IV – D; V – E
b) I – D; II – B; III – E; IV – C; V – A
c) I – D; II – A; III – E; IV – C; V – B
d) I – E; II – D; III – C; IV – B; V – A
e) I – C; II – A; III – D; IV – E; V – B
EM1D-10-34
497. Os nomes dos ácidos oxigenados abaixo
são, respectivamente:
HNO2, HClO3, H2SO3, H3PO4
a) nitroso, clórico, sulfuroso, fosfórico.
b) nítrico, clorídrico, sulfúrico, fosfórico.
c) nítrico, hipocloroso, sulfuroso, fosforoso.
d) nitroso, perclórico, sulfúrico, fosfórico.
e) nítrico, cloroso, sulfúrico, hipofosforoso.
498.Escreva:
a) as fórmulas moleculares do ácido hipoiodoso e do ácido perbrômico;
b) o nome dos compostos de fórmulas H2SO3
e H3PO4.
499. Dê o nome dos seguintes ácidos (aquosos):
a) HBrO3
b) HBrO2
c) HBrO
d) H3AsO3
500.(Vunesp) Ácidos instáveis são ácidos
que se decompõem parcial ou totalmente sob
condições normais de temperatura e pressão,
formando, quase sempre, como produtos de
decomposição, água líquida e um gás. Entre
os pares de ácidos relacionados, é constituído
apenas por ácidos instáveis:
a) H2SO4 e H3PO4.
b) HNO3 e H3BO3.
c) HClO4 e HBr.
d) HI e HF.
e) H2CO3 e H2SO3.
501.Assinale a alternativa que apresenta os
seguintes ácidos: ácido perclórico, ácido fosforoso, ácido periódico e ácido fosfórico.
a) HClO4, H3PO3, HIO3, H3PO3
b) HClO4, H3PO2, HIO4, H3PO4
c) HClO4, H3PO3, HIO4, H3PO4
d) HClO3, H3PO3, HIO3, H3PO3
e) HClO3, H3PO3, HIO4, H3PO4
502.Dê a fórmula estrutural dos ácidos fosfórico, fosforoso e hipofosforoso e indique quais
são os hidrogênios ionizáveis.
Dados: H
P
O
503.Dê a fórmula molecular, a fórmula estrutural e o número de hidrogênios ionizáveis
dos ácidos:
Dados: H
C
a) Ácido fosforoso
b) Ácido carbônico
P
O
504.Monte a fórmula molecular e a estrutural
de cada um dos oxiácidos.
Dados:
H
N
P
O
S
a) Ácido fosforoso
b) Ácido hipofosforoso
c) Ácido nítrico
d) Ácido sulfúrico
505. Alguns elementos, o carbono, por exemplo, formam um único ácido oxigenado, outros, como cloro, enxofre, nitrogênio e fósforo, formam números variáveis de oxiácidos. Observe o exemplo do cloro
e complete a tabela que se segue:
Elemento
Cloro
Bromo
Iodo
Enxofre
Selênio
Telúrio
Fósforo
Boro
Nitrogênio
Carbono
Ácidos oxigenados
Nome oficial
HClO4
Ácido perclórico
HClO3
Ácido clórico
HClO2
Ácido cloroso
HClO
Ácido hipocloroso
506.Dados os ânios abaixo, dê o respectivo nome de cada um, formule e nomeie o ácido correspondente.
Ânion
Nome do ânion
Fórmula do ácido
Nome do ácido
ClO–
Hipoclorito
H+ClO– → HClO
Ácido
hipocloroso
CNO–
IO2–
SO42–
H2PO2–
HPO32–
MnO4–
BrO3–
Cr2O72–
NO3–
CO32–
MnO42–
PO3–
ClO4–
507. Dado o ácido, monte sua fórmula molecular, determine e nomeie o ânion correspondente,
como indicado no modelo abaixo:
Nome do ácido
Fórmula do ácido
Ânion correspondente
Nome do ânion
correspondente
Ácido perclórico
HClO4
H+ClO4– → ClO4–
Perclorato
Ácido hipofosforoso
Ácido carbônico
Ácido sulforoso
Ácido nítrico
Ácido nitroso
Ácido fosforoso
Ácido bórico
Ácido pirofosfórico
Ácido iodoso
Ácido hipocloroso
Ácido ortofosfórico
EM1D-10-34
Ácido metafosfórico
Ácido silícico
508. Escreva a fórmula molecular e dê o nome dos
ácidos correspondentes aos seguintes ânions:
a) F–
d) SO42–
b) Br–
e) PO43–
–
c) NO3
f) CO32–
509.Consultando a tabela de íons, escreva a
fórmula e o nome dos ácidos correspondentes
aos ânions abaixo:
a) Cianeto
b) Cloreto
c) Sulfito
d) Fosfato
e) Sulfato
f) Nitrito
g) Nitrato
510. Pesquise o nome dos ácidos HCl e HClO4 e, por
analogia, escreva o nome dos ácidos HI e HIO4.
511. Dado o ácido abaixo:
H2CO3
a) dê o seu nome oficial;
b) escreva o ânion correspondente;
c) dê o nome deste ânion;
d) monte a sua fórmula estrutural.
Dados: H
O
512. Consulte a tabela de ânions e, para todos
os ácidos oxigenados do fósforo, monte a fórmula molecular, dê o nome oficial e a respectiva fórmula estrutural de cada um.
513.Complete o quadro abaixo:
Fórmula do ácido
C
Nome do ácido
HF
HCl
HBr
HI
H2S
HCN
HNO3
HNO2
H2SO4
H2SO3
H2CO3
Ácido fosfórico (Ácido ortofosfórico)
Ácido fosforoso
Ácido hipofosforoso
Ácido metafosfórico
Ácido pirofosfórico
Ácido hipocloroso
Ácido cloroso
Ácido clórico
Ácido perclórico
Ácido bórico
Ácido permangânico
Ácido dicrômico
Ácido acético (Ácido etanoico)
514. Complete o quadro abaixo.
Dados: H
B
O
Fórmula molecular
e nome do ácido
Mn Cr
Fórmula
Ânions
estrutural derivados
Ácido
hipocloroso
516.Complete o quadro a seguir dando o nome
e a representação do ânion, a fórmula do ácido
e seu respectivo nome.
Ânions e
nomes
Fórmula
do ácido
Nome do
ácido
F–
Cl–
Ácido cloroso
Br–
Ácido clórico
I–
Ácido
perclórico
S2–
H3BO3
CN–
HMnO4
NO–3
H2Cr2O7
Metafosfato
515.Complete a tabela abaixo:
Ânion
Pirofosfato
Iodeto
Fluoreto
Hipoclorito
Clorato
Fosfito
Arsenato
Permanganato
Silicato
Pirossulfato
Bromito
Fosfato
EM1D-10-34
Bicarbonato
Carga
Representação
Hipoclorito
Clorato
Perclorato
Borato
Permanganato
Dicromato
Acetato
(Etanoato)
517. O que é grau de hidratação de um oxiácido? Exemplifique.
518. Alguns ácidos oxigenados podem formar
três ácidos com diferentes graus de hidratação. Estes ácidos recebem prefixos: orto, meta
e piro. O prefixo piro corresponde ao ácido
que apresenta:
a) menor teor de água na molécula.
b) teor de água intermediário entre o orto
e o meta.
c) maior teor de água na molécula.
d) teor de água maior que o orto.
e) teor de água menor que o meta.
519. O ácido pirofosfórico apresenta a seguinte fórmula molecular: H4P2O7. As fórmulas dos
ácidos metafosfórico e ortofosfórico são, respectivamente:
d) H3PO3 e H3PO4.
a) HPO3 e H3PO4.
b) H2PO3 e H3PO4.
e) H4PO4 e HPO2.
c) HPO3 e H4P2O5.
524.Ao se dissociar em água destilada o ácido
ortofosfórico (H3PO4), resulta, como ânion:
a) PO43– (aq), ortofosfato.
b) PO4 + (aq), fosfato.
c) PO43+ (aq), ortofosfato.
d) PO42– (aq), fosfito.
e) HPO32– (aq), hidrogenofosfato.
520.A fórmula molecular do ácido xico é
H3XO3. Qual será a fórmula molecular do:
a) Ácido ortoxico?
b) Ácido metaxico?
c) Ácido piroxico?
525.Conhecendo a fórmula do ácido pirocrômico (H2Cr2O7), comumente chamado de ácido
dicrômico, escreva as fórmulas dos ácidos ortocrômico e metacrômico.
521. A alternativa que indica a correspondência
certa entre a fórmula e o nome de cada ácido é:
1. H3PO3 2. H4P2O7 3. H6Si2O7 4. H2SiO3
5. HBO2 6. H3BO3 7. H4B2O5
A. Ácido ortofosfórico
B. Ácido pirofosfórico
C. Ácido metassilícico
D. Ácido metafosfórico
E. Ácido metabórico
F. Ácido ortobórico
G. Ácido ortofosforoso
H. Ácido persilícico
I. Ácido pirossilícico
a) 2-B, 3-H, 4-C, 5-H, 7-D
b) 2-B, 3-H, 4-C, 5-F, 7-D
c) 1-G, 2-B, 3-I, 5-E, 6-F
d) 1-G, 2-B, 3-H, 5-E, 6-F
e) 1-A, 2-B, 3-I, 5-E, 7-F
522.Escreva a fórmula molecular das substâncias em solução aquosa.
a) Ácido (orto) fosfórico
b) Ácido fosforoso
c) Ácido hipofosforoso
d) Ácido metafosfórico
e) Ácido pirofosfórico
f) Ácido arsênico
g) Ácido crômico
523.O elemento fósforo forma vários ácidos,
dos quais destacamos o ácido metafosfórico,
HPO3, e o ácido pirofosfórico, H4P2O7. Lembrando que num oxiácido, o hidrogênio ionizável,
H +, está sempre ligado ao oxigênio, monte a
fórmula estrutural desses ácidos.
Dados: H
P
O
526.Monte a fórmula molecular dos ácidos
abaixo.
a) Ácido mangânico
b) Ácido permangânico
c) Ácido crômico
d) Ácido dicrômico
527. Dê o nome e/ou as fórmulas dos respectivos ácidos.
a) Ácido ortofosfórico
b) Ácido metabórico
c) H2MnO4
d) H2SiO3
528.Escreva a fórmula molecular dos seguintes ácidos:
a) Ácido permangânico
b) Ácido metarsênico
c) Ácido nítrico
d) Ácido hipobromoso
529. A respeito da substância HCl observa-se,
experimentalmente, que:
• é um gás incolor, de odor forte e irritante;
• está presente no suco gástrico do estômago humano;
• aparece no comércio com o nome de ácido
muriático, sendo utilizada na limpeza de pisos;
• a maioria de suas moléculas sofre ionização em solução aquosa.
Desse modo, pode-se concluir que:
a) o HCl é uma substância iônica.
b) o HCl é um ácido fraco.
c) o HCl é um gás não-tóxico.
d) a ionização pode ser resumida pela equação:
+
−
HC l (g)
H (aq) + Cl (aq) .
Água
e) o suco gástrico não é ácido.
530.Qual das substâncias a seguir apresenta
sabor azedo quando em solução aquosa e está
presente no suco gástrico?
d) HCl
a) Na2S
b) NaCl
e) NaOH
c) CaO
531.O vinagre tem caráter ácido, pois nele
encontramos, predominantemente:
a) Ácido sulfídrico. d) Ácido carbônico.
b) Ácido nítrico.
e) Ácido sulfúrico.
c) Ácido acético.
532.Sejam os produtos:
I.
água de bateria;
II. água mineral com gás;
III. ácido muriático;
IV. cheiro de ovo podre.
Os ácidos presentes nesses produtos são,
respectivamente:
a) HCl, H2CO3, H2SO4 e H2SO3.
b) H3PO4, H2SO4, HCl e HCN.
c) H2SO4, H3PO4, HF e HI.
d) HCl, H2CO3, HF e H2SO4.
e) H2SO4, H2CO3, HCl e H2S.
533.Cite dois ácidos utilizados nos refrigerantes do tipo “cola”.
534.Faça a correspondência:
(( )Ácido sulfúrico
(( )Ácido fluorídrico
(( )Ácido fosfórico
(( )Ácido nítrico
(( )Ácido clorídrico
a) É usado na limpeza doméstica e de peças
metálicas.
b) Ácido usado como desidratante e na solução de baterias.
c) É o ácido utilizado na indústria de explosivos e corantes.
d) Ácido utilizado como acidulante em refrigerantes, goma de mascar e balas.
e) Devido à capacidade de corroer o vidro, é
muito usado na indústria para gravar e obter
efeitos especiais nesse material.
EM1D-10-34
535.Leia o texto e aponte o ácido a que ele
se refere.
“É muito tóxico e, concentrado no ar, é mortal, tem odor de amêndoas amargas, foi usado
no extermínio em massa dos judeus nas câmaras
de gás durante a Segunda Grande Guerra mundial e, ainda hoje, é utilizado em alguns Estados
norte-americanos para matar os condenados à
pena de morte nas câmaras de gás.”
a) Sulfídrico
d) Sulfúrico
b) Cianídrico
e) Fosfórico
c) Carbônico
536.As características de três ácidos inorgânicos são apresentadas a seguir.
1o) É o ácido do suco gástrico e, quando impuro, é chamado de ácido muriático, usado na limpeza de pisos, paredes e superfícies metálicas.
2o) É um ácido bastante instável, isto é,
decompõe-se com muita facilidade em gás carbônico e água. Está presente nas águas minerais gaseificadas, refrigerantes e cervejas.
3o) Apresenta odor de ovo podre, enegrece
objetos de prata e é muito venenoso, pois bloqueia as vias respiratórias e a respiração.
Esses ácidos são, respectivamente:
a) H2CO3, H2S e HCl. d) H2CO3, H2S e HCN.
b) HCl, H2CO3 e H2S. e) H2S, HNO2 e HCl.
c) H2CO3, HCl e H2S.
537. O estômago produz o suco gástrico de caráter ácido para digerir os alimentos ingeridos
pelo indivíduo, porém, em alguns casos, como
de doença ou estresse, há uma produção excessiva de suco, podendo causar gastrite ou úlcera.
Em casos de produção excessiva, além de uma
mudança na dieta alimentar, o médico poderá
indicar uma medicação de caráter básico para
neutralizar o efeito da acidez estomacal. O
principal componente do suco gástrico é o:
a) Ácido sulfúrico. d) Ácido cloroso.
b) Ácido sulfídrico. e) Ácido clórico.
c) Ácido clorídrico.
538.A tabela a seguir apresenta a classificação das substâncias inorgânicas de maior produção nos Estados Unidos, em 1999.
Classificação
Produto
1 lugar
Ácido sulfúrico
2o lugar
Amônia
3 lugar
Ácido fosfórico
4 lugar
Ácido nítrico
o
o
o
As fórmulas químicas das substâncias
classificadas em 1o, 3o e 4o lugares são, respectivamente:
a) H2S, H3PO2 e HNO3
b) H2SO4, H3PO3 e HNO3
c) H2SO4, H3PO4 e HNO2
d) H2SO4, H3PO4 e HNO3
e) H2S, H3PO4 e HNO3
539. Associe a 2a coluna à 1a, considerando os
ácidos:
1. H4P2O7
2. H3PO3
3. H3PO4
4. HClO2
5. HClO3
6. HClO4
7. H2SO3
8. HNO2
a) Fosfórico
b) Fosforoso
c) Nitroso
d) Nítrico
e) Hipofosforoso
f) Pirofosfórico
g) Sulfuroso
h) Cloroso
i) Perclórico
j) Clórico
k) Sulfúrico
A sequência correta das combinações é:
a) 1e – 2f – 3a – 4h – 5b – 6j – 7g – 8d
b) 1f – 2c – 3b – 4j – 5h – 6i – 7a – 8c
c) 1b – 2e – 3f – 4i – 5j – 6h – 7g – 8d
d) 1c – 2b – 3f – 4j – 5i – 6h – 7a – 8d
e) 1f – 2b – 3a – 4h – 5j – 6i – 7g – 8c
540.Leia atentamente o texto a seguir.
Coca-Cola desentope pias?
É muito comum ouvirmos alguém indicar
Coca-Cola para desentupir pias. Será que resolve? O prof. José Atílio Vanin, do Instituto de
Química da Universidade de São Paulo, prestou
alguns esclarecimentos sobre o assunto em matéria publicada no Jornal da USP.
Desentupir pias, a Coca-Cola não desentope,
contrariando o dito popular. A Coca-Cola é um
extrato vegetal de composição variável, ao qual é
adicionado ácido fosfórico em pequena quantidade, como conservante. A confusão se dá porque
esse ácido é usado por fabricantes de material
de limpeza, mas não faz mal ao ser humano.
Nas reações químicas que ocorrem nas células,
várias delas usam o fosfato, que é um componente do ácido fosfórico, explica Vanin. A célula
usa o fosfato no mecanismo de fornecimento de
energia celular, mas há uma ressalva: “O excesso
de fosfato pode reagir com o cálcio, componente
de ossos e dentes, e causar problemas ósseos ou
dentários”. Nada além disso. Segundo o professor, também o excesso de absorção de carboidratos refinados pode causar cáries nos dentes.
Jornal da USP, 3 a 9 de setembro de 1998, p.7.
Escreva a fórmula molecular, o nome oficial e a aplicação do ácido citado na constituição desse refrigerante e indique o outro ácido
que está sempre presente na composição dos
refrigerantes.
541.Defina bases, segundo Arrhenius, e
exemplifique sua dissociação iônica.
542.Leia atentamente o texto:
Alunos tomam soda cáustica durante
aula e passam mal.
Dezesseis alunos de uma escola particular
de Sorocaba, interior de São paulo, foram internados após tomar soda cáustica(hidróxido de
sódio) durante uma aula de química. Os alunos
participavam de um exercício chamado “teste
do sabor”: já haviam provado vinagre, H3CCOOH,
leite de magnésia, Mg(OH)2 , e, por insistência,
provaram a soda cáustica, NaOH, produto utilizado na limpeza doméstica. Em pouco tempo, os
alunos já começaram a sentir os primeiros sintomas: ardência na língua e no estômago, e foram
encaminhados ao Hospital Modelo da cidade.
Adaptado do Diário do Grande
ABC On-line, 19/9/2005.
Agrupe as substâncias citadas segundo
sua funções inorgânicas e indique os íons de
cada uma em solução aquosa.
543.Escreva a equação de dissociação iônica
das seguintes bases.
a) Al(OH)3
b) Mg(OH)2
c) NaOH
d) Ca(OH)2
544. Determine os íons que podemos obter na
dissociação das bases a seguir:
a) Ni(OH)3
b) Ca(OH)2
c) NaOH
545. A única base inorgânica volátil, solúvel
em água, com baixíssimo grau de ionização
em água é:
a) NaOH
b) Ca(OH)2
c) Al(OH)3
d) Fe(OH)3
e) NH4OH
546. Na preparação da argamassa, utiliza-se a
base hidróxido de cálcio, conhecido como cal
extinta ou cal apagada, cuja fórmula é:
a) Ca(OH)2
b) CaO
c) KCl
d) CO2
e) K2O
547. Observe as substâncias a seguir:
1. HCl
2. NaOH
3. Ca(NO3)2
4. NH3
5. C12H22O11
Podemos afi rmar que, em solução aquosa,
são bases de Arrhenius:
a) 1 e 3.
b) 1 e 4.
c) 4 e 5.
d) 3 e 4.
e) 2 e 4.
548. Coloque as bases em ordem crescente de
solubilidade: NaOH, Ca(OH)2 e AgOH.
549. Dê a fórmula molecular e escreva a equação de dissociação da única base inorgânica,
fraca e solúvel em água.
550. Um elemento M forma dois cátions: M + e
M2+. Escreva as fórmulas das bases formadas
por M.
551. Dê as equações de dissociação iônica
para as seguintes bases:
a) NaOH
b) Ca(OH)2
c) LiOH
d) Al(OH)3
e) Pt(OH)4
552. A base hidróxido de amônio é a única
base inorgânica volátil, decompondo-se em
amônia e água, segundo a equação:
⟨NH4OH⟩ (aq) NH3(g) + H2O(l)
Escreva a fórmula estrutural das substâncias presentes na equação mostrada.
553. Faça as fórmulas ou dê nome às seguintes bases:
a) Hidróxido de zinco
b) Hidróxido de alumínio
c) Ba(OH)2
d) KOH
e) NH4OH
554. Na experiência a seguir, compare o brilho das lâmpadas quando os eletrodos estiverem mergulhados em soluções aquosas de:
a) KOH
b) NH4OH
EM1D-10-34
555. Nas condições ambientes, pastilhas de
hidróxido de sódio, expostas ao ar durante
várias horas, transformam-se em um líquido
claro. Este fenômeno ocorre porque o hidróxido de sódio:
a) absorve água da atmosfera.
b) reage com o oxigênio do ar.
c) combina-se com o hidrogênio do ar.
d) reage com o nitrogênio do ar.
e) produz água ao se decompor.
556.Escreva os nomes oficiais das seguintes
bases:
a) NaOH
b) AgOH
c) Sr(OH)2
d) LiOH
e) CsOH
557. O hidróxido de amônio é uma base que
apresenta forte caráter covalente. Assinale a
afirmação que explica esse fato.
a) É uma base instável, que se decompõe em
NH3 e H2O.
b) É uma base solúvel e forte.
c) É uma base que apresenta metal.
d) Não é uma base.
e) Não é solúvel em água.
558.Assinale a alternativa que apresenta dois
produtos caseiros com propriedades alcalinas.
a) Suco de limão e vinagre.
b) Coca-Cola e leite.
c) Leite de magnésia e sabão.
d) Coca-Cola e água de cal.
e) As alternativas a e b estão corretas.
559.Faça a fórmula das bases:
a) Hidróxido de amônio
b) Hidróxido de zinco
c) Hidróxido de alumínio
560.Complete o quadro abaixo:
Fórmula da base
Nomenclatura
oficial
NaOH
Hidróxido de
potássio
Hidróxido de cálcio
NH4OH
561.Bases fortes são aquelas que são produzidas pela reação de seus respectivos metais
com água, formando gás hidrogênio:
→
Metal + H2O → base forte + H2
Os metais alcalinos reagem com água fria,
enquanto os alcalinoterrosos só reagem com
água quente (vapor). As bases de metais alcalinos e alcalinoterrosos são bases fortes, exceto
o Be(OH)2, que é considerado uma base fraca e
anfótera (reage com ácido e base).
O Be(OH)2 é uma base molecular, já que o
berílio é bivalente e faz duas ligações covalentes, não satisfazendo a teoria do octeto.
Com base nas informações acima, escreva a
fórmula estrutural:
a) Ca(OH)2
b) Be(OH)2
562.Faça as fórmulas ou dê nome às seguintes bases:
a) Hidróxido de estrôncio
b) Hidróxido de alumínio
c) Ba(OH)2
d) LiOH
e) NH4OH
563.Escreva a fórmula dos seguintes compostos:
a) Hidróxido de sódio
b) Hidróxido de cálcio
c) Hidróxido de amônio
d) Hidróxido de alumínio
e) Hidróxido de zinco
f) Hidróxido de magnésio
564.Classifique as bases descritas de acordo
com a força e a solubilidade em água.
a) RbOH
b) Ba(OH)2
c) Fe(OH)2
d) NH4OH
565.Um elemento A, de nome natal, forma
duas bases: uma com Nox = + 2 e outra com
Nox = + 3. Aplicando a nomenclatura usual,
que nomes você daria a essas bases?
566.Dê o nome usual às bases abaixo:
a) CuOH
b) Fe(OH)3
c) Ni(OH)2
d) Pb(OH)4
e) Sn(OH)4
f) AuOH
567. Complete o quadro abaixo:
Fórmula da base
Nomenclatura oficial
Nomenclatura usual
Ni(OH)3
Hidróxido de cobalto III
Hidróxido estânico
Au(OH)2
Hidróxido de platina IV
Hidróxido cuproso
Co(OH)2
Hidróxido de níquel II
Hidróxido áurico
Fe(OH)3
EM1D-10-34
568.Monte a fórmula de cada uma das bases
abaixo:
a) Hidróxido de amônio
b) Hidróxido ferroso
c) Hidróxido plumboso
d) Hidróxido platínico
e) Hidróxido áurico
f) Hidróxido cúprico
571. O papel de tornassol, vermelho e umedecido, torna-se azul quando em contato com
vapores de:
a) iodo.
b) álcool etílico.
c) cloreto de hidrogênio.
d) cloro.
e) soda cáustica.
569.Da caverna ao arranha-céu, o homem
percorreu um longo caminho. Da aldeia, passou à cidade horizontal e, desta, à verticalização. O crescente domínio dos materiais e o
conhecimento de processos químicos tiveram
papel fundamental nesse desenvolvimento.
Uma descoberta muito antiga e significativa foi o uso de Ca(OH) 2 para a preparação da
argamassa. O Ca(OH) 2 tem sido muito usado,
também, na pintura de paredes, processo
conhecido como caiação, em que, reagindo
com um dos constituintes minoritários do
ar, forma carbonato de cálcio de cor branca.
Dê o nome oficial e comercial do Ca(OH) 2 e
escreva a equação de dissociação dessa base
em água.
572.Num determinado experimento, três
soluções aquosas, límpidas e transparentes
estavam acondicionadas em três recipientes
distintos A, B e C. Para caracterizar essas
substâncias, um cientista utilizou apenas
o indicador fenolftaleína (incolor) e observou que, nos recipientes A e C, não houve
nenhuma alteração, porém, no recipiente B,
ocorreu o aparecimento de uma coloração
avermelhada.
Em função do exposto, assinale a alternativa correta.
a) As soluções dos recipientes A e C são ácidas.
b) Somente a solução do recipiente B é básica.
c) As soluções dos recipientes A e C são neutras.
d) As soluções dos recipientes A e C são básicas.
e) Com os dados fornecidos no texto, não
se pode definir o caráter ácido ou básico das
soluções.
570.Um alvejante de solução de amônia é
branco, entretanto, se adicionarmos solução
de fenolftaleína, adquire coloração:
a) amarela.
d) verde.
b) rosa.
e) laranja.
c) azul.
573.Num recipiente contendo uma substância
A, foram adicionadas gotas de fenolftaleína,
dando-lhe coloração rósea. Adicionando-se
uma substância B em A, a solução apresenta-se incolor. Com base nessas informações, podemos concluir que:
a) A e B são bases.
b) A é um ácido e B é uma base.
c) A é uma base e B é um ácido.
d) A e B são ácidos.
e) A e B são sais neutros.
574. Complete o quadro abaixo, indicando a
cor de cada solução abaixo:
Indicador
Vinagre
Leite de
magnésia
Fenolftaleína
Tornassol azul
576. O hidróxido de magnésio em água (leite de magnésia) é consumido como laxante e
antiácido. De acordo com a equação a seguir,
pede-se apontar a soma das afirmativas corretas sobre o Mg(OH)2.
H 2O
Mg(OH)2(s) Mg2+ (aq) + 2 OH– (aq)
01.É uma substância básica.
02.Em água, é pouco solúvel.
04.Em água, produz uma solução neutra.
08.Em água, produz um cátion e dois ânions.
16.Tem duas cargas positivas e uma negativa.
32.Dissolvê-lo em água é um processo químico.
577. Faça a correspondência correta entre a
base e sua respectiva aplicação:
1. NaOH
3. Mg(OH)2
2. Ca(OH)2
4. NH4OH
a) Usada na preparação da argamassa;
b) Produzida a partir do NaCl;
c) Comercializada como leite de magnésia;
d) Base fraca que só existe em solução.
579.Assinale a associação correta do ácido ou
da base com sua utilização.
a) Ácido sulfúrico, usado em refrigerantes
gaseificados.
b) Amônia, usada na fabricação de produtos
de limpeza doméstica.
c) Ácido clorídrico, usado em baterias de automóveis.
d) Hidróxido de sódio, utilizado como antiácido estomacal.
580.Sabor adstringente (característica dos
hidróxidos) é o que percebemos quando comemos uma banana verde (não madura). Que
substância abaixo teria sabor adstringente?
Corel Stock Photos
575. Um estudante de química fez um teste com
duas amostras de água, de procedências diferentes. No primeiro copo, adicionou fenolftaleína e
a solução permaneceu incolor. No segundo copo,
adicionando o mesmo composto, a solução ficou
vermelha. O que se pode concluir?
578.Qual das bases abaixo é utilizada na extração da celulose e na obtenção do papel?
a) Hidróxido de amônio
b) Hidróxido de cálcio
c) Hidróxido de sódio
d) Hidróxido de alumínio
e) Hidróxido de lítio
a) CH3COOH
b) NaCl
c) Al(OH)3
d) C12H22O11
e) H3PO4
581.Quantidades adequadas de hidróxido de
magnésio podem ser usadas para diminuir a
acidez estomacal. Qual ácido, presente no estômago, é o principal responsável pelo baixo
pH do suco gástrico? Escreva a equação de
dissociação do hidróxido de magnésio.
Informação: baixo pH significa elevada
acidez e vice-versa.
582.O suco gástrico necessário à digestão
contém ácido clorídrico que, em excesso, pode
Respostas
457. Número de cátions igual ao número de
ânions, correto.
Eletricamente neutra, correto
Não conduz eletricidade, falsa.
458.D
459.D
460.C
461. D
1
= 0,1= 10%
10
2
H2SO4 : a = = 0, 67 = 67%
3
8
HNO3 : a = = 0, 8 = 80%
10
H S < H2SO4 < HNO3
∴ 2
Força ácida
462.a) H2S : a =
HO
2
b) HNO3 (l)
H+ (aq) + NO3− (aq)
463.E
464.D
465.E
466.D
467. C
EM1D-10-34
468.A
469.Ácido é todo composto que, em solução aquosa, ioniza-se, produzindo, exclusivamente como cátion, o H +. Atualmente,
sabemos que o H + se une à molécula de água
formando o cátion H 3O + (hidrônio ou hidroxônio).
Exemplo
HCl H+ + Cl– ou
HCl + H2O H3O + + Cl–
470.Hidrácidos – Não possuem oxigênio: HCl,
HBr, HCN.
Oxiácidos – Possuem oxigênio: H2SO4,
HNO3, HClO3.
471. Monoácidos: HCl, HBr, HNO3, H3PO2 (exceção: dos 3 H só 1 H +)
Diácidos: H2S, H3PO3 (exceção: dos 3 H só
2 H +)
Triácidos: H3PO4
Tetrácidos: H4SiO4, H4P2O7
472.E
473. a)
b)
c)
d)
e)
Hidrácido, monoácido, forte
Oxiácido, diácido, moderado
Oxiácido, diácido, moderado
Hidrácido, diácido, fraco
Oxiácido, triácido, moderado
c) Ácido telurídrico
474. C
475.Hidrácidos: ácidos sem oxigênio.
Ácidos fortes: HI > HBr > HCl
Ácido moderado: HF
Ácido fraco: HCN
486.a) H – F
b)
c) H – C ≡ N
Oxiácidos: ácidos com oxigênio.
m = no O – no H +
Ácidos fortes: m=3 e m=2 → HClO 4,
HMnO 4, HNO3, H2SO 4
Ácido moderado: m=1 → H3PO4, H2SO3,
H3PO3 (2H +), H3PO2 (1H +)
Ácido fraco : m = 0 → HClO, H3BO3
476. a)
b)
c)
d)
e)
f)
Hidrácido, monoácido, moderado
Oxiácido, triácido, forte
Oxiácido, diácido, forte
Hidrácido, diácido, fraco
Oxiácido, triácido, moderado
Hidrácido, tetrácido, fraco
477. D
488.H +Br– → HBr = ácido bromídrico
H + S–
→ H2S = ácido sulfídrico
H + CN– → HCN = ácido cianídrico
489.a) Ácido clorídrico: H – Cl
b) Ácido sulfídrico:
S
c) Ácido cianídrico: H – C ≡ N
478.D
479. Apenas 1, o qual está ligado ao oxigênio.
480.V, V, F, F e V
481.a)
b)
c)
d)
e)
487. Elementos do grupo VI A que formam ácidos: S, Se e Te.
H + S–
→ H2S = ácido sulfídrico
H + Se– → H2Se = ácido selenídrico
H +Te– → H2Te = ácido telurídrico
HF
HCl
HBr
HI
HCN
482.Ácido cianídrico:
H + CN– = HCN
Ácido isocianídrico:
H + NC– = HNC
São hidrácidos, ácidos sem oxigênio.
483.C, D, B e A
484.C
485.a) Ácido sulfídrico
b) Ácido selenídrico
490.a)
b)
c)
d)
e)
f)
g)
Ácido fluorídrico
Ácido clorídrico
Ácido cianídrico
Ácido sulfídrico
Ácido iodídrico
Ácido bromídrico
Ácido isocianídrico
491. a) H +[Fe(CN) 6]3– = H3[Fe(CN) 6]
b) H +[Fe(CN) 6]4– = H4[Fe(CN) 6]
492.B
493.a) HClO4 = ácido perclórico
HClO2 = ácido cloroso
HClO = ácido hipocloroso
b) HBrO4 = ácido perbrômico
HBrO2 = ácido bromoso
HBrO = ácido hipobromoso
c) HIO4 = ácido periódico
HIO2 = ácido iodoso
HIO = ácido hipoiodoso
494.D
495.a) H2SO4: ácido sulfúrico
H2SO3: ácido sulfuroso
b) H2SeO4: ácido selênico
H2SeO3: ácido selenoso
c) H2TeO4: ácido telúrico
H2TeO3: ácido teluroso
d) HNO3: ácido nítrico
HNO2: ácido nitroso
496.C
497. A
498.a) Ácido hipoiodoso: HIO
Ácido perbrômico: HBrO4
b) H2SO3: ácido sulfuroso
H3PO4: ácido fosfórico
499.a)
b)
c)
d)
Ácido brômico
Ácido bromoso
Ácido hipobromoso
Ácido arsenioso
503.a) Ácido fosforoso
Fórmula molecular: H3PO3
Fórmula estrutural:
Número de hidrogênios ionizáveis
(ligados ao oxigênio): 2
b) Ácido carbônico
Fórmula molecular: H2CO3
Fórmula estrutural:
O
Número de hidrogênios ionizáveis
(ligados ao oxigênio): 2
504.a) Ácido fosforoso: H3PO3
O
H
500.E
C
O
P
O
H
H
b) Ácido hipofosforoso: H3PO2
501.C
502.H3PO4: ácido fosfórico (ácido-chave ou
oxiácido-padrão)
O
H
O
P
H
H
c) Ácido nítrico: HNO3
T
O
H3PO3: ácido fosforoso (ácido fosfórico –
1 oxigênio)
2 H+
H3PO2: ácido hipofosforoso (ácido fosfórico – 2 oxigênios)
1 H+
H
O
N
O
d) Ácido sulfúrico: H2SO4
O
H
O
S
O
O
H
EM1D-10-34
505.
Elemento
Bromo
Iodo
Enxofre
Selênio
Telúrio
Fósforo
Boro
Nitrogênio
Carbono
Ácidos oxigenados
Nome oficial
HBrO4
Ácido perbrômico
HBrO3
Ácido brômico
HBrO2
Ácido bromoso
HBrO
Ácido hipobromoso
HIO4
Ácido periódico
HIO3
Ácido iódico
HIO2
Ácido iodoso
HIO
Ácido hipoiodoso
H2SO4
Ácido sulfúrico
H2SO3
Ácido sulfuroso
H2SeO4
Ácido selênico
H2SeO3
Ácido selenoso
H2TeO4
Ácido telúrico
H2TeO3
Ácido teluroso
H3PO4
Ácido fosfórico
H3PO3
Ácido fosforoso
H3PO2
Ácido hipofosforoso
H3BO3
Ácido bórico
HNO3
Ácido nítrico
HNO2
Ácido nitroso
H2CO3
Ácido carbônico
506.
Ânion
Nome do ânion
Fórmula do ácido
Nome do ácido
CNO–
Cianato
H+CNO– → HCNO
Ácido ciânico
IO2–
Iodito
H+IO2– → HIO2
Ácido iodoso
SO42–
Sulfato
H+SO42– → H2SO4
Ácido sulfúrico
H2PO2–
Hipofosfito
H+H2PO2– → H3PO2
Ácido hipofosforoso
Fosfito
H HPO3 → H3PO3
Ácido fosforoso
MnO4–
Permanganato
H+MnO4– → HMnO4
Ácido permangânico
BrO3–
Bromato
H+BrO3– → HBrO3
Ácido brômico
Cr2O72–
Dicromato
H+Cr2O72– → H2Cr2O7
Ácido dicrômico
NO3–
Nitrato
H+NO3– → HNO3
Ácido nítrico
Carbonato
H CO3 → H2CO3
Ácido carbônico
MnO42–
Manganato
H+MnO42– → H2MnO4
Ácido mangânico
PO3–
Metafosfato
H+PO3– → HPO3
Ácido metafosfórico
ClO4–
Perclorato
H+ClO4– → HClO4
Ácido perclórico
HPO3
2–
CO3
2–
2–
+
+
2–
507.
Nome do ácido
Fórmula
do ácido
Ânion
correspondente
Nome do ânion
correspondente
Ácido hipofosforoso
H3PO2
H2PO2–
Hipofosfito
Ácido carbônico
H2CO3
CO
Ácido sulfuroso
H2SO3
SO32–
Sulfito
Ácido nítrico
HNO3
NO3–
Nitrato
Ácido nitroso
HNO2
NO
Nitrito
Ácido fosforoso
H3PO3
HPO32–
Fosfito
Ácido bórico
H3BO3
BO33–
Borato
Ácido pirofosfórico
H4P2O7
P2O74–
Pirofosfato
Ácido iodoso
HIO2
IO2–
Iodito
Ácido hipocloroso
HClO
ClO
Hipoclorito
Ácido ortofosfórico
H3PO4
PO43–
Ortofosfato
Ácido metafosfórico
HPO3
PO
–
3
Metafosfato
Ácido silícico
H4SiO4
4–
4
SiO
Silicato
2–
3
–
2
–
Carbonato
EM1D-10-34
508.a) H +F– → HF: ácido fluorídrico
b) H+Br– → HBr: ácido bromídrico
c) H + NO3– → HNO3: ácido nítrico
d) H + SO42– → H2SO4: ácido sulfúrico
e) H +PO43– → H3PO4: ácido fosfórico
f) H + CO32– → H2CO3: ácido carbônico
510. HCl: ácido clorídrico → HI: ácido iodídrico.
HClO4: ácido perclórico → HIO4: ácido periódico
509.a) HCN: ácido cianídrico
b) HCl: ácido clorídrico
c) H2SO3: ácido sulfuroso
d) H3PO4: ácido fosfórico (ácido ortofosfórico)
e) H2SO4: ácido sulfúrico
f) HNO2: ácido nitroso
g) HNO3: ácido nítrico
512. Ácido
511. a) Ácido carbônico
b) H2CO3 → H + CO32– → ânion correspondente: CO32–
c) Ânion carbonato
Fórmula molecular
Ácido fosfórico
H3PO4
Ácido fosforoso
H3PO3
d)
H O
C
O
H O
Fórmula estrutural
H
H
H
O
O
O
H
O
H
O
H
Ácido hipofosforoso
H3PO2
P
P
O
H
O
O
P
H
O
H
O
Ácido metafosfórico
H
HPO3
P
O
H
Ácido pirofosfórico
O
O
O
H4P2O7
H
O
O
P
O
P
H
O
O
H
513.
Fórmula
do ácido
Fórmula
do ácido
Nome do ácido
HF
Ácido fluorídrico
H3PO3
Ácido fosforoso
Ácido hipofosforoso
Nome do ácido
HCl
Ácido clorídrico
H3PO2
HBr
Ácido bromídrico
HPO3
Ácido metafosfórico
HI
Ácido iodídrico
H4P2O7
Ácido pirofosfórico
H 2S
Ácido sulfídrico
HClO
Ácido hipocloroso
HCN
Ácido cianídrico
HClO2
Ácido cloroso
HNO3
Ácido nítrico
HClO3
Ácido clórico
HNO2
Ácido nitroso
HClO4
Ácido perclórico
H2SO4
Ácido sulfúrico
H3BO3
Ácido bórico
H2SO3
Ácido sulfuroso
HMnO4
Ácido permangânico
H2CO3
Ácido carbônico
H2Cr2O7
Ácido dicrômico
H3PO4
Ácido fosfórico
(Ácido ortofosfórico)
H3C – COOH
Ácido acético
(Ácido etanóico)
514.
Fórmula molecular e
nome do ácido
Fórmula estrutural
Ânions derivados
HClO
Ácido hipocloroso
H – O – Cl
ClO– Hipoclorito
HClO2
Ácido cloroso
H – O – Cl → O
ClO–2 Clorito
HClO3
Ácido clórico
H
O
O
Cl
ClO–3 Clorato
O
O
HClO4
H
Ácido perclórico
O
Cl
O
ClO–4 Perclorato
O
H3BO3
H
Ácido bórico
O
O
H
O
H
B
BO33 – Borato
O
HMnO4
H
Ácido permangânico
O
Mn
O
MnO–4 Permanganato
O
O
EM1D-10-34
H2Cr2O7
Ácido dicrômico
H
O
Cr
O
O
O
Cr
O
O
H
Cr2O72– Dicromato
515.
Ânion
Carga
Representação
Pirofosfato
4–
P2O7
Iodeto
1–
I
Fluoreto
1–
F
Hipoclorito
1–
ClO
Clorato
1–
ClO3
Fosfito
2–
HPO3
Arsenato
3–
AsO4
Permanganato
1–
MnO4
Silicato
4–
SiO4
Pirossulfato
2–
S2O7
Bromito
1–
BrO2
Fosfato
3–
PO4
Bicarbonato
1–
HCO3
516.
Ânions e nomes
Fórmula do ácido
Nome do ácido
F–
Fluoreto
HF
Ácido fluorídrico
Cl–
Cloreto
HCl
Ácido clorídrico
Br–
Brometo
HBr
Ácido bromídrico
I– Iodeto
HI
Ácido iodídrico
S2–
Sulfeto
H 2S
Ácido sulfídrico
CN–
Cianeto
HCN
Ácido cianídrico
NO–3
Nitrato
HNO3
Ácido nítrico
PO–3
Metafosfato
HPO3
Ácido metafosfórico
ClO–
Hipoclorito
HClO
Ácido hipocloroso
ClO–3
Clorato
HClO3
Ácido clórico
ClO–4
Perclorato
HClO4
Ácido perclórico
BO33 –
Borato
H3BO3
Ácido bórico
MnO–4
Permanganato
HMnO4
Ácido permangânico
Dicromato
H2Cr2O7
Ácido dicrômico
Acetato (etanoato)
H3C – COOH
Ácido acético (etanoico)
Cr2O72– H3C – COO–
517. O grau de hidratação é o número de “moléculas de água” que podem ser retiradas da
fórmula do composto que origina o oxiácido,
e, para tanto, utilizamos os prefixos orto,
meta e piro para diferenciá-los.
Exemplos
H3PO4 = ácido fosfórico ou ácido ortofosfórico
−
H2O
= ácido metafosfórico
HPO3
2 ⋅ H3PO4 = H6P2O8
Ácido
fosfórico
ou ácido
ortofosfórico
H6P2O8
−
H2 O
= ácido pirofosfórico
H4P2O7
518. B
519. A
520. a) H3XO3
b) HXO2
c) H4X2O5
521.C
522.a)
b)
c)
d)
e)
f)
g)
H3PO4
H3PO3
H3PO2
(H3PO4 – H2O) = HPO3
(2 · H3PO4 – H2O) = H4P2O7
H3AsO4
H2CrO4
523.Fórmula estrutural: H4P2O7
H
O
O P
H O
O
O H
P O
O H
Fórmula estrutural: HPO3
O
O
H
P
O
524.A
EM1D-10-34
525.Ácido ortocrômico = H2CrO4
Ácido metacrômico = não é possível (não
perde água).
526. a)
b)
HMnO4
c)
d)
Ácido mangânico: H+MnO42– = H2MnO4
Ácido permangânico: H +MnO4– =
Ácido crômico: H + CrO42– = H2CrO4
Ácido dicrômico: H+Cr2O72– = H2Cr2O7
527. a) Ácido ortofosfórico: H3PO4 (também
pode ser chamado de ácido fosfórico)
b) Ácido metabórico: HBO2
c) H2MnO4: ácido mangânico
d) H2SiO3: ácido metassilícico
528.a)
b)
c)
d)
Ácido permangânico: HMnO4
Ácido metarsênico: HAsO3
Ácido nítrico: HNO3
Ácido hipobromoso: HBrO
529.D
531.C
530.D
532.E
533.O ácido carbônico e o ácido fosfórico.
534.B, E, D, C e A
537. C
535.B
538.D
536.B
539. E
540.O ácido fosfórico, H3PO4, acidulante
em bebidas refrigerantes. O outro ácido que
está presente nas águas minerais gaseificadas, refrigerantes e cervejas é o H2CO3, ácido
carbônico, um ácido bastante instável, isto
é, decompõe-se com muita facilidade em gás
carbônico e água.
541.Para Arrhenius, as bases (também chamadas de álcalis) são compostos que, em solução aquosa, dissociam-se ionicamente, liberando como ânions, exclusivamente, íons
hidroxila (OH–)
NaOH(s) → Na + (aq) + OH– (aq)
Fe(OH)3(s) Fe3+ (aq) + 3 OH– (aq).
542.– Vinagre: H3CCOOH: ácido
H3CCOOH(aq) H3CCOO– (aq) + H + (aq)
– Leite de magnésia, Mg(OH)2, e soda
cáustica, NaOH : bases.
Mg(OH)2(s) Mg2+ (aq) + 2 OH– (aq)
NaOH(s) → Na + (aq) + OH– (aq)
543.a) Al (OH)3(s) Al3+(aq) + 3 OH– (aq)
b) Mg(OH)2(s) Mg2+ (aq) + 2 OH– (aq)
c) NaOH(s) → Na + (aq) + OH– (aq)
d) Ca(OH)2(s) → Ca2+ (aq) + 2 OH– (aq)
544.a) Ni e OH
b) Ca2+ e OH–
c) Na + e OH–
3+
545.E
550.M + OH–⇒ MOH
M2+ OH– ⇒ M(OH)2
Íon hidróxido é sempre 1–: OH–
551.a) NaOH
Na + + OH–
–
546.A
2
b)
547. E
548.AgOH < Ca(OH)2 < NaOH
c) LiOH
Li + + OH–
H2 O
d) Al(OH)3
Al3 + + 3 OH−
HO
2
e) Pt(OH)4
Pt 4 + + 4 OH−
549.NH4OH
NH4OH NH4 + + OH–
552.
�
553.a)
b)
c)
d)
e)
Zn(OH)2
Al(OH)3
Hidróxido de bário
Hidróxido de potássio
Hidróxido de amônio
560.
Fórmula da base
Nomenclatura
oficial
NaOH
Hidróxido
de sódio
KOH
554.a) Brilho intenso, (base forte), alta
concentração de íons livres.
b) Brilho fraco (base fraca), baixa concentração de íons.
555.A
556.a) Hidróxido de sódio
b) Hidróxido de prata
c) Hidróxido de estrôncio
d) Hidróxido de lítio
e) Hidróxido de césio
557. A
558.C
559. a) NH4OH
b) Zn(OH)2
c) Al(OH)3
Ca(OH)2
NH4OH
Hidróxido de
potássio
Hidróxido
de cálcio
Hidróxido de
amônio
561.a) Ca2+ [O–H] –
[O–H] –
b) H – O – Be – O – H
562.a)
b)
c)
d)
e)
Sr(OH)2
Al(OH)3
Hidróxido de bário
Hidróxido de lítio
Hidróxido de amônio
563.a) NaOH
b) Ca(OH)2
c) NH4OH
d) Al(OH)3
e) Zn(OH)2
f) Mg(OH)2
564.a) Forte e solúvel
b) Forte e pouco solúvel
c) Fraca e insolúvel
d) Fraca e solúvel
565.A(OH)2 – hidróxido de natal II ou nataloso
A(OH)3 – hidróxido de natal III ou natálico
567. Fórmula da base
568.a)
b)
c)
d)
e)
f)
566.a) CuOH: hidróxido cuproso
b) Fe(OH)3: hidróxido férrico
c) Ni(OH)2: hidróxido niqueloso
d) Pb(OH)4: hidróxido plúmbico
e) Sn(OH)4: hidróxido estânico
f) AuOH: hidróxido auroso
Nomenclatura oficial
Nomenclatura usual
Ni(OH)3
Hidróxido de níquel III
Hidróxido niquélico
Co(OH)3
Hidróxido de cobalto III
Hidróxido cobáltico
Sn(OH)4
Hidróxido de estanho IV
Hidróxido estânico
Au(OH)2
Hidróxido de ouro II
Hidróxido auroso
Pt(OH)4
Hidróxido de platina IV
Hidróxido platínico
CuOH
Hidróxido de cobre I
Hidróxido cuproso
Co(OH)2
Hidróxido de cobalto II
Hidróxido cobaltoso
Ni(OH)2
Hidróxido de níquel II
Hidróxido niqueloso
Au(OH)3
Hidróxido de ouro III
Hidróxido áurico
Fe(OH)3
Hidróxido de ferro III
Hidróxido férrico
NH4+OH– → NH4OH
Fe2+ OH– → Fe(OH)2
Pb2+ OH– → Pb(OH)2
Pt4+ OH– → Pt(OH)4
Au3+ OH– → Au(OH)3
Cu2+ OH– → Cu(OH)2
569.Nome oficial: hidróxido de cálcio.
Nomes comerciais: cal hidratada, cal extinta e cal apagada.
Dissociação iônica:
574.
Indicador
Vinagre
Leite de
magnésia
Fenolftaleína
Incolor
Rosa
Tornassol azul
Vermelho
Azul
572.B
575.1o copo: como a solução ficou incolor com
fenolftaleína, pode ser ácida ou neutra.
2o copo: como a solução ficou vermelha
com fenolftaleína, podemos garantir que esta
é básica.
Obs. – A solução do 1o copo poderia ser
levemente básica, pois a viragem da fenolftaleína ocorre em pH ≅ 8 (levemente básica a
25 °C).
573.C
576.11 (01 + 02 + 08)
H 2O
Ca(OH)2(s) → Ca2+ (aq) + 2 OH– (aq)
570.B
571. E
EM1D-10-34
577. 1-B, 2A, 3-C, 4-D
586.A
578.C
587.a) O chá-mate comporta-se como um
indicador, alterando sua coloração na presença de um ácido (limão).
b) Para voltar à coloração inicial, deveremos neutralizar o ácido, e, para tal, uma
substância de caráter básico deve ser utilizada.
579.B
580.C
581.HCl
H 2O
Mg(OH)2 Mg2+ + 2 OH–
582.C
583.E
588.a) Ácido fosfórico: H3PO4
Hidróxido de magnésio: Mg(OH)2
b)
HO
2
H3PO4 (ácido) ⇒ H3PO4
3 H+ + PO34 −
HO
584.São corretas: A, B, C, D
585.D
2
Mg(OH)2 (base) ⇒ Mg(OH)2
Mg2 + + 2 OH−
589.Qual é a fórmula molecular dos sulfetos e
dos fluoretos de metais alcalinoterrosos (M)?
Dados: números atômicos S = 16 e F = 9.
590.(Fuvest-SP) Um elemento metálico M forma um cloreto de fórmula MCl 3. A fórmula de
seu sulfato é:
a) M2SO4
c) M2(SO4)3
e) M(SO4)3
b) MSO4
d) M(SO4)2
591. Uma pessoa consome, por ano, em média,
por meio da alimentação, de 3 a 5 kg de sal (a
média mundial é 5 kg, mas o Brasil fica em 3 kg,
segundo dados da Associação Brasileira de Extratores e Refinadores de Sal – Abersal). A falta de
sódio gera fraquezas, apatia, náuseas e cãibras. O
excesso dele também é prejudicial, pois, à medida
que o organismo retém água, o líquido aumenta o
volume sanguíneo, provocando a hipertensão.
Considerando essas informações e seu
conhecimento químico sobre essa substância, assinale a alternativa incorreta.
a) O sal de cozinha é a reunião entre moléculas de sódio e moléculas de cloro.
b) O sal pode ser obtido na reação entre o ácido clorídrico (HCl) e a soda cáustica (NaOH).
c) O sal apresenta um aglomerado de íons
na sua estrutura, ocasionado pela transferência de elétrons de um átomo de Na para
um átomo de Cl.
d) O sal de cozinha comercializado é uma
mistura, pois apresenta iodo e outros componentes em sua composição.
593.Uma solução aquosa de ácido sulfúrico
foi adicionada a uma solução aquosa de hidróxido de sódio, ocorrendo a neutralização
total. Depois da evaporação da água, restou
um composto sólido.
Escreva a equação que representa a reação
ocorrida.
595. (FGV-SP) A reação: x Ca(OH)2 + y H2SO4 →
→ z A + w B, depois de corretamente balanceada,
resulta para a soma x + y + z + w no número:
a) 4
b) 5
c) 6
d) 7
e) 10
596. Para a produção do sal K2SO4, é necessária
a reação entre as seguintes substâncias e seus
respectivos coeficientes estequiométricos:
a) HNO3 + K(OH)2
b) H2SO4 + 2 KOH
c) 2 H2SO4 + 1 KOH
d) H2SO3 + KOH
e) H2SO3 + K2OH
597. Equacione as equações de neutralização
total.
a) Ácido fosforoso e leite de magnésia
b) Ácido hipofosforoso e água de cal
c) Ácido pirofosfórico e soda cáustica
d) Ácido metafosfórico e hidróxido de amônio
e) Ácido bórico e hidróxido estânico
598.
Wikimedia
592.Escolha a alternativa que contém exclusivamente sais.
a) HCl – H2S – H2O
b) NaBr – CaO – H3PO2
c) Ca 3(PO4)2 – P2O5 – Na2SO4
d) Al2(SO4)3 – LiCl – Ca(NO3)2
e) HBr – NaBr – Na2O
594.Neutraliza-se uma solução aquosa de ácido nítrico com amônia. Com a evaporação da
água, cristaliza-se o composto:
a) NH4NO3
b) NH3NO2
c) NH3NO3
d) NO3
e) NH3
Os fogos de artifício, que iluminam as noites festivas, apresentam elementos químicos
que possuem elétrons, os quais são excitados
com a explosão da pólvora. O retorno do elétron ao estado fundamental emite um fóton
de energia luminosa ou outra radiação eletromagnética. As diferentes cores dos fogos de
artifício são provenientes da combustão do
clorato ou perclorato de potássio combinados
com sais de metais, como: nitrato, carbonato
ou sulfato de estrôncio, que, após excitação,
emitem luz com coloração vermelha; nitrato,
clorato ou carbonato de bário, que emitem
luz verde; nitrato de magnésio (luz branca);
carbonato ou sulfeto de cobre II (luz verde),
carbonato de sódio (luz amarela).
Marque a alternativa que contém as fórmulas corretas de alguns compostos citados no
texto.
a) KClO3, SrCO3, Ba(NO3)2, Mg(NO3)2, CuSO4,
Na2CO3
b) KCl, Sr(NO3)2, BaCO3, MgNO3, CuSO4, Na2CO3
c) KClO4, SrCO3, Ba(ClO3)2, MgNO3, CuS, Na2CO3
d) KClO3, SrSO4, BaCO3, Mg(NO3)2, CuS, Na2CO3
e) KClO3, Sr(NO2)2, BaCO3, Mg(NO3)2, CuCO3,
NaCO3
602.Monte a fórmula dos sais a seguir.
a) Cloreto férrico
b) Sulfato plumboso
c) Nitrito de potássio
d) Perclorato de sódio
e) Sulfeto de cádmio
f) Sulfito de bário
g) Carbonato de cromo III
599.(Fuvest-SP)Faça o que se pede a seguir.
a) Dê os nomes dos compostos representados
pelas fórmulas H2SO4 e NH3.
b) Escreva a equação da reação entre esses
compostos e dê o nome do sal normal formado.
a) permanganato de potássio, sulfito de magnésio e hipoclorito de sódio.
b) manganato de potássio, sulfato de magnésio e clorito de sódio.
c) ácido mangânico, sulfito de magnésio e
clorato de sódio.
d) permanganato de potássio, sulfato de
magnésio e hipoclorito de sódio.
e) manganato de potássio, sulfato de magnésio e cloreto de sódio.
600. À reação total entre ácido cloroso, HClO2,
e hidróxido de cálcio, Ca(OH)2, dá-se o nome de
____________________ e forma-se um composto
cuja fórmula e nome corretos são, respectivamente, ____________e ____________________ .
a) ionização – CaClO2 – clorato de cálcio
b) ionização – Ca(ClO) – hipoclorito de cálcio
c) neutralização – Ca(ClO2) – clorito de cálcio
d) desidratação – CaCl2 – cloreto de cálcio
e) neutralização – CaClO2 – clorato de cálcio
601.O molibdato de amônio é usado como
fonte de molibdênio para o crescimento das
plantas. Sabendo que este elemento, de símbolo Mo, pertence à mesma família do cromo,
Cr, e que a fórmula do íon cromato é CrO2–
,
4
monte a fórmula deste sal.
603.As substâncias I, IV e VI são, respectivamente, denominadas oficialmente de:
Substância
Aplicação
I.
KMnO4
Agente bactericida
II.
NaNO3
Aditivo alimentar
III.
H3BO3
Água boricada
IV.
MgSO4
Ação laxativa
V.
KI
Preventivo para
evitar o bócio
VI.
NaClO
Água sanitária
VII.
NH4OH
Produtos de limpeza
604.Na Idade Média, era usual o emprego de
óxido de chumbo (IV) como pigmento branco em telas. Em nossos dias, com o aumento do teor de H2S na atmosfera, proveniente
da queima de combustíveis fósseis, pinturas
dessa época passaram a ter suas áreas brancas
transformadas em castanho escuro, devido à
formação de sulfeto de chumbo II. No trabalho
de restauração dessas pinturas, são empregadas soluções diluídas de peróxido de hidrogênio, que transformam o sulfeto de chumbo II
em sulfato de chumbo IV, um sólido branco.
Monte as fórmulas do sulfeto de chumbo II e
do sulfato de chumbo IV e indique os nomes
usuais de cada um desses sais.
605.(Fuvest-SP) A seguir aparecem os nomes
alquímicos e os nomes modernos de três compostos químicos: natro = carbonato de sódio,
sal de Epson = sulfato de magnésio e sal de
Glauber = sulfato de sódio. O elemento químico comum às três substâncias é:
a) H
d) C
b) Na
e) O
c) S
606. A fórmula com o respectivo nome correto que se obtém ao se fazer a combinação
entre os íons Fe2+, Fe3+ OH– e SO42– é:
a) Fe2(SO4)3; sulfato de ferro III.
b) Fe(OH)2; hidreto ferroso.
c) KSO4; sulfato de potássio.
d) Fe(OH)2; hidróxido férrico.
e) Fe2SO4; sulfato de ferro II.
607.(Fuvest-SP) Bromato de potássio, sulfito
de amônio, iodeto de sódio e nitrito de bário
são representados, respectivamente, pelas seguintes fórmulas:
a) KBrO3, (NH4)2SO3, NaI, Ba(NO2)2.
b) KBrO4, (NH4)2SO3, NaI, Ba(NO2)2.
c) KBrO3, (NH4)2SO3, NaI, Ba(NO3).
d) KBrO3, (NH4)2SO3, NaIO3, Ba(NO2)2.
e) KBrO3, (NH4)2SO4, NaI, Ba(NO2)2.
608.O fosfato de cálcio é um sólido branco
usado na agricultura como fertilizante. Ele
pode ser obtido pela reação entre hidróxido
de cálcio e ácido fosfórico. As fórmulas do hidróxido de cálcio, ácido fosfórico e fosfato de
cálcio são, respectivamente:
a) Ca(OH), HPO4, CaPO4.
b) Ca(OH)2, H3PO4, Ca2(PO4)3.
c) Ca(OH)2, H2PO4, CaPO4.
d) Ca(OH), H3PO4, CaPO4.
e) Ca(OH)2, H3PO4, Ca 3(PO4)2.
EM1D-10-44
609. (UFRGS-RS) No processo de produção do sal
refinado, a lavagem do sal marinho provoca a
perda do iodo natural, sendo necessário, depois,
acrescentá-lo na forma de iodeto de potássio.
Outra perda significativa é a de íons
magnésio, presentes no sal marinho na forma de cloreto de magnésio e sulfato de
magnésio. Durante esse processo, são também adicionados alvejantes como o carbonato de sódio.
As fórmulas representativas das substâncias destacadas acima são, respectivamente:
a) KI, MgCl, MgSO4 e NaCO3.
b) K2I, MgCl2, Mg2SO4 e NaCO3.
c) K2I, Mg2Cl, MgSO4 e Na(CO3)2.
d) KI, MgCl2, MgSO4 e Na2CO3.
e) KI2, Mg2Cl, Mg(SO4)2 e NaCO3.
610. Assinale a alternativa em que existe correlação entre a fórmula e o nome dos compostos.
a) NH4CNO – cianeto de amônio
b) Ca2(NO3)3 – nitrato de cálcio
c) KBrO3 – bromato de potássio
d) NaClO – clorato de sódio
e) Al2S3 – sulfito de alumínio
611.O NaNO3, componente da pólvora, e o
Al(OH)3, antiácido estomacal, são, respectivamente:
a) nitrato de sódio e hidróxido de alumínio.
b) nitrato de sódio e óxido de alumínio.
c) nitrito de sódio e óxido de alumínio.
d) nitrito de sódio e hidróxido de alumínio.
e) citrato de sódio e óxido de alumínio.
612.Os íons Fe (II) e Co (III) combinam-se
com os ânions nitrato, cloreto, sulfato e cianeto e formam compostos salinos. Assinale
as alternativas em que esses compostos estão
corretamente formulados:
a) Fe(NO3)2, FeCl2, FeSO4, Fe(CN)2, Co(NO3)3,
CoCl 3, Co2(SO4)3, Co(CN)3.
b) Fe3(NO3)2, FeCl2, Fe(SO4)2, FeCN, Co(NO3)3,
CoCl 3, Co2(SO4)3, Co(CN)2.
c) FeNO3, FeCl2, Fe3(SO4)2, FeCN, Co(NO3)2,
CoCl, Co2(SO4)3, Co(CN)3.
d) Fe(NO3)2, FeCl, Fe(SO4)2, FeCN, CoNO3, Co3Cl3,
Co(SO4)3, Co2(CN)3.
613. Os sais apresentam solubilidades diferenciadas em água, basicamente em função
das espécies envolvidas e da temperatura.
Dessa forma, a detecção de íons Ba2+, numa
solução aquosa, pode ser feita adicionando-se
outra solução tendo íons:
a) cloreto.
d) nitrato.
b) amônio.
e) sulfato.
c) brometo.
614.(PUC-SP) Um estudante pretende separar
os componentes de uma amostra contendo três
sais de chumbo II: Pb(NO3)2, PbSO4 e PbI2, após
analisar a tabela de solubilidade a seguir.
Solubilidade em água
Substância
Fria
Quente
Iodeto de
chumbo II
Insolúvel
Solúvel
Nitrato de
chumbo II
Solúvel
Solúvel
Sulfato de
chumbo II
Insolúvel
Insolúvel
Estão corretas as afirmativas:
a) I e III.
d) II e IV.
b) I, II e IV.
e) I, III e IV.
c) II, III e IV.
616.(Vunesp) Acetato de chumbo (II), sulfato de alumínio, cloreto de amônio e nitrato
de sódio são alguns dos sais usados na preparação de soluções saturadas para banho-maria. As fórmulas desses sais são, respectivamente:
a) PbAc; AlS; NH2Cl; NaNO4.
b) Pb2(CH3COO)3; Al2S3; NH4Cl; Na 3N.
c) Pb2CH3COO; Al2(SO3)3; NH3Cl; NaNO3.
d) CH3CO2; Al2SO3; NH3Cl2; NaNO2.
e) Pb(CH3COO)2; Al2(SO4)3; NH4Cl; NaNO3.
Ele propôs o seguinte procedimento:
“Adicionar água destilada em ebulição à mistura, agitando o sistema vigorosamente. Filtrar
a suspensão resultante, ainda quente. Secar o
sólido obtido no papel de filtro; este será o sal A.
Recolher o filtrado em um béquer, deixando-o
esfriar em banho de água e gelo. Proceder a uma
nova filtração e secar o sólido obtido no papel
de filtro; este será o sal B. Aquecer o segundo
filtrado até a evaporação completa da água; o
sólido resultante será o sal C.”
Os sais A, B e C são, respectivamente:
a) Pb(NO3)2, PbSO4 e PbI2.
b) PbI2, PbSO4 e Pb(NO3)2.
c) PbSO4, Pb(NO3)2 e PbI2.
d) PbSO4, PbI2 e Pb(NO3)2.
e) Pb(NO3)2, PbI2 e PbSO4.
617. São pouco solúveis em água os seguintes
pares de sais:
d) K2CrO4 e Na2CrO4.
a) BaCl2 e PbCl2.
b) MgSO4 e BaSO4.
e) AgBr e PbS.
c) PbSO4 e Pb(NO3)2 .
615.Analise as afirmativas abaixo sobre as
propriedades gerais de várias substâncias
inorgânicas.
619. São solúveis em água os seguintes pares
de sais:
a) BaCl2 e PbCl2.
b) MgSO4 e BaSO4.
c) PbSO4 e Pb(NO3)2.
d) K2CrO4 e Na2CrO4.
e) AgBr e PbS.
I.
Os nitratos, os acetatos e os sais de metais alcalinos são solúveis em água.
II. Os Cl–, Br– e I–, em geral, são insolúveis
em água, com exceção de PbCl2, AgBr e Hg2I2,
que apresentam boa solubilidade.
III. Os sulfetos, em geral, são insolúveis em
água.
IV. Os carbonatos, em geral, apresentam
boa solubilidade em água, exceto os de metais
alcalinos, que são muito insolúveis.
618.Dê as fórmulas e indique a solubilidade
dos sais:
a) permanganato de potássio;
b) oxalato de cálcio;
c) iodeto de potássio;
d) sulfato de amônio;
e) borato de sódio;
f) sulfato ferroso;
g) nitrato de prata;
h) perclorato de potássio;
i) cloreto de prata.
620.Assinale a alternativa que apresenta
apenas sais solúveis:
a) NaBr, (NH4)2SO4, (NH4)3PO4 e (NH4)2S.
b) Hg2I2, KNO3, PbSO4 e Ca(CN)2.
c) AgBr, PbSO4, Fe2S3 e Ca 3(PO4)2.
d) LiNO3, CaCO3, PbBr2 e AgCl.
e) (NH4)2CO3, KCl, NaNO3 e AgI.
621.São citados abaixo diversos sais. Agrupe-os, segundo a solubilidade em água: NaCl,
Ca(NO3)2, CaCO3, Na2CO3, AgBr, KI, PbCl 2, BaS,
Na 3PO4, Al2S3, (NH4)2S, Fe(CN)3.
Sal solúvel
Sal insolúvel
622.Qual é a alternativa que apresenta apenas sais insolúveis?
a) NaBr, (NH4)2SO4, (NH4)3PO4, e (NH4)2S.
b) KNO3, Li2SO4, CaI2 e NaCN.
c) AgBr, PbSO4, Fe2S3 e Ca 3(PO4)2.
d) (NH4)2CO3, KCl, NaNO3 e AgI.
e) Hg2I2, KNO3, PbSO4 e Ca(CN)2.
623.Escreva as equações de neutralização
total do ácido e da base, dê o nome do sal
formado e classifique-o quanto à solubilidade
em água:
a) ácido sulfuroso e hidróxido de ferro III;
b) ácido bromídrico e hidróxido de cálcio.
624.Consulte a tabela de solubilidade em
água e classifique os sais abaixo:
e) AgCl
a) Na2S
b) BaS
f) PbCl2
c) CaS
g) CaCO3
d) CaCl2
625. Associe a primeira coluna com a segunda e
assinale a alternativa que representa a sequência correta de I a V.
I.
Sal neutro.
II. É uma base fraca e solúvel.
III. Sal ácido.
IV. É um dos produtos da reação do ácido clorídrico com zinco metálico.
V. É um ácido forte.
(A)N H4OH
(B)H2
(C)NaCl
(D)H NO3
(E)NaHSO4
a) I–A, II–B, III–C, IV–D, V–E
b) I–E, II–A, III–D, IV–C, V–B
c) I–B, II–A, III–C, IV–D, V–E
d) I–C, II–A, III–E, IV–B, V–D
626.Embora os avanços de tecnologia das telecomunicações tenham sido muito grandes
no século passado, o papel continua sendo um
dos meios mais eficazes de difusão e de registro do conhecimento humano. Na produção
da matéria-prima utilizada pela indústria do
papel, destacam-se a solução de hidrogenossulfito de cálcio e o cloro gasoso como branqueadores e do sulfito de cálcio, que dá nome
a um dos tipos de papel, o sulfite. Considerando essa informação e os conhecimentos sobre
funções inorgânicas, monte a fórmula molecular dos sais citados no texto, indicando todos
os possíveis nomes de cada um deles.
627. Os íons carbonato e bicarbonato, juntamente com o gás carbônico dissolvido, ajudam
a manter a acidez do sangue dentro dos padrões normais para o funcionamento saudável do corpo humano. Represente esses íons
e escreva a fórmula e o nome oficial dos compostos formados pela combinação de cada um
deles com o cátion sódio.
628.O hidrogenocarbonato de sódio, conhecido comercialmente como bicarbonato de
sódio, é usado como antiácido estomacal por
ser capaz de reagir com o excesso de ácido clorídrico, presente no suco gástrico, resultando
em um sal e um gás responsável pela eructação (“arroto”). Qual é o nome do sal produzido
nessa reação?
EM1D-10-44
629. Aftas são feridas que aparecem na língua
e na parte interna da boca por causa do excesso
de acidez na saliva. É costume popular “queimá-las” (termo impróprio, do ponto de vista científico) com bicarbonato de sódio ou fazer um
gargarejo com uma solução aquosa desse composto. O fundamento desse “saber popular” está
no fato de o íon bicarbonato, graças à hidrólise,
produzir solução básica, a qual consegue neutralizar a acidez bucal responsável pelas aftas.
Qual é a fórmula do bicarbonato de sódio e como
podemos classificar essa substância?
630.(Vunesp) Os sais nitrato de estrôncio,
hidrogenossulfito de alumínio, sulfato de antimônio (III) e clorato de bário são utilizados
em diferentes fogos de artifício. As fórmulas
desses compostos são, respectivamente:
a) SrNO2, AsHSO2, Sb2(SO3)3, BaClO2
b) Sr(NO3)2, AlHSO3, At2(SO4)3, BaClO4
c) SrNO3, AsHSO3, Sb(SO4)3, BaClO3
d) Sr(NO3)2, Al(HSO3)3, Sb2SO4, Ba(ClO4)2
e) Sr(NO3)2, Al(HSO3)3, Sb2(SO4)3, Ba(ClO3)2
631.Sulfato de potássio, hidrogenofosfato de cálcio, sulfato de amônio e nitrato de
amônio são compostos químicos que fazem
parte de misturas usadas como fertilizantes
na agricultura.
a) Escreva as fórmulas químicas desses compostos.
b) A qual função inorgânica pertencem esses compostos? Qual é a classificação de cada
um deles?
632. Quando se reage 1 mol de hidróxido de
potássio, KOH , com 1 mol de ácido fosfórico,
H3PO4, e 1 mol da mesma base com 1 mol de ácido sulfúrico, H2SO4, obtêm-se, respectivamente:
a) KH2PO4 e KHSO4.
b) K2HPO4 e KHSO3.
c) K 3HPO4 e K2SO3.
d) KH2PO3 e K2SO4.
e) K2HPO3 e K2SO4.
c) 3 mols de NaH2PO4.
d) 2 mols de Na 3PO3.
e) 1 mol de NaH2PO2 e 1 mol de Na2HPO3.
636.Com relação aos ácidos, bases e sais, pode-se afirmar que:
(( )em água, a ionização completa do ácido fos.
fórico é representada por H3PO4 3 H+ + PO3–
4
(( )cloreto de amônio em água produz uma
solução aquosa contendo íons cloreto e íons
amônio.
(( )o composto NaH2PO4 denomina-se hidrogenofosfato dissódico.
(( )na neutralização de um ácido por meio de
uma base ocorre: H + (aq) + OH– (aq) → H2O(l).
637. Sobre a classificação do sais, considere as
seguintes proposições:
I.
MgBrCl é um sal duplo quanto ao ânion.
II. NaKSO4 é um sal duplo quanto ao cátion.
III. NaCl é um sal ácido.
IV. Mg(OH)Cl é um sal básico.
V. NaHCO3 é um sal neutro.
Assinale a alternativa correta.
a) Apenas uma proposição é incorreta.
b) Apenas as proposições I e II são corretas.
c) Apenas as proposições III e IV são corretas.
d) Apenas as proposições I, II e IV são corretas.
e) Todas as proposições são corretas.
638.Complete, corretamente, o quadro abaixo:
Fórmula
Cu2CO3
Fe(OH)3
KHSO4
633.Escreva a equação da reação entre 1 mol
de H3PO4 e 1 mol de KOH e dê o nome do sal
formado.
Mg(NO3)2
634.Complete a equação a seguir e dê o nome
do sal formado: 1 CuOH + 1 H2S.
NH4MnO4
635.(Vunesp) A reação de 1 mol de ácido fosfórico, H3PO4, com dois mols de hidróxido de
sódio NaOH produz:
a) 2 mols de Na 3PO4.
b) 1 mol de Na2HPO4.
Nomenclatura
Na2S
CuSO4 · 5 H2O
KAl(SO4)2
639. O que são sais duplos? Exemplifique.
640. O que são sais hidratados? Exemplifique.
641. Classifique os sais abaixo quanto à presença de oxigênio, ao número de elementos químicos constituintes, à natureza dos íons presentes
e à presença de água em seu retículo.
a) Na2SO3
b) Ca(HCO3)2
c) CaSO4 · 2 H2O
d) MgSO4 · 2 H2O
648.Na correspondência entre fórmulas e
funções a que pertence, qual das alternativas
não está correta?
a) LiKSO4 é um sal ácido.
b) Ca(OH)Cl é um hidroxissal.
c) CaCl2 · 2 H2O é um sal hidratado.
d) NaHCO3 é um hidrogenossal.
e) KNO3 é um sal neutro.
642.Quais são a função inorgânica, o nome
e como podemos classificar a pedra-ume, atualmente conhecida como alúmem comum,
[KAl(SO4)2]?
649.Pela análise da tabela abaixo, é incorreto afirmar:
643.Associe corretamente, de cima para baixo, a coluna da esquerda com a da direita.
1. Na2B4O7 · 10 H2O
( ) sal básico
2. Ca(OH)Br
( ) sal duplo
3. K 3[Fe(CN) 6]
( ) sal ácido
4. MgHCO3 ( ) sal hidratado
644.Quantos elementos químicos compõem o
sulfato cúprico penta-hidratado?
645.Dos pigmentos conhecidos atualmente
como “azuis de ferro”, um deles é o hexacianoferrato (II) de ferro (III), também conhecido como ferrocianeto férrico. Monte a fórmula desse pigmento, indique a qual função
inorgânica pertence e classifique-o quanto à
presença de oxigênio, ao número de elementos
constituintes e à presença de água.
646.A hidroxiapatita [Ca5(PO4)3(OH)], sintetizada em laboratório, é utilizada para a preparação de implantes ósseos e dentários. Este
composto biocerâmico pode ser obtido por
meio de gotejamento de soluções de nitrato de
cálcio e de fosfato de amônio em uma solução
aquecida de nitrato de amônio.
a) Indique qual é a função inorgânica e classifique-a quanto à presença de oxigênio, ao
número de elementos, à natureza dos íons e à
presença de água.
b) Escreva a fórmula molecular do nitrato de
amônio.
EM1D-10-44
647. Escreva:
a) os nomes dos compostos NH4HCO3 e NaNO2;
b) as fórmulas dos compostos fosfito de sódio
e bissulfato de amônio.
Substância
Aplicação
I.
KMnO4
Agente bactericida
II.
NaNO3
Aditivo alimentar
III.
H3BO3
Água boricada
IV.
MgSO4
Ação laxativa
V.
KI
Preventivo para
evitar o bócio
VI.
NaClO
Água sanitária
VII.
NH4OH
Produtos de limpeza
a) I é bactericida devido à sua ação oxidante.
b) II é um sal proveniente da reação entre
uma base fraca e um ácido fraco.
c) III é classificada como um ácido fraco.
d) V é um sal solúvel em água.
e) VII torna cor-de-rosa a fenolftaleína.
650.(UFSCar-SP) Dentre as substâncias
cujas fórmulas são fornecidas a seguir:
NaHCO3, Mg(OH) 2 e CH 3COOH, pode(m) ser
empregada(s) para combater excesso de acidez estomacal:
a) NaHCO3, apenas.
b) Mg(OH)2, apenas.
c) CH3COOH, apenas.
d) NaHCO3 e Mg(OH)2, apenas.
e) NaHCO3, Mg(OH)2 e CH3COOH.
651.O reboco das paredes de casas pode ser
feito com a aplicação de uma pasta feita de
argamassa com água. A argamassa é uma
mistura de areia com cal extinta, Ca(OH) 2.
Nas paredes, a pasta vai endurecendo por
causa da evaporação da água e subseqüente
reação do hidróxido de cálcio com gás carbônico do ar. Além da areia, qual outra substância constitui o reboco seco? Qual é seu
nome oficial? Justifique com uma equação
química.
652.(UFMG) A acidez de uma limonada será
diminuída ao se colocar nela:
a) açúcar.
b) álcool.
c) bicarbonato de sódio.
d) sal.
e) vinagre.
653.A sequência numérica correta obtida na
associação das substâncias da coluna A com as
afirmações da coluna B, de cima para baixo, é:
A
B
1. BaSO4
(( )usada em alvejante doméstico
2. NaCl
(( )um dos componentes
do soro fisiológico
3. CaSO4
(( )usada como contraste
em radiografias de estômago
4. NaClO
(( )Adicionada ao sal de
cozinha
5. KI
(( )usada na fabricação de
giz
654.Os solos muito ácidos são, em geral, impróprios para o cultivo de vegetais. A correção da
acidez do solo poderia ser realizada pelos agricultores, por meio da adição de:
a) NH4NO3
d) CaCO3
b) KCl
e) (NH4)2SO4
c) BaCl2
655.Um fermento químico utilizado para fazer bolos é o bicarbonato de amônio, também
chamado carbonato ácido de amônio. Quando
aquecido, este sal se decompõe em dióxido de
carbono, amônia e água. Escreva a equação química desse processo, explique como esta reação
favorece o crescimento do bolo e indique a qual
função inorgânica pertence esse composto.
656.Dentre os sais presentes na água do mar,
aquele que também compõe o soro fisiológico
usado na reidratação de pessoas é o:
a) CaCO3
b) NaCl
c) MgCl2
d) MgSO4
e) NaI
657. Analise o texto: “NH4NO3 e KNO3 têm
sua utilização controlada por órgãos governamentais. Isso porque, se por um lado podem ser utilizados como (I), por outro são
(II)”.
Para completá-lo corretamente, as lacunas
(I) e (II) devem ser preenchidas, respectivamente, por:
a) alimentos e drogas psicotrópicas.
b) vernizes e explosivos.
c) fertilizantes e explosivos.
d) alvejantes e drogas psicotrópicas.
e) analgésicos e explosivos.
658.(Fuvest-SP) As esculturas de Rodin, expostas em São Paulo, foram feitas, em sua
maioria, em bronze e algumas em mármore.
Os principais componentes desses materiais
são:
Bronze
Mármore
a)
Cu, Zn
CaO
b)
Fe, Sn
CaCO3
c)
Fe, Zn
CaO
d)
Cu, Sn
CaSO4
e)
Cu, Sn
CaCO3
659.Relacionando as substâncias da coluna A
com as informações da coluna B, a sequência
numérica correta, encontrada em B, de cima
para baixo, é:
A
B
1) CaCO3
( ) Salitre, usado na
fabricação de fertilizantes
( ) Presente em antiácidos
( ) Um dos constituintes
3) Ca(OH)2
da casca de ovo
( ) Gesso, usado
4) NaHCO3
na ortopedia
( ) Cal extinta ou
5) CaSO4· 2 H2O
cal apagada
2) NaNO3
a) 1, 2, 3, 5, 4
b) 2, 5, 1, 4, 3
c) 2, 4, 1, 5, 3
d) 3, 4, 5, 1, 2
e) 3, 1, 5, 4, 2
660.Faça a correspondência entre a fórmula
da substância e sua respectiva aplicação listada logo a seguir.
e) NaClO
a) NaF
f) KCl
b) NaHCO3
g) H3PO4
c) HCl
d) KIO3
661.(Vunesp) Que são óxidos? Dar exemplo de
um óxido ácido e de um óxido básico. Indicar
a fórmula mínima e especificar, em cada caso,
se o óxido é molecular ou iônico.
662.Algumas substâncias químicas são conhecidas por nomes populares. Assim temos,
por exemplo, sublimado corrosivo (HgCl 2),
cal viva (CaO), potassa cáustica (KOH) e espírito de sal (HCl). O sublimado corrosivo,
a cal viva, a potassa cáustica e o espírito
de sal pertencem, respectivamente, às funções:
a) ácido, base, óxido e ácido.
b) sal, sal, base e ácido.
c) ácido, base, base e sal.
d) sal, óxido, base e ácido.
e) ácido, base, sal e óxido.
663.Para reciclar o alumínio, a partir de latinhas de refrigerantes descartadas, usam-se
apenas 5% da energia necessária para produzi-las a partir do óxido de alumínio presente
no minério bauxita. A fórmula de óxido de
alumínio é:
Dados os grupos: Al (IIIA ou 13); O (VIA
ou 16)
d) Al2O
a) AlO
e) Al2O3
b) AlO3
c) AlO2
664.Dê a nomenclatura correta para as substâncias: K2O, NaClO, Mg(OH)2 e CO2.
665.Escreva as fórmulas dos óxidos a seguir.
(( )Aditivo do sal de cozinha, exigido por
lei.
(( )Usado como desinfetante.
(( )Usado como acidulante em bebidas.
(( )Usado na prevenção contra as cáries.
(( )Usado na limpeza de pedras de mármores.
a) Óxido de lítio
d) Óxido de alumínio
b) Óxido de estrôncio e) Óxido de zinco
c) Óxido de cálcio
f) Óxido de prata
666.Escreva as fórmulas dos óxidos a seguir.
a) Monóxido de carbono
b) Dióxido de carbono
c) Dióxido de enxofre
d) Trióxido de enxofre
e) Dióxido de nitrogênio
f) Monóxido de nitrogênio
g) Tetróxido de dinitrogênio
h) Tetróxido de triferro
667. Escreva as fórmulas dos óxidos a seguir.
a) Óxido de manganês II
b) Óxido de manganês III
c) Óxido de manganês IV
d) Óxido de manganês VI
e) Óxido de manganês VII
f) Tetróxido de trimanganês
668.
I.
2 Nal + Cl2 → 2 NaCl + I2
II.
∆
CaCO3
→ CaO + CO
2
III. 3 CaO + P2O5 → Ca 3(PO4)2
IV. SO3 + H2O → H2SO4
A respeito dos produtos obtidos pelas
reações acima equacionadas, é incorreto afirmar que há:
a) dois sais.
b) dois óxidos.
c) um gás.
d) somente uma substância simples.
e) dois ácidos.
669. Assinale a alternativa que apresenta a fórmula correta dos sais: iodato de potássio, óxido
de cálcio e hipobromito de alumínio.
a) KIO4, Ca(OH)2, AlBrO3
b) KIO4, CaO, Al(BrO2)3
c) KIO4, Ca2O, Al(BrO)3
d) KIO3, CaO2, Al(BrO)2
e) KIO3, CaO, Al(BrO)3
670.(UFMG) Considere os seguintes compostos inorgânicos: óxido ferroso, óxido férrico,
dióxido de enxofre, trióxido de enxofre, óxido de bário, peróxido de bário. As fórmulas
correspondentes às referidas substâncias, na
ordem apresentada, são:
a) Fe2O3, FeO, SO2, SO3, BaO2 e BaO.
b) Fe2O3, FeO, SO3, SO2, BaO2 e BaO.
c) FeO, Fe2O3, SO3, SO2, BaO e BaO2.
d) FeO, Fe2O3, SO2, SO3, BaO e BaO2.
671. Os elementos carbono e alumínio podem
combinar-se com o oxigênio, originando os
compostos:
d) CO2, Al2O3.
a) C2O3, Al2O3.
b) CO2, Al 3O4.
e) CO2, AlO.
c) CO, AlO.
672.Na combustão do magnésio, a substância
produzida é um:
Dados: Mg (II A); N (V A); O (VI A); Cl (VII A).
a) óxido molecular de fórmula MgO2.
b) sal iônico de fórmula MgCl2.
c) sal iônico de fórmula Mg3N2.
d) óxido molecular de fórmula Mg2O.
e) óxido iônico de fórmula MgO.
673. Vários óxidos fazem parte do nosso dia a
dia e são de grande importância econômica. Por
exemplo, o óxido de alumínio e o óxido de cromo III são matérias-primas para a extração do
alumínio e do cromo, respectivamente. O óxido
de zinco é utilizado em pomadas e o óxido de
magnésio, em produtos de higiene. O óxido de
ferro III é utilizado como pigmento em tintas,
para a obtenção da cor vermelha. Assinale a
alternativa que contém, respectivamente, as
fórmulas de todos os óxidos citados acima.
a) AlO – Cr2O3 – ZnO – Mg2O – FeO
b) Al2O3 – Cr3O3 – Zn2O – Mg2O – Fe2O3
c) Al2O3 – Cr2O3 – ZnO – MgO – Fe2O3
d) Al2O3 – Cr2O3 – ZnO – Mg2O – FeO
e) Al2O3 – CrO – Zn2O – MgO – Fe2O3
674. Nomeie os óxidos a seguir.
a) Na2O
e) Fe2O3
f) SO2
b) MgO
g) N2O5
c) Al2O3
d) FeO
h) K2O
675. Escreva a fórmula dos óxidos a seguir.
a) Óxido cuproso
b) Óxido cúprico
c) Óxido de prata
d) Óxido de zinco
e) Monóxido de carbono
f) Heptóxido de dicloro
676. Os nomes oficiais das substâncias com as
fórmulas químicas CaHPO4, SO3, Ba(OH)Cl são,
respectivamente:
a) fosfato de cálcio, óxido de enxofre, cloreto
de bário.
b) fosfato de cálcio, trióxido de enxofre, hidroxicloreto de bário.
c) hidrogenossulfato de cálcio, trióxido de
enxofre, cloreto básico de bário.
d) hidrogenofosfato de cálcio, trióxido de
enxofre, cloreto básico de bário.
e) fosfato ácido de cálcio, monóxido de enxofre, cloreto básico de bário.
677. A alternativa que apresenta o dióxido de
enxofre, o dióxido de carbono e o heptóxido
de dicloro é:
d) SO2, CO e Cl2O3
a) SO2, CO2 e ClO4
b) SO3, CO2 e ClO3
e) SO2, CO2 e Cl2O3
c) SO2, CO2 e Cl2O7
678.(UERJ) As fotocélulas são dispositivos
largamente empregados para acender lâmpadas, abrir portas, tocar campainhas etc. O seu
mecanismo baseia-se no chamado “efeito fotoelétrico”, que é facilitado quando se usam
metais com energia de ionização baixa. Os
metais que podem ser empregados para esse
fim são: sódio, potássio, rubídio e césio.
a) De acordo com o texto anterior, cite o metal mais eficiente para a fabricação das foto-
células, indicando o nome da família a que ele
pertence, de acordo com a tabela de classificação periódica.
b) Escreva a fórmula mínima e o nome do
composto formado pelo ânion O2– e o cátion
potássio.
679. Para as substâncias de fórmulas AgClO4,
(NH4)2Cr2O7, BaO e HNO2 indique:
a) o nome de cada composto;
b) a função química a qual cada composto
pertence.
680.Dê a fórmula molecular dos seguintes
compostos:
a) Óxido de cálcio
b) Monóxido de carbono
c) Dióxido de enxofre
d) Dióxido de nitrogênio
681.Na Idade Média, era usual o emprego de
óxido de chumbo (IV) como pigmento branco em telas. Em nossos dias, com o aumento
do teor de H2S na atmosfera, proveniente da
queima de combustíveis fósseis, pinturas dessa
época passaram a ter suas áreas brancas transformadas em castanho-escuro, devido à formação de sulfeto de chumbo (II). No trabalho de
restauração dessas pinturas, são empregadas
soluções diluídas de peróxido de hidrogênio,
que transformam o sulfeto de chumbo (II) em
sulfato de chumbo (II), um sólido branco. A
fórmula do óxido de chumbo (IV) e a função
química do sulfeto e de sulfato de chumbo (II)
são, respectivamente:
a) Pb4O; sais.
b) PbO2; sais.
c) PbO; bases.
d) PbO2; óxidos.
e) PbO; ácidos.
682.Dados os seguintes compostos: K2O, H2O,
HCl, CuNO3, HClO4, CuO, Al(OH)3, Ca3(PO4)2,
Ca(OH)2, Fe2O3, SO2(OH)2 podemos afirmar que:
01.HCl e CuO são sais.
02.Ca 3(PO4)2 e Fe2O3 são ácidos.
04.K2O, H2O e Fe2O3 são óxidos.
08.CuNO3, HClO4 e CuO são bases.
16.o perclorato de hidrogênio e o cloreto de
hidrogênio são ácidos em soluções aquosas.
32.Ca 3(PO4)2 e H2O são bases.
64.Ca(OH)2 e SO2 (OH)2 são bases.
Dê a soma das respostas corretas.
683.Qual é a alternativa que apresenta os anidridos correspondentes, respectivamente, ao
ácido sulfúrico, H2SO4, ácido carbônico, H2CO3,
ácido silícico, H2SiO3 e ácido perclórico, HClO4?
a) SO2 – CO2 – SiO2 – ClO4
b) SO3 – CO2 – SiO2 – ClO4
c) SO3 – CO2 – SiO2 – Cl2O7
d) SO2 – CO – SiO2 – Cl2O3
e) SO2 – CO – SiO2 – Cl2O7
684.(UFRJ) Os óxidos são compostos binários
em que o elemento mais eletronegativo é o
oxigênio. Existe uma relação entre a classificação dos óxidos e as reações em que eles
participam: óxidos básicos por hidratação
produzem bases, enquanto óxidos ácidos por
hidratação produzem ácidos.
a) Apresente a equação da reação de hidratação do óxido de cálcio e classifique-o.
b) Escreva a fórmula estrutural do óxido que,
por hidratação, produz o HClO.
685.A água da chuva é melhor condutora de
corrente elétrica quando provém de ambientes
onde, no momento da chuva, o ar atmosférico
encontra-se poluído por:
a) partículas de carbono.
b) partículas de amianto.
c) monóxido de carbono.
d) óxidos ácidos.
e) óxidos básicos.
686.Quando soluções aquosas saturadas de hidróxido de bário (água de barita), Ba(OH)2(aq),
são expostas ao ar, forma-se um precipitado
branco. Essa propriedade torna a “água de barita” um importante reagente analítico. O fenômeno descrito deve-se à:
a) precipitação de óxido de bário, por evaporação de água da solução, indicando perda de
água do sistema.
b) precipitação de gel de hidróxido de bário,
por absorção de água, indicando ganho de
água pelo sistema.
c) precipitação de carbonato de bário, por
absorção de dióxido de carbono, indicando a
presença desse gás no ar.
d) precipitação de óxido de bário, por absorção do gás oxigênio, indicando a presença
deste gás no ar.
687. Em lâmpadas descartáveis de flash das
antigas máquinas fotográficas, a luminosidade provém da reação do magnésio e do oxigênio no bulbo de vidro. Assim, após o uso de
uma dessas lâmpadas, pergunta-se:
a) A massa total da lâmpada aumenta, diminui ou permanece constante? Justifique.
b) Quais são a equação balanceada dessa reação e o nome do produto formado?
c) Como podemos classificar essa substância?
Justifique.
688.(ITA-SP) Considere os seguintes óxidos
(I, II, III, IV e V):
I.
CaO
IV. P2O5
II. N2O5
V. SO3
III. Na2O
Assinale a opção que apresenta os óxidos
que, quando dissolvidos em água pura, tornam o meio ácido.
a) Apenas I e IV
d) Apenas II, IV e V
b) Apenas I, III
e) Apenas III e V
c) Apenas II e III
689.Assinale a opção que apresenta um óxido
que, dissolvido em água, produz uma solução
aquosa ácida.
d) N2O
a) Na2O
b) CO2
e) H2O2
c) NO
690.A floresta Amazônica contém, em média, 15.000 toneladas de biomassa por km2. Os
principais elementos constituintes da biomassa são C, H, N, O, S e P. Nas grandes queimadas,
cerca de 50% dessa biomassa (7.500 toneladas)
é transformada em vários gases. As quantidades dos principais gases produzidos são: 24.000
toneladas de CO2, 1.600 toneladas de CO, 32
toneladas de CH4, 34 toneladas de NO e NO2, e
12 toneladas de SO2. É produzida, também, em
torno de 1,5% (224 toneladas) de cinza, que é
constituída essencialmente por óxidos, fosfatos e sulfatos de sódio, potássio, cálcio e magnésio. Nas cinzas, há substâncias que podem
reagir com ácidos e neutralizá-los. São fórmulas corretas de algumas dessas substâncias:
a) NaO, CaO e K 3PO4.
b) Na2O, Ca2O e K2O.
c) NaSO4, K 3PO4 e CaSO4.
d) MgO, K2O e Na2O.
e) CaO, Na 3PO4 e KNO3.
691.Em uma das etapas do processamento da
cana-de-açúcar para produção do etanol, a garapa (caldo de cana) é tratada com um óxido
que neutraliza os ácidos livres e precipita as
proteínas. Qual dos óxidos a seguir é empregado com essa finalidade?
a) SO3
d) H2O
b) CO2
e) CaO
c) NO
692.Em relação à equação química representada abaixo, é correto afirmar:
Na2O(s) + H2O(l) → 2 NaOH(aq)
a) o Na2O(s) não pode ser considerado um
óxido, pois reage com a água.
b) o Na2O(s) é considerado um sal, pois reage
com a água para formar uma base.
c) o Na2O(s) é considerado um óxido básico,
pois reage com a água, para formar uma base.
d) o Na2O(s) é considerado um óxido ácido,
pois, ao reagir com a água, forma uma base.
e) o Na2O(s) é considerado um óxido básico,
pois neutraliza uma base.
693.(UEL-PR) Qual dos seguintes elementos
químicos forma um óxido sólido com propriedades básicas?
a) Cloro
d) Criptônio
b) Fósforo
e) Bário
c) Carbono
694.De modo bem simples e visível, mostrou-se para crianças que, na respiração, o ar que
inspiramos e o ar que expiramos são “coisas”
diferentes. Assim, foi pedido que observassem
o que ocorria quando:
I.
o ar borbulhava em um aquário;
II. o ar era soprado através de canudo em
um um copo contendo uma solução aquosa
de hidróxido de cálcio, previamente preparada.
Qual é o nome do gás expirado por meio do
canudo e qual a equação química que explica
a turvação ocorrida na situação II? Justifique
sua resposta.
695. A argamassa, que é um produto usado
por pedreiros para assentar tijolos, é uma
mistura de cal extinta, areia e água. A cal
extinta (hidróxido de cálcio) combina-se com
o gás carbônico do ar, produzindo carbonato de cálcio, que endurece e prende a areia
e, consequentemente, os tijolos. A equação
corretamente balanceada que representa a
reação entre a cal extinta e o gás carbônico
é:
Dado: Ca (Z = 20)
a) Ca(HCO3)2 + CaO → 2 CaCO3 + H2O
b) CaO + H2O → Ca(OH)2
c) Ca(OH)2 + CO2 → CaCO3 + H2O
d) 2 CaOH + CO2 → 2 CaCO3 + H2O
e) 2 CaHCO3 + CaO → CaCO3 + H2O
696. (Unicamp-SP) Para manter a vela acesa, na aparelhagem a seguir esquematizada,
bombeia-se, continuadamente, através do sistema.
Sentido do ar
bombeado
Vela acesa
Bomba de ar
(para aquário)
I
Contém solução
de hidróxido de
cálcio, Ca(OH)2,
para reter o
gás carbônico,
CO2, do ar.
II
III
Contém solução
de hidróxido
de cálcio
a) O que se observará no frasco III, após um
certo tempo?
b) Escreva a equação química que representa
a reação no frasco III.
697. Vários óxidos anfóteros (óxidos que reagem com ácidos e bases e não reagem com
a água) apresentam importância econômica,
tais como: Al 2O3 é matéria-prima da qual se
extrai o alumínio; Cr 2O3 é fonte de cromo
usado na fabricação de aço inox; ZnO é utilizado em pomadas medicinais; PbO usa-se
em baterias e o MnO2 é usado em pilhas e
nas baterias alcalinas. Entre os elementos
químicos constituintes dos óxidos mencionados acima, assinale os de transição externa:
a)
b)
c)
d)
e)
Al, Pb e Zn.
Cr, Zn e Mn.
Cr, Pb e Mn.
Mn, Al e Pb.
Al, Pb e Cr.
698. Classifique os óxidos em ácido, básico,
neutro, anfótero, duplo ou peróxido.
a) CaO
f) Na2O
b) H2O2
g) ZnO
h) Mn3O4
c) Fe3O4
d) Al2O3
i) CO2
e) NO
j) K2O2
699. Classifique os óxidos em ácido, básico,
neutro, anfótero, duplo ou peróxido.
SO2, As2O3, CO, Li2O, N2O3, Mn3O4, Cr2O3,
N2O5, SO3, K2O, Cu2O, Pb3O4, SrO2, As2O5, Ag2O,
Hg2O, Na2O2, P2O3, CuO, Fe2O3, N2O, BaO2, Fe3O4,
Al2O3, MgO2, P2O5, FeO, NO, CO2, Na2O, Sb2O3,
HgO, CaO2, ZnO e Li2O2
700. Faça a correspondência.
( ) Rb2O2
a) Óxido ácido
b) Óxido básico
( ) Mn2O7
c) Óxido neutro
( ) Fe3O4
d) Óxido anfótero
( ) N2 O
e) Óxido duplo
( ) Ag2O
f) Peróxido
( ) ZnO
701. Os escapamentos dos veículos automotores emitem gases como o monóxido (CO) e o
dióxido de carbono (CO2), o óxido de nitrogênio (NO), o dióxido de enxofre (SO2) e outros.
Sobre esses gases, pede-se:
a) a função inorgânica a que pertencem;
b) os possíveis nomes para cada um desses
compostos;
c) a classificação de cada um deles;
702. O que é um óxido anfótero? Exemplifique.
703. A alternativa que apresenta, respectivamente, óxido ácido, óxido básico, óxido neutro e óxido misto é:
a) CO, CaO, SO3 e Na2O4
b) N2O5, BaO, NO e Pb3O4
c) CO2, Al2O3, Fe3O4 e Cl2O
d) N2O, MgO, CO2 e Mn3O4
e) SO2, K2O, CO e K2O2
704.
N2O5 + H2O → 2 HNO3
CO + H2O → não há reação
K2O + H2O → 2 KOH
Nas equações acima, do comportamento
mostrado pelos óxidos conclui-se que:
a) K2O é um peróxido.
b) CO é um óxido neutro ou indiferente.
c) K2O é um óxido ácido.
d) N2O5 é um óxido básico.
e) CO é um óxido ácido.
705. Os principais poluentes do ar nos grandes
centros urbanos são o gás sulfuroso (SO2) e o
monóxido de carbono (CO). O SO2 é proveniente das indústrias que queimam combustíveis
fósseis (carvão e petróleo). Já o CO provém da
combustão incompleta da gasolina em veículos
automotivos desregulados. Sabendo-se que o SO2
(causador da chuva ácida) e o CO (causador de
inibição respiratória) são óxidos, suas classificações são, respectivamente:
a) anfótero e neutro.
b) básico e ácido.
c) ácido e anfótero.
d) ácido e básico.
e) ácido e neutro.
706.Muitas pessoas já ouviram falar de “gás
hilariante”. Mas será que ele realmente é capaz
de provocar o riso? Na verdade, essa substância, o óxido nitroso (N2O), descoberta há quase 230 anos, causa um estado de euforia nas
pessoas que a inalam. Mas pode ser perigosa:
na busca de uma euforia passageira, o gás já
foi usado como droga e, em várias ocasiões, o
resultado foi trágico, como a morte de muitos
jovens. Sobre o óxido nitroso, responda:
a) Como é classificado?
b) Que tipo de ligação une seus átomos?
c) Que outra nomenclatura também pode ser
usada?
707. O que são peróxidos? Exemplifique.
708. Na respiração animal, o ar expirado pode
ser distinguido do ar inspirado borbulhando-os separadamente em soluções aquosas de hidróxido de cálcio. Qual é o critério usado para
fazer essa diferenciação? Represente o fato
observado por meio de uma equação química.
709. As características A, B, C correspondem,
respectivamente, aos gases:
I.
Na forma sólida, é conhecido como gelo-seco e é considerado o principal responsável
pelo efeito estufa.
II. Apresenta cor castanho-avermelhada e
tem importância na destruição da camada estratosférica de ozônio.
III. Apresenta odor de ovo podre e enegrece
objetos de prata.
a) CO2, H2S e NO2
b) NO2, H2S e CO2
c) NO2, CO2 e H2S
d) CO2, NO2 e H2S
710. (Fuvest-SP) Cal viva é óxido de cálcio
(CaO).
a) Escreva a equação da reação da cal viva
com a água.
b) Por que, na agricultura, a cal viva é adicionada ao solo?
711. Analise as afirmativas a seguir:
1. Apresenta cheiro característico de ovo podre e escurece objetos de prata.
2. É um óxido bastante nocivo à saúde, devido à sua grande afinidade com a hemoglobina,
interferindo no processo de oxigenação das
células.
3. É conhecido comercialmente por cal viva,
a qual se transforma em cal extinta ao ser
misturada à água.
As características A, B e C correspondem,
respectivamente, a:
a) SO2, NO e CaO.
b) H2S, CO2 e Ca(OH)2.
c) SO3, CO e CaO.
d) H2SO4, NO2 e Ca(OH)2.
e) H2S, CO e CaO.
712. Desde a Antiguidade, o homem desenvolve atividades relacionadas com o conhecimento químico. Essas atividades são chamadas por alguns historiadores da química
como “artes práticas químicas”. Uma dessas
“artes” é o uso de pigmentos e corantes. A
tabela a seguir mostra alguns pigmentos encontrados em escavações na Ágora de Atenas:
Cor
Pigmento
Fórmula química
Hematita
Fe2O3
Cinábrio
HgS
Realgar
As2S
Ocres amarelos
Fe2O3 · H2O
Orpigmento
As2S3
Verde
Malaquita
Cu(OH)2 · CuCO3
Azul
Azurita
Cu(OH)2 · 2 CuCO3
Calcário
CaCO3
Gesso
CaSO4 · 2 H2O
“Chumbo branco”
Pb(OH)2 · 2 PbCO3
Vermelho
Amarelo
Branco
A respeito dos pigmentos mostrados na tabela, é correto afirmar que:
a) o cinábrio é o sulfeto mercuroso.
b) a hematita é o óxido de ferro (III).
c) o chumbo branco é um carbonato básico de chumbo (IV).
d) a malaquita e azurita são sais normais.
e) o gesso é o sulfato de cálcio anidro.
713.A energia do Sol, ao atingir a superfície
da Terra, transforma-se em calor. Ele é irradiado, mas não se dissipa de todo. Uma parte não
atravessa a camada de gases-estufa. Sem essa
camada a envolver Terra, a temperatura média na sua superfície seria de –19 °C. Graças
ao efeito estufa, ela é de 14 °C. A maioria dos
gases-estufa é produzida naturalmente, caso do
metano (CH4), produto da decomposição da matéria orgânica. Outros são o vapor de água, o
dióxido de carbono (CO2), o ozônio (O3) e o óxido nitroso (N2O): eles retêm calor. Quando são
acrescentados à camada, aumenta a retenção, e
a temperatura sobe. Tudo indica que esse fenômeno está ligado à industrialização. A queima
de derivados de petróleo, carvão e gás natural
aumenta a concentração de gases-estufa. A elevação da temperatura no século XX foi de 0,6
°C, com margem de erro de 0,2 °C.
Atualidades vestibular 2004. Almanaque
Abril. São Paulo: Abril, 2004. p. 91.
Os gases CO2 e N2O, mencionados no texto, são
classificados, respectivamente, como óxidos:
a) ácido e neutro.
b) básico e ácido.
c) ácido e ácido.
d) neutro e básico.
e) ácido e básico.
714. Um agricultor necessita fazer a calagem
do solo (correção da acidez do solo) para o cultivo de hortaliças e nesse processo utilizará
cal virgem (CaO). Com base na informação acima, assinale a(s) proposição(ões) correta(s):
01. Cal virgem reage com água segundo a
equação: CaO + H20 → Ca(OH)2.
02. A calagem é um processo de neutralização.
04. A dissociação de hidróxido de cálcio em
água libera íons (OH) –, que neutralizam os
íons H + presentes no solo.
08. Cal virgem é um óxido básico.
16. O nome oficial da cal virgem é óxido de
cálcio.
Indique a soma das alternativas corretas.
715. Uma das principais impurezas que existem
na gasolina, no óleo diesel e no carvão mineral é
o enxofre, representado pelo símbolo S. Quando
esses combustíveis são utilizados, a queima do
enxofre produz o dióxido de enxofre (SO2). Considere as seguintes proposições:
I.
O enxofre rômbico e o enxofre monoclínico são isótopos.
II. O anidrido sulfuroso, SO2, é um composto cuja estrutura de Lewis é representada por
um átomo de enxofre, central, fazendo uma
ligação covalente coordenada com um átomo
de oxigênio e uma ligação covalente dupla
com o outro átomo de oxigênio.
III. O dióxido de enxofre é um óxido ácido e
pode ser chamado de anidrido sulfuroso.
IV. O trióxido de enxofre reage com a água,
formando o ácido sulfúrico, H2SO4, um dos
causadores da chuva ácida.
Dados: O (z=8) e S (z=16)
Marque a alternativa correta.
a) Somente a proposição II é verdadeira.
b) Somente as proposições II e III são verdadeiras.
c) As proposições I, II e IV são verdadeiras.
d) As proposições I e IV são verdadeiras.
e) As proposições II, III e IV são verdadeiras.
716. Sejam os gases A, B e C seguintes:
Gás A é o principal responsável pela chuva
ácida.
Gás B entre suas aplicações está o seu
uso na fabricação de produtos de limpeza
doméstica.
Gás C é o principal responsável pelo efeito
estufa.
Quais são os gases A, B e C, respectivamente?
a) SO2, NO e CO2
b) CO , NO e H2S
c) SO2, NH3 e CO2
d) CO2, NH3 e NO2
e) NO2, CH4 e NO
717. (UFRGS-RS) São apresentadas a seguir
substâncias químicas, na coluna 1, e uma possível aplicação para cada uma delas, na coluna 2.
Coluna 1
1. H2SO4
2. NaClO
3. H2O2
4. Mg(OH)2
5. NaCl
Coluna 2
(( )descorante de cabelos
(( )antiácido estomacal
(( )água sanitária
(( )conservação de alimentos
(( )solução de baterias automotivas
Associando as substâncias químicas, na
coluna 1, com as aplicações correspondentes,
na coluna 2, a sequência correta de preenchimento dos parênteses, de cima para baixo, é:
a) 3, 4, 2, 5, 1.
d) 2, 3, 4, 1, 5.
b) 2, 3, 1, 5, 4.
e) 3, 2, 1, 4, 5.
c) 3, 4, 1, 5, 2.
718.(UFTM-MG) “Savanização da Amazônia”:
Pesquisadores brasileiros do Inpe (Instituto
Nacional de Pesquisas Espaciais) indicam o
tamanho do estrago que o aquecimento global vai fazer na Amazônia. Os resultados dos
estudos são alarmantes, pois, até o final deste
século, 18% da área que hoje é mata deve virar
uma vegetação rala, semelhante ao cerrado.
www1.folha.uol.com.br/folha/ciencia/
ult306u16367.shtml 24/04/2007. Adaptado.
Na queima de floresta e de combustíveis
fósseis, são liberados gases responsáveis pela
efeito estufa e que também contribuem para
a formação de chuva ácida. Os principais poluentes gerados são: gás carbônico, monóxido de carbono, óxidos de enxofre e óxido de
nitrogênio(NOx).
Dentre os poluentes citados, o principal
responsável pelo aquecimento global e um dos
poluentes classificados como óxido ácido são,
respectivamente:
c) CO2 e NO.
e) SO2 e NO.
a) CO e NO2.
b) CO e SO2.
d) CO2 e NO2.
719. No acidente ocorrido na República dos
Camarões, muitas pessoas morreram intoxicadas pelos gases sulfídrico e sulfuroso. Suas
fórmulas são, respectivamente:
a) H2S e SO3. c) H2S e SO2. e) H2SO4 e SO2.
b) S e SO2.
d) SO2 e SO3.
720.Para remover dióxido de carbono do ar
respirado pelos astronautas nas espaçonaves,
utiliza-se o hidróxido de lítio sólido. Qual é
a fórmula, o estado físico e o nome oficial do
produto formado?
Respostas
589.Metais alcalinoterrosos: M2+
S = 1s2 2s2 2p6 3s2 3p4 → S2–
16
F
= 1s2 2s2 2p5 → F–
9
2+ 2–
M S → MS
M2+F– → MF2
597. a) H2HPO3
590.C
591.A
592.D
593. H2SO4 + 2 NaOH → Na2SO4 + 2 H2O
594.A
595.B
596.B
→ MgHPO3 + 2 H2O
H
3PO3 + Mg (OH)2
b) HH2PO2
H3PO2 + Ca (OH)2 → Ca (H2PO2 ) + 2 H2O
2
2
c)
H4P2O7 + 4 NaOH → Na4P2O7 + 4 H2O
d) HPO3 + NH4 OH → NH4PO3 + H2O
e)
4 H3BO3 + 3 Sn (OH)4 → Sn3 (BO3 ) + 12 H2O
4
598.D
604.S2– = ânion sulfeto e SO42– = ânion sulfato
Pb2+ S2– → PbS = sulfeto plumboso
Pb4+SO42– → Pb(SO4)2 = sulfato plúmbico
599.a) H2SO4 (ácido sulfúrico)
NH3 (amônia)
b) H2SO4 + 2 NH3 → (NH4)2SO4 (sulfato
de amônio)
605.E
609.D
613. E
606.A
610.C
614.D
600.C
607.A
611. A
615. A
608.E
612.A
616. E
601.Cátion amônio: NH4+
Ânion molibdato: MoO42–
NH4 +MoO42– → (NH4)2MoO4
602.a)
b)
c)
d)
e)
f)
g)
603.D
Fe3+ Cl– → FeCl 3
Pb2+ SO42– → PbSO4
K+ NO2– → KNO2
Na + ClO4– → NaClO4
Cd2+ S2– → CdS
Ba2+ SO32– → BaSO3
Cr3+ CO32– → Cr2(CO3)3
617. E
618.a)
b)
c)
d)
e)
f)
g)
h)
i)
KMnO4, solúvel
CaC2O4, insolúvel
KI, solúvel
(NH4)2SO4, solúvel
Na 3BO3, solúvel
FeSO4, solúvel
AgNO3, solúvel
KClO4, solúvel
AgCl, insolúvel
619. D
621.
620.A
Sal solúvel
Sal insolúvel
NaCl
CaCO3
Ca(NO3)2
AgBr
Na2CO3
PbCl2
KI
Al2S3
BaS
Fe(CN)3
Na3PO4
(NH4)2S
629.Cátion sódio: Na +
Íon bicarbonato: HCO3–
Na +HCO3– = NaHCO3
É um oxissal, quaternário, hidrogenossal
e anidro.
630.E
622.C
623.
a) 3 H2SO3 + 2 Fe(OH)3 → Fe2(SO3)3 + 6 H2O
Fe2(SO3)3 = sulfito de ferro III (sulfito férrico) = sal insolúvel
b) 2 HBr + Ca(OH)2 → CaBr2 + 2 H2O
CaBr2 = brometo de cálcio = sal solúvel
624.a)
b)
c)
d)
e)
f)
g)
628.Sal: NaCl = cloreto de sódio;
Veja a reação:
NaHCO3(s) + HCl(aq) → NaCl(aq) +
<H2CO3(aq)>
No estudo dos ácidos, aprendemos que o
ácido carbônico é instável e decompõe-se em:
NaHCO3(s) + HCl(aq) → NaCl(aq) + CO2(g) +
H2O(l)
Na2S → solúvel
BaS → solúvel
CaS → solúvel
CaCl2 → solúvel
AgCl → insolúvel
PbCl2 → insolúvel
CaCO3 → insolúvel
625.D
626.Cátion cálcio: Ca2+
Ânion sulfito: SO32–
Ânion hidrogenossulfito: HSO3–
Ca2+ SO32– = CaSO3 = sulfito de cálcio
Ca2+HSO3– = Ca(HSO3)2 = hidrogenossulfito de cálcio, sulfito(mono)ácido de cálcio ou
bissulfito de cálcio.
627. Cátion sódio: Na +
Ânion carbonato: CO32–
Ânion bicarbonato: HCO3–
Na + CO32– = Na2CO3: carbonato de sódio
Na +HCO3– = NaHCO3: carbonato (mono)
ácido de sódio, hidrogenocarbonato de sódio
ou bicarbonato de sódio.
631. a) Sulfato de potássio: K+ SO42– = K2SO4
Hidrogenofosfato de cálcio: Ca2+HPO42– =
= CaHPO4
Sulfato de amônio: NH4 + SO42– = (NH4)2SO4
Nitrato de amônio: NH4+NO3– = NH4NO3
b) Função sal: K2SO4 → oxissal, ternário,
anidro e normal
CaHPO4 → oxissal, quaternário, anidro e
hidrogenossal
(NH4)2SO4 → oxissal, quaternário, anidro
e normal
NH4NO3 → oxissal, quaternário, anidro e
normal
632.A
633.
3
H+
H+
H+
634.
4
2
–
OH
CuHS
sulfeto ácido de
cobre I ou
hidrogenossulfeto
de cobre I (cuproso)
635.B
636.V, V, F, V
637. D
4
2
• di-hidrogenofosfato
de potássio
• fosfato diácido de
potássio
+ H2O
638. 1. Cu2CO3: carbonato de cobre I (cuproso)
2. Fe(OH)3: hidróxido de ferro III (férrico)
3. KHSO4: hidrogenossulfato de potássio; sulfato ácido de potássio ou bissulfato de
potássio.
4. Mg(NO3)2: nitrato de magnésio
5. Na2S: sulfeto de sódio
6. CuSO4 · 5 H2O: sulfato de cobre II
(cúprico) penta-hidratado
7. NH4MnO4: permanganato de amônio
8. KAl(SO4)2: sulfato de potássio e alumínio
644.Sulfato cúprico penta-hidratado:
CuSO4 · 5 H2O. Portanto, temos quatro
elementos químicos, cobre (Cu), enxofre (S),
oxigênio (O) e hidrogênio (H).
639.São sais derivados de dois ácidos (ou
duas bases) diferentes.
Exemplos:
– LiKSO4
– BaBrCl
647. a) NH4HCO3 = bicarbonato de amônio ou
carbonato ácido de amônio ou hidrogenocarbonato de amônio
NaNO2 = nitrito de sódio
b) fosfito de sódio = Na2HPO3
bissulfato de amônio = NH4HSO4
640.São sais que cristalizam com uma ou
mais móleculas de água (água de cristalização
ou água de hidratação).
Exemplos:
– CuCl2 · 2 H2O
– CuSO4 · 5 H2O
641.a) Na2SO3 → oxissal, ternário, normal e
anidro.
b) Ca(HCO3)2 → oxissal, quaternário, hidrogenossal e anidro.
c) CaSO4 · 2 H2O → oxissal, quaternário, normal e hidratado.
d) MgSO4 · 2 H2O → oxissal, quaternário, normal e hidratado.
642.O alúmem comum é um sal formado por
dois cátions, portanto um sal duplo, e seu
nome oficial é sulfato de potássio e alumínio.
Curiosidade: esse alúmem comum ou pedra-ume é usado na coagulação do sangue de
pequenos cortes e na fabricação de corantes.
643.(2) sal básico
(3) sal duplo
(4) sal ácido
(1) sal hidratado
645.Fe3+[Fe(CN) 6]4– = Fe4[Fe(CN) 6]3
Esse composto é um sal não oxigenado,
ternário e anidro.
646.a) Esse composto é um sal oxigenado,
quaternário, hidroxissal e anidro.
b) NH4 + NO3– = NH4NO3
648.A
649.B
650.D
651.Ca(OH)2(aq) + CO2(g) → CaCO3(s)
CaCO3(s) = carbonato de cálcio
652.C
653.(4) Usada em alvejante doméstico.
(2) Um dos componentes do soro fisiológico.
(1) Usada como contraste em radiografias de estômago.
(5) Adicionada ao sal de cozinha.
(3) Usada na fabricação de giz.
654.D
∆
655. NH4HCO3(s) → NH3(g) + CO2(g) + H2O(l)
O bicarbonato de amônio é um hidrogenossal. Quando aquecido, origina gases, cuja expansão favorece o crescimento da massa do bolo.
656.B
659.C
657. C
660.D, E, G, A, C
658.E
661.Óxidos são compostos binários que contêm oxigênio, em que este é o elemento mais
eletronegativo.
Ex.: óxido ácido = CO2 → molecular
óxido básico = CaO → iônico
662.D
663.E
664.K2O: óxido de potássio
NaClO: hipoclorito de sódio
Mg(OH)2: hidróxido de magnésio
CO2: dióxido de carbono
679. a)
b)
680.a) Óxido de cálcio: CaO
b) Monóxido de carbono: CO
c) Dióxido de enxofre: SO2
d) Dióxido de nitrogênio: NO2
665.a) Li2O
b) SrO
c) CaO
d) Al2O3
e) ZnO
f) Ag2O
681.B
666.a)
b)
c)
d)
e)
f)
g)
h)
683.C
CO
CO2
SO2
SO3
667. a) MnO
b) Mn2O3
c) MnO2
NO2
NO
N2 O 4
Fe3O4
d) Mn2O5
e) Mn2O7
f) Mn3O4
682.20 (04 + 16)
684.a) CaO
+ H2O → Ca(OH)2
Óxido
básico
670.D
672.E
685.D
669.E
671.D
673.C
686.C
Óxido de sódio
Óxido de magnésio
Óxido de alumínio
Óxido ferroso (de ferro II)
Óxido férrico (de ferro III)
Dióxido de enxofre
Pentóxido de dinitrogênio
Óxido de potássio
675.a) Cu2O
b) CuO
c) Ag2O
676. D
d) ZnO
e) CO
f) Cl2O7
677. C
678.a) Família: metais alcalinos.
O metal alcalino com menor energia
de ionização é o césio (Cs).
b) K+ O2– ⇒ K2O = óxido de potássio
Base
b) O — Cl
|
Cl
668.E
674. a)
b)
c)
d)
e)
f)
g)
h)
Perclorato de prata: AgClO4
Dicromato de amônio: (NH4)2 Cr2O7
Óxido de bário: BaO
Ácido nitroso: HNO2
Sal: AgClO4; (NH4)2Cr2O7
Óxido: BaO
Ácido: HNO2
687. a) Como o sistema é fechado, obedecendo
à lei de Lavoisier (lei da conservação das massas),
a massa da lâmpada permanece constante.
b) Mg(s) +
1
O (g) → MgO(s)
2 2
MgO(s) = óxido de magnésio
c) É um óxido básico, pois, em reação
com água, forma uma base ou um hidróxido.
688.D
689.B
690.D
692.C
691.E
693.E
694.CO2(g) = gás carbônico, dióxido de carbono ou anidrido carbônico.
CO2(g) + Ca(OH)2(aq) → CaCO3(s) + H2O(l)
Como é um óxido ácido, óxido formado
por não metal, reage com a base da solução,
formando um sal insolúvel, CaCO3(s), deixando a solução turva enquanto precipita.
695.C
696.a) Observa-se a turvação da solução.
b) Ca(OH) 2 (aq) + CO2(g) → CaCO3 (s) +
+ H2O(l)
697. B
698.Óxido ácido: CO2
Óxido básico: CaO, Na2O
Óxido neutro: NO
Óxido anfótero: Al2O3, ZnO
Óxido duplo: Fe3O4, Mn3O4
Peróxido: H2O2, K2O2
702.São óxidos dos elementos de eletronegatividade intermediária, isto é, dos elementos
da região central da tabela periódica. Exemplos: ZnO e Al2O3
703.B
704.B
705.E
706.a) Óxido neutro
b) Ligação covalente
c) Monóxido de dinitrogênio
707. Peróxidos são óxidos formados por cátions das famílias dos metais alcalinos (X=IA;
X2O2) e dos metais alcalinoterrosos (Y=IIA:
YO2) e pelo grupo O2−
2 .
Exemplos: H2O2, Na2O2, BaO2
708.O ar expirado possui maior concentração
de CO2(g), que forma um precipitado branco de
carbonato de cálcio.
CO2(g) + Ca(OH)2(aq) → CaCO3(s) + H2O(l)
709.D
699.Óxido ácido: SO2, SO3, N2O3, N2O5, P2O3,
P2O5, CO2
Óxido básico: Li2O, Na2O, K2O, CuO, Hg2O,
HgO, Ag2O, FeO, Cu2O
Óxido neutro: NO, N2O, CO
Óxido anfótero: As2O3, As2O5, ZnO, Al2O3,
Fe2O3, Cr2O3, Sb2O3
Óxido duplo: Fe3O4, Pb3O4, Mn3O4
Peróxido: Li2O2, Na2O2, MgO2, CaO2, SrO2,
BaO2
713.A
700.f, a, e, c, b, d
714. 31 (01 + 02 + 04 + 08 + 16)
701.a) função óxido
b) CO = monóxido de carbono ou óxido
de carbono II.
CO2 = óxido de carbono IV ou dióxido
de (mono) carbono ou anidrido carbônico.
NO = monóxido de nitrogênio, óxido
de nitrogênio II ou óxido nítrico (monóxido
de azoto).
SO2 = dióxido de enxofre, óxido de
enxofre IV
c) O CO2 e o SO2 são óxidos ácidos ou
anidridos, enquanto o CO e o NO são óxidos
neutros ou indiferentes.
715.E
710.a) CaO + H2O → Ca(OH)2
b) Para corrigir a acidez excessiva do
solo.
711. E
712. B
716. C
717. D
718.D
719. C
720.2 LiOH(s) + CO2(g) → Li2CO3(s) + H2O(l)
Li2CO3(s) = carbonato de lítio