1
Análise de metais em amostras ambientais utilizando ICP-MS
Aluno: Lorreine dos Santos Cursino Ferreira
Orientador: Adriana Gioda
1
Introdução
A atmosfera urbana é um grande veículo de transporte de várias partículas. Essas partículas
presentes no ar entram em suspensão e conseguem se locomover longas distancias (Alves, 2005).
Infelizmente, muitas dessas partículas são de natureza antropogênica e podem, não só causar problemas
climáticos, impactos no meio ambiente, mas também problemas de saúde para a população.
As partículas, conhecidas como material particulado (MP), são compostas de várias substâncias e
elementos, tais como os metais. Os metais como zinco, cobre, chumbo, cadmio entre outros, são um grupo
de elementos da tabela periódica. Alguns, em pouca quantidade, são vitais para a vida dos seres vivos;
outros não possuem nenhuma função dentro dos organismos e quando ultrapassam certa concentração,
acabam se tornando extremamente tóxicos (Shaltout et al., 2013)
O teor de metais associados a partículas presentes na atmosfera em áreas urbanas cresceu de
maneira significativa com o aumento dos rejeitos industriais e queima de combustível. Esses metais
presentes nas partículas em suspensão acabam sendo depositados e acumulam-se na superfície de plantas
e árvores. Muitas plantas possuem a capacidade de absorver esses metais. Devido a essa propriedade,
certas plantas são utilizadas como biomonitores em áreas industriais e urbanas. Esses biomonitores
poderão ser analisados em laboratório, como uma forma de controle ambiental, permitindo também
encontrar a natureza e proveniência da poluição em certo local (Hu et al., 2014). O papel das plantas como
bioacumuladores tem algumas vantagens em relação aos filtros, como o menor custo e a possibilidade de
estudo direto do impacto do material particulado atmosférico em organismos vivos (Al-Masri, et al., 2006).
Os biomonitores em estudos de monitoramento ambiental fornecem um melhor entendimento do impacto
ambiental, atuando como bioindicadores da qualidade do ar ou bioacumuladores de poluentes
atmosféricos.
Certas indústrias, como as de couro, participam de maneira ativa na poluição atmosférica. O Brasil
é um dos maiores produtores de couro do mundo, principalmente pelo potencial de rebanho bovino que
possui, o qual desempenha um papel importante para a economia brasileira. O setor de curtume apresenta
um grande impacto ambiental, pois em seu processo produtivo, gera uma excessiva carga de resíduos
sólidos, líquidos e gasosos, além de grande consumo de água, lenha, energia e produtos químicos (cromo,
sal comum, soda cáustica, ácidos, solventes, corantes, óleos e resinas). Atualmente, existem dois processos
de curtimento i) curtimento ao cromo e ii) curtimento vegetal, onde ao redor de 90 % das peles do mundo
são curtidas como o cromo, a causa de sua boa resistência e maleabilidade. Porém, segundo a Norma
Brasileira (NBR) 10004, da Associação Brasileira de Normas Técnica (ABNT) 1, classifica o cromo como
resíduo classe I, ou seja, perigoso (Cr6+). Já o Conselho Nacional do meio ambiente (CONAMA) 2 estabelece
que a concentração máxima de Cr+6 nos efluentes descartados seja inferior a 0.5 ug g-1 e para Cr+3inferior a
2 ug g-1. E a, Agency for Toxic Substances and Disease Registry (ASTDR) 3, diz que a toxidade do cromo VI
aos seres humanos inclui, além do câncer, danos ao estômago, ao fígado e aos rins, sensibilização e
irritação da pele e é altamente tóxico aos animais, plantas e micro-organismos. Portanto, é necessário
avaliar o nível de poluição causado por este setor ao meio ambiente.
2
Objetivos
Este trabalho teve por objetivo quantificar as concentrações de diferentes metais (Cr, Co, Zn, Pb,
Cu, Cd e outros) em amostras de plantas coletadas ao redor de indústrias do couro para avaliar a poluição
2
ambiental causada por estas indústrias. A técnica multielementar ICP-MS (espectrometria de massa com
plasma acoplado indutivamente) foi utilizada para a análise desses metais.
3
3.1
Métodos
Local de coleta
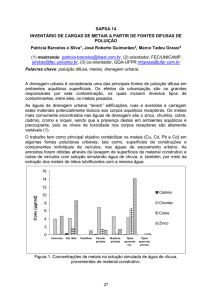
As amostras de plantas contendo partículas, Figura 1, foram coletadas em Nova esperança do Sul
no Rio Grande do Sul em uma região próxima a curtumes.
Figura 1: Plantas coletadas
Podemos observar na imagem as folhas com um tipo de material particulado depositado de cor
escura.
3.2
Preparo das amostras
Foram coletados dois tipos de plantas, uma com material particulado depositado na superfície
(preta e viscosa) e outra sem partículas (Figura 2), consideradas como brancos.
Figura 2: Amostras limpas
3
Figura 3: Amostras com material particulado depositado
Figura 4: Pó retirado das plantas
O pó foi retirado delicadamente das plantas e colocado em um tubo de 50,0 mL. As plantas limpas
e sem pó foram também colocadas separadas em tubos de 50,0 mL. Cada tubo continha 6 folhas de cada
amostra. Após a separação, as folhas foram lavadas com água ultrapura sob agitação e liofilizadas durante 3
dias. Após a secagem, as plantas foram moídas até virarem pó e pesadas na balança da marca com precisão
de 0,0001 g.
3.3
Extração das amostras
Extração com ácido nítrico e bombonas
A extração foi realizada em frascos fechados de Teflon. No caso das bombonas, a amostra foi
pesada na bombona. Adicionou-se 2,0 mL de ácido nítrico em cada e a abertura foi feita na chapa de
aquecimento com temperatura a 180 oC durante 2 horas.
3.4
Análise
A curva analítica utilizada no momento da análise no ICP-MS depende muito dos elementos
analisados. Nesta analise quase todos os elementos foram analisados, mas a prioridade eram os elementos
seguintes: Cr, Co, Cu, Cd, Pb, Ni.
3.4.1
Caracterização elementar
Todas as amostras foram diluídas em 10 vezes e 20 vezes com água ultrapura. Foram realizadas
caracterizações multielementares das amostras, por espectroscopia de massa com plasma indutivamente
acoplado (ICP-MS), (ELAN600-SCIEX, Perkin Elmer). A verificação da eficiência de extração do método foi
feita a partir da análise de amostras certificadas de plantas, tais como o SRM 1515 Apple leaves. Foram
feitas quadruplicadas dos 3 tipos de amostras (limpas, sem pó e o pó), pesando 0,1 g de cada amostra. A
amostra certificada foi feita em duplicata, e foi pesado 0,01 g. Em todas as amostras adicionou-se 2,0 mL de
ácido nítrico bidestilado.
4
3.4.2
Espectrometria de Massa com Plasma Indutivamente Acoplado (ICP-MS)
Nas determinações realizadas, utilizou-se o ICP-MS modelo DRC II (PerkinElmer-Sciex, EUA). Não
houve problemas nas determinações, uma vez que não se utilizou o dispositivo para eliminação de
interferências, a célula de reação dinâmica (DRC) que este último modelo possui, e as condições
experimentais foram mantidas iguais, como pode ser visto na Tabela 1.
Tabela 1: Condições de análise do ICP-MS
Parâmetro
Potência RF
Plasma
Auxiliar
Vazão de Ar nebulizador
Leituras por replicatas
Replicatas
Dwell time
Operação do detector
Isótopos utilizados para quantificação
Padrão interno
Valor
1300 W
15 L min-1
1,2 L min-1
0,42 L min-1
2
3
50 ms
Dual mode
51
V , 60Ni
103
Rh+
As soluções de calibração foram preparadas com utilizando soluções estoque Perkin Elmer 29 (Al, V,
Cr, Mn, Fe, Ni, Cu, Zn, Ga, Se, Cd e Pb), PerkinElmer 12 (Mo, Nb, P, S, Ta, Ti), Perkin Elmer 17 (La, Y), Merck
IV (Al, Ba, Ce, Cd, Cr, Cu, Fe, Ga, K, Li, Mg, Ni, Pb, Na, Sr, Zn), PerkinElmer 15 (Fe, Ca, K, Mg, Na) e padrões
individuais de Sb, Ti, Au Br e Sn todos com 1000 μg L-1 de concentração. As concentrações da curva de
calibração variaram de 10 μg L-1 a 100 μg L-1, e o padrão interno de calibração foi uma solução de
concentração 400 μg L-1 de Rh a 1 % de HNO3. As soluções de calibração receberam 100 μL de HNO3, a fim
de evitar a precipitação dos padrões, uma vez que a matriz da curva é aquosa.
Os elementos, massas atômicas, os limites de detecção (LD) e quantificação (LQ) estão apresentados na
Tabela 2.
5
Tabela 2: Parâmetros analíticos para a técnica de ICP-MS: Elemento, LD e LQ
Elemento
Li
Be
Na
Mg
Al
K
V
Cr
Mn
Fe
Co
Ni
Cu
Zn
Ga
As
Se
Sr
Ag
Cd
Ba
Tl
Pb
Bi
Rb
Ca
Nb
Mo
Cs
7
9
23
24
27
39
51
53
55
57
59
60
65
66
69
75
82
88
107
114
138
205
208
209
85
44
93
95
133
LD (mg L-1)
0,015
0,016
3,568
0,491
2,554
3,564
0,024
0,190
0,095
41,607
0,013
0,150
0,112
1,492
0,008
0,040
0,548
0,021
0,014
0,006
0,051
0,001
0,139
0,008
0,006
84,591
0,004
0,021
0,001
LQ (mg L-1)
0,050
0,052
11,775
1,621
8,427
11,761
0,078
0,628
0,314
137,304
0,042
0,496
0,371
4,925
0,026
0,131
1,808
0,070
0,046
0,020
0,170
0,004
0,457
0,027
0,020
279,150
0,013
0,070
0,004
A calibração realizada foi do tipo externa, e o modelo estatístico adotado na regressão linear pelo
método dos mínimos quadrados foi do tipo y = ax. Os limites de detecção e quantificação foram calculados
segundo as equações (1 e 2), respectivamente. Na equação 1, “s” representa o desvio padrão amostral de
10 leituras do branco da curva de calibração (água ultrapura acidificada com HNO3), e “a” representa o
coeficiente angular da equação da reta.
LD = (3 x s)/a (1)
LQ = 3,3 x LD (2)
4
Resultados
Para avaliar a precisão das analises, utilizou-se o material de referência o SRM 1515. Os resultados para os
elementos mais importantes seguem na tabela abaixo:
6
Tabela 3: Recuperação do SRM 1515
Elemento Recuperação (%)
Cr
75,8
Co
78,9
Cu
114
Cd
103
Pb
104
Ni
70
Figura 5: Porcentagem de extração de material certificado (SRM)
Como pode ser observado a recuperação para o material certificado foi boa (76-114 %), o que
evidencia que a extração foi feita corretamente e que os dados apresentados estão certos.
Segue abaixo a tabela com todos os elementos analisados no equipamento. Para avaliar como a
planta atua como um biomonitor analisou-se três diferentes amostras: A1 (folhas limpas), A2 (Folhas após
ser limpas do pó) e A3 (pó obtido das folhas)
7
Tabela 4: Elementos analisados nas amostras em ug.g-1
Elemento
Li
7
Be
9
Na
23
Mg
24
Al
27
K
39
V
51
Cr
53
Mn
55
Fe
57
Co
59
Ni
60
Cu
65
Zn
66
Ga
69
As
75
Se
82
Sr
88
Ag
107
Cd
114
Ba
138
Tl
205
Pb
208
Bi
209
Rb
85
Ca
44
Nb
93
Mo
95
Cs
133
A1
A2
A3
0,06
0,24
1,73
<0.016
<0.016
0,14
9,79
22,12
294,64
1990,01 1959,97 1029,47
23,88
50,98
5117,92
10629,89 14277,02 8367,75
0,04
0,14
16,90
0,24
1,64
96,02
246,06
2935,49 170,70
67,96
165,19 5132,17
0,06
0,29
2,05
1,22
4,17
3,18
7,41
3,33
23,66
40,15
41,36
112,53
1,91
6,71
2,61
<0.04
<0.04
2,03
<0.5
<0.5
<0.5
36,07
93,14
17,79
<0.014
<0.014
0,23
0,06
0,15
0,17
71,60
302,65
54,97
<0.001
<0.001
0,03
0,05
0,19
7,53
< 0.008
<0.008
0,13
10,53
9,43
14,57
6817,29 13315,93 1125,27
199,83
368,05 29459,59
3710,72
587,42 2007,84
0,02
0,03
0,70
A Tabela 5 apresenta as concentrações (n=4) medias dos elementos analisados e a recuperação (70-114%)
do material de referencia SRM 1515 Apple leaves. Esses elementos foram separados, pois são considerados
de maior importância. Eles são considerados os de maior impacto atmosférico proveniente de curtumes.
Tabela 5: Resultados
Amostras (n=4, ug.g-1)
A1
A2
A3
Recovery (%) SRM1515
53
Cr
0,24
1,64
96,02
71
59
Co
0,06
0,29
2,05
79
65
Cu
3,33
7,41
23,66
114
114
Cd
0,06
0,15
0,17
104
208
Pb
0,05
0,19
7,53
104
60
Ni
1,22
3,18
4,17
70
8
As figuras abaixo mostram a comparação das médias entre os tipos de amostra para cada elemento.
9
Figura 6: Gráficos ilustrativos das concentrações de metais para cada amostra
10
5
Discussão de resultados
Analisando os resultados obtidos foi possível observar que as concentrações mais baixas dos
elementos poluentes foram encontradas para as plantas consideradas limpas, e as mais altas
concentrações forem encontradas no pó.
Os resultados demonstram altos teores tanto para o cromo quanto para o cobre. A legislação possui
um limite rigoroso para as emissões de cromo presente nos efluente de industrias de couro, mas para as
emissões atmosféricas, a legislação é muita fraca e não leva em consideração as emissões provenientes do
cromo que entra em suspensão durante o processo.
6
Conclusões
A alta concentração de Cr encontrada nas amostras de plantas é um reflexo da contaminação
proveniente das indústrias de couro na região. Esse elemento foi eliminado durante o processo de queima
de restos de couros e outros resíduos tratados com produtos químicos contendo cromo. Com esse trabalho
pudemos verificar que as plantas podem ser bons biomonitores da poluição atmosférica em regiões de
curtumes.
11
7
Referências
Alves, C. (2005). Aerossóis atmosféricos: perspectiva histórica, fontes, processos químicos de
formação e composição orgânica. Química Nova, 28(5), 859–870
Hu, Y., Wang, D., Wei, L., Zhang, X., & Song, B. (2014). Bioaccumulation of heavy metals in plant
leaves from Yan׳an city of the Loess Plateau, China. Ecotoxicology and Environmental Safety, 110, 82–8.
doi:10.1016/j.ecoenv.2014.08.021
Shaltout, A. a, Khoder, M. I., El-Abssawy, a a, Hassan, S. K., & Borges, D. L. G. (2013). Determination
of rare earth elements in dust deposited on tree leaves from Greater Cairo using inductively coupled
plasma mass spectrometry. Environmental Pollution (Barking, Essex : 1987), 178, 197–201.
doi:10.1016/j.envpol.2013.03.044
A. Gioda, B.S. Amaral, I.L. Monteiro, T.D. Saint'Pierre, Chemical composition, sources, solubility and
transport of aerosol trace elements in a tropical region, J.Environ. Monit. 13 (2011) 2134–2142
Smichowski, P., Marrero, J., Gómez, D. Inductively coupled plasma optical emission spectrometric
determination of trace element in PM2,5 airborne particulate matter collected in an industrial area of
Argentina. Microchemical Journal, 80, 2005, p.9– 17.
Al-Masri,M.S., Al-Kharfan, K., Al-Shamali, K. Speciation of Pb, Cu and Zn determined by sequential
extraction for identification of air pollution sources in Syria. Atmospheric Environment, 40, 2006, p.753–
761.
He, Z.L., Yang, X.E., Stoffella, P.J. Trace elements in agroecosystems and impacts on the environment.
Journal of Trace Elements in Medicine and Biology, (2005) 19, 125–140.
Associação Brasileira de Normas Técnicas. NBR 10.004/2004 - Resíduos sólidos - Classificação.
Biotemas. 2004;18(2):7-18. doi:10.5007/21407.
Michel Miguel Elias Temer Lulia V-P, Francisco Gaetani S-E, Paulo Guilherme Francisco Cabral S,
Resoluções vigentes publicadas entre setembro de 1984 e janeiro de 2012. do:CONAMA
ASTDR. Agency for Toxic Substances and Disease Registry. Toxicol Profile Chromium.
2012;(September):592..
Abril G a., Wannaz ED, Mateos AC, Pignata ML. Biomonitoring of airborne particulate matter
emitted from a cement plant and comparison with dispersion modelling results. Atmos Environ.
2014;82:154-163.