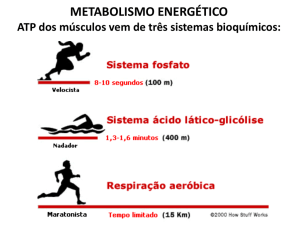
METABOLISMO
METABOLISMO
• Metabolismo é o conjunto de transformações
(reações químicas) que as substâncias químicas
sofrem no interior dos organismos vivos
(células).
• Estas reações são responsáveis pelos
processos de síntese e degradação dos
nutrientes na célula e constituem a base da vida,
permitindo o crescimento e reprodução das
células, mantendo as suas estruturas e
adequando respostas aos seus ambientes.
• Anabolismo
A parte do metabolismo que se refere à
complexidade de substâncias num organismo, ou
seja, a partir de moléculas mais simples, são
criadas moléculas mais complexas.
• Catabolismo
A parte do metabolismo que se refere à
assimilação ou processamento da matéria
adquirida para fins de obtenção de energia. Parte
sempre de macromoléculas, que contêm
quantidades importantes de energia (glicose,
triglicéridos,
etc).
Estas
substâncias
são
transformadas de modo a que restem, no final,
micromoléculas, pobres em energia (H2O, CO2,
NH3), aproveitando, o organismo, a formação e
libertação de energia resultante deste processo.
Relações
energéticas
entre anabolismo e
catabolismo
CAMINHOS METABÓLICOS
• Os “caminhos” metabólicos são séries de reações enzimáticas
interligadas, que produzem produtos específicos.
• Os processos catabólicos e anabólicos estão relacionados da
seguinte maneira:
nos processos catabólicos, complexos compostos (metabólitos)
são “partidos” em produtos mais simples;
o a energia livre libertada neste processo é conservada pela
consequente síntese de ATP a partir de ADP+Pi, ou pela redução
do coenzima NADP+ para NADPH.
o
• O ATP e o NADPH são as mais importantes fontes de energia
para as reações anabólicas.
• O acetil-coenzimaA participa na maior parte dos processos
catabólicos.
Caminhos Metabólicos do Organismo
Considerações Termodinâmicas
• Os mecanismos metabólicos são irreversíveis.
o
Uma reação altamente exergónica é irreversível; se se tratar de uma
reação em vários passos, se um deles for irreversível, então todo o
processo se torna irreversível.
• Todos os mecanismos metabólicos têm um primeiro passo
cometido.
o
Embora a maioria das reações metabólicas estejam muito próximas do
equilíbrio químico, há quase sempre uma reação exergónica irreversível
num dos primeiros passos do metabolismo.
• Os mecanismos catabólico e anabólico são diferentes.
o
Se um metabolito é convertido noutro metabolito por um processo
exergónico, tem que ser fornecida energia livre para converter o
segundo metabolito novamente no primeiro e assim diferentes caminhos
de reação têm de ser tidos em conta pelo menos nalguns passos.
Estrutura do fosfato inorgânico (ATP)
O ATP (adenosina trifosfato), que aparece em todas as formas de vida conhecidas,
consiste numa adenosina (adenina+ribose) na qual três grupos fosforil (-PO32-) estão
sequencialmente ligados por uma ligação fosfoéster e duas ligações fosfoanídricas.
A importância biológica do ATP assenta na grande quantidade de energia que
acompanha a quebra das suas ligações fosfoanídricas.
Grupos Funcionais -Tipos de Reações
Reação de oxidação redução
Grupos funcionais
METABOLISMO DOS
GLÚCIDOS
ENERGIA DO METABOLISMO
• Cada macromolécula é dividida noutras mais pequenas.
• Glúcidos – açúcares simples
• Lípidos – ácidos gordos e glicerol
• Proteínas – aminoácidos
• Cada etapa da sua cisão deve ser um processo
controlado.
• ATP – unidade básica de transferência de energia.
NADH – NICOTINAMINA ADENINA DINUCLEÓTIDO
FADH2 – FALVINA ADENINA DINUCLEÓTIDO
VISÃO GERAL DOS PROCESSOS
CATABÓLICOS
PROTEÍNAS
GLÚCIDOS
LÍPIDOS
1ª ETAPA
AMINOÁCIDOS
AÇUCARES
SIMPLES
ÁCIDOS
GORDOS
GLICÓLISE
PIRUVATO
ATP
2ª ETAPA
ACETIL CoA
CICLO DO ÁCIDO
CÍTRICO
FOSFORILAÇÃO
OXIDATIVA
3ª ETAPA
ATP
• Fígado e vesícula biliar
o
o
Produzem sais biliares.
Emulsionam as gotas de gorduras – digestão
mais fácil.
• Intestino delgado
Degradação posterior.
Produz aminoácidos, hexoses, ácidos gordos e
glicerol.
o Desloca materiais para o sangue para serem
transportados às células.
o
o
PRIMEIRA ETAPA
• Hidrólise dos alimentos em subunidades mais
pequenas (sistema digestivo).
o
Glândulas salivares
Segregam amilase – digere amido.
o
Estómago
Segrega HCl – desnatura as proteínas e pepsina.
o
Pâncreas
Segrega enzimas proteolíticos e lipases.
Degradam proteínas e lípidos.
SEGUNDA ETAPA
• Conversão de monómeros numa forma que
pode ser oxidada completamente.
Açúcares – começa com a glucose ou frutose –
convertida em acetil-CoA.
o Aminoácidos – todos os desaminados podem
entrar em qualquer etapa.
o Ácidos gordos – convertidos em acetil-CoA.
o
TERCEIRA ETAPA
• Oxidação completa de nutrientes e a produção
de ATP.
o
o
o
Tudo é convertido em acetil-CoA
O acetil entra no ciclo do ácido cítrico
Onde é convertido em CO2 e energia (ATP)
METABOLISMO DA GLUCOSE
VIAS METABÓLICAS A PARTIR DA
GLUCOSE-6-P
Glucose
Ácido Láctico
Poliósidos
Fermentação
Glicólise
Glucose-6-P
Ciclo de Krebs
Ácido Pirúvico
CO2 + H2O
Ácidos Gordos
Glicerol
Aminoácidos
Lípidos
Proteínas
Pentoses
Ácido Pirúvico
GLICÓLISE
Catabolismo da Glucose
• 1ª etapa do metabolismo dos glúcidos.
• Os açúcares simples são degradados em
piruvato.
• Processo anaeróbico (Fermentação) – não é
necessário oxigénio.
• Todos os seres vivos utilizam este processo.
A glicólise é o processo que leva à “quebra” da glucose. É
a sequência de dez reações enzimáticas, na qual uma
molécula de glucose é convertida em duas moléculas de
gliceraldeído-3-fosfato. Dos três piruvatos carbónicos há o
aparecimento de 2 ATP’s. A glicólise é extremamente
importante pois tem um papel de destaque no fornecimento
de energia sob a forma de ATP e na preparação da
glucose e outros compostos para seguintes degradações
oxidativas.
• A glicólise pode ser decomposta em duas partes:
• Parte I (Investimento energético – reações 1-5)
o
Na sua fase inicial a glucose é fosforilada e partida de forma
a “aguentar” duas moléculas de fosfato. Este processo
consome 2 ATP’s.
• Parte II (Recuperação energética – reações 6-10)
o
As duas moléculas de gliceraldeído-3-fosfato são
convertidas em piruvato, com a redução de 4 ATP’s.
• Assim a glicólise vai ter um balanço total positivo de 2
ATP’s, visto que na fase inicial são gastos dois ATP’s.
Equação geral da glicólise
Parte I
ENZIMAS E REAÇÕES DA PARTE I
• Hexocinase: Primeira utilização do ATP:
o
A reação 1 da glicólise é a transferência de um grupo fosforil do ATP
para a glucose, formando glucose-6-fosfato (G6P), numa reação
catalisada pelo enzima hexocinase.
• Isomerase fosfoglucosídica:
o
A reação 2 da glicólise é a conversão do G6P em frutose-6-fosfato
(F6P), através da ação do enzima isomerase fosfoglucosídica
(transformação de uma hexose numa pentose).
• Fosfofrutocinase: segunda utilização de ATP:
o
A reação 3 da glicólise é catalisada pelo enzima fosfofrutocinase. Este
último fosforila o F6P, formando fructose-1,6-bifosfato (FBP ou F1,6P).
Esta reação é semelhante à reação 1 e também se dá na presença do
ião Mg2+.
• Aldolase:
o
A reação 4 da glicólise é catalisada pelo aldolase e é onde há a quebra
do FBP para formar duas trioses: gliceraldeído-3-fosfato (GAP) e
dihidroxoacetonofosfato (DHAP).
• Isomerase Fosfotriose:
o
A reação 5 da glicólise, apenas o GAP continua o processo glicolítico.
No entanto, como o GAP e o DHAP são isómeros funcionais aldeídocetona, podem ser interconvertidos por uma reacção de isomerização
por intermédio de um enodiol. O triosefosfato isomerase catalisa este
processo.
Parte II
ENZIMAS E REAÇÕES DA PARTE II
• Gliceraldeído-3-fosfato desidrogenase: primeira formação
energética:
o
A reação 6 da glicólise é a oxidação e fosforilação do GAP pelo NAD+ e
Pi, catalisada pelo enzima gliceraldeído-3-fosfato desidrogenase. Nesta
reação (oxidação aldeídica), uma reação exergónica conduz à síntese
do altamente energético 1,3-bofosfoglicerato (1,3-BPG).
• Fosfoglicerato-cinase: primeira formação de ATP:
o
Na reacão 7 da glicólise forma-se 1 ATP, sobrando 3-fosfoglicerato
(3PG), numa reação catalisada pelo enzima fosfoglicerato-cinase. De
notar a ligação Mg2+-ADP.
• Fosfoglicerato-mutase:
o
Na reação 8 da glicólise 3PG é convertido em 2-fosfoglicerato (2PG)
pelo enzima fosfoglicerato-mutase. Um mutase cataliza a troca
intramolecular de um grupo funcional de uma posição para outra.
• Enolase: segunda formação energética:
o
Na reação 9 o 2PG é desidratado para fosfoenolpiruvato (PEP), numa
reação catalisada pelo enolase.
• Piruvato-cinase: segunda formação de ATP:
o
Na última reação 10 da glicólise, o enzima pirovato-cinase junta a
energia livre resultante da “quebra” do PEP, sintetizando ATP e
formando piruvato.
Três destinos possíveis para o Piruvato
formado na Glicólise
PIRUVATO É O ACEITADOR TERMINAL NA
FERMENTAÇÃO DO ÁCIDO LÁCTICO
• Quando os tecidos humanos não são fornecidos com
oxigénio suficiente para suportar a oxidação aérobica do
piruvato e do NADH produzidos na glicólise, o NAD+ é
regenerado pela redução do piruvato em lactato.
(fígado – ciclo de Cori).
ETANOL É O PRODUTO DA REDUÇÃO NA
FERMENTAÇÃO ALCOÓLICA
• Os microorganismos fermentam a glucose em etanol e
CO2, em vez de lactato. A glucose é convertida em
piruvato pela glicólise, e o piruvato é convertido em
etanol e CO2 num processo de duas etapas:
CICLO DO ÁCIDO CÍTRICO
• Etapa final do metabolismo dos glúcidos, lípidos
e aminoácidos.
• É também chamado de ciclo de Krebs em honra
de Hans Krebs, primeira pessoa a descrevê-lo.
• É um processo com 9 etapas (8+1).
• É um ciclo oxidativo.
Requer oxigénio (Aeróbico)
SÍNTESE DO ACETIL-COEZIMA A
• O acetil-coenzima A é formado do piruvato através de
descarboxilação oxidativa por um complexo multienzimático
(grupo de enzimas associadas entre si não covalentemente que
catalisam dois ou mais passos sequenciais de um processo
metabólico) chamado desidrogenase pirúvica.
• Este complexo possui múltiplas cópias de três enzimas: E1, E2 e
E3.
• O complexo desidrogenase pirúvica catalisa cinco reações
sequenciais:
o O piruvato é oxidado a acetato, com a libertação de CO2.
o Alguma energia da oxidação é conservada pela redução de
NAD+ a NADH.
o Parte da energia restante é armazenada temporariamente,
adicionando a molécula de CoA Acetil-CoA.
ENZIMAS E REAÇÕES DO CICLO DO ÁCIDO
CÍTRICO
• Reação 1: Citrato sintase
o
O enzima citrato sintase medeia a reação da Acetil-CoA e oxaloacetato
a citrato.
• Reação 2: Aconitase
o
Mediador da reação de isomerização do citrato a isocitrato.
• Reação 3: Isocitrato desidrogenase
o
Este enzima conduz à descarboxilação oxidativa do isocitrato a αcetoglutarato.
• Reação 4: a-cetoglutarato desidrogenase
o
Esta reação é a reação de descarboxilação oxidativa do α-cetoglutarato
a succinil-CoA.
• Reação 5: Succinil-CoA sintetase
o Hidrólise da succinil-CoA a succinato por fosforilação do GTP.
• Reação 6: Succinato desidrogenase
o Desidrogenação estereoespecífica do succinato a fumarato.
• Reação 7: Fumarase
o Hidratação estereoespecífica do fumarato a L-malato.
• Reação 8: Malato desidrogenase
o Oxidação do L-malato a oxaloacetato.
REGULAÇÃO DO CICLO DO ÁCIDO
CÍTRICO
• A disponibilidade de substratos, a inibição pelos
produtos e a inibição por feedback por outros
intermediários
do
ciclo,
influenciam
a
operacionalidade deste ciclo.
• O ciclo á assim regulado por mecanismos de
feedback, que coordenam a produção de NADH
com o gasto energético.
NATUREZA ANFIBÓLICA DO CICLO DE
KREBS
Um trajeto metabólico ou é catabólico ou é
anabólico. O ciclo de Krebs é catabólico, pois
envolve degradação e é um importante sistema de
conservação energético nos organismos. No
entanto, muitos dos produtos intermediários deste
ciclo são usados em biossíntese, ou seja, em
reações anabólicas. O ciclo de Krebs é assim
anfibólico (catabólico e anabólico em simultâneo).
Balanço global em termos de número de moléculas de ATP
produzidas por molécula de glucose
• A energia do transporte eletrónico é conservada através da síntese de
ATP pela fosforilação oxidativa:
o Por cada NADH são produzidas cerca de 2,5 moléculas de ATP.
o Por cada FADH2 são produzidas cerca de 1,5 moléculas de ATP.
Fase
NADH
FADH2
ATP
(formado)
ATP
(mobilizado)
Glicólise
2
2,5 X 2 +2 = 7 ou 5*
2
Formação de Acetil
CoA
2
2,5 X 2 + 2 = 7
Ciclo de Krebs
4
2
6 X 2,5 + 2 X 1,5 + 2
(GTP/ATP) = 20
SUB-TOTAL
34 ou 32
Total
2
32 ou 30
Nos músculos e no cérebro 3 ATP
30 ATP por molécula de glucose => 2 Ciclos de Krebs
Uma molécula de glucose => 2 piruvatos
As três etapas do catabolismo das
proteínas, ácidos gordos e hidratos de
carbono na respiração celular.
Etapa 1: oxidação dos ácidos gordos,
glucose alguns aminoácidos produzem
acetil-CoA.
Etapa 2: oxidação de grupos acetil no
ciclo de Krebs inclui quatro passos onde
os eletrões são abstraídos.
Etapa 3: os eletrões são levados pelo
NADH e FADH2 são funilizados para uma
cadeia de transportadores de eletrões
mitocondriais – cadeia respiratória –
reduzindo o O2 a H2O. Esta corrente de
eletrões leva à produção de ATP.
MITOCÔNDRIA
• A mitocôndria é um organelo
celular que possui uma
membrana externa permeável
à maioria das micromoléculas
e uma outra membrana
interna, que contém uma
vasta área de invaginações.
O número de invaginações
chama-se crista e reflete a
atividade respiratória da
célula, pois é aí que se dá o
transporte eletrónico.
FOSFORILAÇÃO OXIDATIVA
A fosforilação oxidativa é um processo pelo qual é
formado ATP quando os eletrões são transferidos
do NADH e do FADH2 para o O2, através de uma
série de transportadores eletrónicos. A fosforilação
ocorre na membrana interna da mitocôndria. O
ciclo de Krebs e a oxidação dos ácidos gordos, que
fornecem a maior parte dos cofatores reduzidos,
dão-se na matriz mitocondrial. A oxidação e a
fosforilação são processos acoplados.
• A transferência eletrónica dá-se passo a passo, do
NADH ou FADH2 para o O2, através de uma série de
transportadores eletrónicos (I, III, IV), o que produz um
bombardeamento de protões para fora da matriz
mitocondrial. Gera-se assim uma força, que consiste
num gradiente de pH e num potencial eletroquímico
transmembranar.
• O ATP é assim sintetizado quando os protões voltam a
entrar na matriz mitocondrial através de um complexo
enzimático (V-ATPase). A cadeia respiratória consiste
em 3 complexos enzimáticos (I, III, IV), ligados por dois
transportadores eletrónicos: CoQ e Citocromo C.
• A energia livre libertada no transporte eletrónico
é conservada de modo a ser utilizada pelo
ATPsintetase. Tal conservação energética é
chamada de acoplamento energético de
transdução de energia.
• Hipótese Quimiosmótica:
o
Esta teoria pressupõe que á acoplamento do
transporte eletrónico gerando a síntese de ATP devido
à criação de um gradiente protónico na membrana
mitocondrial interna.
• Dados experimentais que comprovam a Teoria
de Mitchell:
o
o
o
o
o
1. A fosforilação oxidativa requer membranas
intatas.
2. A membrana mitocondrial interna é impermeável a
iões, pois a sua livre difusão iria descarregar o
gradiente eletroquímico.
3. Durante o transporte eletrónico é gerado um
gradiente protónico através da membrana.
4. Compostos que aumentam a permeabilidade da
membrana a H+, dissipando assim o gradiente
eletroquímico (desacopladores), permitindo o
transporte eletrónico, mas parando a síntese de ATP.
5. O aumento artificial da acidez no exterior da
membrana estimula a síntese do ATP.
FORÇA PROTOMOTRIZ
Força protomotriz = Gradiente Químico (∆pH) + Potencial da membrana
(Em)
∆G= 2.3 RT ∆pH + Z ∆ψ F
Sendo:
o
o
o
Z – carga do protão
∆ψ- potencial da membrana
F- constante de Faraday
∆pH = (pH matriz) – (pH citosol)
METABOLISMO DO GLICOGÉNIO E
GLUCONEOGÉNESE
• O glicogénio funciona nos animais como uma
reserva de glucose (polimerizada) de fácil
mobilidade, sendo uma constante fonte de
glucose/energia para todos os tecidos. O
glicogénio é armazenado principalmente no
fígado.
• O glicogénio é assim um polímero de glicose,
com ligações α-1,4 em cadeia e ligações α-1,6
para as ramificações (cada ramificação tem de 8
a 12 resíduos).
Grânulos e Estrutura do
Glicogénio
• Porquê glicogénio?
1. Regulação dos níveis de glucose no sangue,
pois o gerado pelo metabolismo das gorduras é
insuficiente.
o 2. Libertação da glucose entre refeições e
durante a atividade muscular, pois os músculos
não mobilizam a gordura tão rapidamente como o
glicogénio.
o
• Porquê estrutura ramificada?
o
o
1. Maior solubilidade.
2. Maior número de pontos de metabolização, ou
seja, vai possuir vários extremos não redutores
por onde a remoção sequencial se dá, tendo por
seu lado apenas um extremo redutor.
DEGRADAÇÃO DO GLICOGÉNIO
• A degradação do glicogénio dá-se através de um processo que
inclui 3 enzimas: glicogénio fosforilase, transferase e
fosfoglucomutase.
• 1. Glicogénio fosforilase
• 2. “Debranching enzyme”
(transferase)
• Este enzima remove as
ramificações do glicogénio,
tornando os resíduos de glicose
acessíveis para a ação da enzima
glicogénio fosforilase.
• 3. Fosfoglucomutase
• Converte G1P em G6P, que pode ter vários destinos metabólicos.
SÍNTESE E TRANSPORTE DA
GLUCOSE
CONTROLO DO METABOLISMO DO
GLICOGÉNIO
• A síntese e degradação do glicogénio são exergónicos
em condições fisiológicas, logo, tal facto torna a sua
regulação importante, de acordo com as necessidades
celulares. Assim, o glicogénio fosforilase entra em
“competição” com o glicogénio sintetase, consoante as
necessidades do organismo em questão.
• O controlo dá-se por:
o
1. Regulação alostérica: controlo da concentração de cada
uma dos enzimas anteriores por inibidores.
o
2. Modificações covalentes, por controlo hormonal:
o
o
Insulina, situado no fígado, estimula a síntese do glicogénio.
Epinefrina (músculo) e glucagon (fígado), estimulam a
degradação do glicogénio, mediada pelo AMP cíclico
(cAMP).
3. Regulação em cascata: fosforilação/defosforilação/
controlo hormonal.
o
• Para uma taxa de glucose baixa no sangue, temos:
Para uma taxa alta de glucose no sangue, temos:
CONTROLO DOS NÍVEIS DE
GLUCOSE
• Insulina
Hormona produzida pelas células beta do
pâncreas.
o Armazenada como pro-insulina (forma inactiva)
sob a forma de pequenos grânulos.
o A sua libertação é desencadeada pelo aumento
dos níveis de glucose no sangue.
o Estimula a absorção de glucose nos tecidos pela
ligação a recetores na membrana celular.
Permitindo assim a entrada de glucose na célula.
o
AÇÃO DA INSULINA
• Glucagon
Hormona produzida no pâncreas sob forma inativa.
Baixos níveis de glucose resulta a sua conversão
numa forma ativa e é libertada.
o A sua entrada nas células do fígado (hepatócitos)
resulta na conversão do glicogénio em glucose. A
glucose é libertada no sangue.
o
o
• Epinefrina
o
o
o
Adrenalina – hormona de emergência e combate.
Também atua no sistema nervoso.
Resulta uma prontidão rápida de todos os sistemas.
AÇÃO DO GLUCAGON E DA EPINEFRINA