GABARITO
Química E – Extensivo – V. 5
Exercícios
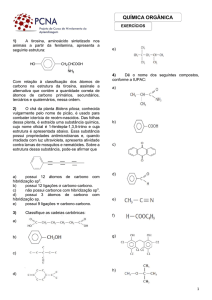
01)a)
b)
02)F – V – V – F
a)Errada. Existem séries homólogas em qualquer
função.
b)Certa. Na série homóloga, cada membro tem um
CH2 a mais. Massa molecular: 14µ.
c)Certa. Ponto de fusão e ebulição crescem com o
aumento da massa.
d)Errada. As propriedades químicas não diferem,
pois os elementos da série homóloga pertencem à
mesma função química.
05)a)CH2 = CH2 (1º membro)
CH2 = CH – CH3 (2º membro)
propeno
b)H2C = CH – CH2 – CH2 – CH3
1-penteno
H3C – CH = CH – CH2 – CH3
2-penteno
06)a)
03)V – V – F – F – V
a)Certa. Possui dois CH2 a mais.
b)Certa. Butano possui dois H2 a mais que o buteno.
CH3 – CH2 – CH2 – CH3 CH2 = CH – CH2 – CH3
Butano Buteno
c)Errada. Não são de série alguma, pois são isômeros
(C3H6).
d)Errada. Pertencem a série homóloga (diferenciam-se
por CH2).
e)Certa. Mesmo número de carbono na cadeia e
funções diferentes.
b)Apresenta isomeria óptica, pois tem carbono assimétrico (4 ligantes diferentes).
Isômeros: anfetamina dextrógira e anfetamina levógira.
04)V – V – F – V – V
07)B
a)Certa. Mesmo número de carbonos na cadeia e
funções diferentes.
b)Certa. A molécula é apolar, faz ligações intermoleculares do tipo dipolo induzido (fracas), portanto,
evapora com facilidade (baixo ponto de ebulição).
c)Errada. VI é o mais volátil por ser apolar.
d)Certa. Possui oxigênio ligado a hidrogênio.
e)Certa. O oxigênio ligado ao hidrogênio na carboxila
gera polaridade na molécula.
Possui 2 carbonos assimétricos diferentes.
Isômeros opticamente ativos. 2n → nº carbonos assimétricos
22 = 4 → d1, d2, 1, 2
Química E
1
GABARITO
11)C
08)D
I. Errada.
2 ligantes iguais.
II. Certa.
4 ligantes diferentes.
I. Errada.
II. Certa.
III.Certa.
4 ligantes diferentes.
III.Certa.
IV.Certa.
4 ligantes diferentes.
V.Errada.
IV.Errada.
2 ligantes iguais.
09)Apenas a substância 3.
12)a)Amina e fenol
b)Noradrenalina
* Carbono assimétrico: 4 ligantes diferentes
10)E
a)Errada. CH3 – CH2 – CH2 – CH3
13)E
a)Errada. Não são isômeros.
b)Errada. É amina primária.
c)Errada. Apenas carbonos primários e secundários.
d)Errada. Não possui carbono assimétrico.
e)Certa.
b)Errada.
c)Errada.
d)Errada.
14)E
e)Certa.
2
Química E
Na isomeria óptica, um isômero corresponde à imagem do outro, como em um espelho. As imagens são
sobreponíveis.
GABARITO
15)B
18)B
16)D
19)D
17)B
20)A
Isômeros ópticos – um é a imagem especular do outro.
21)D
43 ligações sigma (as ligações simples e uma das duas
na dupla).
7 ligações pi (uma das duas na dupla).
2 carbonos assimétricos (*)
Química E
3
GABARITO
22)D
a)Errada. CH3 – CH2 – CH2 – CH2 – CH3 – não apresenta isomeria óptica.
b)Errada.
– não apresenta isomeria óptica.
c)Errada.
– não apresenta isomeria óptica.
d)Certa.
– isomeria óptica.
e)Errada. CH3 – CH2 – CH2 – CH2 – CH2 – CH3 – não apresenta isomeria óptica.
25)E
23)A
Cadeia aromática insaturada, com carbono assimétrico,
de massa molar 206 g/mol
24)B
26)12
01.Errada. o nome correto é 3,4,4-trimetil-2-hexeno.
02.Errada. possui apenas dois isômeros de posição:
1-pentino e 2-pentino.
04.Certa. os ligantes dos carbonos da dupla ligação são
diferentes entre si.
08.Certa. possui um carbono quiral (assimétrico – carbono 2).
16.Errada. I, II e III são insaturados, porém, apenas II tem
carbono sp (tripla ligação).
27)E
a)Errada.
(apenas 3 ligantes)
b)Errada.
c)Errada.
4
Química E
(2 ligantes iguais)
(3 ligantes iguais)
GABARITO
d)Errada.
e)Certa.
29)A
(apenas 3 ligantes)
I. Certa.
II. Certa.
III.Certa. posições I e III.
IV.Errada. nenhum dos dois compostos possui carbono
assimétrico.
(4 ligantes diferentes)
28)A
a)Certa. apenas o triptofano possui carbono assimétrico
(4 ligantes diferentes) e, portanto, tem atividade óptica.
b)Errada. apenas o triptofano é aminoácido (funções amina
e ácido). A serotonina possui as funções amina e fenol.
c)Errada. Além da hidroxilação, a serotonina tem a menos a função ácido.
d)Errada. não possuem a mesma fórmula molecular,
logo, não são isômeras.
e)Errada. apenas a serotonina tem a função fenol.
30)A
a)Certa. nas duas estruturas, nos carbonos da dupla ligação, os ligantes são diferentes entre si (permitem isomeria
geométrica).
b)Errada. nenhuma das duas estruturas possui carbono assimétrico (quiral).
c)Errada. ambas possuem a função fenol (hidroxila ligada ao anel aromático).
d)Errada. a presença do grupo OH (hidroxila) ligado ao anel aromático confere característica ácida, pois o hidrogênio
pode ser liberado.
e)Errada. ésteres são formados a partir de álcoois, e não de fenóis.
31)45
01.Certa.
02.Errada. Apresenta isomeria geométrica.
04.Certa.
08. Certa.
16.Errada. o tolueno é o metil benzeno;
32. Certa.
Química E
5
GABARITO
32)V – F – V – V – F
(V)
(F)
(V)
(V)
(F) Não há isômero de mesma função que o metanoato de metila (a cadeia já é a menor possível para essa função).
33)A
* Carbono quiral (assimétrico) – possui 4 ligantes diferentes entre si
34)B
a)Errada. as três estruturas possuem a função ácido carboxílico, porém, a estrutura I não possui centro quiral.
b)Certa. I é de cadeia aberta sem carbono assimétrico enquanto que II e III possuem parte da cadeia fechada (ciclo),
ambas com carbono assimétrico.
c)Errada. o nome está correto, porém, corresponde ao composto trans.
d)Errada. possui as funções álcool, ácido carboxílico e éster (mencionada na alternativa como cetona).
e)Errada. III possui 6 centros quirais (sinalizados na estrutura com marcação preta ou tracejada).
35)C
36)D
a)Errada. apenas a estrutura I pode apresentar isômeros ópticos, pois somente
ela apresenta carbono assimétrico (carbono 3 a partir da hidroxila).
b)Errada. ambas pertencem à mesma função (álcool). São isômeros de posição.
c)Certa. Carbono 3.
d)Errada. Ambas pertencem à função
álcool.
e)Errada. um dos carbonos da dupla
possui dois ligantes iguais (metil).
6
Química E
Isômeros d e l ⇒ mesma fórmula molecular, estrutural e plana.
São imagens especulares não superponíveis.
GABARITO
37)B
A glicina não possui carbono quiral ⇒ não há isomeria óptica ⇒ não apresenta enantiômeros
38)B
41)C
I e II → 4 ligantes diferentes no carbono.
I.
III.
III.
IV.
42)25
39)D
01.Certa.
02.Errada. Apenas 2 carbonos assimétricos (*).
04.Errada. A cadeia é saturada (entre os carbonos somente
existem ligações simples).
08.Certa. sp3 (ligados a apenas mais um carbono) sp2
(ligados a dois outros carbonos).
16.Certa. 2 carbonos assimétricos = 4 isômeros ativos e
2 inativos.
40)D
a)Errada. Apenas um carbono quiral.
b)Errada. não possui grupo fenol (as hidroxilas
representam álcoois nessa estrutura).
c)Errada. Apenas um carbono quiral.
d)Certa.
e)Errada. Apenas um carbono quiral e 4 grupos
aromáticos.
43)a)A substância apresenta os seguintes grupos funcionais:
ácido carboxílico, álcool e sal de alquilamônio (sal de amônio quaternário).
b)A antopleurina possui 2 carbonos assimétricos diferentes
e, portanto, 4 isômeros opticamente ativos, sendo dois
dextrogiros e dois levogiros. Possui 2 misturas racêmicas
(opticamente inativas) e quatro pares de compostos diastereômeros (que não formam misturas racêmicas). Observação: a antopleurina atua como feromônio de alarme.
Química E
7
GABARITO
44)E
48)B (considerar os compostos I e III)
a)Errada. A fórmula correta da banana é C7H14O2.
b)Errada. os compostos são ésteres.
c)Errada. Ambas possuem ligação π (uma das duas
ligações na ligação dupla).
d)Errada. não são isômeros.
e)Certa.
45)D
Considerando o 2,3-diclorobutano:
49)D
A presença do carbono assimétrico (quiral) permite que
a molécula tenha atividade óptica.
50)A
I. Certa.
II. Errada. possui 3 centros quirais (carbonos assimétricos).
III.Certa. possui carbonos assimétricos, logo, possui
atividade óptica.
IV.Errada. é uma ceto-hexose (hexose que contém um
grupo cetona).
51)B
46)E
a)Errada. nenhuma das duas possui carbono assimétrico e por isso não possuem isômeros ópticos.
b)Errada. não possui carbono assimétrico.
c)Errada. possui as funções fenol e éter, não permitindo tautomeria.
d)Errada. A substância I é um fenol (e não álcool
aromático).
e)Certa. os carbonos 2 e 3 possuem cada um ligantes
diferentes entre si, o que permite a isomeria geométrica.
52)D
a)Errada. São isômeros de cadeia. I tem cadeia aberta
e III tem cadeia fechada.
b)Errada. I não possui isomeria geométrica, IV pode
ter.
c)Errada. O composto IV também apresenta isomeria
óptica (possui carbono assimétrico).
d)Certa. I e II diferem apenas na posição da dupla
ligação, I e III diferem na cadeia (I é aberta e III é
fechada).
e)Errada. São isômeros de posição.
47)B
a)Errada. não são isômeros (as fórmulas moleculares
são diferentes).
b)Certa.
c)Errada. Ambas possuem carbono assimétrico.
d)Errada. não apresentam carbonila nem grupos
fenóis.
53)B
8
A sarcomina possui 1 carbono assimétrico. Logo, terá
dois isômeros opticamente ativos (dextrógiro e levógiro).
Química E
O único composto que possui atividade óptica é o
composto do item B, pois é o único que possui carbono
assimétrico (quiral).
GABARITO
54)D
59)16
A molécula de glicose possui 4 carbonos assimétricos diferentes.
Número de isômeros opticamente ativos: 2n
24 = 16
O número de isômeros opticamente ativos é
dado por 2n, em que n = número de carbonos
assimétricos diferentes.
Como o composto possui 3 carbonos assimétricos diferentes: 23 = 8.
60)B
O único composto que possui carbono assimétrico é o da alternativa b. Antípodas ópticos são isômeros resultantes da assimetria
da molécula.
61)C
55)B
Os enantiômeros são moléculas que se configuram como imagens uma da outra no espelho (especulares) e não são sobreponíveis.
56)A
a)Certa. há na molécula um pequeno ciclo
que mantém os carbonos fixos (sem rotação com seus ligantes), o que permite a
formação de isômeros cis e trans (isomeria
geométrica).
b)Errada. pertence à função éter.
c)Certa. Dois carbonos assimétricos estão
presentes na estrutura. São os carbonos
do ciclo.
d)Errada. possui apenas um carbono terciário
(carbono 2).
62)53
01.Certa. todos os compostos possuem a mesma fórmula molecular.
02.Errada. o carbono possui 3 ligantes iguais. Assim, a molécula
não tem atividade óptica.
04.Certa. nome IUPAC: 2-metil-1-propanol.
08.Errada. são isômeros de cadeia (A tem cadeia normal e B,
cadeia ramificada).
16.Certa. um é a imagem especular do outro.
32.Certa. a diferença entre eles é a posição da hidroxila.
63)C
a)Errada. CH3 – CH = CH – CH3 – apenas isomeria geométrica.
b)Errada.
– apenas isomeria óptica.
57)C
Para haver atividade óptica, os 4 ligantes do
carbono devem ser diferentes entre si.
c)Certa.
d)Certa.
58)08
O número de isômeros opticamente inativos
(mistura racêmica) é dado por:
IOI = 2n–1
128 = 2n–1
27 = 2n–1
7=n–1
n=8
e)Errada.
– apenas isomeria óptica.
– apenas isomeria geo-
métrica.
Química E
9
GABARITO
64)C
– propanona
– todas as ligações simples são sigma.
a)Certa.
b)Certa. Não apresenta isômeros cis-trans.
c)Errada. Não possui carbono quiral.
d)Certa.
e)Errada.
65)E
66)B
A existência de centro quiral (carbono assimétrico) caracteriza a isometria óptica.
67)B
CH3 – CH = CH – CH2 – SH
10
Química E
GABARITO
a)Certa.
b)Errada. – não possui carbono assimétrico (quiral).
c)Certa.
d)Certa. CH3 – CH = CH – CH2 – SH e CH2 = CH – CH2 – CH2 – SH
e)Certa. CH3 – CH = CH – CH2 – SH e 68)C
a)Errada. A isomeria de cadeia ocorre entre compostos de mesma função.
b)Errada. São denominados isômeros ópticos ou enantiômeros.
c)Certa.
d)Errada. Os diasteroisômeros são isômeros ópticos não enantiomorfos, que apresentam propriedades físicas diferentes.
e)Errada. A mistura racênica é opticamente inativa.
69)E
Os compostos que desviam a luz polarizada para a esquerda são chamados levógiros.
70)B e E
a)
b)
c)
d)
e)
O item b estaria errado com o nome 2,4-dicloro-3-nitro pentano
Química E
11