IPT
Química 1
Hidrocarbonetos alifáticos
Classificação
Nomenclatura
Sumário
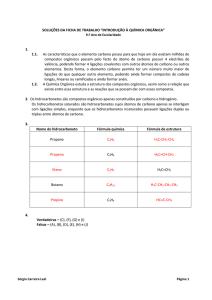
Hidrocarbonetos
Variação da volatilidade com o nº de carbonos
Hidrocarbonetos insaturados
Hidrocarbonetos Aromáticos
Nomenclatura
João Luís Farinha Antunes
Escola Superior de Tecnologia de Tomar
Departamento de Arte, Conservação e Restauro
1
2
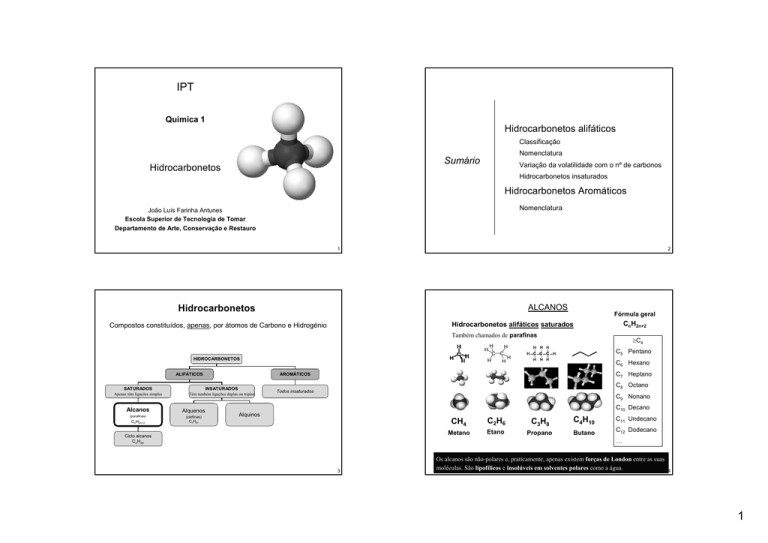
ALCANOS
Hidrocarbonetos
Fórmula geral
CnH2n+2
Hidrocarbonetos alifáticos saturados
Compostos constituídos, apenas, por átomos de Carbono e Hidrogénio
Também chamados de parafinas
≥C4
C5 Pentano
HIDROCARBONETOS
ALIFÁTICOS
SATURADOS
INSATURADOS
Apenas têm ligações simples
Têm também ligações duplas ou triplas
Alcanos
Alquenos
(parafinas)
(olefinas)
CnH2n
CnH2n+2
C6 Hexano
C7 Heptano
AROMÁTICOS
C8 Octano
Todos insaturados
C9 Nonano
C10 Decano
Alquinos
Ciclo alcanos
CnH2n
CH4
C2 H6
C3 H8
C4H10
Metano
Etano
Propano
Butano
C11 Undecano
C12 Dodecano
…
3
Os alcanos são não-polares e, praticamente, apenas existem forças de London entre as suas
moléculas. São lipofílicos e insolúveis em solventes polares como a água.
4
1
Pontos de fusão e ebulição dos hidrocarbonetos. Produtos correntes
P.Fusão
Pontos de fusão e ebulição dos hidrocarbonetos
250
temperatura / ºC
200
s
Gá
150
100
temp ambiente
ido
Líqu
50
0
-50
-100
Sólido
-150
-200
-250
0
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
nº de átomos de carbono
fusao
ebulição
P. ebulição
Estado a
/oC
/oC
25oC
CH4
-182
-164
gas
etano
C2 H6
-183
-89
propano
C3 H8
-190
-42
butano
C4H10
-138
-0.5
pentano
C5H12
-130
36
hexano
C6H14
-95
69
heptano
C7H16
-91
98
octano
C8H18
-57
125
nonano
C9H20
-51
151
decano
C10H22
-30
174
undecano
C11H24
-25
196
dodecano
C12H26
-10
216
C20H42
37
343
C30H62
66
450
nome
fórmula
metano
Gás doméstico
líquido
Éteres de petróleo
Gasolina
C5 –C12
White Spirit
C9 –C12
Querosene (petróleo)
C9 –C16
Gasóleo C15 –C18
…
eicosano
…
triacontano
Gás natural
naftas
Variação do estado físico dos hidrocarbonetos com a temperatura
sólido
Ceras de parafina
C20 a C40
Boiling points and structures of hydrocarbons, www.elmhurst.edu, 20/2/08
5
Ceras microcristalinas
C35 a C60
6
Polietileno C100->500.000
Grupos alquilo
Hidrocarbonetos ramificados
nomenclatura
Derivam de alcanos por abstracção de um átomo de hidrogénio.
O respectivo nome obtém-se por
1º Selecciona-se a cadeia mais comprida e dá-se –lhe o nome do alcano
correspondente;
substituição da terminação ano do alcano correspondente por ilo.
2º numeram-se os carbonos a partir da ponta mais ramificada;
3º identificam-se os grupos ramificados;
– CH3
– C2 H5
– C3 H7
– C4 H9
–R
Metil(o)
Etil(o)
Propil(o)
Butil(o)
Alquil(o)
met
et
prop
but
CH4
C2H6
C3H8
Metano
Etano
Propano
C4H10
Butano
CnH2n+1
3º adicionam-se os nomes dos grupos ramificado, com indicação da sua posição, como
prefixo, ao início do nome da cadeia principal, separados por hífenes.
(os prefixos são colocados por ordem alfabética)
Exemplo
R
CnH2n+2
Alcano
7
Grupo etilo (C2H5)
na posição 5
Cadeia mais
comprida
8
2
n (normal), iso
Carbonos primários, secundários e terciários
Normal - n
Os átomos de Carbono são classificados segundo o respectivo grau de
substituição por outros carbonos.
Quando não existem ramificações ou quando o grupo funcional se
encontra no Carbono 1 (sem ramificações, quando existem grupos funcionais)
Carbono primário
C
C
C
C
C
C
C
C
C
C
C
C
C
C
C
C
O H
Carbono secundário
Carbono terciário
n-octanol
n-octano
es
Carbono quaternário
d
tá
te
en
tam
c
e
ir
a um outro átomo de carbono.
do
liga
dois outros átomos de carbono.
três outros átomos de carbono.
quatro outros átomos de carbono.
C
ISO
C
Quando a ramificação ocorre no carbono 2
iso propilo
C
C
C
C
C
C
C
C iso-octano
C
C
1º
C C
(ou 2-metil-heptano)
2º
2º
C
iso butilo
C
3º
C
C
C
C
1º
1º
C 1º
C C C 1º
C 1º
4º
1º
C
9
10
Hidrocarbonetos insaturados
Ligações duplas conjugadas
são hidrocarbonetos com duplas e triplas ligações
Alifáticos
--
H3C
alquenos (duplas ligações)
CH3
conjugadas
alquinos (triplas ligações)
Alternadas com uma ligação simples
Aromáticos (triplas duplas ligações em anéis hexagonais)
Alquenos
H3C
O nome obtém-se substituindo a terminação ano do alcano correspondente por eno,
adicionando, em prefixo, o nº do carbono onde se inicia a dupla ligação.
CH3
Não conjugadas
Duas ligações de intervalo
Os alquenos com várias duplas ligações chamam-se polienos (dieno, trieno, …)
As ligações conjugadas são menos reactivas e mais estáveis
Eteno
etileno
1,3-pentadieno
1-buteno
11
12
3
Hidrocarbonetos aromáticos
Nomenclatura dos compostos aromáticos
São derivados do benzeno. Têm um anel aromático ou benzénico.
Os grupos substituintes são numerados, de 1 a 6, à volta do anel benzénico
Também chamados de arenos por analogia com os alquenos
(que é a base do nome) de forma a resultar nos números mais baixos.
orto
Quando só há 2 substituintes podem designar-se por orto, meta e para
as posiçoes 1,2 , 1,3 e 1,4, respectivamente
meta
Ex:
H
Benzeno
C6H6
H
H
H
O benzeno não é utilizado em restauro devido à
sua muito elevada toxicidade
Cl
CH
H
H
C
C
C
H
C
C
C
CH
CH
H
H
Não confundir com benzina, que é uma mistura de
hidrocarbonetos alifáticos (C5,C6, e C7) e aromáticos
1,2,3-tri metil benzeno
C
C
C
C
C
C
para
Cl
1,4-di cloro benzeno
ou
para di cloro benzeno
1-etil-2-metil-benzeno
ou
orto etil metil benzeno
Sem espaços entre os prefixos
Alguns (muitos) compostos derivados do benzeno têm nomes próprios.
Ex: Tolueno (metil benzeno) C6H5CH3; Fenol (hidroxi benzeno) C6H5OH
13
14
Hidrocarbonetos aromáticos importantes em CR
Grupos aromáticos substituintes
Quando anel benzénico é o grupo substituinte noutra cadeia toma o nome de fenil(o)
Xileno
Tolueno
H
H
Ex:
C
C
C
H
H
H
Grupo fenilo
C
C
C
C
C
C6H4(CH3)2
C6H5CH3
C
C
O xileno é uma mistura de 3 isómeros
C
C
C
C
C
3-fenil-octano
C6H5 –
Outro grupo substituinte importante é o benzil(o) C6H5CH2--
H
H
orto-xileno
C
H
Ex:
meta-xileno
para-xileno
H
H
Comercialmente é chamado Xilol (de forma incorrecta)
H
Comercialmente é chamado
H
Cloreto de benzilo
4-benzil-octano
Toluol (de forma incorrecta)
Grupo benzilo
C6H5 CH2 –
O White Spirit é uma mistura de hidrocarbonetos contendo
cerca de 20 % de aromáticos.
15
16
4
fim
João Luís Farinha Antunes
Instituto Politécnico de Tomar
Departamento de Arte, Conservação e Restauro
[email protected]
17
5