INDICE
RESUMO
3
ABSTRACT 4
TABELAS
5
INTRODUÇÃO
6
MATERIAL E MÉTODOS 7
DESENVOLVIMENTO
8
Definição de conceitos 8
Epidemiologia 9
Fisiopatologia 10
Manifestações Clínicas 17
Exames Complementares de Diagnóstico 17
Tratamento 22
CONCLUSÃO
30
REFERÊNCIAS BIBLIOGRÁFICAS
31
Resumo
Sarcopenia pode ser considerada uma síndrome geriátrica caracterizada por perda de
massa muscular e força e/ou performance física sendo que é necessário a documentação de
dois dos três critérios anteriormente citados para se estabelecer o diagnóstico. Esta condição
pode ter consequências muito graves, como é exemplo a síndrome de fragilidade no idoso.
Atualmente a sarcopenia afeta mais de 50 milhões de pessoas em todo o mundo e pode
vir a afetar mais de 200 milhões de indivíduos nos próximos 40 anos, sendo que é um
problema atual e com importância crescente na sociedade.
Em relação à fisiopatologia desta condição há que realçar um estado de inflamação
crónica
decorrente
do
envelhecimento,
alterações
na
fisiologia
do
músculo,
neuroenvelhecimento, alterações hormonais, sedentarismo, alterações intrínsecas do músculo
esquelético e redução tanto da resposta anabólica ao exercício físico como da resposta
anabólica à nutrição.
Os exames complementares de diagnóstico podem ser divididos em 4 classes: métodos
para determinação de massa muscular, métodos para avaliar a força muscular, métodos para a
determinação de performance física e marcadores biológicos.
O tratamento e prevenção mais adequados passam pela combinação de nutrição
apropriada com treino de resistência, estando a aplicação de métodos farmacológicos
reservada para situações particulares. Novos fármacos encontram-se atualmente em processo
de investigação.
PALAVRAS CHAVE: Envelhecimento, Sarcopenia, Fisiopatologia, Diagnóstico, Tratamento
Abstract
Sarcopenia can be considered a geriatric syndrome characterized by loss of muscle
mass and strength and/or physical performance; to establish this diagnosis is necessary the
documentation of at least two of the three previous criteria. This condition can have very
serious consequences, as the frailty syndrome in the elderly.
Currently, sarcopenia affects over than 50 million people worldwide and it could
affect more than 200 million people over the next 40 years. It is an actual problem and its
importance is increasing in our society.
The pathophysiology of this condition includes the state of chronic inflammation due
to aging, changes in muscle physiology, neuro-aging, changes in hormone levels, sedentary
lifestyle, intrinsic alterations of skeletal muscle and the reduction of both the anabolic
response to physical exercise and the anabolic response to nutrition.
The diagnostic exams can be divided into 4 classes : methods for measuring muscle
mass, muscle strength methods, methods for the determination of physical performance and
biological markers .
Proper nutrition in combination with resistance training are the most suitable resourses
for treatment and prevention of this condition. Application of pharmacological methods still
reserved for particular situations. New drugs are currently under investigation.
KEY WORDS: Aging, Sarcopenia, Pathophysiology, Diagnosis, Treatment
Tabelas
Tabela 1-Métodos para avaliar a massa e imagem muscular [32]
Introdução
Ao longo do ultimo século tem-se assistido a uma alteração na distribuição da
população mundial pelas diversas faixas etárias, em que se observa um aumento da
longevidade em especial nos países desenvolvidos atingindo alguns deles uma esperança
média de vida superior a 80 anos, em oposição com a esperança média de vida do inicio do
século vinte que era cerca de 45-50 anos. Durante o período de 2000 a 2030, estima-se que a
população com mais de 65 anos continue a crescer em número, e que esse aumento represente
um incremento de cerca de 6,9% a 12% na população mundial. Como se pode imaginar, esta
alteração demográfica que se observou e se irá continuar a observar nos próximos anos tem
consequências no que respeita à prestação de cuidados de saúde, à distribuição de cuidados e
a nível económico. [1]
O envelhecimento pode ser visto como um período em que há declínio da função da
maioria dos órgãos e sistemas devido a mecanismos intrínsecos e/ou extrínsecos, existindo
perda progressiva de tecidos saudáveis e acumulação de órgãos e tecidos com função
reduzida. De acordo com Berhard Strehler o envelhecimento é universal, intrínseco,
progressivo e deletério (irreversível). [2] Um idoso saudável é aquele que tem uma vida social
satisfatória, boa condição física e psicológica, apesar de poder ter algumas disfunções como
um certo grau de alteração cognitiva, hipertensão, sarcopenia, osteoporose e outras alterações
associadas a disfunção de órgão alvo. Pode-se então falar em envelhecimento fisiológico,
sendo distinto do envelhecimento patológico que se associa a doenças como as oncológicas,
cardiovasculares, entre outras. [3]
Uma das alterações mais marcantes do envelhecimento ocorre a nível muscular, em
que se observa uma alteração na constituição e diminuição do volume de massa magra com
repercussão funcional importante. Este artigo de revisão foca-se então na sarcopenia no
envelhecimento (do grego “sarx” (carne) +”penia”), abordando esta temática no que respeita à
sua definição, epidemiologia, fisiopatologia, manifestações clínicas, exames auxiliares de
diagnóstico e terapêutica, com o objectivo de na prática clínica se poder reconhecer esta
entidade mais precocemente e propor terapêutica adequada, evitando algumas consequências
nefastas que poderão advir.
Material e Métodos
Para elaborar este artigo de revisão, realizou-se uma pesquisa nas bases de dados
Pubmed/MedLine recorrendo ao serviço de pesquisa da biblioteca do CHUC (Centro
Hospitalar Universitário de Coimbra), com a utilização de palavras chave: Sarcopenia e
Envelhecimento. Numa primeira fase foi fornecida uma listagem de artigos (contendo título,
abstract, autores, datas e revistas onde foram publicados), e de seguida foram selecionados
em função da atualidade da publicação e da potencial relevância para o fim em causa.
O presente artigo de revisão foi redigido com recurso à literatura publicada até ao
momento, e as fontes de informação utilizadas encontram-se devidamente referenciadas.
Desenvolvimento
Definição de Conceitos
O termo sarcopenia que deriva do grego “sarx” (carne) +”penia” foi pela primeira vez
abordado por Irwin Rosenberg em 1989 que o definiu como sendo a perda de massa muscular
que ocorre durante o envelhecimento. [4,5] Atualmente e de acordo com a definição de 2010
da “European Working Group on Sarcopenia in Older People”, pode ser considerado uma
síndrome geriátrica caracterizada por perda de massa muscular e força e/ou performance
física com inevitável aumento do risco de limitação de mobilidade, incapacidade motora,
diminuição da qualidade de vida e morte [6,7], sendo que é necessário a documentação de
dois dos três critérios anteriormente citados para se estabelecer o diagnóstico. A perda de
massa muscular deve corresponder a 2 ou mais desvios padrão a baixo da média da massa
muscular da população jovem de referência, sendo esta documentada por densitometria
(DEXA-“Dual-Energy X-ray Absormetry”) ou análise da impedância bioelétrica (BIA); A
perda de força muscular pode ser diagnosticada por força de preensão da mão ou extensão do
joelho; A reduzida performance física pode ser demonstrada com score reduzido de acordo
com a “Short Physical Performance Battery” . [6]
É necessário descartar outros fatores que condicionariam diminuição da força
muscular que não a perda de massa magra tais como: alteração do metabolismo energético no
músculo, alterações nas inserções tendinosas, alterações na unidade motora, alterações na
microcirculação relacionadas com a libertação de óxido nítrico e a mio-esteatose (infiltração
de adipócitos no músculo) [8,9]. Para além disso será também importante distinguir a
sarcopenia decorrente do envelhecimento de outras formas de perda de músculo secundárias
como a “fome”, malnutrição,
prolongada inatividade física (como exemplo: pessoas
acamadas), embora todos eles se enquadrem num conjunto de factores que contribuem para a
natureza multifatorial deste síndrome.
Sarcopenia deve também ser diferenciada de caquexia, sendo esta ultima definida
como uma síndrome associada a uma doença de base em que há perda de massa muscular
com ou sem perda de massa gorda. Na caquexia a inflamação é o ponto chave da
fisiopatologia e a perda de peso a clinica dominante. Desta forma pode-se dizer que muitas
pessoas com caquexia também têm sarcopenia, ao passo que muitas pessoas sarcopénicas não
podem ser consideradas caquéticas, podendo a caquexia ocorrer em qualquer idade. A
caquexia pode ser vista como uma forma acelerada de sarcopenia relacionada com a idade.
[10,11] Por sua vez a caquexia também deve ser diferenciada de “fome” (“starvation”) e
apesar de não ser totalmente reversível com a terapêutica nutricional de suporte, a reduzida
ingesta de nutrientes tem um papel muito importante no mecanismo fisiopatológico da
caquexia; sendo assim nem todos os doentes malnutridos são caquéticos, ao passo que todos
os doentes com caquexia são malnutridos.[12]
Epidemiologia da Sarcopenia
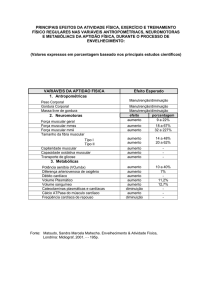
A partir da quarta década de vida observa-se uma perda progressiva de massa
muscular, cerca de 8% por década até aos 70 anos e cerca de 15% nas décadas seguintes, o
que resulta num decréscimo de cerca de 40% na circunferência muscular do braço entre os 30
e os 60 anos. Em relação há força muscular (medido através da força de extensão do joelho),
verifica-se uma perda de cerca de 10-15% por década até aos 70 anos e 25-40% nas décadas
seguintes. De acordo com a literatura é também possível verificar que a perda de massa
muscular é maior no homem que na mulher. [13,14] O compromisso funcional que advém da
perda de massa muscular acarreta consigo um aumento da morbilidade e mortalidade, que por
sua vez representa uma enorme despesa para o Serviço de Saúde. Nos Estados Unidos os
custos atribuídos à sarcopenia no ano 2000 foram estimados em 18,5 biliões de dólares. [15]
A prevalência da sarcopenia observada nos diferentes estudos não é uniforme, já que
existem diferenças na população idosa estudada e na população jovem de controlo (jovens
saudáveis), bem como nas técnicas de medição da massa muscular. Desta forma, a
prevalência da sarcopenia nos idosos com idades entre a sexta e fim da sétima década de vida
varia entre 5% e 13%, aumentando para valores compreendidos entre os 11% e 50% para a
população com 80 anos ou mais. De acordo com a Organização Mundial de Saúde a
população com idade maior ou igual a 60 anos no ano de 2000 era de 600 milhões, sendo que,
no ano 2025 se prevê um aumento desse numero para 1,2 biliões. Desta forma, de acordo com
a prevalência da sarcopenia na população e com os números da Organização Mundial de
Saúde, atualmente a sarcopenia afecta mais de 50 milhões de pessoas em todo o mundo e
pode vir a afectar mais de 200 milhões de indivíduos nos próximos 40 anos. [1,6]
Fisiopatologia
- Alterações na fisiologia do músculo e neuroenvelhecimento
As alterações decorrentes do envelhecimento sobre o músculo, refletem-se em perda
de unidades motoras lentas e rápidas, com perda mais acelerada de unidades motoras rápidas
(neurónio motor+fibra muscular); Para além disso verifica-se ainda atrofia das fibras
musculares tipo II (fibras glicolíticas rápidas).
À medida que as unidades motoras são perdidas (por desenervação), as restantes
unidades vão recrutar as fibras musculares que se encontram desenervadas havendo por isso
uma adaptação. Desta forma há uma conversão de fibras do tipo II em tipo I, à medida que as
fibras tipo II são recrutadas por unidades motoras lentas; como resultado, há pouca alteração
na área total ocupada por fibras tipo I, havendo no entanto um aumento do percentual de
músculo ocupado por fibras tipo I. Há então diminuição da área seccional de músculo,
diminuição do numero total de unidades motoras rápidas, enquanto que o numero de fibras
musculares tipo I sofre pouca alteração (resultado da adaptação que foi mencionada
anteriormente), e o percentual de área muscular ocupado por fibras lentas(tipo I) aumenta.
Tudo isto se traduz numa alteração drástica na função muscular, com diminuição da força
muscular, falta de precisão motora e pode ser a causa do tremor típico observado nos idosos.
[16,17]
Outros níveis do sistema nervoso são também afectados, como o córtex motor, medula
espinhal, neurónios periféricos, e junção neuromuscular. Na medula espinhal há uma perda
preferencial de neurónios motores alfa que suprem unidades motoras rápidas. Nos nervos
periféricos observa-se uma alteração nas bainhas de mielina. Na junção neuromuscular, como
já indicado anteriormente, há um aumento do numero de ramificações dos axónios terminais
por mecanismos adaptativos secundários à desenervação.[18]
Outra alteração morfológica corresponde à infiltração do músculo esquelético por
lípidos, quer dentro de adipócitos, quer diretamente nos miócitos. No primeiro caso, verificase que durante o envelhecimento as células satélite musculares desenvolvem um fenótipo de
adipócito, no entanto este processo continua parcialmente desconhecido no que diz respeito
há sua extensão e distribuição (lípidos intermusculares); No segundo caso, a deposição de
lípidos dentro dos miócitos parece ser consequência da redução da capacidade oxidativa das
fibras musculares (lípidos intramusculares) [19, 20]. Pode-se então falar de obesidade
sarcopénica. Os doentes sarcopénicos com obesidade tem maior tendência a ter problemas de
mobilidade e incapacidade motora. A sarcopenia e a obesidade tem então uma ação sinérgica.
Neste tipo de sarcopenia, a IL-6 (interleucina-6) tem uma importante atividade catabólica,
pois o sua produção relaciona-se com a existência de gordura abdominal. Para além disso o
aumento de gordura corporal (em particular da gordura abdominal) contribui também para a
redução dos níveis de testosterona e GH (hormona do crescimento) e para o aumento de
cortisol, citocinas pró-inflamatórias e outros fatores que contribuem para o estado de
inflamação crónica. [21]
- Causas Hormonais
Durante o envelhecimento há alteração na produção e na sensibilidade do organismo à
ação de hormonas circulantes. No âmbito desta revisão vou me focar nas alterações que
decorrem na ação da insulina, hormona de crescimento (GH), factor de crescimento
semelhante à insulina (IGF-1), cortisol, vitamina D e na testosterona, apesar de também
poderem ocorrer alterações noutras hormonas.[1]
Em relação à insulina verifica-se uma redução na síntese proteica secundária à
insulino-resistência bem como uma “reduzida redução” da inibição da proteólise pela insulina
ou ingestão de alimentos. [22]
Existem duas formas de produção de IGF-1; uma delas resulta de interação de GH
com o fígado, e outra resulta da produção diretamente no músculo. Com o envelhecimento há
redução dos níveis circulantes de GH que por sua vez causam redução dos níveis circulantes
de IGF-1, assim como também existe redução da produção local deste factor. A IGF-1 tem
efeitos anabólicos no músculo, favorecendo a síntese proteica, a diferenciação e proliferação
de mioblastos e tem efeitos neurotróficos (favorecendo os mecanismos adaptativos de reenervação). É importante referir que baixos níveis de IGF-1 no idoso estão também
associados a reduzida força de extensão do joelho bem como reduzida velocidade de passada.
Pode parecer lógico usar como tratamento injeções de GH, no entanto não há relato que tal
tratamento pudesse aumentar a força muscular, apesar do possível aumento de massa
muscular; além disso o seu tratamento a longo prazo teria efeitos adversos inaceitáveis.[1,22]
Relativamente ao papel do cortisol no envelhecimento, é importante referir que há
uma redução da sensibilidade do eixo hipotálamo-hipofise-supra-renal, havendo um aumento
dos níveis de cortisol circulante com aumento da exposição dos tecidos orgânicos aos
glucocorticoides.[1]
Os níveis de vitamina D circulantes diminuem significativamente com o
envelhecimento, sendo que tal diminuição está relacionada com a sarcopenia, quedas, fratura
do fémur e aumento da morbilidade e mortalidade no idoso, devendo ser um ponto importante
a explorar do ponto de vista terapêutico. O anabolismo muscular diminui quando os níveis de
vitamina D são reduzidos, quer por aumento da degradação miofibrilhar quer pela redução da
síntese proteica. [23]
No homem os níveis de testosterona livre no soro diminui em cerca de 40% dos 25 aos
75 anos; Uma vez que a testosterona está correlacionada com a produção de cadeias pesadas
de miosina e com força muscular, com a redução da sua concentração durante o
envelhecimento, há uma diminuição da massa muscular e em menor grau da força. Os níveis
de testosterona podem ser considerados como um factor major no declínio da função
muscular no idoso. A testosterona está também relacionada com a inibição da via que
transforma as células satélite musculares em adipócitos. Na mulher a concentração de
testosterona diminui rapidamente entre os 20 e os 45 anos no entanto a sua importância para
manter a massa e força muscular não é clara. Apesar dos níveis de testosterona entre os 43 e
os 73 anos estarem relacionados com a massa muscular e força,
a literatura sugere que a
mulher produz testosterona suficiente para ter o efeito anabólico.[22,24]
Outro aspecto importante é a redução da concentração de desidroepiandrosterona (um
percursor da testosterona) com o envelhecimento. Uma vez que esta hormona inibe a
produção de interleucina 6 (IL-6), existe um aumento deste mediador inflamatório
condicionando um estado de inflamação crónica promovendo o catabolismo.[22, 24]
- Causas Inflamatórias
A inflamação pode ser o factor chave na fisiopatologia da sarcopenia decorrente do
envelhecimento. No idoso assistimos a um baixo grau de inflamação crónica, que pode ser
demonstrado por aumento da concentração de citocinas pró-inflamatórias e reagentes de fase
aguda, como o factor de necrose tumoral alfa (TNF-alfa), interleucina 1 e 6 (IL-1 e IL-6) e a
proteína C reativa (PCR). O aumento das citocinas pró-inflamatórias resulta num estimulo
para a degradação das proteínas musculares e uma inibição da sua síntese. O sistema
ubiquitina-proteossoma é a via mais importante na degradação de proteínas musculares. Esta
via é ativada pelas citocinas pró-inflamatórias citadas anteriormente e por hormonas como o
cortisol e a angiotensina, assim como por espécies reactivas de oxigénio (ROS). [1]
O TNF-alfa tem um papel fundamental na fisiopatologia desta síndrome, ativando
cinases e factores intracelulares responsáveis pela indução da proteólise, estando também
associada a alteração do factor de iniciação 4E, diminuindo a síntese proteica por diminuição
da iniciação e transcrição. [1,22] Um efeito indireto da TNF-alfa no metabolismo proteico
pode também ser a inibição da ação da insulina no músculo.[22]
O tecido adiposo é responsável pela produção de IL-6 e resistina. Desta forma há uma
relação entre o adipócito e a degradação proteica, fazendo com que a obesidade contribua
para um estado inflamatório crónico que condiciona perda muscular. As citocinas próinflamatórias estão também relacionadas com a diminuição do apetite, diminuição da
mobilidade do intestino e atraso no esvaziamento gástrico. [22]
As espécies reativas de oxigénio (ROS), que são resultado do metabolismo oxidativo,
acumulam-se ao longo do tempo e vão contribuir para alterações degenerativas celulares.
Como a mitocôndria produz ROS, o DNA mitocondrial é muito afetado, sendo que a
frequência de mutações no DNA mitocondrial é maior nos músculos extremamente
sarcopénicos. No entanto o papel da mitocôndria na fisiopatologia da sarcopenia permanece
em investigação. Sabe-se apenas que a alteração na mitocôndria pode afectar o transporte de
electrões e condicionar a respiração celular, podendo estar envolvida na redução do consumo
máximo de oxigénio que ocorre com a idade. [25]
- Sedentarismo e Imobilidade
Durante o envelhecimento, há tendência para a inatividade física e sedentarismo. De
igual forma, também se verifica um aumento do número de quedas, o que faz com que
inúmeros idosos fiquem acamados. Os estudos demonstram que existe uma redução da massa
muscular sem alterações significativas na massa gorda em idosos que ficam acamados durante
10 dias, ao passo que estes efeitos são apenas notórios quando o período de imobilidade nos
adultos jovens é de 28 dias. Isto demonstra que as pessoas idosas têm maior tendência a
perder massa muscular quando ficam acamados.[26]
- Alterações Intrínsecas do Músculo Esquelético
Os estudos que dizem respeito a alterações no número de células satélite musculares
não são consensuais, existindo alguns que afirmam que o seu número diminui enquanto
noutros o seu número não se altera. Há evidencia que a alteração da capacidade regenerativa
do músculo diminui devido a alterações nos reguladores moleculares que atuam na célula
satélite muscular, chamados de factores reguladores miogénicos (MRF- Myogenic Regulatory
Factors). A expressão destes factores encontra-se diminuída em indivíduos idosos. Outro
factor envolvido é a miostatina, que tem uma ação inibitória na diferenciação e proliferação
dos miócitos através da supressão da expressão dos MRFs. [27, 28]
- Outros Mecanismos
Durante o envelhecimento existe um comprometimento/redução tanto da resposta
anabólica ao exercício físico como da resposta anabólica à nutrição.
A resposta anabólica à alimentação no idoso encontra-se reduzida, estando esta
relacionada tanto com a qualidade de proteína consumida como com as alterações hormonais
decorrentes do envelhecimento, assim como com a resistência a insulina. Estudos baseados no
balanço do nitrogênio indicam que os requisitos proteicos aumentam com a envelhecimento e
que as proteínas “rápidas” (soro do leite) são mais benéficas que as “lentas” (caseína) na
estimulação da síntese proteica. O mecanismo fisiopatológico desta redução da resposta
anabólica parece estar relacionado com um defeito na via de ativação dos aminoácidos de
cadeia ramificada, sendo por isso importante do ponto de vista terapêutico aumentar a
disponibilidade de aminoácidos de cadeia ramificada.[22] Está demonstrado que uma mistura
de aminoácidos essenciais contendo leucina aumentam mais a síntese proteica que outras
formas de proteína; O mecanismo pelo qual a leucina estimula a tradução de proteínas está
relacionado com o aumento da concentração intracelular desse aminoácido promover a
ativação de uma proteína cinase denominada alvo da rapamicina (mTOR). O mTOR estimula
a síntese proteica através de ativação de proteínas reguladoras chave. Para além da resposta
anabólica reduzida, não se pode deixar de referir que o reduzido aporte nutricional do idoso,
em particular a quantidade de proteínas ingeridas, é comum e constitui também uma causa da
perda de massa magra.[29]
A resposta anabólica ao exercício de resistência ocorre através do reforço da síntese
proteica muscular. Apesar de os idosos continuarem a ter resposta anabólica, esse mecanismo
é menos eficaz que nos adultos jovens. Da mesma forma, os estudos que analisam o grau de
proteólise muscular após exercício sugerem que a proteólise é mais intensa e permanece
durante mais tempo nos indivíduos idosos.[22]
Manifestações Clínicas
A perda de massa muscular conduz a uma diminuição da força (“Kratopenia”) e
potência muscular (produto de força muscular com a velocidade de contração –
“Dynapenia”), estando estas manifestações relacionadas com um maior risco de mortalidade
do que a perda muscular por sí só. A incapacidade de desenvolver uma adequada potência
muscular é uma das causas do síndrome de fragilidade. Um idoso “frágil” é um individuo
com maior risco de quedas, fraturas, incapacidade, dependência, hospitalização recorrente e
mortalidade, sendo que tem uma menor capacidade de resposta a estímulos nocivos
apresentando maior vulnerabilidade fisiológica. Os indicadores da síndrome de fragilidade
incluem auto-relato de fadiga, incapacidade de subir um vão de escadas, incapacidade de
andar um quarteirão, coexistência de mais de cinco patologias e perda de peso recente
(especialmente da massa magra). Esta síndrome deve ser considerada uma condição que
precede a incapacidade, podendo ser denominada de pré-incapacidade. A sua prevalência
corresponde a 50% da prevalência da sarcopenia. Um idoso com incapacidade não consegue
desempenhar as atividades do dia a dia, perdendo a sua autonomia e independência. [30,31]
Exames Complementares de Diagnóstico
Em relação aos exames complementares de diagnósticos estes podem ser dividos em 4
classes: métodos para medição de massa muscular, métodos para avaliação da força muscular,
métodos para a determinação de performance física e marcadores biológicos.[32]
Os métodos para determinação da massa muscular incluem: densitometria (DEXA“dual energy X-ray absorptiometry”), antropometria, análise de impedância bioelétrica (BIA“Bioelectrical
Impedance
Analysis”),
ressonância
magnética
(RMN),
tomografia
computadorizada
(TC),
excreção
urinária
de
creatina,
ultrassom
e
tomografia
computadorizada periférica quantitativa (pQCT-“peripheral quantitative computerized
tomography”). [32]
A densitometria (DEXA) é uma técnica que permite análise da composição corporal,
sendo a escolha de rotina na determinação da densidade mineral óssea. Expõe o individuo a
uma dose baixa de radiação, é pouco dispendioso, é necessário um técnico especializado, um
centro especializado, e o tempo de execução é de cerca de 15min. Para além disso, a
densitometria pode sobrestimar a massa magra de um individuo com edemas, pois não
diferencia a água de tecido muscular.
A antropometria é um método com custos reduzidos, fácil de usar, no entanto tem
baixa validade e exatidão.
A análise da impedância bioelétrica (BIA) é um teste de rotina para estudo da
composição corporal. A BIA não expõe o individuo a radiação, os custos associados são
reduzidos, não necessita de pessoal especializado, é portátil podendo ser realizado à cabeceira
do doente, o tempo de execução é reduzido (5 minutos), mas por outro lado é menos sensível
e especifico que a densitometria. A BIA, tal como a DEXA, também pode sobrestimar a
massa magra na presença de edema.
A TC e RMN são os métodos mais específicos, sendo os Gold Standart na
determinação da massa muscular. Como nos dão a imagem em cortes axiais, são também
excelentes métodos para avaliar a qualidade muscular através da determinação da densidade
muscular e infiltração intramuscular de gordura. Estes métodos são bastante dispendiosos,
necessitando de pessoal e centros especializados, a sua execução é demorada (15-20 minutos)
não sendo por isso usados como testes de rotina. Uma vantagem da RMN em relação a TC
reside no facto de esta não expor o doente a elevadas doses de radiação.
A determinação da excreção urinária de creatinina é um indicador especifico da massa
muscular total. Como desvantagens pode considerar-se que a excreção urinária de creatinina
varia ao longo do dia, a excreção urinaria pode ser influenciada com a ingestão de carne, e
seria necessário colheitas de urina de 24horas.
A utilização de ultrassom é um método económico e não expõe o doente a radiação;
No entanto é necessário pessoal especializado para a sua realização, existem dificuldades para
avaliar a qualidade muscular e não nos permite avaliar a massa muscular total do individuo
A tomografia computadorizada periférica quantitativa (pQCT) consiste num aparelho
de TC portátil que mede a área seccional e analisa a composição corporal das extremidades
sendo que para a sua execução não é necessário pessoal altamente especializado. Expõe o
individuo a doses baixas de radiação, e foi inicialmente desenvolvido para avaliar os
parâmetros ósseos tendo menos aplicabilidade a nível muscular.
Tabela 1-Métodos para avaliar a massa e imagem muscular [32]:
DEXA
Vantagens
Desvantagens
-Pouco dispendioso;
-Baixa dose de radiação;
-Sensível;
-Técnico e centro especializado;
-Analisa a composição corporal (massa
-Falsos resultados quando doente
gorda, massa magra, osso) no corpo
apresente edema.
inteiro ou numa zona especifica;
-Disponível em vários locais.
Antropometria
-Fácil acesso e ausência de custos.
-Não dá informações sobre a
qualidade do músculo;
-Informação muito limitada e
operador dependente;
-Influenciada por comorbilidades
e estado nutricional.
BIA
Pouco dispendioso;
-resultados baseados na
Portátil;
resistência corporal;
Resultados estão logo disponíveis.
-não fornece informação sobre a
qualidade do músculo;
-afectado pelo estado de
hidratação;
- os resultados são menos
específicos que a RMN, TC e
DEXA.
TC e RMN
-Avalia a qualidade do músculo;
-Exposição a Radiação (TC)
-Permite cortes seccionais em áreas
-Necessário técnicos e centro
especificas.
especializado;
-Muito dispendioso;
-Resultados não são imediatos.
Excreção Ur.
-Tem correlação com a massa muscular - Resultados não são imediatos;
Creatinina
total.
-Influenciado pela alimentação;
-Variação diária da excreção.
Ultrassom
-Pouco dispendioso;
- Operador dependente;
-Consegue-se aceder a músculos
-Não dá informação sobre a
específicos.
massa muscular total;
-Dificuldade técnica para aceder à
qualidade muscular.
pQTC
-Portátil;
-Baixa dose de radiação;
-Permite cortes seccionais.
-Inicialmente foi criado para
avaliar os parâmetros ósseos,
tendo por isso menos
aplicabilidade no músculo.
Os valores de cut-off num estudo de Baumgarher publicado em 1998 sobre a
prevalência da Sarcopenia no Novo México, são de 7,26 Quilogramas/metro quadrado para
homens e 5,45 Quilogramas/metro quadrado para mulheres usando como método de medição
de massa muscular a densitometria (DEXA). Neste estudo inicialmente fez-se um ajustamento
da massa muscular apendicular em relação ao peso corporal (massa muscular da perna+braço
a dividir pelo quadrado da altura). De seguida considerou-se sarcopenia como um valor
correspondente a 2 ou mais desvios padrão a baixo do valor de massa apendicular ajustada da
média dos adultos de referencia. [33,34] Existem outros valores de cut-off definidos por
outros autores e com base noutros métodos de diagnóstico, no entanto tais dados saem fora do
âmbito desta revisão.
Em relação aos métodos para avaliar a força muscular, existem dois tipos de métodos:
os dinamómetros (que medem a força isométrica) e aparelhos mais complexos que nos dão
medição de potência muscular (produto da força muscular com a velocidade de contração).
Uma vez que a sarcopenia é uma condição sistémica que não se limita a um grupo muscular
específico, a medição de força muscular nos vários compartimentos musculares está
correlacionada. Desta forma, um método eficaz e simples de avaliar a força muscular no idoso
será através da força de preensão da mão com um dinamómetro [32]
Os métodos mais utilizados para avaliar a performance física incluem o “Short
Physical Performance Battery” (que é baseado na velocidade da passada, na capacidade de um
individuo se levantar de uma cadeira e testes de equilíbrio), o teste dos 400m de passada e o
teste 6 minutos. [35,36,37]
Os marcadores biológicos como citocinas pró-inflamatórias, anemia, níveis de
albumina sérica reduzidos, níveis plamáticos de Selénio reduzidos, biomarcadores de lesão
axidativa (como o oxLDL- “Oxidized low-density lipoprotein”, que resulta da peroxidação da
lipoproteina de baixa densidade (LDL)) apresentam uma baixa especificidade para a perda de
massa magra e de força muscular tendo por isso uma utilidade limitada no diagnóstico, uma
vez que são também marcadores de outras patologias. Em relação à medição dos níveis
circulantes de ubiquitina-proteossoma, apesar de constituir um marcador específico de
proteólise, a sua relação com a sarcopenia no idoso ainda não foi estudada. [32]
Tratamento
A Sarcopenia é uma condição de etiologia multifatorial que pode ser tratada por
múltiplos métodos. Dentro das estratégias disponíveis, o exercício físico (treino de
resistência) em combinação com uma nutrição adequada constituem a forma mais eficaz de
prevenir e tratar a sarcopenia. [1]
- Exercício
Durante a atividade física, a contração muscular causa uma libertação de factores de
crescimento muscular que ativam as células satélite e favorecem a síntese proteica,
contribuindo para a regeneração muscular (processo que se torna menos eficaz com o
envelhecimento). A prática de exercício físico, mais especificamente treino de resistência, tem
como consequências ganhos a nível de força e massa muscular. É importante considerar que
com o envelhecimento surgem limitações para a pratica deste tipo de exercício, quer do ponto
de vista osteoarticular quer cardiovascular, que condicionam os seus efeitos, sendo essas
limitações mais evidentes nos indivíduos mais idosos, mais “frágeis” ou com fraco suporte
social. Por outro lado, o treino de resistência não deve ser descontinuado, pois isso teria como
consequência uma perda rápida dos benefícios adquiridos com a sua prática. [38]
Existem diferentes estudos descritos sobre o efeito do treino de resistência na força e
massa muscular. Frontera et al que realizou um estudo em que indivíduos do sexo masculino
entre os 60 e 72 anos foram submetidos a treino de resistência durante 12 semanas e
Fiantarone et al que realizou um estudo semelhante com homens e mulheres entre os 87 e 96
anos submetidos a treino de resistência durante 8 semanas obtiveram resultados semelhantes;
Em ambos os casos se obtive um ganho de massa muscular de cerca de 10% e um ganho em
termos de força muscular de cerca de 170%. Desta forma, pode-se concluir que existe uma
diferença enorme entre os ganhos de força e de massa muscular decorrente da prática de
treino de resistência, sendo que os ganhos no que respeita a força muscular superam de longe
os ganhos de massa muscular.
A perda de força muscular é mais evidente que a perda de massa em indivíduos
sedentários, e por sua vez os ganhos de força muscular superam os ganhos de massa em
indivíduos sujeitos a treino de resistência. Pode se então considerar que tamanho de músculo
não é equivalente a qualidade muscular e que não é o ponto determinante da função muscular.
[39,40]
-Farmacologia
No homem idoso os níveis de testosterona diminuem a um ritmo de 1% por ano de
forma que 20% dos homens na sexta década de vida e 50% na oitava têm hipogonadismo.
[41] Esta redução de testosterona está relacionada com perda de força e massa muscular,
assim como com uma deterioração do status funcional. [42] Por sua vez na mulher ocorre
uma redução dos níveis circulantes de estrogénio com a menopausa que tem como
consequência uma diminuição da força e massa muscular, uma vez que os estrogénios podem
ser convertidos perifericamente em testosterona. As hormonas sexuais têm também uma ação
supressora nas citocinas inflamatórias que por sua vez têm efeitos catabólicos no músculo.
No homem jovem que pratica treino de resistência a administração de doses superiores
à concentração fisiológica de testosterona está associada a um aumento muito acentuado de
massa e força muscular. No homem idoso com hipogonadismo, a administração de
testosterona aumenta a massa muscular, a força e reduz o percentual de massa gorda. Em
relação aos indivíduos idosos que não tem hipogonadismo a eficácia na administração de
testosterona na força e massa muscular é inconclusivo. [41] Nos idosos com síndrome de
fragilidade a administração de 50 mg por dia de testosterona durante 6 meses demonstrou um
aumento da massa magra assim como um aumento na força muscular, sendo este incremento
maior quando combinado com exercício físico e com uma nutrição adequada. [43] Os efeitos
da administração de testosterona na redução do numero de quedas, redução do numero de
mortes, e aumento da autonomia no idoso continuam por estudar. [41]
A administração de testosterona no tratamento do idoso com
sarcopenia é
controverso, devido aos potenciais efeitos secundários (como exemplo: acne, alterações na
forma e tamanho dos testículos, edemas, alterações no desempenho sexual, obstrução urinária,
apneia do sono, depressão [44]). Atualmente, apenas se recomenda a administração de
testosterona em homens com sinais e sintomas de deficiência de androgénios (incluindo
reduzida massa muscular e força) e com níveis séricos baixos de testosterona, sendo que a
ausência de benefícios após seis meses de tratamento justifica uma revisão e uma possível
mudança de estratégia terapêutica. Está contraindicada a administração de testosterona em
indivíduos com cancro da próstata, eritrocitose, hiperviscosidade sanguínea, apneia obstrutiva
do sono não tratada, sintomas do trato urinário baixo e insuficiência cardíaca grau III e IV.
[41]
Os moduladores seletivos dos receptores de androgénios (SARMS- “Selective
Androgen Receptor Modulators”) são agentes não esteroides que se ligam ao receptor de
androgénios presente no músculo, órgãos sexuais e osso. Estes agentes têm menor efeito na
estimulação prostática e resultam numa menor virilização, tendo por isso menor número de
efeitos secundários. Têm efeitos anabólicos, constituindo uma potencial arma terapêutica na
sarcopenia, com aplicação tanto na mulher como no homem. No entanto, estes agentes
farmacológicos ainda se encontram numa fase precoce de ensaios clínicos. [45]
Como com o envelhecimento ocorre uma redução dos níveis séricos de
desidroepiandrosterona (um percursor da testosterona) que por sua vez têm um efeito antiinflamatório [22], seria de esperar que administração deste agente resultasse em alterações
benéficas a nível muscular, o que de facto não se verifica. Desta forma, e apesar de ter um
efeito benéfico no aumento da densidade óssea, não é recomendado o seu uso no tratamento
da sarcopenia no idoso. [46]
Como já foi referido anteriormente, a mulher tem uma redução da força e massa
muscular na altura da menopausa. Estas alterações parecem ser consequência tanto das
alterações hormonais como também de alterações no estilo de vida da mulher (como o
sedentarismo). A terapêutica hormonal de substituição faz com que as mulheres possam ter
uma melhoria da qualidade de vida com aumento da auto-estima o que traz muitos benefícios
no pós menopausa. Apesar destes benefícios, os estudos sobre os efeitos dos estrogénios em
mulheres pós menopausa na força e massa muscular não são consensuais existindo estudos
que demonstram ganho tanto de força como de massa magra enquanto outros não se verifica
qualquer alteração. Em relação a mulheres idosas existem poucos estudos realizados até ao
momento, pelo que não se consegue concluir a eficácia e a aplicabilidade dos estrogénios no
tratamento da sarcopenia no idoso [41]
Como já abordado anteriormente, o envelhecimento tem como consequência uma
redução nos níveis circulantes de hormona de crescimento (GH) e IGF-1. Em indivíduos
idosos do sexo masculino, diversos ensaios clínicos relatam ausência de beneficio da
suplementação de GH com o exercício de resistência ou com outras hormonas anabólicas no
que respeita a hipertrofia muscular, força, e expressão de IGF-1. [47] No entanto, num ensaio
clínico realizado em mulheres obesas na pós menopausa foi demonstrado que a administração
de GH (com ou sem combinação com IGF-1) resulta numa redução de peso e massa gorda
superior à adquirida com o exercício ou a dieta isoladamente, sem intervir na quantidade de
massa magra. [48] Apesar da administração exógena de GH constituir terapêutica de algumas
condições (como por exemplo a deficiência primária de GH, a deficiência adquirida de GH, e
como tratamento da caquexia associada ao HIV) a sua aplicação no tratamento da sarcopenia
no idoso ainda não foi testada no que respeita a segurança e eficácia em ensaios clínicos
duplamente cegos. Por outro lado a administração de GH está associada a inúmeros efeitos
secundários que limitam a sua aplicação clínica (exemplo: diabetes, ginecomastia, artralgias,
edemas, síndrome do túnel cárpico). Da mesma forma, a biologia complexa da ação da GH no
organismo bem como a sua pulsatibilidade biológia constituem também pontos que limitam a
sua aplicação no tratamento da sarcopenia. [41,44]
A concentração sérica de vitamina D vai diminuindo com o envelhecimento, sendo
esta deficiência vitamínica um achado muito prevalente na população idosa. É recomendada a
determinação da concentração sérica de vitamina D em todos os idosos com sarcopenia, sendo
que deve ser iniciada suplementação naqueles cuja concentração seja inferior a 100 nmol/L. A
perda de força proximal e a miopatia induzida por estatinas constituem manifestações clínicas
típicas deste défice vitamínico. A suplementação com vitamina D no tratamento da sarcopenia
tem como benefício o aumento de força muscular e redução do risco de quedas e de fracturas.
[41,49]
Encontram-se em investigação possíveis estratégias de tratamento da sarcopenia e da
caquexia, entre as quais se destaca a utilização de grelina, o antagonista do receptor da
melanocortina 4 a nível central (MC4R), a utilização de leptina, e o antagonista da miostatina
no músculo. Em relação a utilização de grelina no tratamento da caquexia em doentes
crónicos, destaca-se um ensaio clínico realizado em 25 doentes com doença pulmonar
obstrutiva crónica em que a administração de injeções subcutâneas de um análogo da grelina
resultou num aumento da massa magra e melhoria da função motora. [50] Não foram
publicados até ao momento resultados sobre a sua aplicabilidade no tratamento da sarcopenia.
Em relação ao antagonismo do receptor central da melanocortina 4 (MC4R), foi demonstrado
num modelo animal (rato) com caquexia cardíaca que esse bloqueio aumentava tanto a massa
gorda como a massa magra. [51] Os resultados deste antagonismo no Ser Humano ainda não
foram publicados até ao momento. O papel da leptina na fisiopatologia da sarcopenia não é
claro, no entanto sabe-se que a leptina pode influenciar a síntese proteica a nível muscular
podendo constituir uma arma terapêutica no futuro. [41] Em relação à miostatina, sabe-se que
esta é expressa no músculo esquelético e que tem como ação a inibição da síntese proteica e
inibição do crescimento muscular. Desta forma, a inibição da miostatina pode constituir uma
estratégia terapêutica do futuro no tratamento da sarcopenia e da distrofia muscular. [41]
Como já abordado anteriormente, a inflamação parece ter um papel fundamental na
fisiopatologia da sarcopenia, levando-nos a pensar que do ponto de vista terapêutico os antiinflamatórios pudessem constituir uma arma poderosa para prevenir e impedir a progressão
desta síndrome. Sabe-se por exemplo que a talidomida aumenta o peso e a quantidade de
massa magra em doentes com SIDA, resta-nos por isso aguardar que sejam realizados ensaios
clínicos sobre o efeito dos agentes anti-inflamatórios em idosos sarcopénicos. [1,22,41]
A suplementação de creatina é essencial para aumentar as reservas energéticas
extramitocondriais através da formação de fosfocreatina, contribuindo para um aumento da
capacidade física e ganhos a nível de massa e força muscular. Para além disso a creatina
também parece ser responsável pela diminuição do catabolismo proteico e por aumentar o
ritmo de síntese proteica. A creatina pode também ser responsável pela modulação de genes
específicos do músculo, como a miogenina, e em combinação com treino de resistência
parece também reforçar
a ativação das células satélite musculares. [41] Desta forma a
creatina aumenta tanto a massa muscular como a força de extensão/flexão do joelho em
indivíduos idosos. A creatina causa também retenção de fluidos que pode resultar em edemas
periféricos, sendo um ponto negativo para a sua aplicação no idoso.
Nutrição
Como já abordado anteriormente, a nutrição desempenha um papel importantíssimo na
fisiopatologia da Sarcopenia, pelo que constitui também um ponto chave no tratamento desta
condição. Uma nutrição adequada, em particular a ingestão de proteínas, é essencial para a
manutenção da massa muscular. A quantidade de proteína adequada num idoso é de 1,25 a
1,50 g/kg/dia, sendo maior do que a o valor que é recomendado para um adulto (0,8 g/kg/dia),
sugerindo então que as necessidades proteicas no idoso podem estar aumentadas. [53] Alguns
estudos foram realizados para verificar o efeito de uma ingestão diária de proteína elevada no
idoso. Num estudo verificou-se que o turnover proteico é reforçado quando a proteína
corresponde a cerca de 12-21% da fonte energética diária. [54] Noutro estudo, em que se
utilizou uma dose diária de proteína de 3g/kg/dia durante 10 dias, não se verificou alteração
na síntese proteica a nível muscular, nem na massa muscular total. Neste mesmo estudo
verificou-se também que uma carga diária de proteína muito elevada causa um aumento da
taxa de filtração glomerular nos jovens e uma diminuição da função renal no idoso, sugerindo
que uma carga proteica muito elevada pode ser prejudicial nos indivíduos idosos. [55] Noutro
estudo ainda, em que se realizou um “follow-up” de 3 anos de idosos que consumiam uma
dose diária de proteína superior à recomendada no adulto, verificou-se que um consumo mais
elevado de proteína causa uma menor redução da massa magra apendicular. [56]
Em relação ao tipo de proteína ingerida, é necessário referir que as proteínas de maior
valor biológico têm maior impacto a na inibição da protéolise a nível muscular. Foi também
demonstrado que as proteínas “rápidas” (soro do leite) são mais benéficas que as “lentas”
(caseína) na estimulação da síntese proteica. [22] Uma mistura de aminoácidos essenciais
contendo leucina aumenta mais a síntese proteica que outras formas de proteína; o mecanismo
pelo qual a leucina estimula a tradução de proteínas está relacionado com o aumento da
concentração intracelular desse aminoácido promover a ativação de uma proteína cinase
denominada alvo da rapamicina (mTOR). O mTOR estimula a síntese proteica através de
ativação de proteínas reguladoras chave. [29] Alguns dos alimentos que contêm leucina são:
leite, queijo, carne, atum, amendoim e ovos.
Outro ponto importante a considerar é a distribuição da ingestão proteica ao longo do
dia. De acordo com a literatura, nos idosos é mais benéfico uma ingestão de cerca de 80% da
proteína total diaria numa refeição (almoço) que uma ingestão espaçada de pequenas
quantidades de proteína. [22] Este tipo de estratégia é chamado de “pulse protein pattern”, e
causa uma maior retenção de proteínas no idoso assim como um balanço de nitrogénio “mais
positivo”. Esta estratégia tem como vantagens: uma refeição rica em proteína ao almoço faz
com que a concentração de aminoácidos aumente drasticamente no organismo e de seguida as
pequenas refeições contendo pequena quantidade de proteína e maior quantidade de hidratos
de carbono vão ser responsáveis por um aumento da insulina pós-prandial que limita a perda
proteica por redução da proteólise. A “pulse protein pattern” faz com que os idosos possam
recuperar até certo ponto a resposta anabólica à nutrição, e representa uma forma mais
adequada e segura de fornecer mais quantidade de proteína aos indivíduos idosos. [22, 53]
Conclusão
A sarcopenia é uma causa muito importante de morbilidade e mortalidade no idoso.
Com o aumento da esperança média de vida e com envelhecimento atual da população
mundial esta síndrome geriátrica ganha um destaque especial pelo que deve ser melhor
entendida a sua fisiopatologia para que se possa proceder a uma intervenção terapêutica
adequada. Para além disso, será importante também uniformizar uma estratégia diagnóstica
para que se consiga reconhecer esta condição o mais precocemente possível com a finalidade
de prevenir eventuais complicações.
Em relação ao tratamento, reconhece-se que a melhor intervenção passa pela nutrição
adequada em associação com treino de resistência, estando o tratamento farmacológico
reservado para situações específicas. Apesar de ser o tratamento com melhores resultados
demonstrados até ao momento, muitas das vezes a sua aplicação não é possível, uma vez que
alguns idosos não têm suporte familiar que lhes permita efetuar uma alimentação rigorosa
assim como a prática de exercício físico pode ser contra-indicada por comorbilidades
existentes no idoso. Seria importante realizar um estudo sobre a influencia dos antiinflamatórios no tratamento da sarcopenia, uma vez que a inflamação parece ter um papel
importante na patogénese desta síndrome geriátrica.
Referencias Bibliográficas
1. Cuiying Wang , Li Bai. Sarcopenia in the elderly: Basic and clinical issues. Geriatr
Gerontol Int 2012; 12: 388–396
2. Strehler BL. Time, cells, and aging. Academic Press, New York; 1997
3. Goto M. Inflammaging (inflammation+aging): a driving force for human aging based
on an evolutionary antagonistic pleiotropy theory? BioScience Trends 2008 (6):218230
4. Rosenberg IH. Summary comments. Am J Clin Nutr 1989;50:1231-3
5. Rosenberg
IH.
Sarcopenia:
origins
and
clinical
relevance.
J
Nutr
1997;127(5(Suppl.)):990S-1S
6. Cruz-Jentoft AJ, Baeyens JP, Bauer JM, Boirie Y, Cederholm T, Landi F et al.
European consensus on definition and diagnosis: report of the European Working
Group on Sarcopenia in Older People. Age Ageing 2010; 39 (4): 412-423
7. Cruz-Jentoft AJ, Landi F, Topinková E et al. Understanding sarcopenia as a geriatric
syndrome. Curr Opin Clin Nutr Metab Care 2010; 13 (1):1-7
8. Narici MV, Maffulli N. Sarcopenia: characteristics, mechanisms and funcional
significance. Br Med Bull 2010; 95: 139-59
9. Morley JE. Anorexia, sarcopenia and aging. Nutrition 2001; 17: 660-5
10. Evans WJ, Morley JE, Argiles J, et al. Cachexia: a new definition. Clin Nutr
2008;27:793-9
11. Buford TW, AntonSD, Judge AR, et al. Models of accelerated sarcopenia: critical
pieces for solving the puzzle of age-related muscle atrophy. Ageing Res Rev 2010;
9(4):369-83
12. Muscaritoli M, Anker SD, Argiles J et al. Consensus definition of sarcopenia,
cachexia and pre-cachexia:joint document elaborated by special interest Groups (SIG)
“cachexia-anorexia in chronic wasting diseases” and “nutrition in geriatrics”. Clin
Nutr 2010; 29(2):154-159
13. Grimby G, Saltin B. The ageing muscle. Clin Physiol 1983;3:209
14. Goodpaster BH, Park SW, Harris TB et al. The loss of skeletal muscle strength, mass,
and quality in older adults: the health, aging and body composition study. J Gerontol
A Biol Sci Med Sci 2006; 61: 1059–1064.
15. Janssen I, Shepard DS, Katzmarzyk PT, Roubenoff R. The healthcare costs of
sarcopenia in the United States. J Am Geriatr Soc 2004;52(1):80-5
16. Lexell J, Downham DY. The occurance of fibre type grouping in healthy human
muscle: a quantative study of cross-sections of whole vastus lateralis from men
between 15 and 83 years. Acta Neuropathol 1991; 81:377-381
17. Lexell J, Downham DY, Larson Y, Bruhn E, Morsing B. Heavy-resistence training in
older Scandinavian men and women: short- and long-term effects on arm and leg
muscles. Scand J Med Sci Sports 1995; 5:329-341
18. Gordon T. Hegedus J, Tam SL. Adaptative and maladaptative motor axonal sprouting
in aging and motorneuron disease. Neurol Res 2004; 26:174-185
19. Shefer G, Van de Mark DP, Richardson JB, Yablonka-Reuveni Z. Satellite-cell pool
size does matter: defining the myogenic potency of aging skeletal muscle. Dev Biol
2006; 294:50-66
20. Kraegen EW, Cooney GJ. Free fatty acids and skeletal muscle insulin resistence. Curr
Opin Lipidol 2008;19:235-241
21. Jensen GL. Inflammation: roles in aging and sarcopenia. JPEN J Parenter Enteral Nutr
2008;32(6):656-9
22. Walrand S, Guillet C, Salles J et al. Physiopathological Mechanism of Sarcopenia.
Clin Geriatr Med 2011; 27:365-385
23. Morley JE. Vitamin D redux. J Am Med Dir Assoc 2009; 10:591-2
24. Haren MT, Siddiqui AM, Armbrecht HJ et al. Testosterone modulates gene expression
pathways regulating nutrient accumulation, glucose metabolism and protein turnover
in mouse skeletal muscle. Int J Androl 2010
25. Hiona A, Leeuwenburgh C. The role of mitochondrial DNA mutations in aging and
sarcopenia: implications for the mitochondrial vicious cycle theory of aging. Exp
Gerontol 2008; 43:24-33
26. Kortebein P. Ferrando A, Lombeida J, Wolfe R, Evans WJ. Effect of 10 days of bed
resto n skeletal muscle in healthy older adults. JAMA 2007; 297 (16):1772-4
27. Gallegly JC, Turesky NA, Strotman BA, Gurley CM, Peterson CA, DupontVersteegden EE. Satellite cell regulation of muscle mass is altered at old age. J Appl
Physiol 2004; 97:1082-1090
28. McCroskery S, Thomas M, Maxwell L, Sharma M, Kambadur R. Myostatin
negatively regulates satellite cell activation and self-renewal. J Cell Biol 2003.
162:1135-1147
29. Millward DJ, Fereday A, Gibson NR et al. Efficiency of utilization of wheat and milk
protein in healthy adults and apparent lysine requirements determinated by a single
meal (1-13C) leucine balance protocol. Am J Nutr 2002;76:1326-34
30. Abellan van Kan G, Rolland YM, Morley JE, Vellas B. Frailty: toward a clinical
definition. J Am Med Dir Assoc 2008; 9:71-2
31. Fried LP, Ferrucci L, Darer J et al. Untangling the concepts of disability, frailty, and
comorbidity: implications for improved targeting and care. J Gerontol A Biol Sci Med
Sci 2004;59:255-63
32. M. Pahor, T. Manini, M. Cesari. Sarcopenia: clinical evaluation, biological markers
and other evaluation tools. The Journal of Nutrition, Health and Aging 2009
33. Janssen I. The Epidemiology of Sarcopenia. Clin Geriatr Med 2011; 27 355-363
34. Baumgartner RN, Koehler KM, Gallagher D, et al. Epidemiology of Sarcopenia
among the elderly in New Mexico. Am J Epidemiol 1998;147(8):755-63
35. Ettinger WH, Burns R, Messier SP, Applegate WB, Rejeski WJ, Morgan T et al. The
Fitness Arthritis and Seniors Trial (FAST): a randomized trial comparing aerobic
exercise and resistance exercise to a health education program on physical disability in
older people with knee osteoarthritis. JAMA 1997; 277:25-31.
36. Newman AB, Simonsick EM, Naydeck EM, Kritchevsky SB, Nevitt M, Pahor M, et
al. Association of long-distance corridor walk performance with mortality,
cardiovascular disease, mobility limitation, and disability. JAMA 2006;295(17):201826.
37. Guralnik JM, Ferrucci L, Simonsick EM, Salive ME, Wallace RB. Lower-extremity
function in persons over the age of 70 years as a predictor of subsequent disability. N
Engl J Med 1995;332(9):556-61.
38. Liu CJ, Latham NK. Progressive resistance strenght training for improving physical
function in older adults. Cochrane Database Syst Rev 2009
39. Fiatarone MA, Marks EC, Ryan ND, Meredith CN, Lipsitz LA, Evans WJ. Highintensity strength training in nonagenarians. Effects on skeletal muscle. JAMA 1990;
263:3029- 3034.
40. Frontera WR, Meredith CN, O'Reilly KP, Evans WJ. Strength training and
determinants of VO2max in older men. J Appl Physiol 1990; 68:329-333.
41. Rolland Y, Onder G, Morley JE et al. Current and Future Pharmacologic Treatment of
Sarcopenia. Clin Geriatr Med 2011; 27:423-447
42. Morley JE, Haren MT, Kim MJ, Kevorkian R, Perry HM. Testosterone, aging and
quality of life. J Endocrinol Invest 2005; 28:76-80
43. Srinivas-Shankar U, Roberts SA, Connolly MJ, et al. Effects of testosterone on muscle
strength, physical function, body composition, and quality of life in intermediate-frail
and frail elderly men: a rondomized, double blind, placebo-controlled study. J Clin
Endocrinol Metab 2010;95(2):639-50
44. Brotto M, Abreu EL. Sarcopenia: Pharmacology of Today and Tomorrow. Journal of
Pharmacology and Experimental Therapeutics 2012.
45. Gao W, Reiser PJ, Cross CC, Phelps MA, Kearbey JD, Miller DD et al. Selective
androgen receptor modulator treatment improves muscle strength and body
composition and prevents bone loss in orchidectomized rats. Endocrinology 2005;
146:4887-4897
46. Baker WL, Karen S, Kenny AM. Effects of dehydroepiandrosterone on muscle
strength and physical function in older adults: a systematic review. J Am Geriatr Soc
2011;59(6):997-1002.
47. Taaffe DR, Pruitt L, Reim J et al. Effect of recombinant human growth hormone on
the muscle strength response to resistance exercise in elderly men. J Clin Endocrinol
Metab 1994; 79: 1361–1366.
48. Thompson JL, Butterfield GE, Gylfadottir UK et al. Effects of human growth
hormone, insulin-like growth factor I, and diet and exercise on body composition of
obese postmenopausal women. J Clin Endocrinol Metab 1998; 83: 1477–1484.
49. Latham NK, Anderson CS, Reid IR. Effects of vitamin D supplementation on
strength, physical performance, and falls in older persons: a systematic review. J Am
Geriatr Soc 2003;51(9):1219-26
50. Garcia JM, Polvino WJ. Effect on body weight and safety of RC-1291, a novel, orally
available ghrelin mimetic and growth hormone secretagogue: results of a phase I,
randomized, placebo-controlled, multiple-dose study in healthy volunteers. Oncologist
2007; 12: 594–600.
51. Scarlett JM, Bowe DD, Zhu X, Batra AK, Grant WF, Marks DL. Genetic and
pharmacologic blockade of central melanocortin signaling attenuates cardiac cachexia
in rodent models of heart failure. J Endocrinol 2010; 206: 121– 130.
52. Brose A, Parise G, Tarnopolsky MA. Creatine supplementation enhances isometric
strength and body composition improvements following strength exercise training in
older adults. J Gerontol A Biol Sci Med Sci 2003; 58:11-9.
53. Malafarina V, Uriz-Otano F, Iniesta R, Guerrero LG. Effectiveness of Nutritional
Supplementation on Muscle Mass in Treatment of Sarcopenia in Old Age: A
Systematic Review. Journal of the American Medical Directors Association 2013;1017
54. Pannemans DL, Halliday D, Westerterp KR. Whole body protein turnover in elderly
men and women: responses to two protein intakes. Am J Clin Nutr 1995; 61:33-8
55. Walrand S, Short K, Bigelow M, et al. Effect of high protein diet on insulin sensivity,
leucine kinetics, and renal function in healthy elderly humans. Am J Physiol
Endocrinol Metab 2008
56. Houston DK, Nicklas BJ, Ding J, et al. Dietary protein intake is associated with lean
mass change in older, community-dwelling adults: the Health, Aging, and Body
Composition (Health ABC) Study. Am J Clin Nutr 2008; 87: 150-5